Fe3O4基β-环糊精聚合物的制备及吸附性能
魏雨诗,王锐,林壮,姜恒,霍明仁,陈欣悦,梁晓艳,张重阳
(辽宁石油化工大学石油化工学院,辽宁 抚顺 113001)
目前,大多数聚合物[1]和热敏纸[2]的合成中都使用双酚A(BPA),其废水的排放对环境造成危害,污染食物链。日常生活中长期接触双酚化合物对健康造成多种不良影响,因此有效去除水体中的BPA是一个重要问题。处理有机污染物的技术有臭氧氧 化[3]、电 化 学 氧 化[4]、光 催 化 氧 化[5]、膜 过 滤[6]、UV辐射(R16)[7]和吸附[8]等,其中吸附法因具有成本低、操作方便、效率高、无有害副产物等独特优势而受到广泛关注。近年来,人们开发了多种材料作为吸附剂来提取水环境中的污染物,例如活性炭[9]、石墨烯[10]、MOFs[11]和β-环糊精基材料[12-14]。β-环糊精(β-CD)是一种生物降解产品,物美价廉,环境友好。此外,β-CD具有丰富的羟基亲水性表面和疏水性内柱腔的分子特性[15],可以有效地捕获适当大小和极性的有机分子,已发展成为一种很有前途的吸附剂[16]。然而,β-CD良好的水溶性使其难以从水溶液中分离,这限制了β-CD在水处理中的广泛应用。因此,人们努力制备高吸附容量和具备可分离性的β-CD衍生不溶体系。此外,由于磁性对外部磁场的强烈响应,一些功能部件(例如磁性Fe3O4)也被引入这些系统中,以提高其可分离性和可恢复性。基于这一思路,文献[12-13,17-18]报道了几种具有类似β-CD结构特征的磁性β-CD聚合物和含β-CD的复合材料。然而,这些复合材料通常包含多个成分,合成过程复杂,同时综合吸附剂的吸附能力有待进一步提高[19-22]。
本文采用简便可行的工艺合成了磁性粒子包埋在β-环糊精聚合物(β-CDP@Fe3O4)中的新型二元吸附剂,并考察了其对BPA的吸附性能。交联不改变原有的β-CD的空腔结构,改性后的Fe3O4被包裹在β-CDP的网状结构中,使最终的吸附剂具有磁性。由于BPA分子与β-CD腔的尺寸匹配[23-24],因此β-CDP@Fe3O4吸附剂在水溶液中对BPA表现出良好的吸附性能。
1 实验部分
1.1 实验试剂与仪器
试剂:β-环糊精(纯度为98%)、Fe3O4(纯度为99%),Aladdin试剂有限公司;双酚A(纯度为98%)、环氧氯丙烷(分析纯)、盐酸(分析纯)、NaOH(分析纯)、甲醇(分析纯)、丙酮(分析纯)、活性炭,国药集团化学试剂有限公司。
仪器:ZD-2自动电位滴定仪,上海大普仪器有限公司;S-4800扫描电子显微镜,日立高科技公司;HY-4调速多用振荡器,金坛市大地自动化仪器厂;SQP赛多利斯电子天平,北京赛多利斯科学仪器有限公司;YZ1515X-A蠕动泵,保定兰格恒流泵有限公司;84-1磁力搅拌控温电热套、DF-101S集热式恒温加热磁力搅拌器,山东鄄城华鲁电热仪器有限公司;JJ-1精密增力电动搅拌器,常州国华电器有限公司。
1.2 β-CDP@Fe3O4的合成
参照文献[25]合成β-CD。在200 mL三口瓶中依次加入23.4 g β-CD和24.0 mL质量分数为20%的NaOH溶液,在323 K的温度下搅拌至透明;向其中加入6.0 g Fe3O4,搅拌均匀后分次缓慢滴加15.6 mL环氧氯丙烷,形成凝胶后恒温2.5 h。用蒸馏水将上述研磨后的凝胶洗涤至滤液呈中性,再用100.0 mL丙酮分2次浸泡,每次浸泡10 min后抽滤;得到的产物在338 K的温度下干燥12.0 h,然后在378 K的温度下干燥2.0 h,研细过100目筛,得到β-CDP@Fe3O4,称重约28.1 g。
1.3 静态吸附实验
向含有50.0 mL质量浓度为100 mg/L的BPA标准溶液的锥形瓶中加入0.1 g β-CDP@Fe3O4,在振荡器上以一定的转速进行吸附,吸附饱和后停止振荡;使用注射器吸取5.0 mL待测液,在280 nm处进行吸光度测定。吸附率和吸附量的计算公式如下:
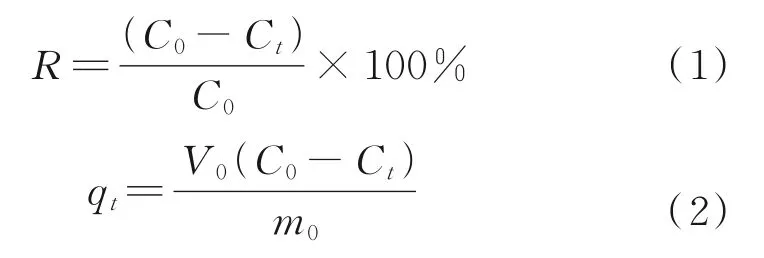
式中,R为吸附率,%;C0和Ct分别为BPA溶液初始和t时刻的质量浓度,mg/L;qt为t时刻的吸附量,mg/g;V0为BPA溶液的体积,L;m0为β-CDP@Fe3O4的质量,g。
1.4 吸附动力学模型
动力学研究了准一级、准二级以及粒子内扩散三种模型,计算公式如下:
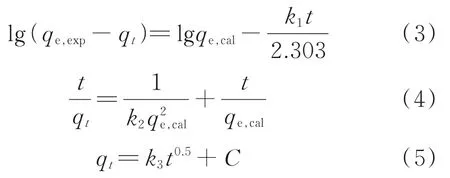
式中,qe,cal和qe,exp分别为吸附达到平衡时β-CDP@Fe3O4对BPA吸附量的计算值和实验值,mg/g;k1为准一级反应速率常数,min-1;k2为准二级反应速率常数,g/(mg·min);k3为粒子内扩散常数,mg/(g·min1/2);t为反应时间,min;C为常数,mg/g。
1.5 动态吸附实验
图1为动态吸附实验装置图。填充柱底部预先装入少量石英棉,然后将一定质量的β-CDP@Fe3O4填入。利用蠕动泵调节流量,每隔一定时间取样并测定溶液吸光度。
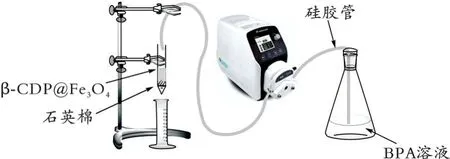
图1 动态吸附实验装置图
1.6 再生性能的考察
静态再生实验:采用磁铁聚集吸附BPA后的β-CDP@Fe3O4,倾倒溶液后,加入10.0 mL甲醇进行解吸,重复5次后直接进行吸附实验。
动态再生实验:当吸附到达饱和点后,先通入蒸馏水洗去残留在β-CDP@Fe3O4表面的BPA,随后通入甲醇解吸,最后再通入蒸馏水,当检测流出液的吸光度为0时,开始进行吸附实验。
2 结果与讨论
2.1 β-CDP@Fe3O4的表征
图2为β-CDP@Fe3O4、β-CD和环氧氯丙烷的FTIR谱图。

图2 β-CDP@Fe3O4、β-CD和环氧氯丙烷的FTIR谱图
从 图2可 以 看 出,β-CDP@Fe3O4在3 063、1 255、906、853 cm-1处未出现三元环醚的特征吸收峰,在723 cm-1处未出现C-Cl的特征吸收峰,表明β-CD和环氧氯丙烷经历了开环取代反应;β-CD和β-CDP@Fe3O4在1 030 cm-1处的吸收峰归因于腔内C-O和C-O-C的伸缩振动,2 921、2 928 cm-1处的吸收峰归因于-CH2的反对称伸缩振动,706、707 cm-1处的吸收峰归因于-CH2的面内摇摆振动,说明β-CDP@Fe3O4仍保留着β-CD原本的内部空腔结构。
将Fe3O4和β-CDP@Fe3O4吸附前后及再生后的SEM图进行对比,结果见图3。

图3 样品的SEM图
从图3可以看出,尺寸不一的多面体Fe3O4表面被黏稠物质覆盖,说明Fe3O4被嵌入到β-CD与环氧氯丙烷聚合后的空间网状结构中,但Fe3O4中的孔隙仍大量存在。Fe3O4和β-CDP@Fe3O4的BET比表面积分别为35.3 m2/g和29.5 m2/g,也进一步证明了上述分析。通过对比β-CDP@Fe3O4吸附前后和再生后的SEM图可以看出,饱和吸附后β-CDP@Fe3O4的孔隙和外表面几乎被BPA完全覆盖,再生后又现出了β-CDP@Fe3O4的表面形貌,同时出现了一些孔隙。
2.2 β-CDP@Fe3O4吸附BPA的静态吸附实验
2.2.1 单因素考察 分别考察了吸附时间、pH、吸附剂质量和BPA初始质量浓度对吸附性能的影响,结果见图4。吸附条件:(a)pH=5.6,V0=50.0 mL,C0=100 mg/L,m0=0.10 g;(b)m0=0.10 g,C0=100 mg/L,V0=50.0 mL,t=120 min;(c)pH=5.6,C0=100 mg/L,V0=50.0 mL,t=120 min;(d)pH=5.6,V0=50.0 mL,m0=0.10 g,t=120 min。
从图4(a)可以看出,当吸附时间为10 min时,β-CDP@Fe3O4对BPA的吸附率已达到80%左右;吸附时间大于10 min时,吸附率变化缓慢。其原因是:吸附开始时,β-CDP@Fe3O4表面存在大量的吸附位点,BPA分子可以快速吸附到这些位点上;随着吸附的进行,吸附位点变少,BPA分子要克服空间位阻寻找剩余吸附位点,因此吸附速率变缓[26]。当吸 附 时 间为100 min时,β-CDP@Fe3O4表面的吸附位点几乎全部被占用,基本达到平衡状态。因此,为了确保充分吸附,将吸附时间设为120 min。
从图4(b)可以看出,当pH从2增加至8时,吸附剂的吸附性能没有明显变化;当pH从8增加至10时,吸附率略微下降;当pH继续增加至12时,吸附率急剧下降。其原因是:β-CDP@Fe3O4对BPA的吸附作用主要是氢键和疏水作用,在较低pH条件下氢键易于形成,而BPA的酸度系数(pKa)为9.7[27],较 高 的pH促 进BPA发 生 电 离,此 时 氢 键难于形成,从而导致吸附性能下降。
从图4(c)可以看出,随着吸附剂质量的增加,吸附率逐渐增大,吸附量持续减少。这是因为增加β-CDP@Fe3O4用量使吸附位点增加,而BPA质量浓度是一定的,所以吸附率增加。但是,如果吸附剂质量过大,则剩余大量吸附位点。为充分利用吸附剂,选择其质量为0.10 g,此时吸附率和吸附量分别为91.3%和45.600 mg/g。
从图4(d)可以看出,随着BPA初始质量浓度增加,吸附量呈逐渐增加的趋势;当BPA初始质量浓度为350 mg/L时,吸附量达到最大值(113.600 mg/g)。这是因为:当BPA初始质量浓度较小时,β-CDP@Fe3O4的吸附位点未被完全占据就已达到吸附平衡,当BPA初始质量浓度增大时,吸附位点不足,吸附率降低。由于吸附率超过90%即可认为吸附饱和,而BPA初始质量浓度为40~100 mg/L时,吸附率基本不变,结合吸附剂利用率和经济效益,选取BPA初始质量浓度为100 mg/L作为实验的最优质量浓度。

图4 吸附时间、pH、吸附剂质量和BPA初始质量浓度对吸附性能的影响
2.2.2 吸附动力学 表1为β-CDP@Fe3O4吸附BPA的三种动力学模型常数及相关系数。由表1可知,三种浓度下的准二级动力学模型的相关系数均大于0.999 0,且平衡时对BPA吸附量的计算值更接近实验值,说明BPA在β-CDP@Fe3O4表面的吸附过程符合准二级动力学模型,化学吸附是速率控制步骤;粒子内扩散模型的参数值较低,表明BPA的吸附主要发生在β-CDP@Fe3O4表面。
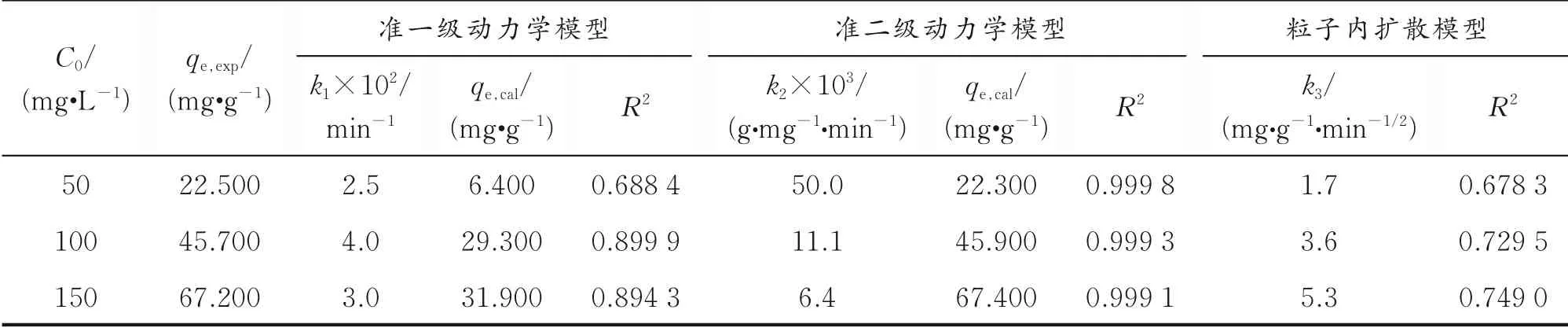
表1 β-CDP@Fe3O4吸附BPA的三种动力学模型常数及相关系数
2.3 β-CDP@Fe3O4吸附BPA的动态吸附实验
2.3.1 动态吸附性能考察 图5为液时空速和BPA初始质量浓度对β-CDP@Fe3O4动态吸附性能的影响。Ct/C0=0.1为穿透点,流出液Ct/C0=0.9为饱和点[28]。从图5(a)可以看出,随着液时空速从20 h-1增加到72 h-1,穿透时间变短,穿透曲线向左移动并变陡。根据吸附传质原理,传质系数随液时空速的增加而增加,导致β-CDP@Fe3O4表面传质阻力减小,BPA与其接触时间缩短,从而导致吸附饱和时间和穿透时间变短[29]。从图5(b)可以看出,随着BPA初始质量浓度的增加,穿透时间和饱和时间变短,曲线变陡,这是由于随着BPA初始质量浓度增加,BPA从液相主体扩散到固-液界面的传质驱动力变大,导致吸附带缩短,穿透点提前[30]。
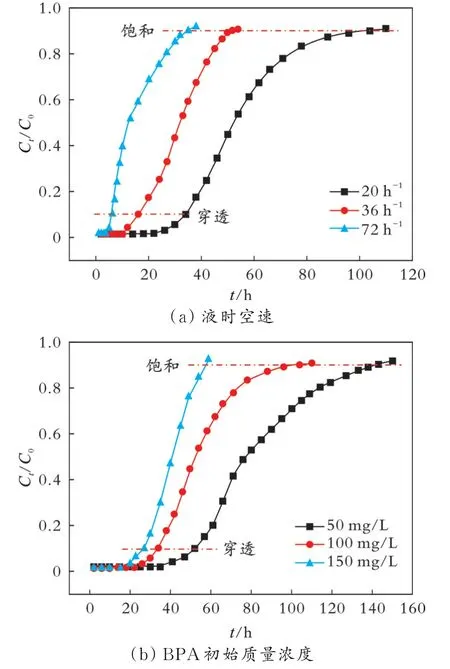
图5 液时空速和BPA初始质量浓度对β-CDP@Fe3O4动态吸附性能的影响
2.3.2 Thomas模 型 拟合 Thomas模 型通常假设在动态吸附过程中存在平推流作用[31],是动态吸附穿透曲线的常见模型之一,其对数表达式见式(6)。
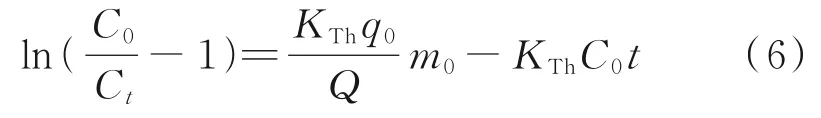
式 中,KTh为β-CDP@Fe3O4吸 附BPA的Thomas模型常数,mL/(mg·h);q0为饱和吸附量,mg/g;Q为体积流量,mL/min。
通过线性拟合得到了Thomas模型及其参数,结果见图6和表2。
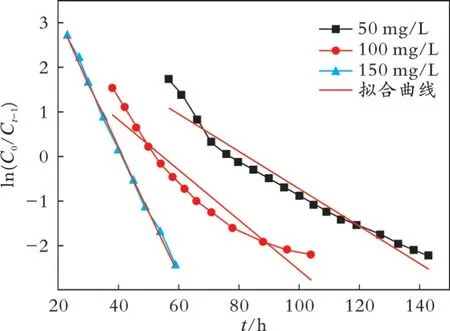
图6 β-CDP@Fe3O4吸附BPA的Thomas模型
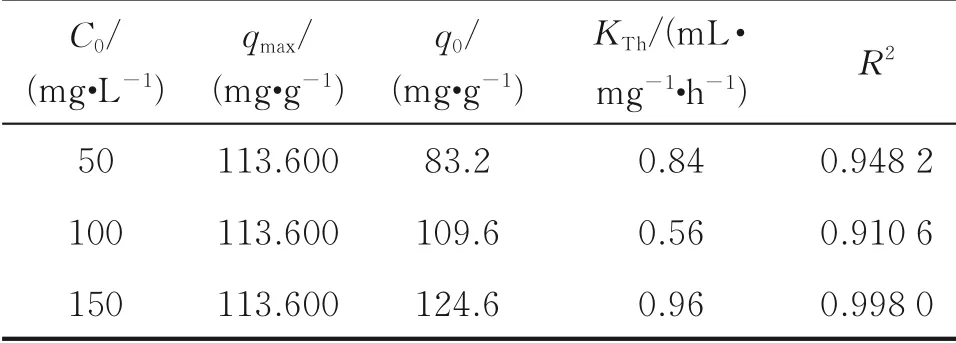
表2 β-CDP@Fe3O4吸附BPA的Thomas模型参数
从图6和表2可以看出,拟合得到的不同条件下的饱和吸附量与实验测得结果(113.600 mg/g)相近,不同操作条件下Thomas模型拟合的相关系数R2均大于0.9,表明该模型能够描述BPA在β-CDP@Fe3O4上的吸附过程。
2.4 β-CDP@Fe3O4的再生性能考察
对β-CDP@Fe3O4的再生性能进行了静态和动态实验研究,结果见图7。静态实验条件:BPA初始质量浓度为100 mg/L,吸附剂质量为0.10 g,BPA溶液体积为50.0 mL,吸附时间为120 min。从图7(a)可以看出,初始吸附率为91.3%,经过6次吸附-解吸循环,吸附率始终稳定在93.4%~95.3%,表明β-CDP@Fe3O4具有很好的再生性能。动态实验条件:液时空速为20 h-1,间隔2 h取样一次。从图7(b)可以看出,经过4次吸附-解吸循环,穿透时间分别为34.0、29.0、30.0、32.0 h,由于取样间隔时间为2.0 h,可以认为4次吸附结果基本一致,进一步证实了β-CDP@Fe3O4优异的再生性能。
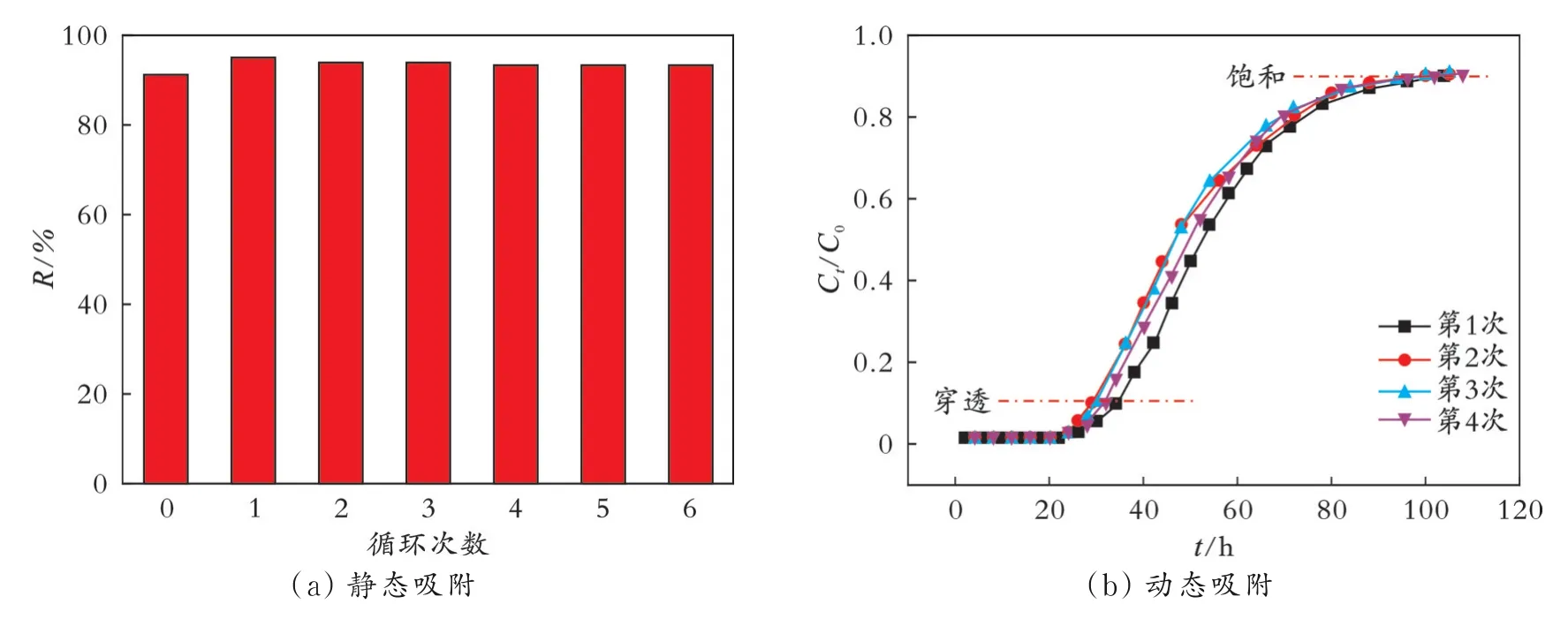
图7 β-CDP@Fe3O4静态和动态吸附BPA的再生性能
2.5 吸附机理
β-CD是一种具有圆台结构的环状寡糖[32],窄口端有7个伯羟基,宽口端有14个仲羟基,它能与大小和极性相似的分子以氢键、疏水作用相结合形成主客体包合物进行吸附[33]。β-CD与环氧氯丙烷的聚合主要是羟基和环氧自由基的取代。羟基使环氧基团开环,然后去除HCl重新形成环氧基团,在碱性介质中水解后与β-CD和环氧氯丙烷分别多次反应,最终得到具有空间网状结构的β-CDP,并将Fe3O4包覆在内。根据Material studio模拟,BPA的分子旋转直径为0.642 nm,而β-CD宽边内径为0.780 nm[23]。因 此,BPA分 子 很 容 易 进 入β-CDP@Fe3O4的内腔而被包合。结合吸附动力学结果,β-CDP@Fe3O4对BPA的吸附过程可分为3个阶段,如图8所示。首先,BPA与β-CDP@Fe3O4宽口侧仲羟基结合,通过氢键快速附着在吸附剂表面;其次,由于疏水效应扩散到内腔并形成包合物;最后,当吸附达到饱和时,系统进入动态平衡状态,即膜扩散、层间扩散和动态平衡3个阶段。
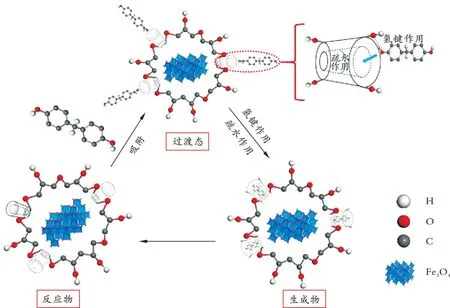
图8 β-CDP@Fe3O4对BPA的吸附机理
2.6 β-CDP@Fe3O4与其他吸附剂对BPA吸附的对比
表3为β-CDP@Fe3O4与其他吸附剂对BPA吸附性能对比结果。由表3可知,与其他吸附剂相比,β-CDP@Fe3O4具有良好的竞争力,其主要表现为吸附量大,再生性能好。
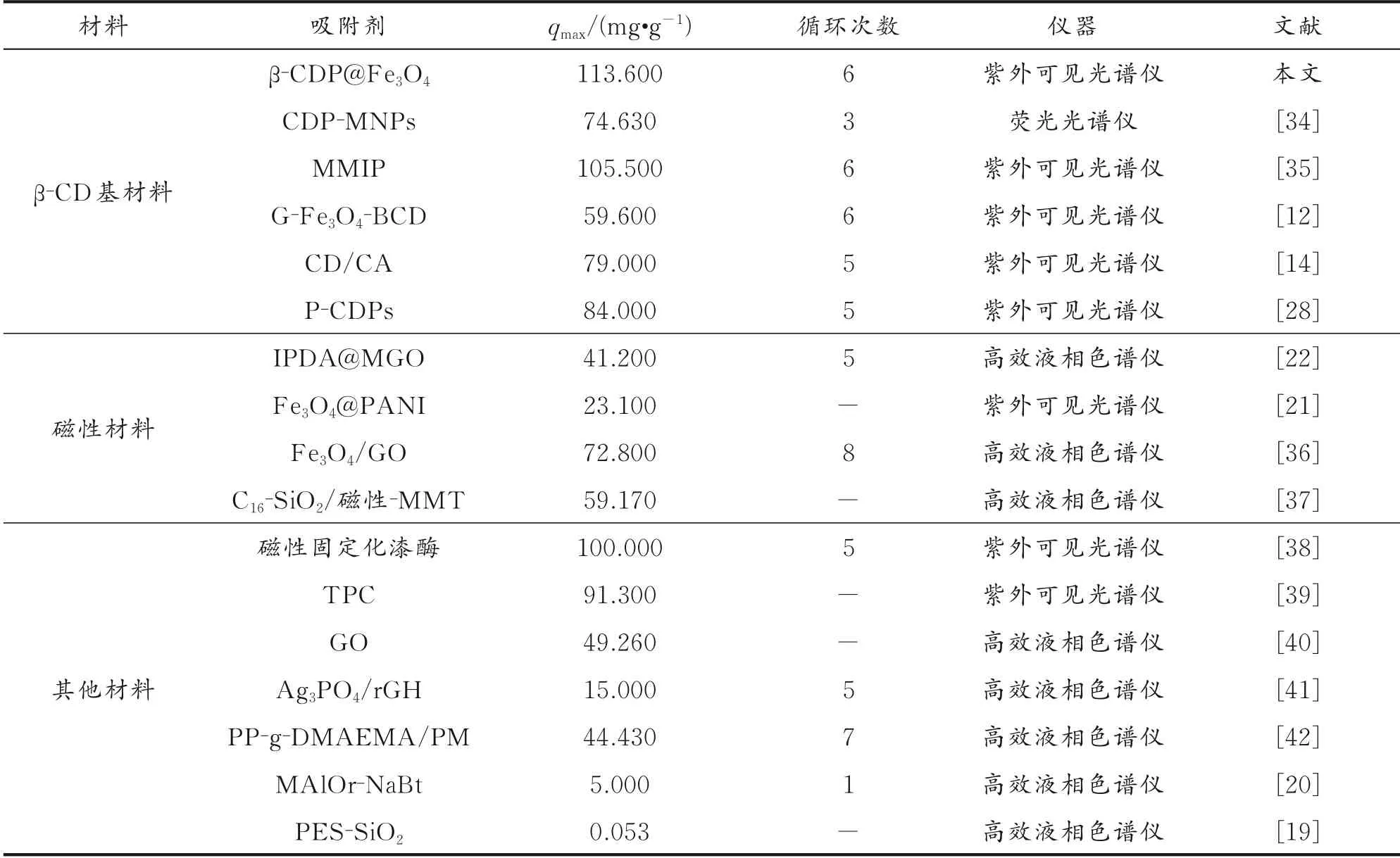
表3 β-CDP@Fe3O4与其他吸附剂对BPA吸附性能对比结果
3 结论
(1)将合成的β-CDP@Fe3O4用于吸附水溶液中的BPA,在液时空速为20 h-1的条件下吸附100 mg/L BPA,穿透时间和饱和时间分别为34 h和104 h,平衡吸附量109.600 mg/g,接近静态实验的最大吸附量113.600 mg/g;动态吸附过程符合Thomas模型。
(2)β-CDP@Fe3O4吸附BPA的机理表明,吸附过程主要发生在吸附剂表面,在膜扩散阶段形成氢键,反应速度快;疏水作用影响层间的扩散,从而控制整个吸附过程的吸附速率;pH(pH≥8)对吸附性能的影响表现为BPA的电离破坏氢键的形成。
(3)β-CDP@Fe3O4吸附BPA的实验结果表明,β-CDP@Fe3O4具有良好的再生性能,可重复使用且绿色环保。

