卡瑞利珠单抗致牙龈及唇化脓性肉芽肿1例报道及文献回顾
李蕴喆, 卜令学, 庞宝兴, 王烨, 刘风芝, 杨楠, 陈晨, 王双义
1.青岛大学附属医院口腔医学中心,青岛大学口腔医学院,青岛市口腔数字医学与3D打印工程实验室,山东 青岛(266003); 2.青岛大学附属医院病理科,山东 青岛(266003)
免疫治疗是目前最受关注的肿瘤治疗方法之一,在多种实体恶性肿瘤中有显著疗效。卡瑞利珠单抗(SHR-1210)是目前常用的国产程序性细胞死亡受体-1(programmed cell death-1,PD-1)抑制剂,其最常见的免疫相关不良事件是反应性毛细血管增生症(reactive capillary hemangiomas,RCH),主要发生在头部、面部和躯干的皮肤表面,但发生于口腔黏膜的不良反应少有报道。本文报道1 例应用卡瑞利珠单抗治疗肝癌的患者,治疗期间除发生全身皮肤的反应性毛细血管增生外,下唇及牙龈黏膜出现了化脓性肉芽肿病变,并对相关文献进行复习,以期为临床提供参考。
1 临床资料
1.1 病史及检查
患者,女,62 岁,1 个月前发现上颌牙龈肿物,约“蚕豆”大小,下唇肿物约“黄豆”大小,无疼痛、易出血,自行涂抹中药粉剂,具体成分及用量不详,无效果。肿物生长迅速,影响进食,于2021 年12 月14 日来本院口腔颌面外科就诊。该患者肝癌病史5 年,行经导管肝动脉化疗栓塞术治疗8 次后,于6 个月前开始应用卡瑞利珠单抗(生产批号:S20190027,苏州盛迪亚生物有限医药有限公司,中国),用法为200 mg 静脉注射,3 周1 次,同时口服瑞戈非尼(患者自行国外代购碧康制药股份有限公司药品,产地:孟加拉国),160 mg/d。2 个月前患者发现腹部皮肤有多个“红斑”,迅速突起于皮肤表面,遍及全身皮肤。
查体:全身多发肿物(图1),呈紫红色,大小不一,部分肿物表面破溃。上颌腭侧牙龈及下唇多发肿物(图2)。左上颌前牙区腭侧牙龈肿物(图2a)约2.0 cm × 1.0 cm × 1.0 cm,质韧,有蒂,触之易出血。下唇多个肿物,约0.5 cm× 0.5 cm× 0.5 cm,圆形,表面破溃、结痂(图2b),口腔卫生状况一般,部分龈缘充血。21~23 牙齿无明显松动。
1.2 牙龈及唇化脓性肉芽肿治疗及随访结果
牙周基础治疗后,给予聚维酮碘漱口液漱口,口服抗生素,经患者同意后在局麻下行左上颌前牙区腭侧牙龈肿物(图2c)及下唇肿物(图2d)切除术,牙周支持治疗。术后病理诊断:左上颌前牙区腭侧牙龈肿物为化脓性肉芽肿/肉芽肿型血管瘤,下唇为化脓性肉芽肿/肉芽肿型血管瘤伴灶性出血坏死。病理检查显示:病变由纤维性间隔分隔,呈分叶状。由增生的内皮细胞构成的小叶组成,小叶内含较小、多少不一的血管腔隙,内皮细胞呈多边形或短梭形,细胞界限不清。表皮形成围领状,部分包绕病变。间质水肿,富于炎细胞。表皮呈化脓性改变(图3)。
术后2 个月复诊,左上颌前牙区腭侧牙龈肿物切除术后愈合较好,牙龈颜色、质地正常(图2e);下唇愈合良好(图2f)。但因全身皮肤病变的不断形成,患者心理难以承受,与其肿瘤科医生沟通后,已停止免疫治疗2 个月,目前仅使用瑞戈非尼靶向药物,患者口内未发现新生肿物,全身皮肤肿物也有所减少。
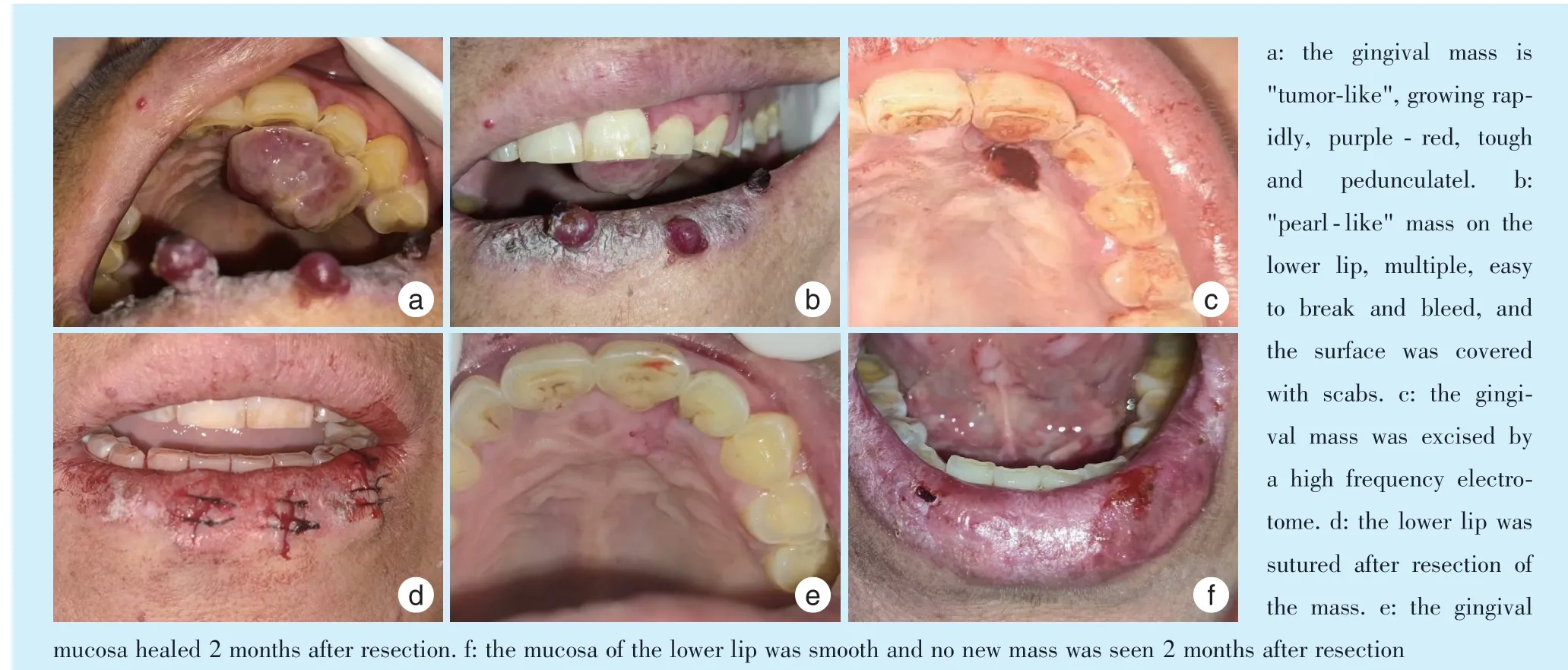
Figure 2 A patient with hepatocellular carcinoma developed pyogenic granulomatous lesions in the mouth after 4 months of camrelizumab administration图2 肝癌患者使用卡瑞利珠单抗4 个月后口腔出现化脓性肉芽肿性病变
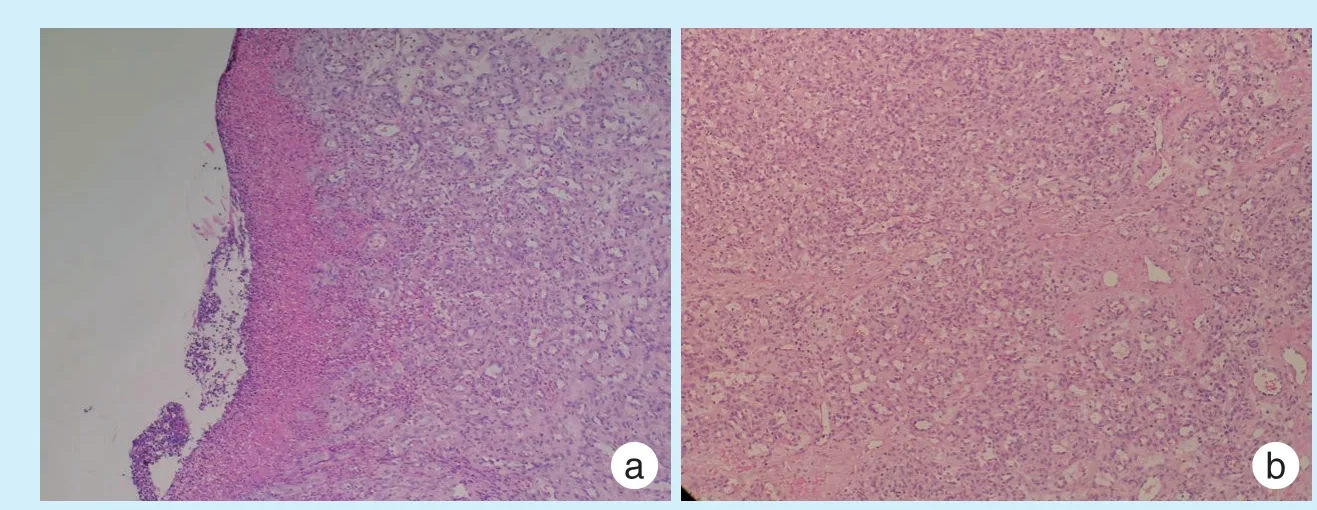
Figure 3 Histopathological findings of the lower lip and gingiva biopsies图3 下唇及牙龈化脓性肉芽肿活检组织病理学观察
2 讨 论
肿瘤可诱导T 淋巴细胞和B 淋巴细胞等免疫细胞表面PD-1 信号传导[1-2],同时肿瘤细胞过度表达其配体(主要是PD-L1)[3],二者结合后引起免疫抑制[4],进而利于肿瘤细胞的生长和繁殖。免疫治疗是指恢复免疫系统和肿瘤细胞之间的平衡,主要包括单克隆抗体类免疫检查点抑制剂(immune checkpoint inhibitor,ICIs)、治疗性抗体、癌症疫苗、细胞治疗[5]。免疫检查点抑制剂与细胞毒性或靶向药物的抗肿瘤机制不同,其通过阻断负调节因子来激活内源性免疫细胞以杀死肿瘤细胞[6-7]。PD-1 和PD-L1 通路的免疫检查点阻断已成为乙肝病毒导致的晚期肝细胞癌(hepatocellular carcinoma,HCC)、肺癌、黑色素瘤、肾细胞癌、头颈部鳞状细胞癌等癌症中最具潜力的治疗策略之一[1,8-10]。2019 年5 月31 日,经国家药品监督管理局批准,我国自主研发的PD-1 抑制剂卡瑞利珠单抗(SHR-1210,Camrelizumab,艾瑞卡)获批上市。该药物可用于多种恶性肿瘤的治疗,包括肝癌、食管鳞癌、胃/胃食管交界处癌、鼻咽癌、霍奇金淋巴瘤、B 细胞淋巴瘤和非鳞状、非小细胞肺癌[11-12]。
随着卡瑞利珠单抗应用越来越多,临床上发现RCH 是其最常见特殊不良反应,并且仅在接受卡瑞利珠单抗治疗的患者中发现[6],主要发生在头部、面部和躯干的皮肤上,皮肤RCH 的发病率约为80%[13-15],仅在少数情况下,可并发其他部位的RCH[16],发生于口腔甚少。Wang 等[16]报道全国范围内的多中心2 期卡瑞利珠单抗治疗晚期肝癌试验,217 例受试者中RCH 在口腔中的发生率为1.4%(口腔黏膜2 例,牙龈1 例),按形态可分为“红痣样”、“珍珠样”、“桑椹样”、“斑块样”、“瘤样”。本研究报道病例中,肿物组织病理学改变均表现为化脓性肉芽肿/肉芽肿型血管瘤,通过检索相关文献,目前未见报道。单纯的口腔化脓性肉芽肿发病机制涉及多种因素,但确切原因尚不清楚,目前认为损伤可能导致促血管生成因子和抗血管生成因子失衡,轻微创伤引起的反应性肉芽组织可能是促成因素,其他可能的诱发因素包括感染和先前存在的血管畸形[17]。因此考虑:口腔黏膜的RCH 容易因进食受到损伤,合并细菌感染,致使患者口腔RCH 在细菌感染的基础上发生化脓性肉芽肿性病理变化。本研究未进行肿物细菌、真菌的感染监测及皮肤肿物活检,未来仍需针对RCH 的病理特征进一步研究分析。
目前RCH 的病因尚未明确,Finlay 等[18]通过实验发现卡瑞利珠单抗(SHR-1210)是人类血管内皮生长因子受体2(vascular endothelial growth factor receptor 2,VEGFR2)的有效激动剂,可能通过激活血管内皮细胞使其增殖为血管瘤。也有研究认为卡瑞利珠单抗可能与皮肤中的PD-1 表达细胞靶向结合,而这些细胞又可能通过释放趋化因子产生VEGF[19]。在一项对晚期原发性肝癌、胃癌和胃食管交界癌的1 期研究中,卡瑞利珠单抗联合阿帕替尼治疗的患者反应性皮肤毛细血管增生症(reactive cutaneous capillary endothelial proliferation,RCCEP)发生率为12.1%(4/33)[20]。阿帕替尼是抗肿瘤血管生成的药物,是VEGFR2 的受体拮抗剂[21],可能有抑制卡瑞利珠单抗与VEGFR2 结合的作用[22],卡瑞利珠单抗联合阿帕替尼治疗可降低RCH的发生率[23-24]。抗血管生成类药物与PD-1/PD-L1有协同作用[25-26]。该例患者在使用卡瑞利珠单抗治疗的同时,一直使用与阿帕替尼同类型的VEGFR抑制剂瑞戈非尼,其对各种促血管生成受体的抑制作用较强[27],但该患者RCH 症状并未减轻,有待深入探索其发生机制。另据报道,在以铂类为基础的化疗中添加抗PD-1/PD-L1 药物临床疗效较好,并且不会导致治疗非小细胞肺癌和小细胞肺癌的意外毒性[28],可能需要进一步大样本随机对照研究为临床提供循证医学证据。Wang 等[29]通过系统性回顾及分析发现在任何级别的不良事件中,联合使用卡瑞利珠单抗的安全性优于单用。
RCH 大多数不需要治疗,停药后多可自行消退[13]。最近有研究发现沙利度胺对于RCH 的预防可能有效[30]。本例患者牙龈及下唇RCH 发生肉芽肿性病变,生长迅速,影响进食及口腔功能,应首选手术切除。术后复诊,牙龈及下唇均已愈合,术前进行对应牙齿的洁治可有效防止病变的复发,因此建议在免疫治疗前进行口腔检查,去除口腔黏膜的炎性刺激因素并定期进行口腔卫生维护治疗。
【Author contributions】 Li YZ collected the data and wrote the article. Wang SY, Bu LX, Pang BX revised the article. Liu FZ, Yang N,Chen C were responsible for data collection. Wang Y was responsible for the pathological analysis.

