新型冠状病毒感染者器官捐献专家共识
中华医学会器官移植学分会 中国医师协会器官移植医师分会 国家人体捐献器官获取质量控制中心
自2019年12月以来,新型冠状病毒(新冠病毒)感染大流行对全球经济社会带来非常严重的影响,改变了医疗卫生的工作格局[1]。疫情传播、防控和新冠病毒从捐献者传播到受者的潜在风险及其不确定性等,给器官捐献和移植工作带来严重影响和巨大挑战[1-3]。
越来越多的证据表明使用来自新冠病毒感染捐献者的非肺脏器官(肾脏、肝脏和心脏等)似乎是一种安全的做法,无论在获取时是否存在症状,传播的风险都很低[3-5]。目前暂无新冠病毒通过血液传播和捐献器官通过移植传播的直接证据[3-4,6]。为应对新冠病毒感染疫情形势的变化,积极推进器官捐献和移植工作依法依规科学规范开展,最大限度满足终末期器官衰竭患者移植需求,保障人民健康,在国家卫生健康委员会医疗应急司的指导下,中华医学会器官移植学分会组织相关专家,结合我国新冠病毒感染流行形势及器官捐献和移植工作的临床实践,参考国内外相关研究结果及临床研究证据[3-4,7-8],制定了公民逝世后器官捐献《新型冠状病毒感染者器官捐献专家共识》,旨在为新冠病毒感染者捐献器官的获取和应用提供建议,供器官捐献和移植工作者参考。由于有限的证据,共识尚存在不完善之处,随着对于新冠病毒感染认识的不断深入,捐献与移植工作经验的积累及时修订和完善。
1 我国新冠病毒感染防控及捐献器官分配的相关政策
国务院应对新冠病毒感染疫情联防联控机制(简称国务院联防机制)2022年11月11日下发的《关于进一步优化新冠肺炎疫情防控措施科学精准做好防控工作的通知》(“二十条”)[9]和2022年12月7日下发《关于进一步优化落实新冠肺炎疫情防控措施的通知》(“新十条”)[10],对疫情防控政策做出科学调整,新冠病毒感染防控进入新阶段。2022年12月26日国家卫生健康委员会下发“公告”将“新型冠状病毒肺炎”更名为“新型冠状病毒感染”[11],国务院联防机制综合组下发《关于对新型冠状病毒感染实施“乙类乙管”的总体方案》[12],将新冠病毒感染纳入传染病“乙类乙管”。面对新冠病毒感染继续流行,社会人群中普遍存在新冠病毒感染者,推迟新冠病毒抗原或核酸检测阳性者逝世后的器官捐献时间,待病毒检测阴性后再行捐献,将导致相当数量医学上适合移植的器官丢失[1-4]。目前,中国人体器官分配与共享计算机系统(China Organ Transplant Response System,COTRS)要求器官获取组织(Organ Procurement Organization,OPO)在捐献器官分配前上传新冠病毒抗原或核酸检测结果,阳性的捐献者器官分配不受限制。
2 捐献者感染新冠病毒的临床特点
2.1 新冠病毒的流行特点
2019年12月,新冠病毒开始在全球流行,其在人群中流行和传播过程中基因频繁发生突变。截止至2022年底,世界卫生组织提出的“关切的变异株”有5个,分别为阿尔法(Alpha,B.1.1.7)、贝塔(Beta,B.1.351)、伽玛(Gamma,P.1)、德尔塔(Delta,B.1.617.2)和奥密克戎(Omicron,B.1.1.529)。奥密克戎2021年11月开始在人群中出现,相比德尔塔等其他变异株,其传播力和免疫逃逸能力显著增强,在2022年初迅速取代德尔塔成为全球绝对优势流行株。随着新冠病毒在全球的持续传播,新的奥密克戎亚分支将会持续出现。全球数个月以来流行的奥密克戎变异株主要为BA.5.2,但2022年10月份以来免疫逃逸能力和传播力更强的BF.7、BQ.1和BQ.1.1等亚分支及重组变异株XBB的传播优势迅速增加,在部分国家和地区已经取代BA.5.2成为优势流行株[13]。个体在感染BA.5.2或BF.7后产生的中和抗体,在短期内(3个月)会维持相对较高水平,预期对其他奥密克戎变异株分支(包括XBB)有较好的交叉保护作用[14-15]。中国疾病预防控制中心2023年1月4日发布信息显示,我国目前本土流行的新冠病毒绝对优势毒株是BA.5.2和BF.7,也已监测到BF.7、BQ.1、XBB传入,但BQ.1和XBB在我国尚未形成优势传播,2022年10月至12月,报告发现本土XBB病例16例,全部为XBB.1进化分支,主要集中在10月至11月,12月仅1例,我国短期内由XBB系列变异株包括XBB.1.5引发大规模流行的可能性低[16]。目前,未见任何国家报道XBB.1.5致病力增加,无感染者住院比例和病死比例增加的报道,也未见其引起的临床症状与其他奥密克戎变异株的差异[16]。奥密克戎变异株平均潜伏期缩短,多为2~4 d[13,17]。新冠病毒变异株的传播途径和对人体的损害机制相同,主要传播途径包括经呼吸道飞沫和密切接触传播,在相对封闭的环境中经气溶胶传播,接触被病毒污染的物品后也可造成感染,国内外证据显示奥密克戎变异株肺部致病力明显减弱,临床表现已由肺炎为主衍变为以上呼吸道感染为主[13,18]。
2.2 捐献者感染新冠病毒的临床特点
2.2.1 新冠病毒感染捐献者的定义 在新冠病毒感染之日起14 d内,上呼吸道或下呼吸道的新冠病毒抗原或核酸检测结果呈阳性为新冠病毒感染者,有不可逆脑损伤或符合器官捐献医学标准的循环衰竭者死亡后器官捐献被定义为新冠病毒感染捐献者[8],根据国家《新型冠状病毒肺炎诊疗方案(试行第九版)》[19],核酸检测循环阈值(cycle threshold,Ct)值≥35时感染者的传染性很小,不再视为阳性。国际上多项研究已将Ct值≥30时视为低病毒载量,Ct值<30时高病毒载量[20-21]。新冠病毒抗原或核酸检测结果为阴性的捐献者被定义为新冠病毒阴性捐献者。
2.2.2 新冠病毒感染捐献者的临床特点、诊断和临床分型 新冠病毒感染捐献者指具有明确的原发性不可逆的严重脑损伤(如创伤性脑损伤、蛛网膜下腔或颅内出血、心肺复苏后缺血缺氧性脑病、中枢神经系统肿瘤等)、使用机械通气、深度昏迷等情况下合并新冠病毒感染,其临床特点不典型,与普通人群感染相比存在诸多不同之处,且其主观症状无法获取,不可逆性脑损伤及可能合并其他肺部感染对呼吸功能等的影响,给临床诊断带来了困难[22]。目前主要是根据实验室检查(鼻咽拭子、肺泡灌洗液抗原、核酸或二代测序)、流行病学史、临床表现等综合分析进行诊断,多采用鼻咽拭子抗原或核酸检测及肺部影像学诊断。确诊病例的诊断标准参照《新型冠状病毒感染诊疗方案(试行第十版)》,新冠病毒感染捐献者主要根据临床表现、影像学特征等分为轻型、中型、重型和危重型[13]。在有条件的情况下,新冠病毒感染捐献者可进行肺泡灌洗液、血以及器官保存液的新冠病毒二代测序,了解血液及器官中是否存在新冠病毒,指导对捐献者新冠病毒感染的评估和选择、移植受者选择和移植术后管理。
2.2.3 新冠病毒感染对可捐献器官的影响 目前已确定血管紧张素转换酶(angiotensin converting enzyme,ACE)-2为新冠病毒的主要作用受体,其广泛分布于全身各个器官,包括肠道、心脏、肾脏、胰腺、肝脏、肌肉和神经系统[23-24]。尽管新冠病毒主要影响呼吸系统,但现有研究资料多为重型、危重型和死亡病例的研究表明重症新冠病毒感染可影响多个器官[1,18,23-25]。研究发现无论是由病毒直接作用还是感染后的炎症所致,重型、危重型新冠病毒感染者的一个主要特征是脉管系统受到损害,由此导致的血管功能障碍(内皮病变)可引起凝血,影响人体的各种器官,导致其发生损伤甚至功能障碍[23-24,26]。新冠病毒感染后的器官损害可能多为重型或危重型的炎症反应风暴因子所致,此类患者作为器官捐献者时应慎重。
2.2.3.1 肾 脏 有研究结果证实新冠病毒感染重症病程中肾脏是最易受到累及的器官之一,肾脏损害和损害程度与新冠病毒感染的重症程度相关,约28%的新冠病毒感染住院患者被诊断为急性肾损伤(acute kidney injury,AKI),9%接受肾脏替代治疗,但目前对于新冠病毒是否直接感染肾脏并在肾脏中复制尚存在争议[27]。Braun等[28]研究发现60%的患者尸检后发现新冠病毒在肾脏中积累,且新冠病毒与患者生存时间缩短有关。Diao等[29]对6例死亡患者肾脏活组织检查(活检),免疫组织化学(免疫组化)染色发现6个样本的肾组织中都存在新冠病毒NP和S抗原,且与ACE-2明显共表达。但Golmai等[30]对12例新冠病毒感染伴有2期或3期AKI患者进行了肾脏限制性尸检,通过透射电镜观察未发现符合新冠病毒形态描述的明确病毒颗粒,免疫组化染色也未发现新冠病毒,但发现网络蛋白包被的囊泡与病毒颗粒非常相似,直径<20 nm至<500 nm。Sharma等[31]也进行了10例肾脏活检免疫组化染色,但均未发现新冠病毒颗粒。有研究显示尿液中很少检测到新冠病毒,即使尿液中检测到的新冠病毒,其水平也与肾损伤程度无关[32-33]。这些证据均表明在轻型和普通型新冠病毒感染患者中,新冠病毒基本上在肾脏中不表达,在重症或死亡患者的肾脏中可以检测到新冠病毒的表达。
2.2.3.2 肝 脏 新冠病毒感染相关肝损伤的发生率为10.5%~69.0%,不同地区差异较大[34]。中国最大的队列研究包括1 099例新冠病毒感染患者,其中21.3%的患者丙氨酸转氨酶(alanine aminotransferase,ALT)升高,22.2%的患者天冬氨酸转氨酶(aspartate aminotransferase,AST)升高,10.5%的患者胆红素异常[35]。国外迄今为止发表的最大规模的研究报告(包括5 700例新冠病毒感染患者),发现患者的AST和ALT均普遍升高,比例分别为58.4%和39.0%[36]。大多数研究最初认为新冠病毒不太可能感染肝脏,因为ACE-2在肝细胞中的表达较低。该结论与初始的尸检研究结果一致,这些研究均表明新冠病毒一般不会直接累及肝脏[37]。但近来有研究表明ACE-2在胆管细胞中的表达与肺泡2型细胞中的表达相当[38]。Wang等[39]研究证实重症感染者新冠病毒可以直接感染肝细胞,可能是通过替代的ACE-2外受体感染肝细胞,引起明显的细胞病变。这些均为新冠病毒抗原或核酸阳性捐献者捐献肝脏增加了不确定性。Bloom等[40]随访了60例新冠病毒感染住院患者,其中有41例(69.0%)患者在入院时至少有一项肝脏生化指标异常,在治疗过程中,54例(93%)患者的转氨酶高于正常值,但碱性磷酸酶和总胆红素升高较少见。新冠病毒感染合并肝损伤多表现为ALT、AST升高,AST异常更常见,而γ-谷氨酰转移酶及总胆红素升高则较少见。新冠病毒感染合并的肝损伤常发生于重症、男性及有基础肝病的患者中,一项美国多中心研究表明,在新冠病毒感染患者中,有基础肝病者AST异常的比例是无肝病者的3倍,同时,其他指标如γ-谷氨酰转移酶升高在有基础肝病的患者中更为常见,提示有基础肝病(慢性乙型病毒性肝炎、酒精性肝病或非酒精性脂肪性肝病)的患者比无基础肝病的患者更有可能出现肝功能异常[41]。新冠病毒感染重症患者肝功能异常的发生率高于非重症患者,在既往没有肝病的情况下,肝衰竭几乎不会发生,表明新冠病毒感染患者中肝脏受累可能与新冠病毒感染疾病的总体严重程度相关。
2.2.3.3 心 脏 研究发现心脏是新冠病毒感染病程中最易受到累及的器官之一。但其具体机制尚不明确,一方面可能与病毒侵袭心肌细胞有关,另一方面可能与新冠病毒感染导致的全身炎症反应相关[42]。Lindner等[43]分析了39例尸检患者的心脏组织,其中24例检测出新冠病毒,16例病毒载量超过1 000 copies/μg RNA。近期一项关于新冠病毒感染患者的尸检结果的报道显示,新冠病毒感染可导致局部心肌形态不规则、细胞质变暗,以及不同程度的局灶性水肿、间质纤维化和心肌肥厚,但心内膜和心肌不存在炎症细胞浸润,这些变化不足以解释为急性心肌损伤,可能为患者潜在疾病相关的预存病变,如高血压相关的心肌肥厚和过去的缺血性损伤[44]。Wu等[45]研究表明新冠病毒感染患者的肺和心脏组织中都存在大量的炎症浸润物,提示新冠病毒感染肺部的同时可能会引起心肌细胞的炎症反应,有心血管病史的患者更容易发生由新冠病毒感染引起的心肌损伤,尽管没有证据表明这类患者心肌损伤完全是由冠状动脉事件引起的,但不能排除潜在的危险因素使这类患者更容易遭受低氧和细胞因子风暴诱发心肌损伤的可能性;此外,尸检结果显示有轻微的心包积液,浅黄色透明液体和轻度心外膜水肿,进一步提示心包炎症反应可能是新冠病毒感染患者心肌功能障碍的原因之一。在另一项研究中,Xu等[46]在尸检组织病理学中未发现心肌损伤的证据,仅在肺部找到少量间质单核炎症细胞浸润,而心脏组织没有实质性损害。得出这种矛盾的结果可能与研究样本量有关。有研究发现56 963例住院新冠病毒感染患者中仅112例明确或可疑心肌炎,0.24%确诊心肌炎,0.41%疑似心肌炎,心肌炎发生率不足1%,因此认为不能因为不足1%的心肌炎发生率放弃心脏捐献[47]。总体而言,需要进一步收集更多具有明确心肌损伤病例,以进一步研究新冠病毒感染相关心肌损伤的组织病理学特征。目前尚未有轻型和中型病例心脏损伤组织学证据和通过移植心脏导致新冠病毒传播的病例报道。
总之,迄今为止,除肺部以外的大部分器官被新冠病毒直接感染和损伤的证据有限,新冠病毒感染患者发生的肺脏之外的实体器官大部分损伤多为重症和死亡病例,可能多是感染导致的系统性损伤的结果,而不是病毒本身的作用。
3 新冠病毒感染者捐献器官移植
目前,有关新冠病毒抗原或核酸阳性捐献者进行实体器官移植的研究较少。已有的大多数研究结果均表明新冠病毒核酸阳性捐献者并不会增加受者感染新冠病毒的风险,特别是尚无通过血液和捐献器官通过移植感染新冠病毒的直接证据。最初的新冠病毒核酸阳性捐献者发生在未及时诊断新冠病毒感染的情况下,美国疾病控制中心调查了3例捐献者来源的新冠病毒感染,均发生在肺移植受者中,另外6例非肺脏器官移植受者没有出现新冠病毒感染的临床证据。此外,美国疾病控制中心还检查了40例潜在捐献者来源的新冠病毒传播事件,但均无证据显示新冠病毒的肺外器官传播[48]。在本共识编写过程中,收集了近期国内多家器官移植中心应用新冠病毒感染捐献者捐献器官的移植数据,包括肾移植96例,术前受者均为阴性,在围手术期受者新冠病毒核酸阳性5例,经调查此5例受者术前均有新冠病毒感染患者接触史;肝移植49例,术前4例受者为新冠病毒核酸阳性,45例受者为新冠病毒核酸阴性,围手术期受者新冠病毒核酸阳性2例;心脏移植15例,术前受者新冠病毒核酸均为阴性,围手术期无受者新冠病毒核酸阳性。经调查分析,器官移植术后新冠病毒核酸阳性的受者基本可排除由新冠病毒感染者捐献器官带来的感染。
3.1 肾移植
美国克利夫兰诊所回顾性分析了2021年2月1日至2022年1月31日的220例死亡器官捐献肾移植,并根据有无感染新冠病毒及有无新冠病毒感染相关死亡原因将其分为新冠病毒感染不伴有新冠病毒死亡原因组(59例)、新冠病毒感染伴有新冠病毒相关死亡原因组(56例)、新冠病毒阴性组(105例),移植后均未采用瑞德西韦等预防性治疗,移植后新冠病毒感染率(新冠病毒感染不伴有新冠病毒死亡原因组13.6%,新冠病毒感染伴有新冠病毒相关死亡原因组7.1%,新冠病毒阴性组15.2%,P=0.89)和从移植到新冠病毒感染诊断的时间没有差异无统计学意义[49]。该中心在先前的病例报告中已有类似的结论[50]。有研究回顾性分析了美国器官资源共享网络(Organ Procurement and Transplantation Network,OPTN)数据库中的27 294例肾移植受者资料,发现其中281例捐献者在移植前14 d内存在新冠病毒感染,新冠病毒感染组无受者死于新冠病毒感染,而新冠病毒阴性组511例死于新冠病毒感染[5]。此外,多个临床病例报告也表明新冠病毒感染捐献者并不会增加受者移植后新冠病毒感染的风险[8,51-52]。美国克利夫兰诊所的研究显示新冠病毒感染捐献者和阴性捐献者供肾移植后受者病死率、移植物丢失率、移植物功能延迟恢复发生率、急性排斥反应发生率、住院时间、30 d再入院率、血清肌酐水平等差异均无统计学意义[49]。一项使用移植受者科学登记系统(Scientific Registry of Transplant Recipients,SRTR)数据库进行的回顾性研究分析了555例新冠病毒感染捐献者供肾及同时期的30 822例新冠病毒核酸阴性捐献者供肾的移植后结果,发现两组术后6个月内移植物存活率相当(95.5%比95.3%),移植物功能延迟恢复发生率接近,多变量Cox比例风险显示新冠病毒感染捐献者供肾移植调整后移植物丢失风险为0.91(95%可信区间0.49~1.69),捐献者新冠病毒感染状态与移植物存活率无关[8]。
3.2 肝移植
Schold等[8]分析了SRTR数据库2020年3月12日至2021年8月31日移植受者的资料,发现新冠病毒阴性捐献者的10 860例供肝移植受者中1.35%有新冠病毒感染死亡原因,而新冠病毒感染捐献者的147例供肝移植受者中没有报告新冠病毒感染死亡病例。Romagnoli等[53]分析了10例由新冠病毒感染捐献者供肝给10例新冠病毒既往感染或感染症状缓解等具有新冠病毒免疫的肝移植受者,仅2例受者在移植后核酸检测呈阳性,其中1例在术后21 d仍持续阳性,其他8例受者在随访期间均未发现新冠病毒感染。Jayasekera等[54]报道了2例新冠病毒感染捐献者供肝移植受者的资料,移植前2例受者均已接种新冠疫苗,手术当日移植物活检组织新冠病毒核酸阴性,术后均未发生新冠病毒感染。Wall等[55]报道了1例14岁受者接受具有新冠病毒核酸阳性暴露史和症状史的捐献者供肝移植,受者未检出新冠病毒且没有已知的新冠病毒暴露,终末期肝病模型评分为23分,术后7 d受者新冠病毒IgG抗体检测呈阴性,核衣壳IgG呈阳性,提示受者移植手术前曾暴露于新冠病毒,可能存在感染后免疫。Goss等[56]报道了2例儿童肝移植,其中1例捐献者为死于头部创伤的3岁男孩,4次鼻咽拭子检测中1次器官获取新冠病毒核酸阳性,3次支气管肺泡灌洗检测中1次器官获取新冠病毒核酸阳性;另1例捐献者为16月龄的心脏骤停男孩,病因不明,两例2岁的受者在移植后8个月恢复顺利,移植物功能良好,均未发现新冠病毒传播的证据。Nguyen等[57]报道了1例活体肝移植,捐献者在捐献前诊断新冠病毒感染,受者术后接受了新冠病毒感染者恢复期血浆的治疗,术后未发现病毒传播,捐献者和受者都有很好的术后结局。
3.3 心脏移植
目前大多数研究结果均支持新冠病毒感染捐献者心脏移植并不会增加受者新冠病毒感染的风险。Schold等[8]统计了SRTR数据库2020年3月12日至2021年8月31日共计4 785例新冠病毒阴性及62例新冠病毒感染捐献者心脏移植受者资料,1.29%的接受阴性捐献者心脏移植受者有新冠病毒感染死因,而接受新冠病毒感染捐献者心脏移植受者没有新冠病毒感染死因。另一项使用OPTN数据库进行的研究也得出了类似的结论,4 058例接受新冠病毒阴性捐献者及36例接受新冠病毒感染捐献者心脏移植受者中,0.96%(39例)的接受阴性捐献者心脏的受者有新冠病毒感染死因,而接受新冠病毒感染捐献者心脏的受者没有新冠病毒感染死因;接受新冠病毒感染捐献者心脏移植的受者与接受阴性捐献者心脏移植受者的住院时间相似(16.5 d比17.0 d,P=0.51),出院前排斥反应发生率低(8.8%比18.0%,P=0.26);接受新冠病毒感染捐献者心脏移植受者中没有30 d内移植失败或死亡病例;在接受新冠病毒感染捐献者心脏移植受者平均随访89 d期间,病死率为2.9%,低于与接受新冠病毒阴性捐献者心脏移植受者的病死率(8.8%)[5]。Eichenberger等[58]报道了共14例接受新冠病毒感染捐献者心脏移植受者,术后所有受者均未检测出新冠病毒感染,13例恢复良好,除了其中1例心-肝联合移植受者发生了严重并发症(大量出血及高凝状态,之后形成冠状动脉血栓),使用另1例新冠病毒感染捐献者的供心进行紧急二次心脏移植,为评估新冠病毒是否与该例心脏严重并发症有关,对该心脏进行了活检,心脏组织新冠病毒核酸呈阴性,单次右心室活检免疫组化染色显示核衣壳蛋白阳性,但没有其他病理学结果支持存在新冠病毒感染导致的心肌细胞损伤,也没有心肌炎的证据,左心室没有大体或组织学异常,虽然免疫组化结果的重要性尚不清楚,但核酸结果和其余病理发现更支持这些肺外组织中不存在存活的新冠病毒,高凝状态和移植失败的原因最终归因于肝硬化和潜在的原发性心脏病,而不是新冠病毒感染相关的器官衰竭。
4 新冠病毒核酸阳性者器官捐献的建议
新冠病毒为呼吸道病毒,主要经呼吸道飞沫、密切接触和气溶胶传播,到目前为止尚无通过血液和捐献器官通过移植传播的直接证据。根据国家疫情防控政策,我国新冠病毒感染流行形势及临床防控实践,参考国内外相关领域的研究结果及临床应用研究证据,结合器官捐献和移植的工作特点,对感染新冠病毒感染者器官捐献提出以下建议(图1、2),供器官捐献和移植工作参考。
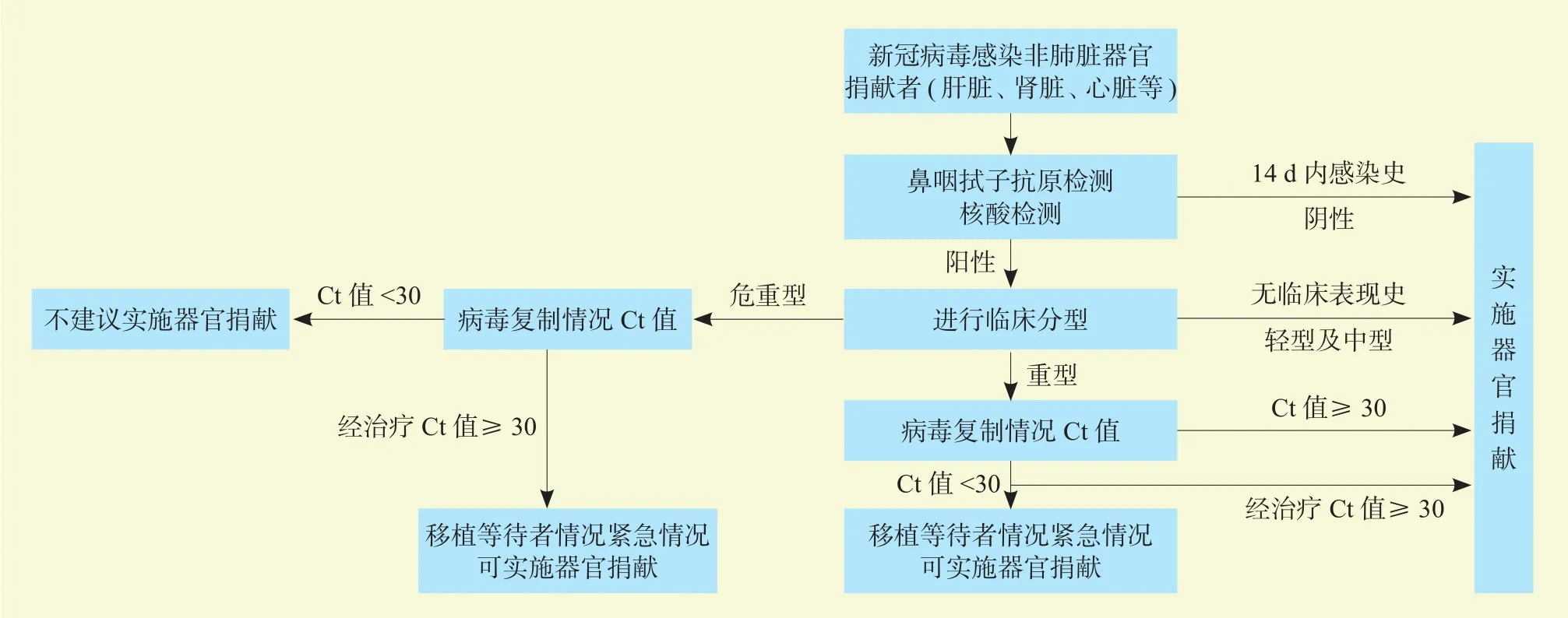
图 1 新冠病毒感染者非肺脏器官捐献流程图Figure 1 Flow chart of non-pulmonary organ donation of donors infected with novel coronavirus
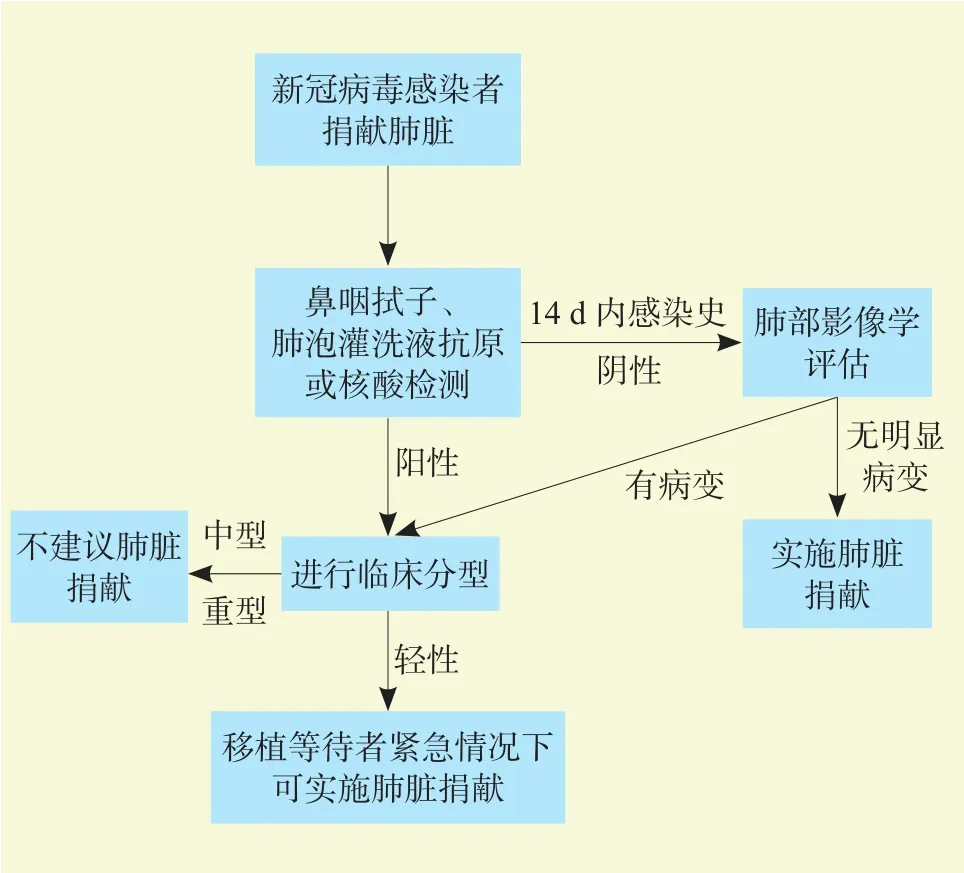
图 2 新冠病毒感染捐献者肺脏捐献流程图Figure 2 Flow chart of pulmonary donation of donors infected with novel coronavirus
4.1 肝脏、肾脏、心脏等非肺脏器官捐献
建议1:捐献者14 d内有新冠病毒感染史,鼻咽拭子抗原或核酸检测阴性,按照按公民逝世后器官捐献流程正常实施捐献。
建议2:捐献者感染新冠病毒,鼻咽拭子新冠病毒抗原或核酸检测阳性,无相关临床病史,按照按公民逝世后器官捐献流程正常实施捐献。
建议3:捐献者感染新冠病毒,鼻咽拭子新冠病毒抗原或核酸检测阳性,临床分型为轻型和中型,按照公民逝世后器官捐献流程正常实施捐献。
建议4:捐献者感染新冠病毒,鼻咽拭子新冠病毒抗原或核酸检测阳性,临床分型为重型,核酸检测低病毒载量(Ct值≥30),可按照按公民逝世后器官捐献流程实施捐献。
建议5:捐献者感染新冠病毒,鼻咽拭子新冠病毒抗原或核酸检测阳性,临床分型为重型,核酸检测高病毒载量(Ct值<30),移植等待者紧急情况下可实施器官捐献;或经抗病毒治疗新冠病毒核酸检测低病毒载量(Ct值≥30)或转阴,可按照按公民逝世后器官捐献流程实施捐献。
建议6:捐献者感染新冠病毒,鼻咽拭子新冠病毒核酸或抗原检测阳性,临床分型为危重型,核酸检测高病毒载量(Ct值<30),不建议捐献器官;鼻咽拭子新冠病毒核酸检测低病毒载量(Ct值≥30),移植等待者紧急情况下可实施器官捐献。
4.2 肺脏捐献
建议7:捐献者14 d内有新冠病毒感染史,鼻咽拭子、肺泡灌洗液抗原或核酸检测阴性,肺部影像学无明显病变,按照按公民逝世后器官捐献流程实施肺脏捐献。
建议8:捐献者感染新冠病毒,鼻咽拭子新冠病毒抗原或核酸检测阳性,临床分型为轻型,移植等待者紧急情况下可实施肺脏捐献。
建议9:捐献者感染新冠病毒,鼻咽拭子新冠病毒抗原或核酸检测阳性,临床分型为中型或重症,不适合肺脏捐献。
总的来说,当前研究的结果支持使用新冠病毒感染者逝世后捐献肝脏、肾脏、心脏等器官进行移植,但在实施过程中要综合考虑OPO、捐献医院、移植医院、捐献与移植团队管理、技术和资源配备等因素,肺脏捐献宜慎重并严格标准。在实施过程中要进一步研究新冠病毒感染者器官利用的最佳实践、移植候选者的风险认知和术后处理预案及移植效果预判,为终末期器官衰竭患者争取最大移植机会。
主审专家:
郑树森 浙江大学医学院附属第一医院
叶啟发 武汉大学中南医院
何晓顺 中山大学附属第一医院
门同义 山东第一医科大学第一附属医院
齐海智 中南大学湘雅二医院
审稿专家:
陈知水 华中科技大学同济医学院附属同济医院
张水军 郑州大学第一附属医院
徐 骁 浙江大学医学院
田 野 首都医科大学附属北京友谊医院
陈静瑜 无锡市人民医院
程 颖 中国医科大学附属第一医院
窦 剑 河北医科大学第三医院
李 波 四川大学华西医院
王伟林 浙江大学医学院附属第二医院
周江桥 武汉大学人民医院
杨 扬 中山大学附属第三医院
丰贵文 郑州大学第一附属医院
王正昕 复旦大学附属华山医院
蒋文涛 天津市第一中心医院
陈文慧 北京中日友好医院
李新长 江西省人民医院
霍 枫 中国人民解放军南部战区总医院
顾 民 南京医科大学第二附属医院
吕国悦 吉林大学白求恩第一医院
董 震 青岛大学附属医院
蒋继贫 华中科技大学同济医学院附属同济医院
黄 洁 中国医学科学院阜外医院
夏家红 华中科技大学同济医学院附属协和医院
徐 鑫 广州医科大学附属第一医院
吴 波 无锡市人民医院
章志丹 中国医科大学附属第一医院
秦 科 广西医科大学第二附属医院
巨春蓉 广州医科大学第一附属医院
孙永康 山西省第二人民医院
张 武 树兰(杭州)医院
张 明 上海交通大学医学院附属仁济医院
杨诏旭 空军军医大学西京医院
孙丽莹 首都医科大学附属北京友谊医院
王 博 西安交通大学第一附属医院
项和立 西安交通大学第一附属医院
林 俊 首都医科大学附属北京友谊医院
范晓礼 武汉大学中南医院

