岩藻黄质固体脂质微胶囊的制备及理化表征
陈雅鑫,林永杰,杨婷,何袅袅,蔡树芸,陈晖,方华,洪专,张怡评*
(1.自然资源部第三海洋研究所,海洋生物资源开发利用工程技术创新中心,福建厦门 361005)(2.福建农林大学食品科学学院,福建福州 350002)
岩藻黄质(Fucoxanthin,FX),亦称褐藻素、岩藻黄素[1,2],是一类有特殊含氧官能团的丙二烯类胡萝卜素[3],在可食用褐藻如昆布、铜藻、羊栖菜等中大量存在[4-6]。有研究表明,岩藻黄质是一类重要的脂溶性功能性化合物,但不能在人体内合成,只能通过饮食摄入[7]。近年来,陆续有岩藻黄质在食品行业的应用报道,如Sasaki等[8]研究了岩藻黄质的添加对碎鸡胸肉的影响,发现其有效改善鸡肉产品外观和延长其保质期;张吉和等[9]在压片糖果中加入岩藻黄质,结果表明有利于降低胆固醇、抑制血糖的上升,开拓了其应用的新领域。除了抗氧化、降血糖产品的应用,以岩藻黄质为主的减肥产品系列是近阶段市场开发的热点,目前市场已开发了天然岩藻黄质的保健软胶囊[10]、岩藻黄质与石榴籽提取物复合产品[11]等,被证实具有一定降脂作用。由此可见,岩藻黄质作为营养功效因子在功能性食品的研究与开发中具有较高商业价值与广泛应用前景。
然而,与其它类胡萝卜类似,长链双键的不饱和结构导致岩藻黄质极易被氧化,尤其光照、高温易使其丧失生物活性[12,13]。此外,我们在前期研究发现,FX在人体胃液中的低pH值环境下极其容易分解,导致肠道不能完全代谢吸收,阻碍了其生物功能的发挥[14,15]。这些问题都严重限制了岩藻黄质在食品产业中的应用。因此,有效提高岩藻黄质稳定性与体内吸收是促进其在功能性食品应用的关键与重点。
固体脂质粒(Solid Lipid Nanoparticles,SLN)是近几年发展起来的一种新型脂基递送系统,亦是毫微粒封装系统。SLN通常由脂肪酸、类固醇或者部分甘油酯、蜡、甘油三酸酯等在室温下为固体的脂质所组成[16]。该运输载体具备稳定性高,释放性慢,又兼具低毒性的优点[17],因此是一种极有发展前景的新型给药系统。目前已有许多该载体用于包埋α-生育酚[18]、姜黄素[19]等活性成分的相关研究,但其用于包埋 FX鲜有报道,且大部分制备方法采用单一固体脂质如乙酸鲸蜡醇酯[20]、十六烷基棕榈酸酯[21]等包埋,包埋率较低。研究表明FX与脂质混合服用能显著提高其生物利用度,保持良好的生物活性[22,23]。此外,将不同熔点、种类的脂质作为壁材结合包埋芯材,可有效增加不规则晶型的比例,削弱芯材被单种固体脂质的高度有序晶格挤出壁材的可能性,从而提高固体脂质粒包埋芯材的能力[24]。
本文拟利用胆固醇与棕榈硬脂作为混合脂质,采用反溶剂沉淀结合超声剪切法制备FX固体脂质微粒(FX-SLN)。再使用明胶、阿拉伯胶作为壁材,通过复合凝聚法复合包埋FX-SLN形成FX-MC。采用单因素和响应面试验优化制备工艺参数,并对微胶囊外观形态、粒径、Zeta电位以及结构性质、热力学性质进行测定与表征。以期增强 FX的稳定性和提高 FX生物利用度,为解决其在实际食品或保健品生产应用中遇到的问题提供参考。
1 材料与方法
1.1 原料
FX晶体(由本实验室从铜藻中提取、分离纯化并采用核磁共振波谱、红外光谱和质谱等检测方法对其进行结构确证与表征,纯度>99%);棕榈硬脂,汕头市明德食品添加剂有限公司;胆固醇,江西华豫源生物科技有限公司;鱼明胶、阿拉伯胶,厦门亿威隆生物科技有限公司;单宁酸,郑州苍宇食品化工产品有限公司,以上材料均为食品级。
1.2 设备与仪器
JY92-IIN超声细胞粉碎机,宁波新芝生物科技股份有限公司;PB100高速剪切均质机,墨西哥Primasci公司;LC-2010AD高效液相色谱仪,日本岛津公司;HZ-9212SB水浴恒温振荡器,太仓市华利达设备有限公司;Hei-VAP Expert旋转蒸发仪,德国Heidolph公司;KQ-500E超声波清洗器,昆山市超声仪器有限公司;FD-IC-50冷冻干燥机,北京博医康实验仪器有限公司;Zetasizer Nano ZS90纳米粒度电位仪,英国Malvern公司;Zeiss Sigma 300扫描电子显微镜,德国Zeiss公司;Nicolet Nexus 470傅里叶红外光谱仪,美国Nicolet公司;Mettler Toledo 200N差示扫描量热仪,美国Mettler公司。
1.3 方法
1.3.1 FX-MC的制备工艺
在文献[20]基础上进行优化工艺流程为:胆固醇、棕榈硬脂在阿拉伯胶溶液(1.5%,m/V)中55 ℃下熔融,待降到40 ℃下时,缓慢加入含有FX晶体的少量的乙醇溶液中,冰浴下在一定的功率下超声破碎处理一定时间,通过反溶剂沉淀反应形成FX-SLNs混悬液。然后与等体积的明胶溶液(1.5%,m/V)混合,高速剪切匀浆均质8 min,转速为20 000 r/min,进行复合凝聚反应。使用φ=10%醋酸调节pH值为3.5~4.5,冰浴下磁力搅拌,转速为500 r/min,冷却至10 ℃以下,缓慢滴加18%单宁酸溶液(在总体系质量分数为0.4%),使微胶囊固化。静置后离心洗涤、冷冻干燥得到FX-MC粉末样品。
1.3.2 FX质量的测定
用高效液相色谱(HPLC)检测FX含量。色谱条件:色谱柱Shim-pack VP-ODS C18(250 mm×4.6 mm,5 μm);流动相为甲醇-水溶液(92:8);流量设定1.0 mL/min;柱温35 ℃;检测波长取450 nm。将不同质量浓度的FX标准溶液过0.22 µm滤膜后进样,以质量浓度和峰面积分别为横、纵坐标作标准曲线,标准曲线方程为Y=46.84X+259.71(R2=0.999 8),将样品峰面积代入曲线求算FX含量。
1.3.3 粒径分布、Zeta电位的测定
使用粒度Zeta电位分析仪对FX-MC的水混悬液(0.1% wt)进行粒度与Zeta电位测量,重复3次测量,并利用尺寸分布跨度得出颗粒的分散系数即体系的PDI值。
1.3.4 包埋率的测定
精密称取5 mg冻干FX-MC,加10 mL pH值7.0的磷盐缓冲液,再加入0.05 g中性蛋白酶,在37 ℃下水浴震荡,使固态微胶囊破壁,然后抽滤,并用无水乙醇洗涤滤纸,收集滤液进行旋转蒸发至干,用适量无水乙醇洗旋蒸瓶,再将旋洗液以8 000 r/min的速度离心20 min,取上清液稀释至一定浓度后,在450 nm处记录其峰面积,根据标准曲线算出微胶囊中FX的浓度,按照以下公式计算得到包埋率:

式中:
A——FX-MC包埋率,%;
C——上清液中FX的含量,µg/mL;
V——上清液的体积,mL;
m——5 mg冻干FX-MC中FX的理论质量,mg。
1.3.5 载药量的测定
精密称取一定质量的微胶囊,测定其中FX的含量,测定方法同1.3.2中FX总量的测定,按下式计算微胶囊的载药量。

式中:
B——FX-MC载药量,%;
m1——微胶囊中FX含量,mg;
m0——微胶囊的总质量,mg。
1.3.6 单因素试验
1.3.6.1 FX与脂质量比对微胶囊的影响
FX:脂质的质量比分别为0.01:1、0.1:1、0.2:1、0.3:1、0.4:1(m/m),其中棕榈硬脂与胆固醇比例为60:40(m/m),加入阿拉伯胶溶液,芯材与壁材质量比为1:20(m/m),250 W超声3 min。加入等体积的含吐温80的明胶溶液,均质后调节pH值为4,再25 ℃恒温磁力搅拌30 min,转速为500 r/min,冰浴下继续搅拌降温至小于10 ℃,加单宁酸固化后即得微胶囊混悬液。
1.3.6.2 棕榈硬脂与胆固醇比例对微胶囊的影响
棕榈硬脂与胆固醇比例为 100:0、80:20、70:30、60:40、50:50(m/m),其他条件与“1.3.6.1”项下制备工艺一致。
1.3.6.3 壁材与芯材质量比对微胶囊的影响
壁材与芯材(FX固体脂质核心)质量比分别为5:1、10:1、20:1、30:1、40:1(m/m),其他条件与“1.3.6.1”项下制备工艺一致。
1.3.6.4 凝聚pH值对微胶囊的影响
凝聚pH值分别为3.5、3.8、4、4.2、4.5,其他条件与“1.3.6.1”项下制备工艺一致。
1.3.6.5 超声条件对微胶囊的影响
超声条件分别为 150 W/5 min、200 W/4 min、250 W/3 min、300 W/2 min、350 W/1 min。其他条件与“1.3.6.1”项下制备工艺一致。
通过单因素实验,综合评估包埋率、粒径和PDI值三项指标,初步筛选出FX-MC的制备条件选择为FX与棕榈油质量比为0.1:1、0.2:1、0.3:1(m/m);芯材与壁材质量比为 1:10、1:20、1:30(m/m),超声条件为200 W/4 min、250 W/3 min、300 W/2 min,为了确定最佳的工艺制备条件,采用响应面试验进行优化。
1.3.7 响应面试验设计
基于单因素试验结果,确定棕榈硬脂与胆固醇的质量比为60:40,凝聚pH值为4.5。根据Box-Behnken设计原理,综合评估包埋率、载药量、粒径和PDI值三项指标,对影响FX-MC综合评分的FX与脂质质量比(A)、芯材与壁材质量比(B)、超声条件(C)这三个影响因素进行响应面优化,各因素均确定三个水平,如表1所示。
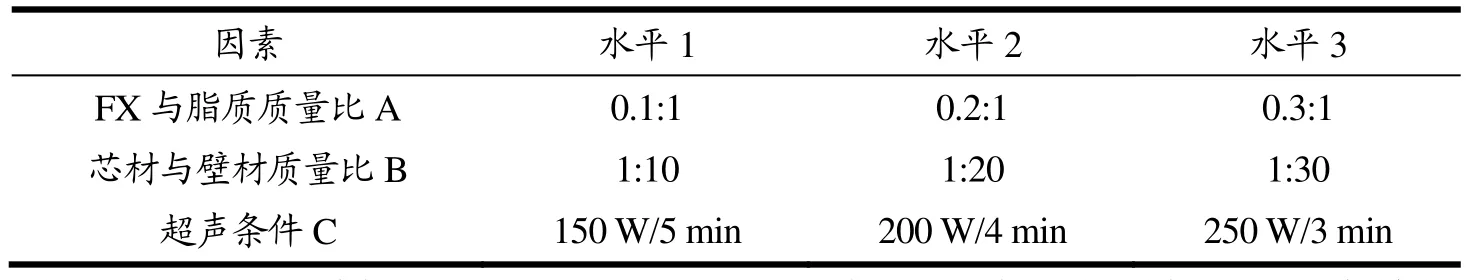
表1 响应面因素水平表Table 1 The factors and levels table of response surface methodology
称取17个实验号所用的FX、棕榈硬脂与胆固醇,明胶溶液和阿拉伯胶溶液,采用1.3.1的微胶囊制备工艺流程和方法,以FX-MC包埋率、载药量、粒径和PDI为考察指标,以指标综合评分为响应值,采用各指标加权综合评分进行计算:0.7(包埋率+载药量)+0.3(粒径评分+PDI评分)。其中粒径与PDI指标评分标准为:(1)粒径:<20 μm,90 分;20~30 μm,60 分;>30 μm,30 分。(2)PDI:<0.3,14 分;0.3~0.6,7分;>0.6,0分。
1.3.8 扫描电子显微镜(SEM)观察
将样品固定,喷金处理后通过Zeiss Sigma 300扫描电子显微镜分别观察 FX晶体、空白微胶囊及FX-MC的表面形态。加速电压为2 kV~3 kV,放大倍数为2 000倍。
1.3.9 傅里叶红外光谱分析(FT-IR)
分别将FX晶体、空白微胶囊及FX-MC进行红外光谱测定,采用溴化钾压片法,扫描条件为:波数范围4 000~400 cm-1,分辨率4 cm-1。测样得到三者的FT-IR谱图,然后进行对比,确认其包埋效果。
1.3.10 差示量热扫描分析(DSC)
分别对FX晶体、空白微胶囊及FX-MC进行差示扫描量热分析,考察三者的热稳定性。测量在氮气为吹扫气体下,温度为20~240 ℃,升温速率为10 ℃/min。
1.3.11 数据处理
每个实验均为 3次,结果以 X±RD表示,通过SPSS 13软件进行分析;采用Origin 2021软件作图;响应面试验结果用Design-Expert 8.0.6软件进行参数优化及方差分析。
2 结果与分析
2.1 FX-MC制备单因素分析
2.1.1 FX:脂质的影响
本试验以微胶囊的包埋率、粒径、PDI作为评价指标,分别探讨了不同质量比的FX和脂质对微胶囊效果的影响,结果见图2。
从图2的数据趋势可以看出,相同的脂质质量下,随着FX添加量的增加,包埋率整体呈下降趋势,这是因为为FX是一种脂溶性营养物质,乳化作用下FX被均匀分散至油相,随着FX逐渐增加,相同质量的脂质不能将其全部包埋,导致游离FX增加,因此微胶囊包封率降低。

图2 FX:脂质对FX-MC的影响Fig.2 The effect of FX to lipid ratios on FX-MC
当FX:脂质=0.5:1(m/m)时,包埋率下降到92.25%,变化极显著(p<0.01),说明此时未被包埋的 FX 量明显增加,因此FX:脂质的合适范围为0.1:1~0.4:1。当FX:脂质为0.2:1时,粒径最小,且体系的PDI最小,为0.5,说明该状态下微胶囊的粒径分布最均匀,体系最稳定。因此,选择FX:脂质=0.2:1(m/m)作为最佳FX-脂质比值。
2.1.2 棕榈硬脂与胆固醇比例的影响
从图3可以看出,相较于棕榈硬脂的单独脂质,采用棕榈硬脂和胆固醇按一定质量比混合而成的混合脂质,制备得到的FX-MC的包埋率明显提高。这是因为单一的棕榈硬脂具有高度规则的晶形结构,容易挤出药物,导致包埋率不高。胆固醇的添加除了扰乱固体脂质规则的晶型结构,还具有调节磷脂双分子层膜的流动性,维持壁材柔韧性的特性[25],最终明显提高包埋率。
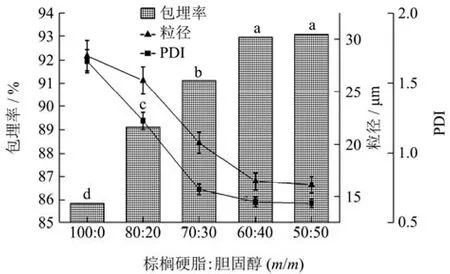
图3 棕榈硬脂:胆固醇对FX-MC的影响Fig.3 Effects of different palm stearin to cholesterol ratios on FX-MC
其中,当胆固醇添加量增加时,微胶囊包埋率随之增大。当胆固醇添加量为总体脂质质量的 40%时,包埋率达到92.97%,此时胆固醇继续增加时,包埋率无明显差异(p>0.05)。同时,该比例下的粒径、PDI基本达到最小,分别为16.48 μm、0.65,当胆固醇继续添加时各指标无明显变化(相比于脂质比=50:50)(p>0.05)。考虑到生产成本,故选择60:40(m/m)作为最佳棕榈硬脂和胆固醇比值。
2.1.3 壁芯比的影响
从图4可以看出,相同的芯材质量下,随着壁材添加量的增加,包埋率呈上升趋势,当壁芯比大于20:1时,包埋率接近100%,变化显著(p<0.05),随后包埋率趋于稳定,说明壁材包裹芯材的含量已趋向饱和。其中,当壁芯比为20:1时,微胶囊的粒径稍大于壁芯比为 40:1时的粒径,为 24.93 μm,但差异不显著(p>0.05),且此时体系的PDI最小,为0.45,说明该体系最稳定,因此选择20:1(m/m)作为最佳壁芯比。
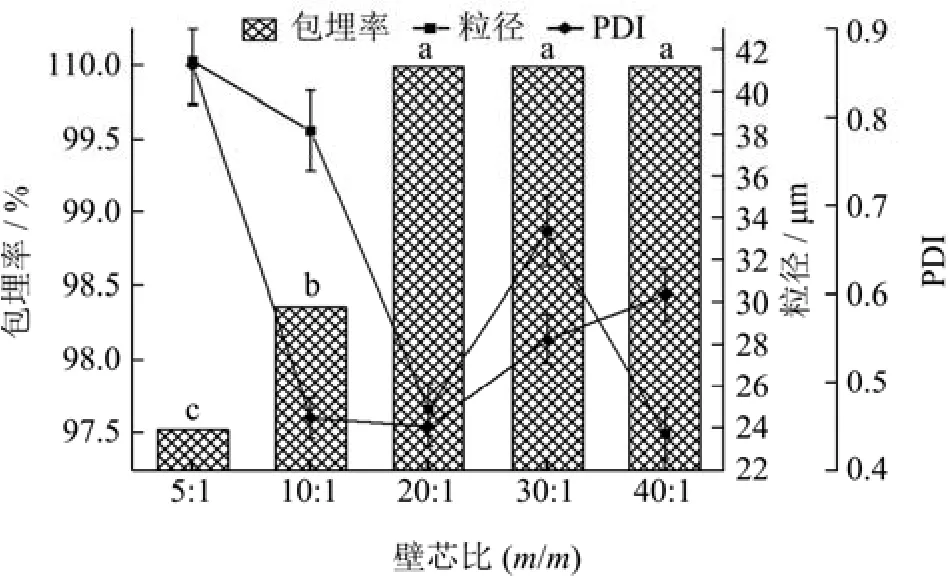
图4 壁芯比对FX-MC的影响Fig.4 Effects of different core-wall ratios on FX-MC
2.1.4 凝聚pH值的影响
阿拉伯胶、明胶胶之间的静电相互作用是受其带电性质的影响,而阿拉伯胶与明胶的带电性质又直接受环境pH值的影响,因此,pH值是影响阿拉伯胶与明胶复合凝聚层反应的关键因素。当环境pH值介于明胶/阿拉伯胶之间即等电点时,才会出现有效的复合凝聚反应。本试验分别探讨了不同凝聚pH值对微胶囊效果的影响,所得结果详见图5。
从图5分析可知,除了pH值为3.5的凝聚条件,pH值3.8~4.5之间不同凝聚pH值对微胶囊包埋率没有显著性差异(p>0.05)。说明此时的环境pH值已经达到明胶/阿拉伯胶体系的等电点的条件,此时微胶囊产率最高,包埋效果最好。当 pH≥3.8时,随着凝聚pH值增加,粒径和PDI都呈下降趋势,一方面,体系中排斥电荷量加大,导致团聚的粒子随着pH值的增加而减少颗粒的絮凝,愈多的单个粒子分散在水溶液中,故测得结果为粒径逐渐减小;另一方面,体系中单个粒子数量的增加使其在微胶囊的分散性提高,故 PDI呈下降趋势。结果发现,当凝聚pH值为4.5时,微胶囊粒径最小,PDI相对较小,因此确定pH值4.5为最佳凝聚pH值。
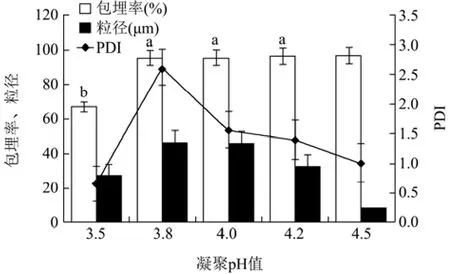
图5 凝聚pH值对FX-MC的影响Fig.5 Effects of different pH on the FX-MC
2.1.5 超声条件的影响
从图6可以看出,不同超声条件对微胶囊包埋率整体上有显著性差异(p<0.05)。当超声时间小于3 min时,包埋率小于90%,偏低。随着超声时间加大,微胶囊包埋率也逐渐增加。粒径大小与超声功率成反比,而PDI值随超声功率的下降而减小。当超声条件为250 W/3 min时,包埋率相对较高,且包埋率和粒径都达到预期的较小值,故选择250 W/3 min作为最佳超声条件。
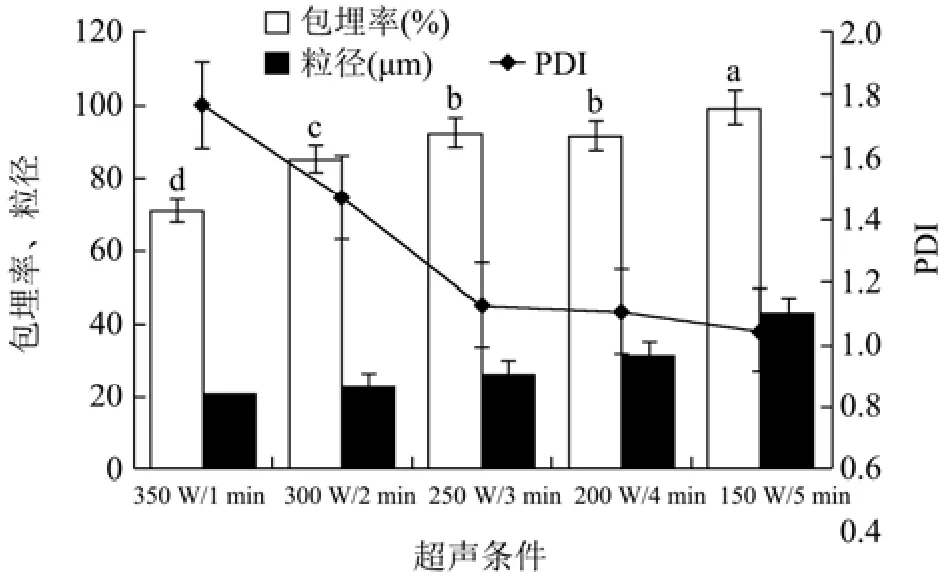
图6 超声条件对FX-MC的影响Fig.6 Effects of different ultrasonic conditions on FX-MC
2.2 FX-MC制备工艺响应面优化分析
2.2.1 实验结果及方差分析
本研究通过响应面试验对FX-MC制备参数进行优化,考察 FX:脂质、壁芯比和超声条件对包埋率与载药量的综合影响,试验设计及结果如表2所示。
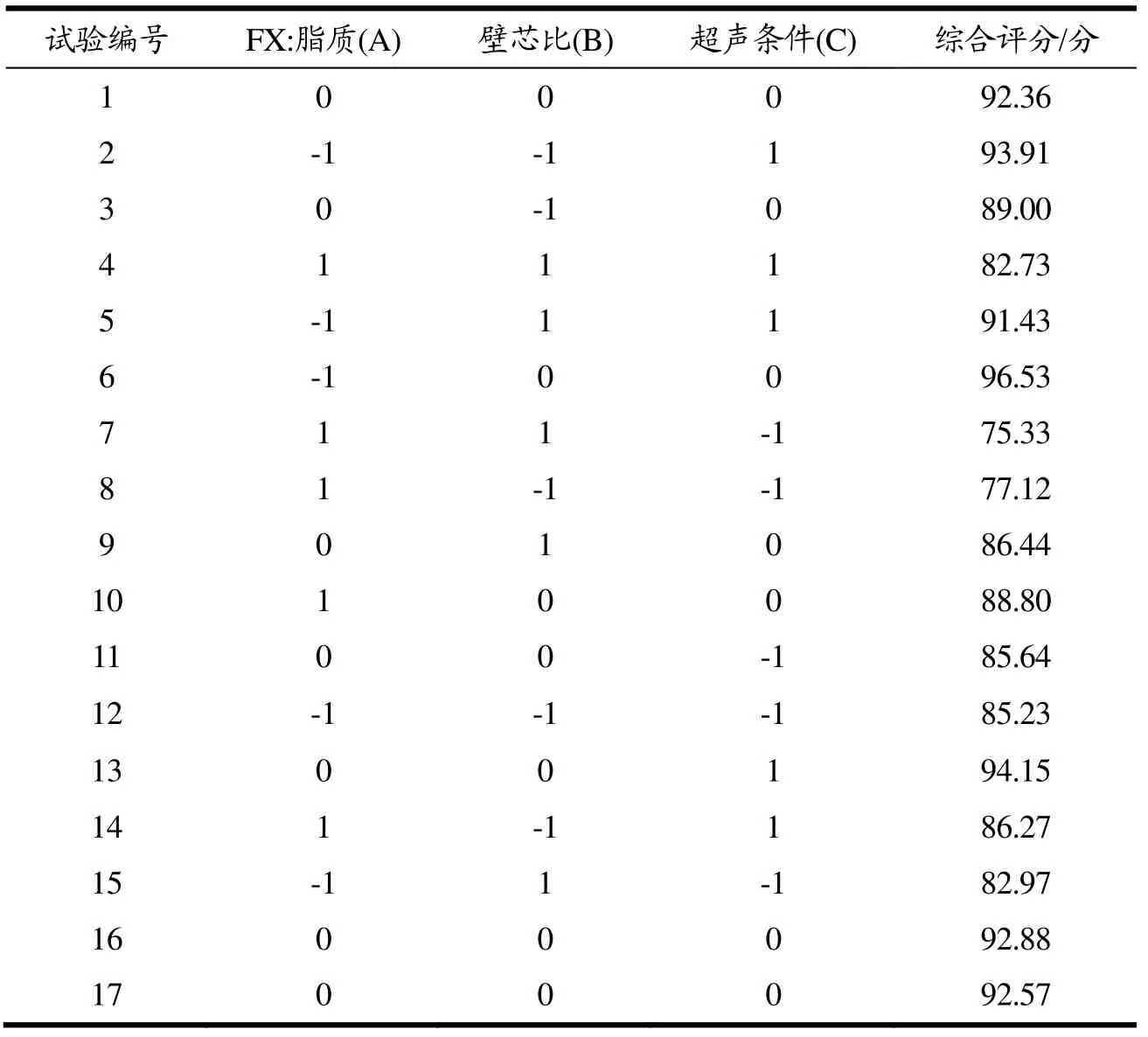
表2 Box-Behnken 试验设计及试验结果Table 2 The response surface designs with experimental results
通过分析整合响应面试验所得数据,得到综合评分和自变量 FX:脂质、壁芯比以及超声条件三个因素之间的回归方程:
Y=92.75-3.99A-1.2B+4.22C-0.058AB-0.059AC-0.26BC-0.19A2-5.14B2-3.03C2
为验证上述回归方程的可行性,需将所得数据进行进一步方差分析,详见表3。
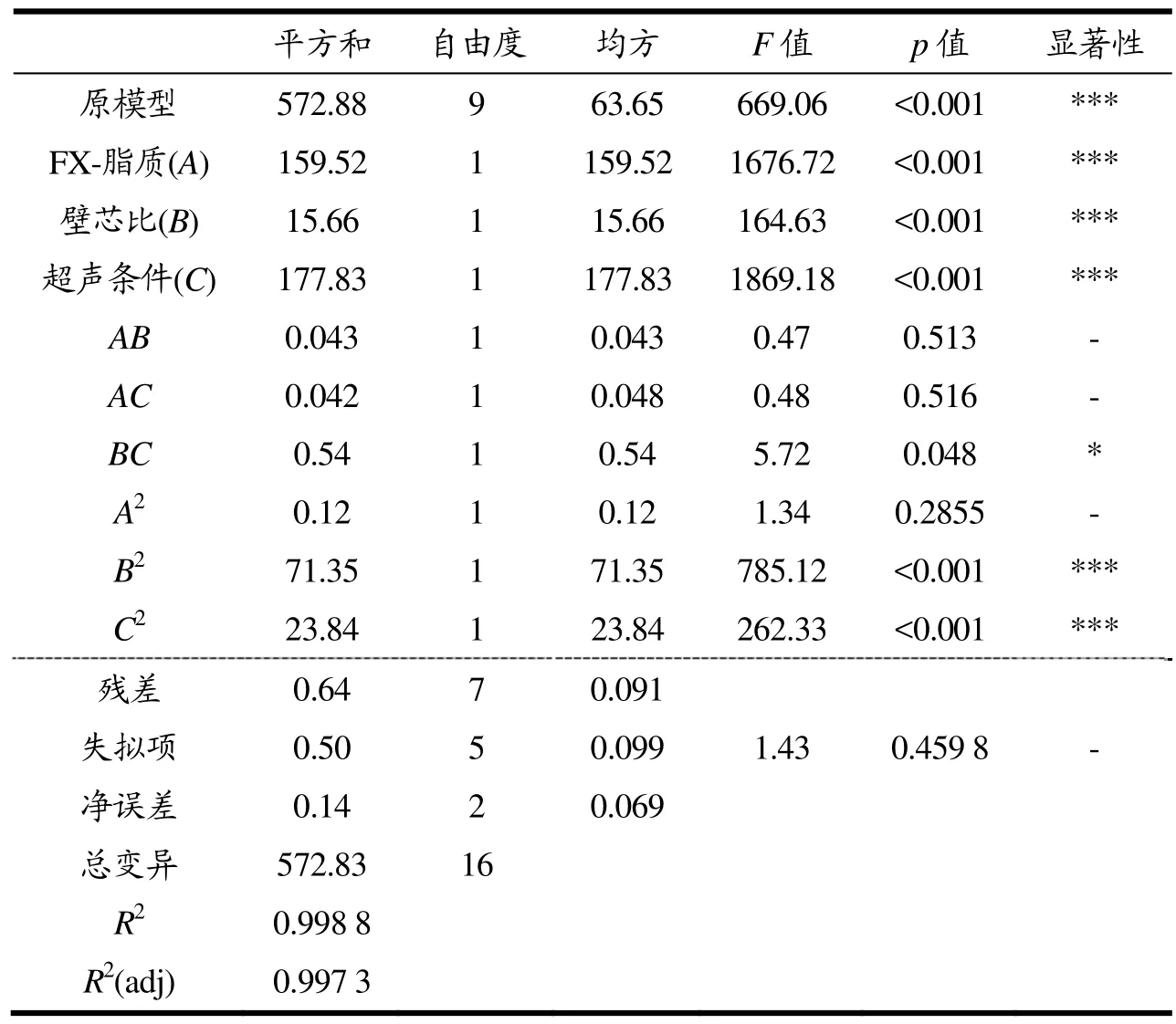
表3 响应面试验方差分析表Table 3 Response surface analysis of variance analysis
通过方差分析表中的p值可以看出,A、B、C三个变量对综合评分皆有较大的影响,根据F值可得影响顺序为C>A>B。另外,表3数据显示,原模型达到高度显著水平(p值<0.001),说明该模型具有统计学意义,其中A、B、C、B2、C2对其的影响均达到了高度显著水平(p<0.001),而BC对其的影响达到了显著水平(p<0.05),且失拟项检验不显著(p=0.459 8>0.05),说明该模型描述较为准确。校正系数[R2(adj)=0.997 3]可看出试验中响应值变化的 99.73%均可用此模型来解释,拟合程度良好,说明该响应模型能够对FX-MC的制备起到一定的分析与预测作用。
2.2.2 各因素之间交互作用的分析
根据上述方程建立两两因素交互的响应曲面图和等高线图,可更直观的分析各个因素对综合评分的影响,分析如下。
图7~9反映了各因素的交互作用以及对响应值的影响。由图分析得到,交互作用的影响大小分别是:BC>AC>AB。其中,B(壁芯比)与C(超声条件)的交互作用最显著,表现为曲面图最陡,等高线呈近圆形。当壁芯比一定时,综合评分随超声功率的升高而提高。原因可能是较高的超声功率有助于乳液的均匀分散,促进微胶囊的形成。

图7 Y=f(A,B)响应曲面立体图及等高线Fig.7 Response surface plot and contour map plot for Y=f(A, B)

图8 Y=f(A,C)响应曲面立体图及等高线Fig.8 Response surface plot and contour map plot for Y=f(A, C)

图9 Y=f(B,C)响应曲面立体图及等高线Fig.9 Response surface plot and contour map plot for Y=f(B, C)
2.3 FX-MC最佳工艺的确定及验证
通过Design Expert 8.0.5软件分析的回归方程,得到 FX-MC 最佳工艺参数:A=0.21,B=25,C=240,利用上述条件预测理论最佳综合评分为97.38分。为了检验模型的可靠性,最终将优化后的微胶囊工艺参数调整为FX:脂质0.2:1(m/m)、壁芯比25:1(m/m)、超声条件240 W/3 min(m/m)。并采用棕榈硬质与胆固醇比例为60:40(m/m),凝聚pH值为4.5,在调整后的条件下进行三次重复试验,所得试验结果与FX-MC形态观察如下。
由表4中得出平均综合评分值为97.07分,与理论预测值 97.38分接近,表明通过响应面法优化得到的FX-MC最佳工艺条件可行性较高,可用于指导实践操作。
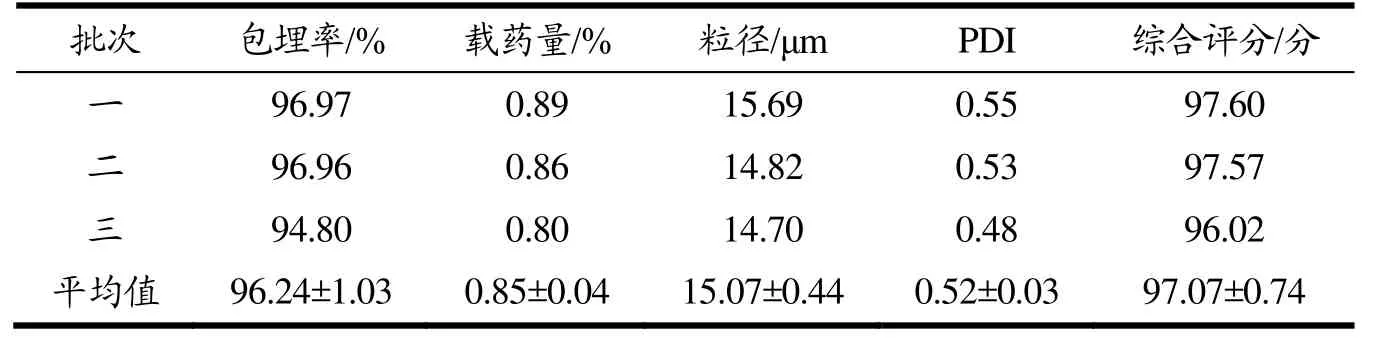
表4 三批次FX-MC各指标的比较Table 4 Comparison of the indexes of three batches of fucoxanthin microcapsules
2.4 理化表征
2.4.1 微胶囊外表形态(SEM)、粒径和 Zeta电位
通过扫描电子显微镜观察包埋前后FX的形态差异可以判断FX-MC是否形成。在图10aA中,由于FX的水溶性低,FX晶体在水中保持固有的长方体形状,尺寸不规则,但整体平均长度大于50 μm。空白微胶囊(图10aB)为凝胶和GA复合凝聚形成的凝胶颗粒,粒径小于500 nm。将空白微胶囊溶于水后晾干观察时,考虑到壁材的水溶性,凝胶颗粒之间容易相互结合,形成不规则的聚集体。在图10aC中,FX-MC呈球形。在10 K放大倍数下,可以清楚地观察到表面比较光滑(图10aC'),没有裂纹,表明经过一定处理后,油脂核均匀地分散在壁材中,使颗粒表面可以通过复杂的内聚反应被壁材完全包裹。此外,固化反应增强了微胶囊的稳定性,防止分解。
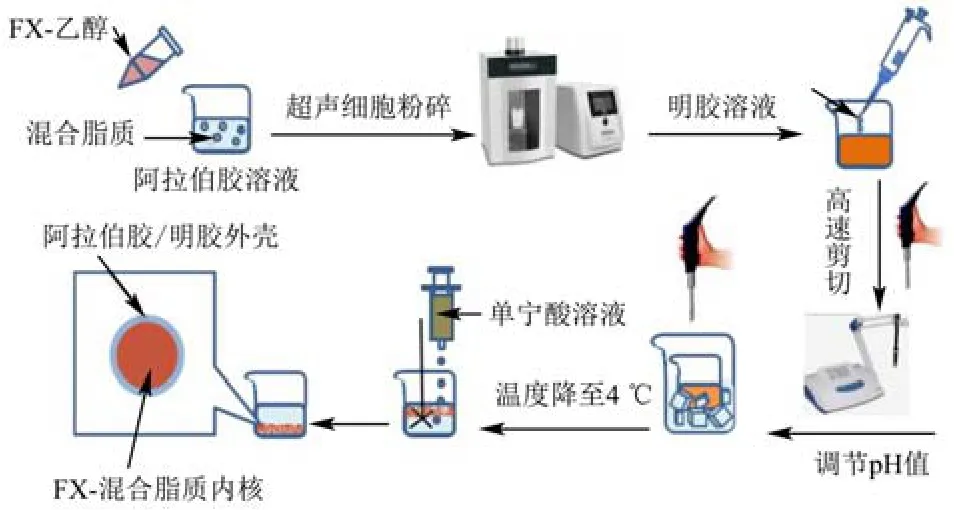
图1 FX-MC制备工艺流程Fig.1 The preparation process of FX-MC
通过各物质SEM图对比分析,FX晶体、空白微胶囊和FX-MC呈现出不同的形态,表明负载FX的微胶囊是一个新相,证明负载FX的微胶囊已经形成。
测定 FX-MC平均粒径为 1 154 nm,电位为-20.71 mV(图10b、10c),PDI值为0.27(数据未显示)。粒径达到微米级,符合微胶囊粒径要求,且粒径相对较小。通常来说,溶液中的Zeta电位值(正或负)越大,反映分子状态相对较稳定。FX-MC电位-20.71 mV,稳定性相对较好,其PDI值也证实了这一点(PDI<0.3)。
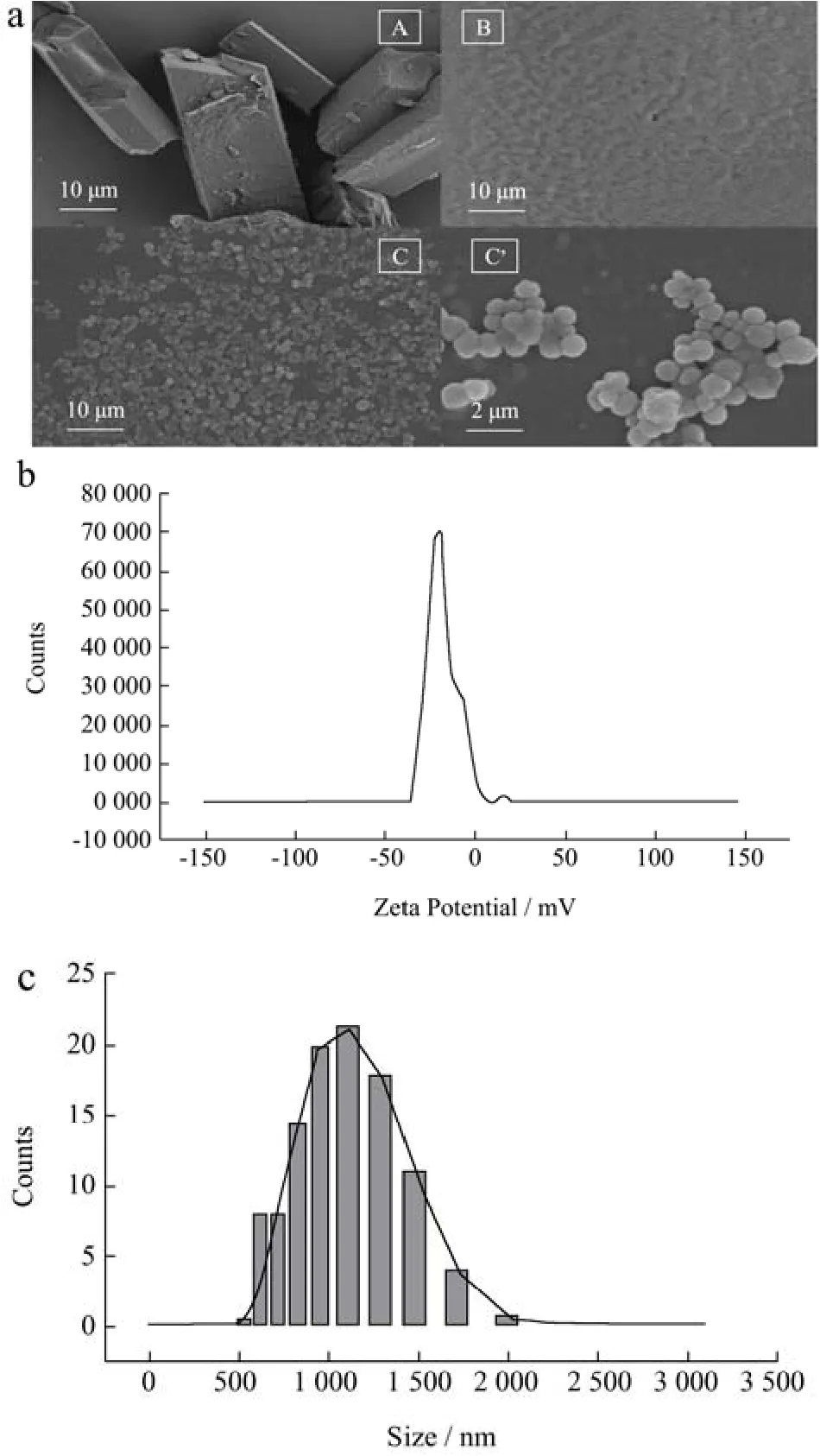
图10 FX晶体(A)、空白微胶囊(B)、FX-MC (C、C’)的外表形态(a),FX-MC的Zeta电位、粒径分布(b、c)Fig.10 The appearance of fucoxanthin crystals (A), blank microcapsules (B), FX-MC (C, C') (a), Zeta potential and particle size distribution of FX-MC (b, c)
2.4.2 微胶囊的结构表征(FT-IR)
FT-IR可用于表征材料的化学结构以及聚合物与药物之间的相互作用。在本研究中,FX晶体、空白微胶囊和FX-MC通过FT-IR方法进行评估,得到的光谱如图11所示。对于纯FX样品(FX晶体),红外吸收光谱在1 928 cm-1处有一个特征峰,这是FX独特的官能团丙二烯键(C=C=C)的特征峰。除此之外,2 858 cm-1处的峰代表-CH的伸缩振动,1 363 cm-1处的峰代表-CH的弯曲振动,3 011 cm-1处的峰代表=CH的弯曲振动,在1 732 cm-1(-C=O拉伸)、1 032 cm-1(-C-O拉伸)处为酯类特征峰;在1 657 cm-1处,表明存在酮类物质(C=O)。此外,968 cm-1的峰值为C-C共轭体系中C-H键的面外弯曲振动的吸收峰,是反式取代乙烯的特征峰,这些分别都是类胡萝卜素具有的特征峰。

图11 FX晶体(FX crystal)、空白微胶囊(blank cystal)、FX-MC的红外光谱图(FT-IR)Fig.11 Infrared spectra (FT-IR) of FX crystal, blank cystal, and FX-MC
观察到,FX-MC样品的红外谱图整体峰型更接近空白微胶囊,其中在约2 800 cm-1、1 500 cm-1以及1 080 cm-1附近波段处(图中阴影部分)产生比壁材特征峰更尖、更大峰强的吸收峰,这可能与微胶囊壁材包载了FX有关。此外,FX-MC在1 928 cm-1处并未出现FX的独特特征峰,推测是由于FX被包埋在壁材里导致红外透过率减少,同时观察到微胶囊中 FX的特征峰出现在3 016 cm-1、1 031 cm-1等处,但是部分峰型被钝化或者被明显削弱,这也证实了前面的推测,即FX活性物质被壁材体系包覆后吸收峰受到一定的屏蔽,且无新的吸收峰形成,由此初步判定,FX以物理结合方式被成功负载到固体脂质微胶囊中,最终形成新的包埋相,这与王枭等[26]报道基本一致。
2.4.3 微胶囊的热力学性质表征(DSC)
通过DSC比较FX晶体,空白微胶囊和FX-MC的热力学性质。Tg表现为结晶聚合物的无定形区域从玻璃态转变为粘性橡胶相,或者后者转变为前者。一般Tg转变温度越高,产品的耐温性越好[27]。因此,在开发基于聚合物的新型产品时,应高度考虑这一特性。
如图12a所示,三种物质的Tg值均向左移动。其中,FX晶体的Tg值小于40 ℃(约38 ℃),接近体温,则易在人体内产生脆弱的晶体结构,被削弱其机械强度,不利于药物代谢和吸收。相较之下,FX-MC的Tg值高于40 ℃,表明聚合物在给药时可以表现出相当硬度的链结构,保证在人体正常体温下能控制药物释放。相比于Noviendri等[28]以聚(L-乳酸-乙醇酸)为载体制备的岩藻黄质微胶囊,Tg值为28.12 ℃,本研究制备的FX-MC耐热值明显更高,一个潜在的原因是带负电的明胶和带正电的阿拉伯胶通过复杂的内聚力,形成凝胶网络结构来包裹 FX,另一个是棕榈硬脂/胆固醇固体脂质形成了具有一定强度的晶形结构, 也提高了其稳定性。在图12b中,观察到三种物质的整体峰值温度向左移动,FX-MC的焓值最高,同样的,陈程莉等[29]发现其花青素微胶囊相比空白微胶囊以及花青素单体的热焓值更高,表明其发生相变(从高弹性到玻璃相)需要最高的热量。上述结果证明,FX-MC相比FX具有更好的热稳定性。
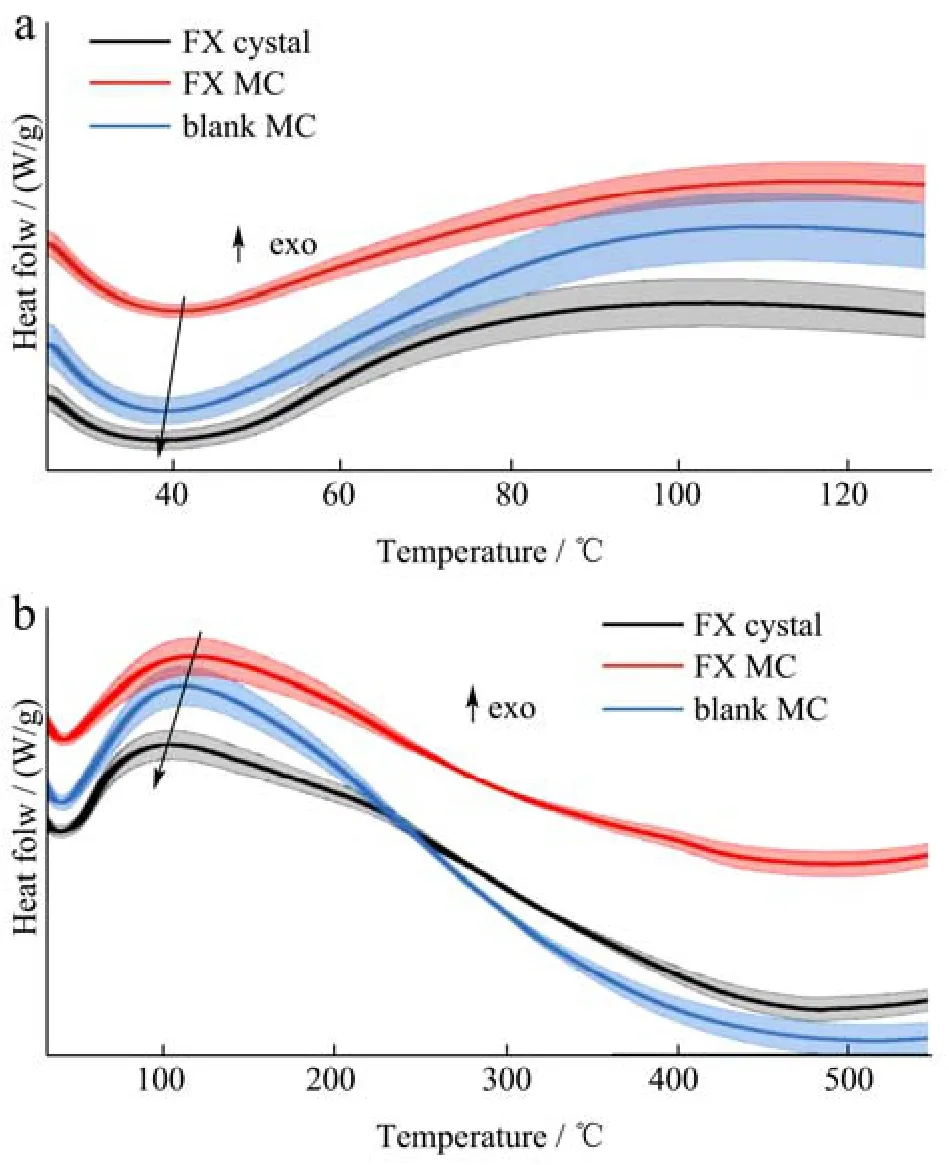
图12 FX晶体(FX crystal)、空白微胶囊(blank MC)、FX-MC的DSC谱图Fig.12 DSC spectra of FX crystals, blank MC, and FX-MC
3 结论
本试验选用混合固体脂质粒(棕榈硬脂/胆固醇)外壳包裹明胶和阿拉伯胶的复合凝聚层对FX进行双重包埋处理,通过响应面工艺优化,以FX-脂质、壁芯比例、超声条件三个条件为自变量建立回归方程,以微胶囊综合评分(包括包埋率、载药量、粒径、PDI)为评价指标,经方差分析可知该响应模型拟合良好,确定最佳工艺条件为:棕榈硬质:胆固醇60:40(m/m)、FX:脂质0.2:1(m/m)、壁芯比25:1(m/m)、凝聚pH值4.5、超声条件240 W/3 min,所制备得到的微胶囊具有较高包埋率,为96.24%,载药量有所提高。尺寸1 154 nm,符合微米级别,水溶液体系较为稳定。FX被成功包埋在脂质-复合凝聚层中,热稳定性明显提高,为提高FX的稳定性和生物利用度提供了新途径。后期将通过加速稳定性和体内生物利用度实验进一步研究FX-MC的稳定性和生物利用度改善情况。本试验方法简单易操作,为FX-MC工业化生产奠定一定理论基础,同时为新的功能食品开发提供价值参考。

