枸橼酸莫沙必利片杂质研究*
刘阿利,王 雪,张贵民
(1.鲁南贝特制药有限公司,山东 临沂 276006;2.国家手性制药工程技术研究中心,山东 临沂 276006;3.药物新制剂研发山东省工程研究中心,山东 临沂 276006)
枸橼酸莫沙必利为选择性5-羟色胺4(5-HT4)受体激动剂,可增强上消化道的胃排空和蠕动,促进肠道胆碱能神经元释放乙酰胆碱,刺激胃肠道而发挥促动力作用[1]。其选择性强,不良反应少,耐受性较好,促胃动力作用强,主要用于缓解慢性胃炎伴有的消化系统症状,也可用于胃食管反流性疾病、糖尿病性胃轻瘫及部分胃切除患者的胃功能障碍[2-5]。该制剂1998 年在日本上市,商品名Gasmotin®;2001 年在中国上市,中文名加斯清®[6]。目前,中国、欧洲、美国等的药典均未收载,日本药典(JP17 版)虽有收载,但也未对特定杂质作明确规定。一致性评价参照日本药典(JP17 版)“Mosapride Citrate Tablets”质 量 标 准[7]及 日 本IF 文件[8],建立本品有关物质检查方法,主要对5种特定杂质进行研究,结果特定杂质莫沙必利柠檬酰胺在液相色谱图中显示2个色谱峰,但是否均为莫沙必利柠檬酰胺,双峰出现的原因以及是否影响该杂质含量的计算等问题仍需进一步研究。本研究中采用高效液相色谱(HPLC)法和超高效液相色谱-四极杆飞行时间质谱(UPLC -Q-TOF-MS)法对莫沙必利柠檬酰胺在有关物质液相检测条件下显示的2个色谱峰进行研究,为枸橼酸莫沙必利片后续相关质量标准研究提供参考。现报道如下。
1 仪器与试药
1.1 仪器
Waters ACQ -2489 型高效液相色谱仪,配备紫外检测器(美国Waters 公司);超高效液相色谱-四极杆串联飞行时间质谱联用仪,包括1290 型超高压液相色谱系统(配备DAD 检测器)、6540BQ-TOF 型四极杆串联飞行时间质谱系统(配备电喷雾离子源)、Mass Hunter工作站软件(美国Agilent 公司);XS105 型电子天平、S210型酸度计(瑞士Mettler Toledo公司)。
1.2 试药
枸橼酸莫沙必利片(自制,批号分别为170701,170702,170703);莫沙必利柠檬酰胺对照品(加拿大TRC 公司,批号为15 -THT -139 -2,含量94.54%);甲酸、乙酸铵、乙腈均为色谱纯;其余试剂均为分析纯;水为超纯水。
2 方法与结果
2.1 检测条件
2.1.1 HPLC 条件
色谱柱:Agilent C18柱(150 mm × 4.6 mm,5 μm);检测器:紫外检测器;流动相:枸橼酸盐溶液(A,取枸橼酸钠8.82 g,加水800 mL 使溶解,用稀盐酸调pH 至4.0,加水至1 000 mL)-乙腈(B),梯度洗脱(洗脱程序见表1);流速:1.0 mL/ min;检测波长:274 nm;柱温:30 ℃;进样量:10 μL。理论板数按莫沙必利峰计应不低于40 000。

表1 梯度洗脱程序Tab.1 Gradient elution program
2.1.2 UPLC-Q-TOF-MS 条件
色谱条件:色谱柱为YMC-Triant C18柱(150 mm×2.1 mm,1.9 μm);检测器为DAD 检测器;流动相为含0.1%甲酸的10 mmol/L 乙酸铵(A)-乙腈(B),梯度洗脱(洗脱程序见表2);流速为0.5 mL/min;检测波长为274 nm;柱温为40 ℃;进样量为0.5 μL。
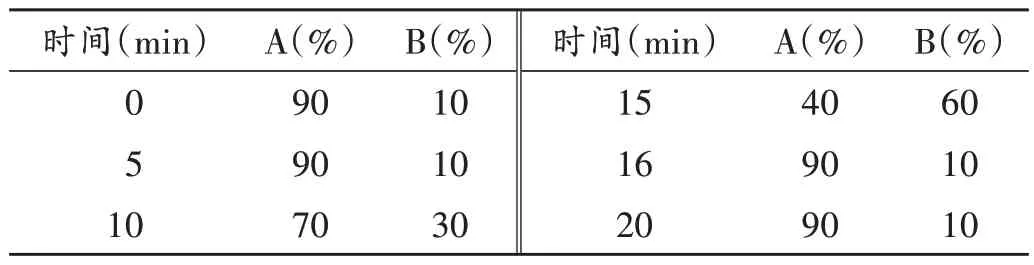
表2 梯度洗脱程序Tab.2 Gradient elution program
质谱条件:电喷雾离子源,正离子扫描模式(ESI+);二级质谱碰撞能量30 eV;毛细管电压4 kV;锥孔电压45 V;碎裂电压60 V;干燥气流速8 mL/min;干燥气温度300 ℃;雾化气压力35 psi;扫描模式MS/MS;扫描范围m/z50~700。
2.2 溶液制备
取样品细粉适量,精密称定,加乙腈-水(40∶60,V/V)溶解并稀释,制成每1 mL 中约含枸橼酸莫沙必利1 mg 的溶液,滤过,取续滤液,即得供试品溶液。精密量取适量供试品溶液,用乙腈-水(40∶60,V/V)定量稀释,制成每1 mL 中约含5 μg 的溶液,即得对照溶液。取莫沙必利柠檬酰胺对照品约10 mg,精密称定,置20 mL容量瓶中,加乙腈-水(40∶60,V/V)溶解并定容,摇匀,即得对照品溶液。
2.3 有关物质检测
精密量取2.2 项下对照溶液适量,按2.1.1 项下HPLC 条件进样,调节检测灵敏度,使主成分色谱峰的峰高为满量程的10%~20%;再精密量取2.2 项下供试品溶液和对照溶液,按2.1.1 项下HPLC 条件进样测定,记录色谱图,见图1,分别按保留时间定位主峰及各杂质峰。可见,莫沙必利柠檬酰胺峰定位处显示2 个明显的色谱峰,保留时间分别为8.434 min 和8.665 min。有文献指出,莫沙必利柠檬酰胺为一对对映异构体,在色谱行为上表现为2个峰[9]。但从莫沙必利柠檬酰胺结构看并非如此(因不含手性中心)。因此,其色谱图中出现双峰的原因仍需进一步研究。

图1 样品有关物质高效液相色谱图Fig.1 HPLC chromatograms of related substances in samples
2.4 双峰质谱解析
取2.2项下对照品溶液适量,按2.1.2项下UPLCQ -TOF -MS 条件进样分析,记录液相色谱图及一级(MS1)和二级(MS2)质谱图,见图2和图3。

图2 对照品溶液高效液相色谱图1,2.Mosapride citric amideFig.2 HPLC chromatogram of reference substance

图3 对照品溶液质谱图1,2.Mosapride citric amideA,C.MS1 B,D.MS2Fig.3 Mass spectra of reference substance
液相色谱图中在12.70 min 和12.76 min 处各出现1 个峰,分别命名为1 号峰和2 号峰。2 个峰一级质谱分子量均与莫沙必利柠檬酰胺相当,二级质谱主要碎片峰离子丰度相当,峰形相似,分子量均高度一致。初步推断两个色谱峰均为莫沙必利柠檬酰胺。
解析质谱,推断莫沙必利柠檬酰胺可能有多种裂解途径(如图4)。按途径a 进行碎裂,失去右侧C20H26ClFN3O9基团后生成碎片m/z109.04,元素组成为C7H6F+。另外可能按途径b 失去左侧C12H17FN2O 基团后生成碎片m/z372.05,进而继续破裂,生成1 个碎片m/z175.02,元素组成为C6H7O6+;另一碎片获得1 个氢得到碎片m/z198.03,元素组成为C9H9ClNO2+。莫沙必利柠檬酰胺可能的裂解碎片分子量与质谱图中二级碎片离子分子量一致,吻合度较高,因此进一步确定2个峰均为莫沙必利柠檬酰胺。
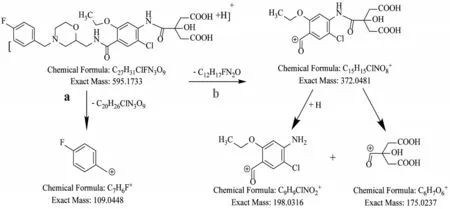
图4 莫沙必利柠檬酰胺可能的裂解途径Fig.4 Possible fragmentation pathway of mosapride citric amide
2.5 双峰存在型式确认
本研究中所用的莫沙必利柠檬酰胺对照品为莫沙必利柠檬酰胺二钠盐,羧酸钠盐为弱酸强碱盐,溶液状态时存在解离现象,在流动相pH 环境中可能有3 种存在型式,各型式之间存在解离平衡,见图5。调节流动相A的pH 分别为2.5,3.0,3.5,3.8,4.0,4.2,4.5,5.0,5.5,6.5,取2.2 项下对照品溶液,按2.1.1 项下HPLC条件进样分析,结果见表3。
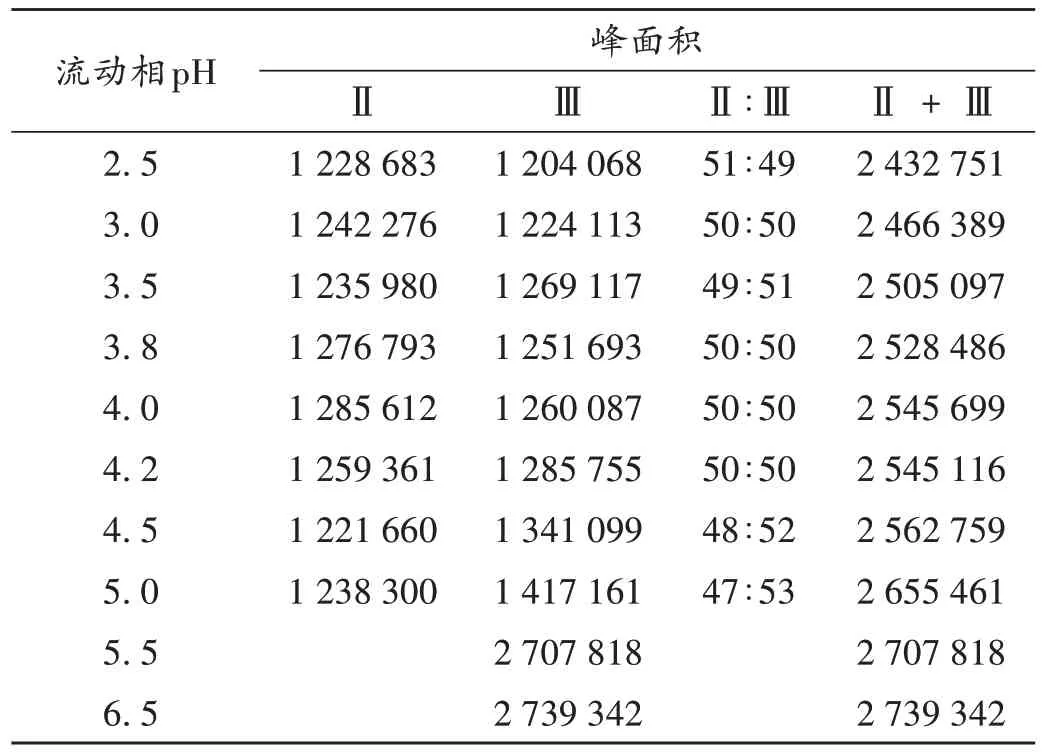
表3 不同流动相pH下莫沙必利柠檬酰胺对照品溶液峰面积Tab.3 The peak area of mosapride citric amide reference substance under different pH values and mobile phases
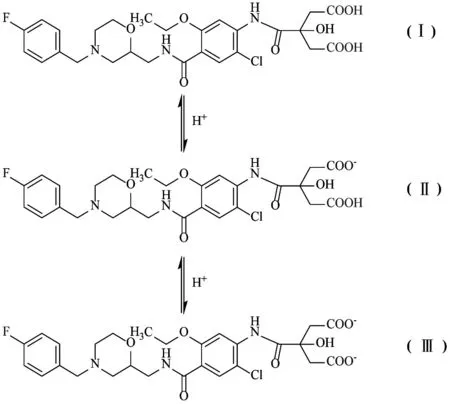
图5 莫沙必利柠檬酰胺对照品溶液可能存在的解离平衡Fig.5 Possible dissociation equilibrium of mosapride citric amide reference substance
根据莫沙必利柠檬酰胺分子结构特征推测,其未解离型式(Ⅰ)仅在低pH 环境中稳定存在。在有关物质色谱项下的pH 环境中,主要以Ⅱ和Ⅲ两种型式存在。在不同pH 环境中,Ⅱ和Ⅲ的比例不同,出峰时间略有差异,液相色谱图峰面积比例也发生显著变化。当流动相A 的pH 在2.5~5.0 范围内,液相谱图中莫沙必利柠檬酰胺始终表现为双峰,即以Ⅱ和Ⅲ两种型式存在;随着流动相pH 的升高,型式Ⅲ的峰面积相对增大,而型式Ⅱ的峰面积相对减小;当流动相A 的pH ≥5.5时,莫沙必利柠檬酰胺液相色谱图由双峰变成单峰,此时2 个羧酸根已完全解离,主要以解离的型式(Ⅲ)存在。因此,莫沙必利柠檬酰胺在有关物质检查液相色谱条件下(pH 4.0)显示双峰。
2.6 方法学考察
线性关系考察:精密量取2.2项下对照品溶液5 mL,置50 mL 容量瓶中,加乙腈-水(40∶60,V/V)定容,摇匀,即得对照品贮备液;精密量取0.1,0.3,0.6,0.8,1.0,1.5,2.0 mL,分别置10 mL 容量瓶中,加乙腈-水(40∶60,V/V)定容,摇匀,制得系列对照品溶液。按2.1.1 项下HPLC 条件进样分析,以峰面积(A)为纵坐标,莫沙必利柠檬酰胺质量浓度(C,μg/mL)为横坐标进行线性回归,得回归方程A=12 926.72C-926.87(r=0.999 7,n=7)。结果表明,莫沙必利柠檬酰胺质量浓度在0.35~7.00 μg/ mL(相当于供试品溶液0.035%~0.70%)范围内与峰面积线性关系良好。根据线性回归方程中的斜率,计算莫沙必利柠檬酰胺校正因子为1.10,在0.9~1.1范围内,可采用不加校正因子的主成分自身对照法计算该杂质含量。
强制降解试验:称取样品细粉适量(约相当于枸橼酸莫沙必利10 mg),精密称定,置10 mL容量瓶中,平行5 份,分别进行热降解(80 ℃烘箱下放置48 h,溶剂定容)、酸降解(2 mL 溶剂,1 mL 1 mol/ L HCl,90 ℃加热30 min,冷却中和,溶剂定容)、氧化降解(2 mL 溶剂,2 mL 3%H2O2,90 ℃加热5 min,冷却,溶剂定容)、碱降解(2 mL溶剂,1 mL 0.1 mol/L NaOH,90 ℃加热10 min,冷却中和,溶剂定容)、光降解(溶剂定容,4 500 lx 光照箱中照射64 h)试验。按2.1.1 项下HPLC 条件进样分析,记录色谱图。结果表明在该色谱条件下主峰与相邻杂质峰之间的分离度符合要求。
定量限和检测限考察:取2.2 项下对照品溶液适量,逐级稀释,按2.1.1 项下HPLC 条件进样分析,记录峰面积。以信噪比(S/N)约为3 或10 时待测成分的进样量分别作为检测限与定量限,结果莫沙必利柠檬酰胺的检测限为0.70 ng,定量限为2.8 ng。
精密度试验:精密量取2.6项下对照品贮备液0.2,1.0,1.5 mL,分别置10 mL 容量瓶中,加乙腈-水(40∶60,V/V)定容,摇匀,作为精密度20%,100%,150%的供试品溶液,各平行3 份,按2.1.1 项下HPLC条件进样分析,记录峰面积。结果莫沙必利柠檬酰胺峰面积的RSD分别为3.96%、0.07%、0.45%(n=3),表明在20%~150% 体积分数范围内仪器精密度较好。
耐用性考察:取2.2项下对照品溶液适量,按2.1.1项下HPLC 条件进样分析。调节流动相A 的pH 为3.8,4.0,4.2,记录莫沙必利柠檬酰胺峰面积之和的变化,考察方法耐用性。结果,流动相A 的pH 在3.8~4.2 范围内变化时,莫沙必利柠檬酰胺双峰总面积的RSD为0.38%,证明该方法耐用性良好。
2.7 样品含量测定
取3批样品适量,各平行3份,分别按2.2项下方法制备供试品溶液,按2.1.1 项下HPLC 条件进样分析,记录峰面积,计算含量。结果批号170701,170702,170703 样品中莫沙必利柠檬酰胺含量分别为0.006%,0.005%,0.007%。
3 讨论
3.1 双峰定性
杂质检测是药物质量控制的关键。液质联用技术在杂质谱分析中的应用越来越广泛,可推测药物中存在的未知杂质结构[10-12]。本研究中建立的UPLC-QTOF-MS 法可有效地对枸橼酸莫沙必利片有关物质色谱图中莫沙必利柠檬酰胺的2个峰进行定性研究,可推导出两个峰的结构。通过一级质谱图可知,两个峰的分子量均与莫沙必利柠檬酰胺一致;进一步推测莫沙必利柠檬酰胺可能的裂解途径,各裂解碎片离子分子量与二级质谱图中二级碎片离子分子量相当,确定色谱图中双峰均为莫沙必利柠檬酰胺峰。
3.2 双峰分析
从莫沙必利柠檬酰胺结构看,其含有2 个羧酸基团,进入液相后,与流动相中的钠离子生成羧酸钠盐,羧酸钠盐为弱酸强碱盐,在不同pH 流动相中发生解离,可能存在保留时间各异的未解离(Ⅰ)、部分解离(Ⅱ)及完全解离(Ⅲ)3 种型式。随着pH 的改变,各型式之间相互转化,液相色谱图中各峰面积的比例也发生显著变化[13]。确定莫沙必利柠檬酰胺双峰现象为其羧酸钠盐的不完全解离所致,液相谱图中双峰为莫沙必利柠檬酰胺的两种存在型式(Ⅱ和Ⅲ),各型式之间存在解离平衡,在一定pH 条件下可相互转化。这在一定程度上可为“色谱图中,同一物质出现双峰”的研究提供新的思路。
3.3 方法评价
本研究中建立了枸橼酸莫沙必利片有关物质检查的UPLC-Q-TOF-MS 法,并以此对特定杂质莫沙必利柠檬酰胺进行研究。采用不加校正因子的主成分自身对照法能快速、有效地检出该杂质。色谱图中双峰均为莫沙必利柠檬酰胺,定量时以两个峰面积之和计算,不会影响该杂质校正因子计算和检测结果。因此,本研究可为枸橼酸莫沙必利片杂质研究及其质量控制提供参考。

