晶格铁在含铁水镁石碳酸盐化中的作用
赵世凤,赵文慧,吴智明,廖立兵,吕凤柱
(非金属矿物与固体废物材料利用北京市重点实验室,矿物材料国家重点实验室,中国地质大学(北京)材料科学与工程学院, 北京 100083)
1 引 言

水镁石在低温和低CO2分压下便能与CO2迅速反应[6-7],发生碳酸盐化。目前已有较多研究者在实验室模拟自然环境研究了水镁石碳酸盐化[8-10]和水镁石中Mg(OH)2组分对CO2固定作用。但较少涉及关于含铁水镁石在CO2存在下的演化。Hostetler等[11]报道了含铁水镁石在地下水中与CO2反应向菱水碳铁镁石[Mg6Fe2CO3(OH)16·4H2O,MgFe-LDHs,层状双氢氧化物]的转化过程。Boschi等[3]发现在富含铁水镁石的蛇纹石化区域,可形成大量LDHs和少量水菱镁石;在贫铁水镁石区域形成大量水菱镁石和少量LDHs。虽然目前已有关于含铁水镁石与CO2反应向MgFe-LDHs转化的报道,但在CO2存在下,含铁水镁石演化规律还没有系统报道,尤其是含铁水镁石在不同氛围下向LDHs演化机理尚不明确。
为探究含铁水镁石在CO2存在下演化规律,本研究以实验室制备的铁含量较高的含铁水镁石为研究对象,研究了其在溶液中,仅CO2存在,O2和CO2充足情况下的演化规律,并辅以模拟计算进行验证,揭示了CO2存在下含铁水镁石演化过程和规律。
2 实验材料与方法
2.1 含铁水镁石的制备
将1.42 g MgCl2·6H2O溶于100 mL纯水中,通N210 min后将0.4 g抗坏血酸和0.35 g FeCl2·4H2O溶于其中,缓慢调节pH值为9~10后继续通N210 min,密封陈化24 h,用乙醇清洗数次,离心,30 ℃真空干燥,即得到含铁水镁石样品,命名为MgFe(OH)2-R。
将1.42 g MgCl2·6H2O溶于100 mL纯水中,通N210 min后将0.59 g FeCl2·4H2O溶于其中,调节pH值为9~10后,在N2氛围下陈化24 h,洗涤干燥后得到晶体铁含量与MgFe(OH)2-R相当的样品MgFe(OH)2-0。
2.2 水镁石与含铁水镁石的演化
将陈化24 h后的含铁水镁石悬浊液通CO2,反应12 h后,离心,室温真空干燥得MgFe(OH)2-1。将0.20 g干燥的MgFe(OH)2-0样品置于100 mL纯水中,通CO2和O2混合气体,反应12 h后室温真空干燥,得MgFe(OH)2-2。Mg(OH)2演化实验与MgFe(OH)2-0演化过程相同,当反应气体为CO2,CO2与O2混合气体时,反应后得到的样品相应的命名为Mg(OH)2-1和MgFe(OH)2-2。
2.3 Materials Studio计算
利用Materials Studio软件在CASTEP程序中利用Perdew-Burke-Ernzerhof (PBE)和generalized gradient approximation (GGA)密度泛函进行分子模拟,计算水镁石,含铁水镁石的结合能和电荷密度差。
2.4 样品表征
使用BRUCKER D8 ADVANCE型X射线衍射仪(XRD)分析样品的物相组成;使用Hysitron TI 950型扫描电子显微镜(SEM)观察样品的微观形貌;使用Thermo escalab 250Xi型 X 射线光电子能谱仪(XPS)分析样品的组成和价态;使用ARLAdvantX IntellipowerTM3600型X射线荧光光谱仪(XRF)分析样品的元素占比;使用Zetasizer Nano ZS90型激光粒度仪测试样品的Zeta电位。
3 结果与讨论
3.1 含铁水镁石的结构和组成表征
利用XPF和XPS结合分析测定样品的元素组成,结果见表1。表1表明样品都含有Fe、Mg、O等元素,MgFe(OH)2-R中Mg∶Fe=34.95∶28.32,MgFe(OH)2-0中Mg∶Fe=23.08∶23.97。

表1 MgFe(OH)2-R和MgFe(OH)2-0的元素组成

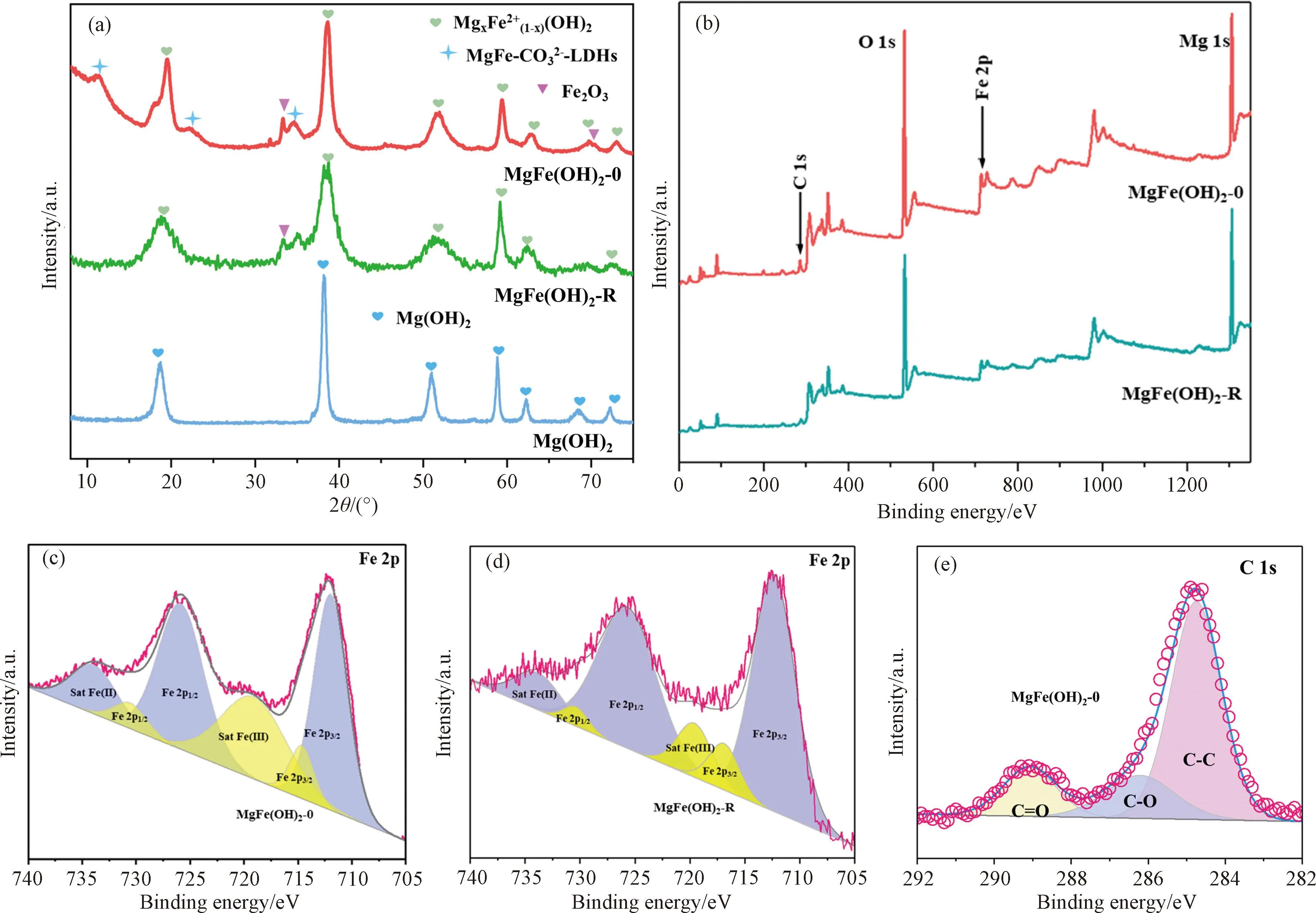
图1 Mg(OH)2,MgFe(OH)2-0,和MgFe(OH)2-R的XRD谱图(a),XPS谱图(b),MgFe(OH)2-0(c)和MgFe(OH)2-R(d)的Fe 2p谱图,MgFe(OH)2-0的C 1s谱图(e)
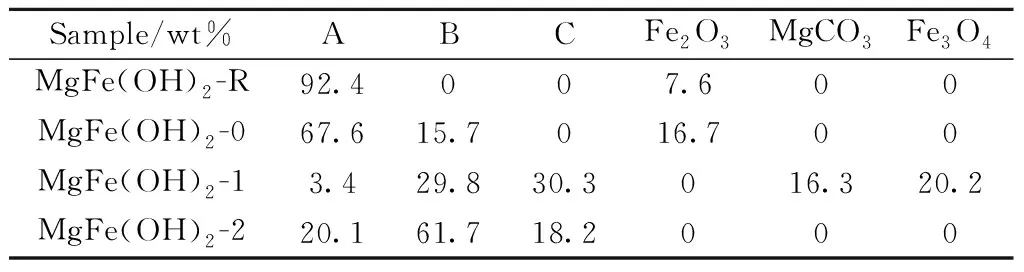
表2 基于XRD测试确定的MgFe(OH)2-X的组成



图2 MgFe(OH)2-0的SEM照片(a, b),MgFe(OH)2-0和Mg(OH)2的Zeta电位图 (c)
3.2 含铁水镁石在CO2存在下的演化机理


图3 MgFe(OH)2-0和Mg(OH)2分别经CO2,O2与CO2 混合体系处理后形成的MgFe(OH)2-1(a),MgFe(OH)2-2(b),Mg(OH)2-1(c)和Mg(OH)2-2(d)的XRD图谱


图4 MgFe(OH)2-1和MgFe(OH)2-2的XPS谱图(a),Fe 2p谱图(b1,b2),O 1s谱图(c1,c2),C 1s谱图(d1,d2)和Mg 1s谱图(e1,e2)

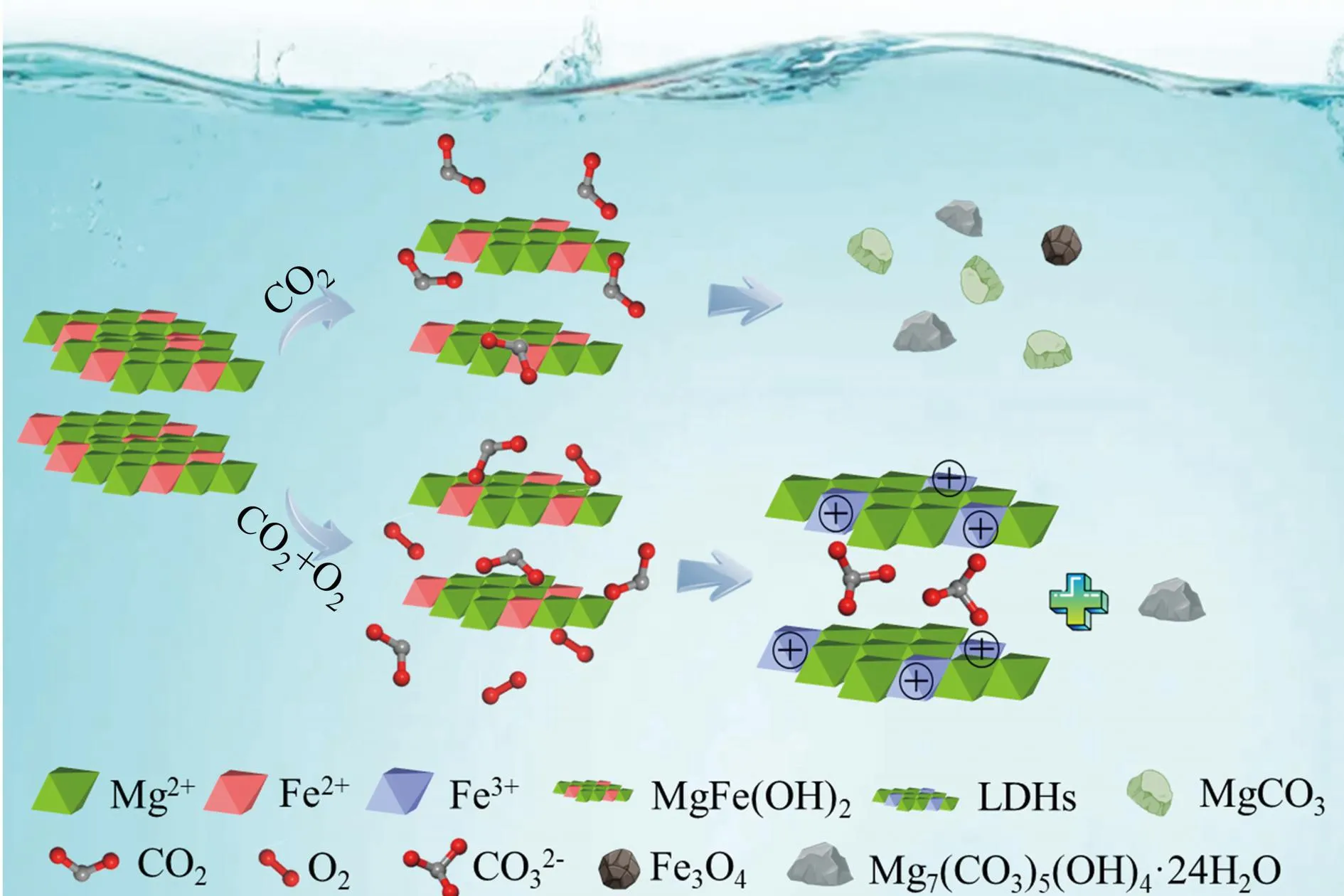
图5 MgFe(OH)2-0在不同气体气氛下的反应示意图
为了验证含铁水镁石晶格Fe2+在水镁石转化过程中的作用,利用Materials Studio软件从结合能及电子转移的角度进行分析。分子模拟结果如图6所示。图6中黄色和蓝色区域分别对应着电子密度的消耗和积累[15]。从电子密度差图可以直观的看到CO2吸附在Mg(OH)2和MgFe-(OH)2-0表面后原子之间的电子重排。CO2在MgFe-(OH)2-0表面时电子密度的消耗和积累更明显,表明他们之间的作用力更强。结合能的大小可以更清楚地反映反应物与吸附剂之间结合能力的强弱,其计算公式如下式所示:

图6 Mg(OH)2 (a),MgFe-(OH)2-0(b)与CO2,MgFe-(OH)2-0 (c),MgFe(III)-(OH)2 (d)与的电子密度差图(本刊纸质版为黑白版,电子版为彩色版)
Ead=Etotal-ECO2-EMg(OH)2/EMg(OH)2-0
(1)
式中:Etotal表示整个体系的能量,EMg(OH)2/MgFe(OH)2-0和ECO2分别代表Mg(OH)2,MgFe(OH)2-0和CO2的能量[16]。

4 结 论


