司美格鲁肽治疗成人非2型糖尿病超重和肥胖患者效果的Meta分析
双丹丹 张惠莉
1 青海大学研究生院(西宁810016);2 青海大学附属医院内分泌科(西宁810012)
在肥胖被定义为一种慢性疾病之前经历了一个漫长的过程。此前,肥胖被普遍认为是个人生活方式选择的结果。随着对肥胖的研究越来越深入,人们逐渐认识到肥胖与多种慢性疾病相关。最终,在2013年美国医学协会将肥胖定义为一种需要一系列干预措施去预防和治疗的疾病[1]。肥胖会缩短人类预期寿命,引起全身许多器官功能受损,与多种慢性疾病相关,比如,2 型糖尿病、心血管系统疾病、慢性肾脏病、非酒精性脂肪肝、骨关节炎、高尿酸血症等[2-5]。目前已有证据表明减重可以降低与肥胖相关疾病的发病率和死亡风险[6]。生活方式干预是减重的首选治疗,也是基础治疗,但是仅通过生活方式干预减重依从性差而导致效果不佳;在生活方式干预的基础上进行药物治疗,有着比单纯改变生活方式更好的减重效果[7]。
目前市面上的减重药物疗效和安全性不尽相同,胰高血糖素样肽-1 受体激动剂(GLP-1RAs)因其优越的减重效果和安全性被认为是最具前景的减重药物之一[8]。GLP-1RAs 最早被用于2 型糖尿病的治疗,随着研究的深入发现该类降糖药还具有减重作用,当前被美国食品与药物管理局批准的用于减重的GLP-1RAs 仅有利拉鲁肽和司美格鲁肽。司美格鲁肽是一种新型长效GLP-1RAs,2021年司美格鲁肽(每周2.4 mg)被批准用于体质指数(BMI)≥27 kg/m2且至少患有一种体重相关疾病(如高血压、2 型糖尿病或高胆固醇)的患者或BMI ≥30 kg/m2以上的患者的慢性体重管理,比利拉鲁肽具有更长的半衰期,仅需每周给药1 次。此前已有不少关于司美格鲁肽减重有效性和安全性的Meta分析,但都是与安慰剂或其他减重药物进行对比,尚无司美格鲁肽与利拉鲁肽减重效果单独对比的Meta分析。本文对近年来司美格鲁肽皮下注射用于减重的研究进行Meta 分析,不仅评价了司美格鲁肽相比安慰剂在成人非2型糖尿病超重和肥胖患者中的减重效果,还单独评价了司美格鲁肽相比利拉鲁肽在目标人群中的减重效果,为临床实践提供循证依据。
1 资料与方法
1.1 检索策略检索Cochrane Library、Embase、
PubMed、中国知网、万方数据知识服务平台及中国生物医学文献服务系统等六大数据库,检索时间从建库至2022年4月。英文检索词包括“semaglutide,Ozempic,rybelsus,obesity,overweight,clinical trial,randomized controlled trial”,中文检索词包括“司美鲁肽、索马鲁肽、司美格鲁肽、超重、肥胖”。最后,手工检索其他相关会议报告、灰色文献及杂志。
1.2 文献纳入和排除标准
1.2.1 纳入标准(1)研究类型为随机对照试验(RCTs);(2)以成人非2型糖尿病超重和肥胖患者为研究对象;(3)试验组干预措施为司美格鲁肽,对照组干预措施为安慰剂或其他药物,全程单药治疗,且疗程≥52 周;(4)主要结局指标包括体质量下降百分比或体质量下降≥5%的患者比例,次要结局指标包括体质量下降值或体质量下降≥10%的患者比例或体质量下降≥15%的患者比例;(5)文献语种为英语或中文。
1.2.2 排除标准(1)重复多次发表的文献;(2)信息报告不全或无法提取数据的文献。
1.3 资料提取由2 名研究人员严格依据纳入和排除标准独立进行筛选文献、提取资料及质量评价,如遇分歧讨论解决或由第三方协助裁决。从最终纳入研究中提取以下资料:第一作者、发表年份、病例数量、年龄、BMI、试验组及对照组干预措施、疗程、主要结局指标、次要结局指标。
1.4 方法学质量评价采用Cochrane 系统评价员手册6.3 偏倚风险评估工具和评价标准对纳入研究进行方法学质量评价,包括:(1)随机序列的产生方法;(2)分配是否实施隐藏;(3)研究者和受试者是否施盲;(4)研究结局的盲法评价;(5)结局指标数据是否完整;(6)是否存在选择性报告的研究结果;(7)是否有其他来源的偏倚[9]。如遇分歧讨论解决或由第三方协助裁决。
1.5 统计学方法运用RevMan 5.4.1 对纳入研究进行Meta 分析。计量资料用均数(mean difference,MD)作为效应统计量,计数资料用比值比(OR)或相对危险度(RR)作为效应统计量,各效应量均用95%置信区间(CI)表达,以P<0.05 差异有统计学意义。采用χ2检验对纳入研究进行异质性检验,通过I2定量判断异质性的大小,若I2<50%、P>0.1,认为纳入研究间异质性小,选用固定效应模型;若I2>50%、P≤0.1,认为纳入研究间异质性较大,选用随机效应模型。最后,行敏感性分析检验Meta 分析结果的稳定性。
2 结果
2.1 文献筛选结果共检索到文献607 篇,其中英文文献569 篇,中文文献38 篇。根据纳入和排除标准,最终筛选出6 篇文献,均为英文文献。6 篇文献报道了6项RCTs,共计纳入4 137例成人非2型糖尿病超重和肥胖患者。文献筛选流程见图1,纳入RCTs 的基本信息见表1。
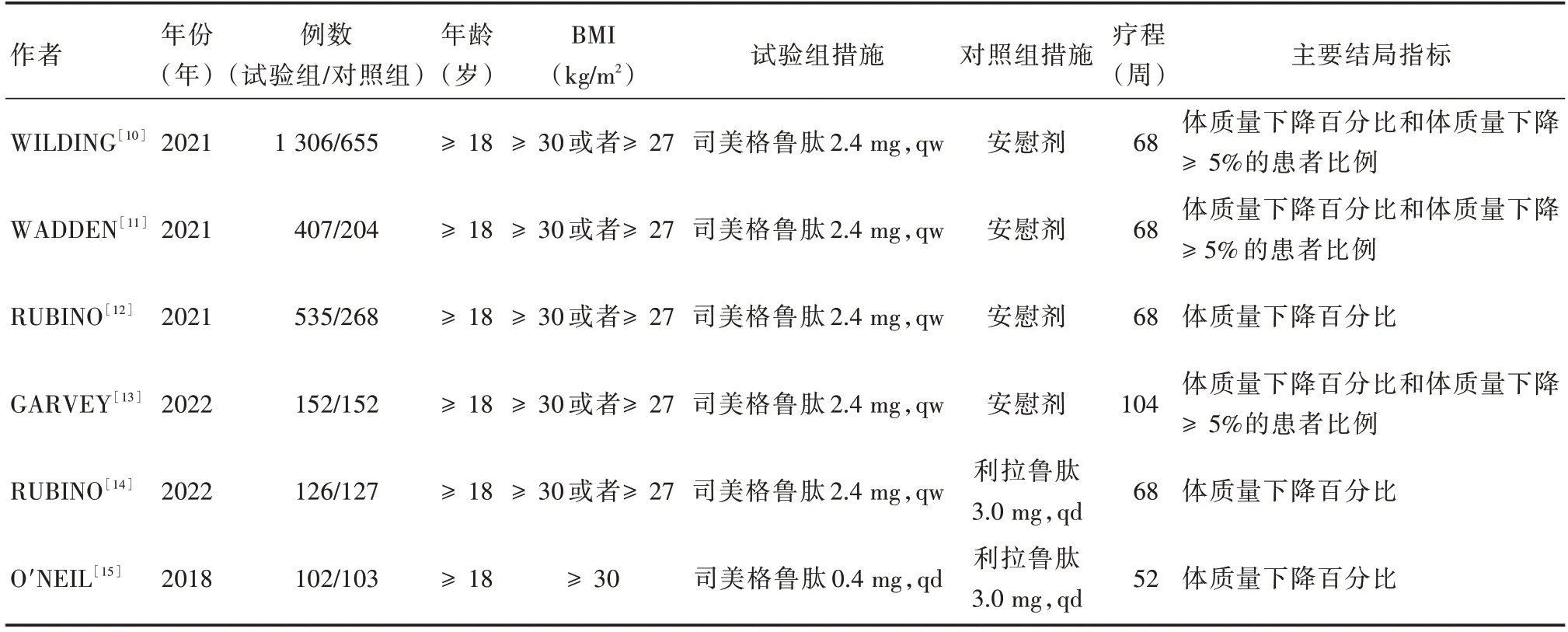
表1 纳入RCTs 基本信息Tab.1 Basic informations of included RCTs
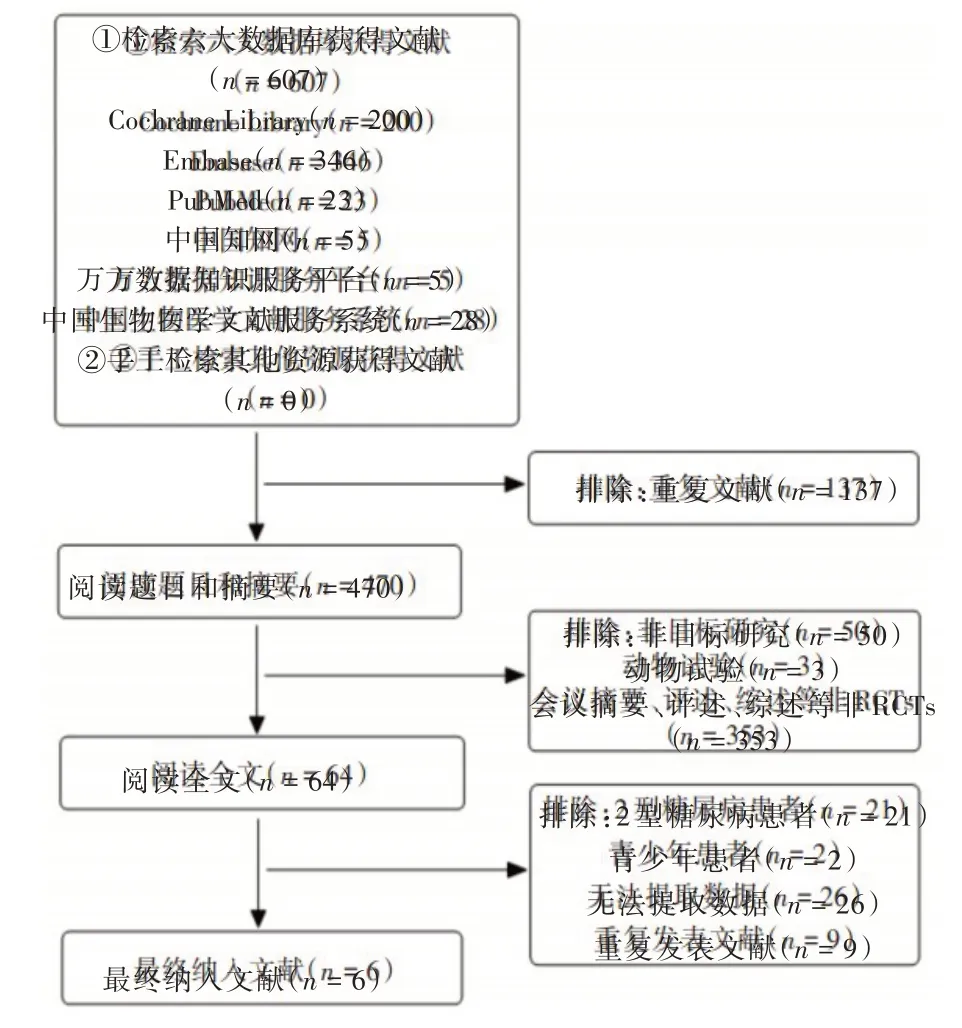
图1 文献筛选流程Fig.1 Document screening process
2.2 方法学质量评价结果对纳入的RCTs 进行方法学质量评价,其中有2 项RCTs(Rubino 2022 和O′Neil 2018),由于试验组和对照组的药物剂量和给药频次不同,可能导致盲法实施偏倚,从而对结局造成一定的影响。除此之外,纳入的RCTs 整体上质量较高,结果见表2。

表2 纳入RCTs 方法学质量评价Tab.2 Methodological quality evaluation of included RCTs
2.3 Meta 分析结果纳入文献中4 项RCTs 以安慰剂为对照,2 项RCTs 以利拉鲁肽为对照,根据对照措施的不同,分别进行分析。
2.3.1 体质量下降百分比6 项RCTs 均报道了患者体质量下降百分比。其中4 项RCTs(3 393 例患者)为司美格鲁肽与安慰剂对比,各项RCTs 间异质性小(P= 0.23,I2= 30%),故选用固定效应模型,结果见图2;2 项RCTs(439 例患者)为司美格鲁肽与利拉鲁肽对比,2 项RCTs 间异质性小(P=0.40,I2= 0),故选用固定效应模型,结果见图3。Meta 分析结果显示,司美格鲁肽组体质量下降百分比显著高于安慰剂组,差异有统计学意义[MD=-12.87,95%CI(-14.28~-11.46),P<0.05];同时,司美格鲁肽组体质量下降百分比也高于利拉鲁肽组,差异有统计学意义[MD = -7.18,95%CI(-10.95~-3.41),P<0.05]。
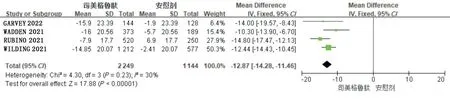
图2 司美格鲁肽与安慰剂对比体质量下降百分比的森林图Fig.2 Forest Plot of the percentage of body mass reduction of smeglutide vs placebo

图3 司美格鲁肽与利拉鲁肽对比体质量下降百分比的森林图Fig.3 Forest Plot of the percentage of body mass reduction of smeglutide vs liraglutide
2.3.2 体质量下降值有5项RCTs报道了患者体质量下降值。其中3项RCTs(3 121例患者)为司美格鲁肽与安慰剂对比,各项RCTs 间异质性小(P=0.54,I2= 0),故选用固定效应模型,结果见图4;2 项RCTs(439 例患者)为司美格鲁肽与利拉鲁肽对比,2 项RCTs 间异质性小(P=0.55,I2=0),故选用固定效应模型,结果见图5。Meta 分析结果显示,司美格鲁肽组体质量下降值显著大于安慰剂组,差异有统计学意义[MD = -12.58,95%CI(-14.07~-11.09),P<0.05];同时,司美格鲁肽组体质量下降值也大于利拉鲁肽组,差异有统计学意义[MD = -7.23,95%CI(-9.99~-4.48),P<0.05]。
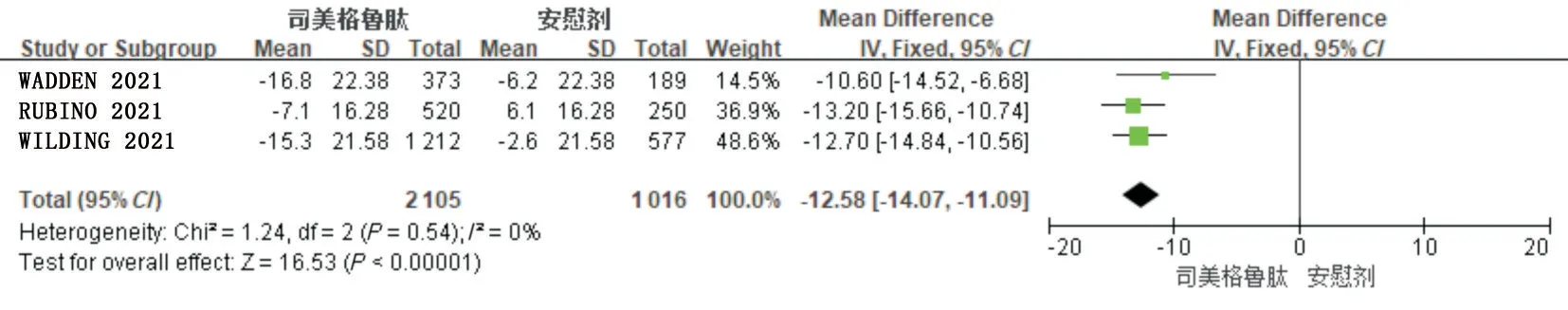
图4 司美格鲁肽与安慰剂对比体质量下降值的森林图Fig.4 Forest Plot of body mass reduction of smeglutide vs placebo
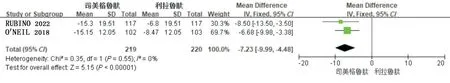
图5 司美格鲁肽与利拉鲁肽对比体质量下降值的森林图Fig.5 Forest Plot of body mass reduction of smeglutide vs liraglutide
2.3.3 体质量下降≥5%的患者比例6 项RCTs 均报道了体质量下降≥5%的患者比例。其中4 项RCTs(3 393 例患者)为司美格鲁肽与安慰剂对比,各项RCTs 间存在异质性(P= 0.005,I2= 76%),故选用随机效应模型,结果见图6;2 项RCTs(439 例患者)为司美格鲁肽与利拉鲁肽对比,2 项RCTs 间异质性小(P=0.17,I2=46%),选用固定效应模型,结果见图7。Meta 分析结果显示,司美格鲁肽组体质量下降≥5%的患者比例显著高于安慰剂组,差异有统计学意义[OR=8.90,95%CI(6.08~13.04),P<0.05];同时,司美格鲁肽组体质量下降≥5%的患者比例也高于利拉鲁肽组,差异有统计学意义[OR= 3.59,95%CI(2.26~5.69),P<0.05]。
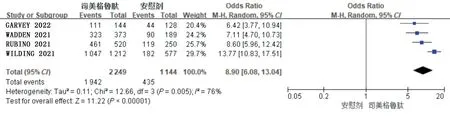
图6 司美格鲁肽与安慰剂对比体质量下降≥5%的患者比例森林图Fig.6 Forest Plot of the proportion of patients with body mass reduction ≥5% of smeglutide vs placebo

图7 司美格鲁肽与利拉鲁肽对比体质量下降≥5%的患者比例森林图Fig.7 Forest Plot of the proportion of patients with body mass reduction ≥5% of smeglutide vs liraglutide
2.3.4 体质量下降≥10%的患者比例6 项RCTs均报道了体质量下降≥10%的患者比例。其中4 项RCTs(3 393 例患者)为司美格鲁肽与安慰剂对比,各项RCTs 间存在异质性(P= 0.03,I2= 65%),故选用随机效应模型,结果见图8;2 项RCTs(439 例患者)为司美格鲁肽与利拉鲁肽对比,2 项RCTs间存在异质性(P= 0.10,I2= 63%),故选用随机效应模型,结果见图9。Meta 分析结果显示,司美格鲁肽组体质量下降≥10%的患者比例显著高于安慰剂组,差异有统计学意义[OR= 12.45,95%CI(8.91,17.39),P<0.05];同时,司美格鲁肽组体质量下降≥10%的患者比例也高于利拉鲁肽组,差异有统计学意义[OR= 5.02,95%CI(2.56,9.84),P<0.05]。
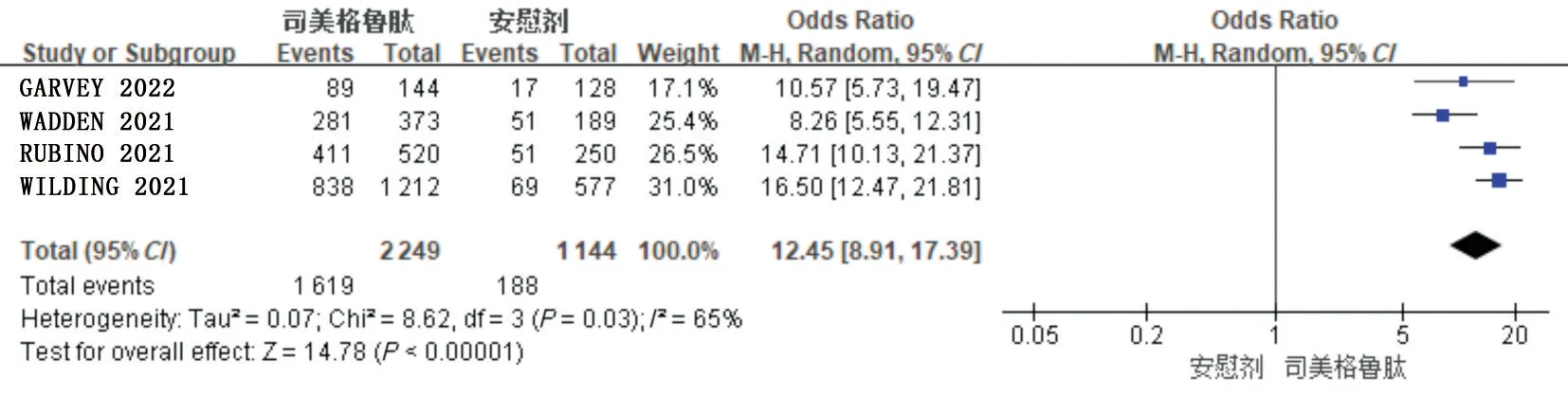
图8 司美格鲁肽与安慰剂对比体质量下降≥10%的患者比例森林图Fig.8 Forest Plot of the proportion of patients with body mass reduction ≥10% of smeglutide vs placebo
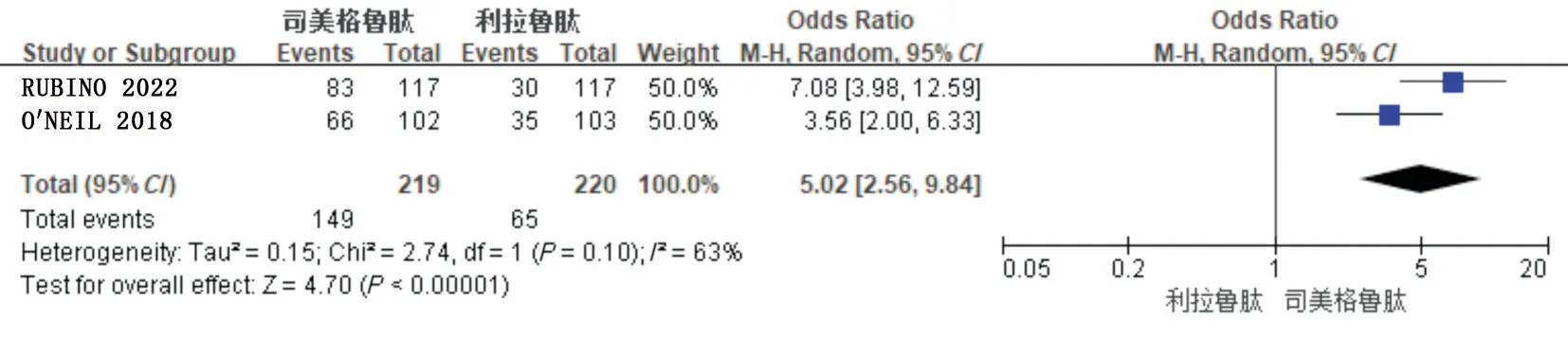
图9 司美格鲁肽与利拉鲁肽对比体质量下降≥10%的患者比例森林图Fig.9 Forest Plot of the proportion of patients with body mass reduction ≥10% of smeglutide vs liraglutide
2.3.5 体质量下降≥15%的患者比例6 项RCTs均报道了体质量下降≥15%的患者比例。其中4项RCTs(3 393 例患者)为司美格鲁肽与安慰剂对比,各项RCTs 间存在异质性(P= 0.03,I2= 66%),故选用随机效应模型,结果见图10;2 项RCTs(439 例患者)为司美格鲁肽与利拉鲁肽对比,2 项RCTs 间异质性小(P= 0.18,I2= 43%),故选用固定效应模型,结果见图11。Meta 分析结果显示,司美格鲁肽组体质量下降≥15%的患者比例显著高于安慰剂组,差异有统计学意义[OR= 14.36,95%CI(9.39~21.96),P<0.05];同时,司美格鲁肽组体质量下降≥15%的患者比例也高于利拉鲁肽组,差异有统计学意义[RR= 3.71,95%CI(2.57~5.34),P<0.05]。

图10 司美格鲁肽与安慰剂对比体质量下降≥15%的患者比例森林图Fig.10 Forest Plot of the proportion of patients with body mass reduction ≥15% of smeglutide vs placebo
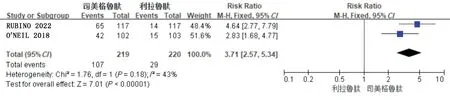
图11 司美格鲁肽与利拉鲁肽对比体质量下降≥15%的患者比例森林图Fig.11 Forest Plot of the proportion of patients with body mass reduction ≥15% of smeglutide vs liraglutide
2.4 敏感性分析采用去除单项研究法对每项指标的合并结果进行敏感性分析,逐一去除RCTs后,合并效应量未发生明显变化,故认为此Meta 分析结果比较稳健。
3 讨论
本研究共纳入6 项司美格鲁肽治疗成人非2型糖尿病超重和肥胖患者的RCTs,分别与安慰剂和利拉鲁肽进行了对比。6 项RCTs 疗程不同,但均>52 周,故按疗程≥52 周进行合并评估。与利拉鲁肽对比的2 项RCTs,司美格鲁肽注射剂量不同,其中一项司美格鲁肽注射剂量为0.4 mg/d,累计相当于2.8 mg/周,故与2.4 mg/周进行合并评估。结果显示,司美格鲁肽皮下注射(2.4 mg/周)治疗成人非2型糖尿病超重和肥胖患者有显著的减重效果,即使与利拉鲁肽相比,司美格鲁肽也有着显著的减重效果,Meta 分析结果与各原始研究文献结果一致。
胰高血糖素样肽-1(GLP-1)是一种由肠道L 细胞分泌的内源性肠促胰岛素激素。人体摄入的食物进入肠道后,刺激L 细胞使其分泌GLP-1,与周围和中枢神经系统的胰高血糖素样肽-1 受体(GLP-1R)结合发挥作用。目前只有一种已知的GLP-1R,它与GLP-1 具有高度的亲和力,广泛分布在肺、大脑、味觉细胞和远端胃肠道。GLP-1 介导的生物信息传导有2 种不同的信号通路,在脑和胰腺中,GLP-1 与GLP-1R 结合激活腺苷酸环化酶诱导的环磷酸腺苷途径(cAMP);在肌肉和肝脏中,可激活cAMP 非依赖性途径。GLP-1 的生物学作用包括参与调节血糖、心血管功能和抑制胃排空以及减少食物摄入。GLP-1 的促胰岛素作用主要通过胰腺介导,而抑制胃排空和减少食物摄入的作用主要通过迷走神经介导。分泌的GLP-1 被释放进入血液循环或淋巴管,通过旁分泌的方式作用于分布在肠黏膜的迷走神经传入神经元,将信号传导至中枢神经系统,抑制胃排空、诱导饱腹感、抑制食欲,从而减少食物的摄入。
司美格鲁肽属于GLP-1RAs,是一种人GLP-1类似物,与天然人GLP-1 具有94%的结构同源性,具有长达1 周的半衰期,可以更好地改善患者的依从性[16]。BLUNDELl 等[17]完成的一项关于司美格鲁肽为期12 周的研究,发现受试者在接受司美格鲁肽治疗全天随意膳食摄入总能量减少了24%,司美格鲁肽对能量摄入的影响与其他GLP-1RAs的研究结果一致,并且司美格鲁肽的这种效应似乎更大,认为司美格鲁肽通过直接作用于下丘脑特定的食欲控制中枢,降低食欲而导致能量摄入减少,其他可能机制包括:改善饮食控制,减少对高脂肪、高能量食物的偏好。另一项为期20 周关于司美格鲁肽对胃排空、食欲和能量摄入影响的研究,有相同的发现,司美格鲁肽能降低食欲并减少能量摄入,但未发现其对胃排空的影响[18]。在基础研究中,关于司美格鲁肽摄食调节作用的机制也有了一定的进展,它通过特定脑区域中GLP-1Rs 的介导,发挥以下作用:包括参与调节食欲、食物摄入、奖赏和食物偏好[19]。司美格鲁肽不但具有良好的减重效果,而且能改善体脂肪分布,带来积极影响,但目前关于这一作用机制的基础研究较少,有待进一步研究[20]。
本文纳入的RCTs,其方法学质量普遍较高,敏感性分析显示Meta 分析结果较稳定。除此之外,本文还具有以下优点:第一,本文所纳入的观察对象均为非2型糖尿病肥胖和超重患者,这为非2型糖尿病欲减重的患者提供了循证依据;第二,与其他关于司美格鲁肽治疗超重和肥胖的Meta分析相比,本文将司美格鲁肽与另一种目前被批准用于治疗肥胖的GLP-1RA 利拉鲁肽单独进行了对比。但本文仍存在一定的局限性,首先,由于纳入文献样本量大小不一,且由于纳入文献较少无法进行分层分析,在一些结局指标中各研究间存在一定的异质性,包括体质量下降≥5%、≥10%、≥15%的患者比例。其次,司美格鲁肽与利拉鲁肽对比只纳入了2 项RCTs,还需要今后更多临床试验的证据支持。此外,本文未对司美格鲁肽在非2型糖尿病肥胖和超重患者中的安全性进行分析,还需进一步评价司美格鲁肽在该类人群中的安全性。最后,由于司美格鲁肽在我国还未被批准用于肥胖患者的治疗,故缺乏我国成人非2型糖尿病超重和肥胖患者的临床试验证据。
综上所述,司美格鲁肽用于成人非2型糖尿病超重和肥胖患者减重效果显著,且优于利拉鲁肽。
【Author contributions】SHUANG Dandan designed and wrote the article.ZHANG Huili guided and reviewed the article,and obtained research funding support.All authors read and approved the manuscript as submitted.

