不同CO2气腹压力对腹腔镜下胃癌根治术病人体温的影响
刘 晨,桑继业,赵明明,李继忠,赵国军*
1.承德医学院,河北 067000;2.承德医学院附属医院
胃癌(gastric cancer)主要发生于胃黏膜上皮,是最常见的恶性肿瘤之一[1]。近年来,由于人们工作压力加剧、饮食结构改变等原因,胃癌病人数量逐年增多,严重危害病人健康、影响生命质量。我国癌症中心数据显示,胃癌在所有恶性肿瘤中发病率居第2 位,病死率居第3 位[2]。目前,手术治疗是治愈胃癌的有效方式,腹腔镜手术作为新型外科治疗技术,可明显改善术后效果、缓解术后疼痛[3]。但是术中时常发生的“低温预警”不容小觑,研究表明,在胃癌根治术中,病人发生低体温的概率约为82%[4]。围术期低体温可导致病人麻醉苏醒延迟,还会增加术中心脑血管系统突发疾病的风险[5]。而腹腔镜手术与传统开腹手术相比,最大的区别就是术中需建立CO2气腹以维持手术视野。对此,有学者认为随着术中CO2的不断补充病人核心体温会持续降低,并建议将CO2纳入导致术中低体温的危险因素中[6-9]。本研究通过观察不同CO2气腹压下腹腔镜胃癌根治术病人核心体温的变化,旨在为临床胃癌病人腹腔镜根治术中选择合适的气腹压力提供参考,从而降低临床低体温发生率,促进病人康复。
1 资料与方法
1.1 一般资料 选择2021 年10 月—2022 年6 月在河北省承德医学院附属医院接受腹腔镜下胃癌根治术治疗的72例胃癌病人作为研究对象,其中男53例,女19例,年龄(62.49±8.46)岁;参与本研究的病人均签订知情同意书,研究过程经过承德医学院附属医院伦理委员会通过并实施方案(编号:CYFYLL2022316)。纳入标准:符合中国临床肿瘤学会(CSCO)发布的《胃癌诊疗指南(2021)》的诊断标准;接受择期腹腔镜手术且无麻醉禁忌证。排除标准:肿瘤广泛转移伴其他脏器切除者;中转开腹者;伴有呼吸系统、心血管疾病、严重肝肾功能障碍、凝血功能障碍等其他脏器损伤或并发症者;术中输血者;因病情需要,术中调节气腹压力者;肥胖[体质指数(BMI)>23.9 kg/m2)]或消瘦(BMI<18.5 kg/m2)。随机将病人分为A组(12 mmHg,1 mmHg=0.133 kPa)和B组(14 mmHg)各36 例。A 组:男27 例,女9 例,年 龄(63.39±8.80)岁;B 组:男26 例,女10 例,年龄(61.58±8.13)岁。两组病人一般资料比较差异无统计学意义(P>0.05),具有可比性。
1.2 干预方法 两组病人均采用气管插管静脉复合麻醉,入室后监测生命体征及气道压力;手术开始后由同一组医生采用腹部5 孔操作法进行手术;两组均使用同一气腹机(厂家:德国STORZ 内窥镜公司,型号:26430520)建立人工气腹,A 组气腹压力为12 mmHg,B 组气腹压力为14 mmHg,将CO2气腹流速控制在20 L/min,直至达到设定的气腹压力值。
1.3 观察指标 ①核心体温变化情况:使用耳温仪测量病人左耳温度,测量的时间节点分别为入室时、气管插管时、手术开始时、气腹建立后10 min、气腹建立后30 min、气腹建立后60 min、气腹建立后90 min、气腹中途停止时、气腹中途停止后30 min、气腹重新建立时、手术结束时共11 个节点,比较两组病人上述节点核心体温变化情况。②低体温发生情况:比较两组病人低体温(核心体温<36.0 ℃)发生情况。
1.4 统计学方法 采用SPSS 26.0 软件对数据进行处理,符合正态分布的定量资料采用均数±标准差(±s)表示,比较采用t检验;两组病人低体温发生率比较采用χ2检验。以P<0.05 为差异有统计学意义。
2 结果
2.1 两组病人术中不同时间点核心体温比较 两组病人在入室时、气管插管时及手术开始时的核心体温差异无统计学意义(P>0.05);但在气腹建立后10 min至手术结束时各时间节点B 组病人核心体温均显著低于A 组,差异有统计学意义(P<0.05),见表1。
表1 两组病人术中不同时间点核心体温比较(±s) 单位:℃
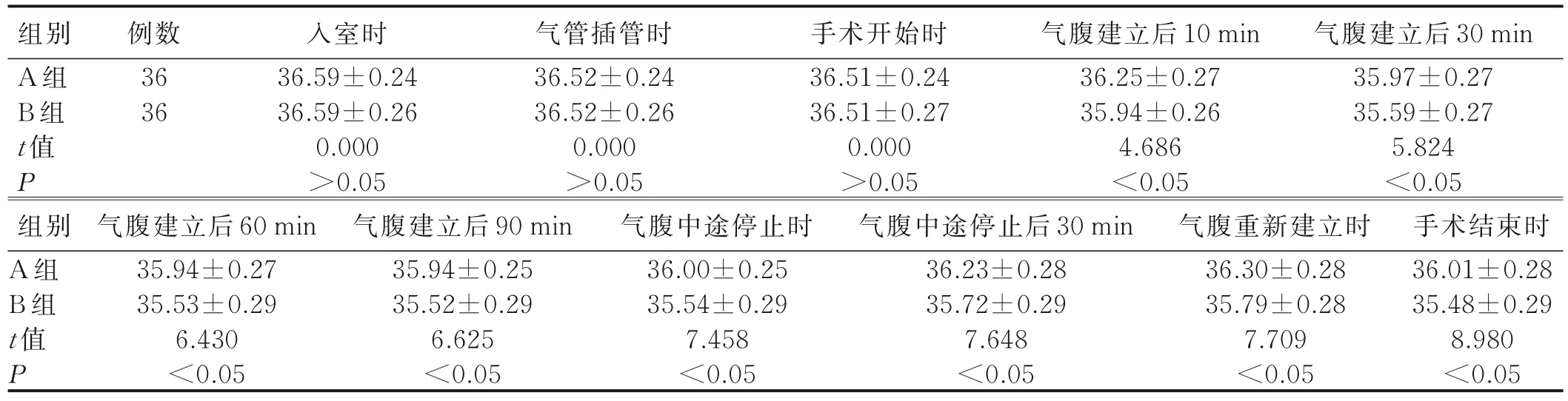
表1 两组病人术中不同时间点核心体温比较(±s) 单位:℃
组别A 组B 组t值P组别A 组B 组t值P例数36 36气腹建立后60 min 35.94±0.27 35.53±0.29 6.430<0.05入室时36.59±0.24 36.59±0.26 0.000>0.05气腹建立后90 min 35.94±0.25 35.52±0.29 6.625<0.05气管插管时36.52±0.24 36.52±0.26 0.000>0.05气腹中途停止时36.00±0.25 35.54±0.29 7.458<0.05手术开始时36.51±0.24 36.51±0.27 0.000>0.05气腹中途停止后30 min 36.23±0.28 35.72±0.29 7.648<0.05气腹建立后10 min 36.25±0.27 35.94±0.26 4.686<0.05气腹重新建立时36.30±0.28 35.79±0.28 7.709<0.05气腹建立后30 min 35.97±0.27 35.59±0.27 5.824<0.05手术结束时36.01±0.28 35.48±0.29 8.980<0.05
2.2 两组病人术中核心体温变化趋势 两组病人在测量的11 个时间点中体温变化趋势大体相同,在入室时至手术开始时,两组病人体温下降趋势无明显差异;在手术开始至气腹建立后10 min,B 组病人核心体温下降的趋势更明显;在气腹建立后30 min 至气腹停止时,两组病人核心体温趋于平稳,其中A 组病人体温有回升的趋势;在气腹重新建立至手术结束时,两组病人的核心体温均处于下降趋势,其中B 组病人下降速度更快、核心体温更低,见图1。
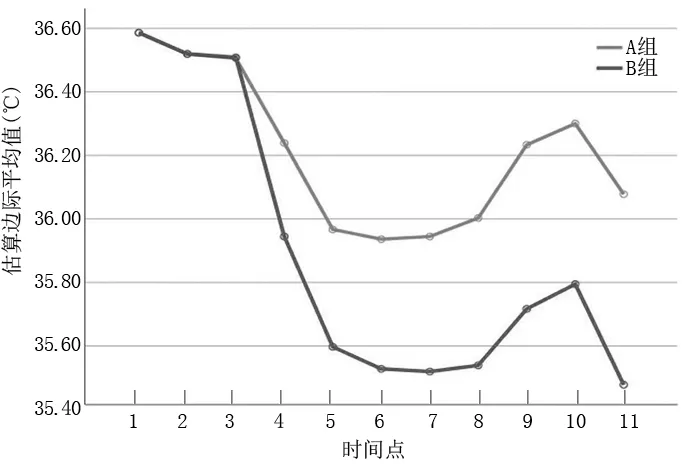
图1 两组病人术中核心体温变化趋势
2.3 两组病人术中低体温发生率比较 A 组病人36例中有18 例术中发生低体温,B 组病人36 例中有34 例术中发生低体温,两组低体温发生率比较差异有统计学意义(P<0.05),见表2。
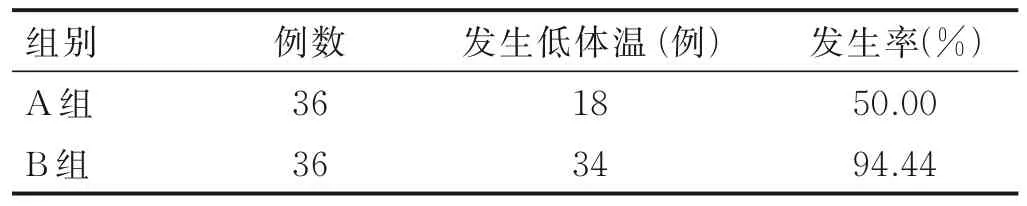
表2 两组病人术中低体温发生率比较
3 讨论
目前,针对胃癌治疗最有效的方式仍为手术切除,手术治疗可以彻底清除病灶、延长病人生命,但由于开腹手术切口大,对机体损伤较大,增加了病人术后伤口感染的风险[10]。自1994 年Kitano 等[11]首次报道腹腔镜下胃部分切除术后,腹腔镜手术凭借手术创伤小、术后并发症少等优点逐渐代替开腹手术。但与此同时,腹腔镜手术也增加了胃癌病人术中低体温发生率[12]。
外科手术病人中有50%~90%经历过围术期体温过低,病人术中核心体温低于正常值约2 ℃,术后手术部位感染发生的概率增加约3 倍,且会延长住院时间20%[13]。术中低体温还可能会导致身体生理机能紊乱,引起出血、心律失常、手术部位感染、术后寒战、麻醉苏醒延迟等多种并发症,对病人的身体和术后恢复造成严重影响[14-17]。梅超[18]通过测量不同气腹压力下行腹腔镜手术的病人,表明CO2气腹压力在12 mmHg、15 mmHg时对病人肝功能、肾功能、心功能的影响均在正常范围内。故本研究将CO2气腹压力设定为12 mmHg(A 组)、14 mmHg(B 组),两种气腹压力均可控。研究结果表明,A 组病人核心体温与B 组相比下降较为缓慢,表明低气腹压力对病人术中体温影响较小,这与胡永利等[19]的报告结果一致。经分析原因可能有以下两方面:第一,手术开始后大量低于机体温度的气体在腹腔内扩散、吸收热量,使病人核心体温迅速下降,而人工气腹压力越高,向病人体内输送的CO2量越多,腹腔内因对流产生的热损失大大增加;第二,高压力的气腹使CO2从腹腔内溢出速度更快,导致病人体内热量流失,核心体温下降。另外,结果显示在建立气腹30 min 后两组病人核心体温几乎不再下降,可能是机体因对流、CO2溢出产生的热损失与机体代谢产热达到平衡。
本研究中两组病人都采用了一次性戳卡穿刺皮肤以提供手术操作通路。与传统戳卡相比,一次性戳卡增加了防滑螺纹设计,与腹壁贴合较好,为精确的手术操作提供了稳定支持。此外,一次性戳卡使用的帽口为通用转换帽,5~12 mm 的手术器械均可进出操作口,解决了“专帽专用”的问题,缩短手术时间的同时,更有效减少了术中CO2的泄漏。
近年来,随着快速康复理念的推广深入,术中病人的体温管理逐步引起临床重视,为降低术中低体温的发生率,建议护理人员着重观察病人在气腹建立后30 min内的体温变化,必要时可采取提高室内温度、增加被单覆盖以及加用升温毯、暖风机、循环水褥等有效措施减缓病人体温的持续下降。
4 小结
综上所述,术中使用12 mmHg 的压力建立气腹有利于减缓病人手术初期体温下降的速度和幅度、降低术中低体温发生率,建议术者在不影响手术质量的前提下尽量选用较低压力的CO2建立气腹。但本研究由于疫情、时间等因素的影响,样本量较少,代表性存在一定的局限,接下来将进一步扩大研究规模,提升样本质量,进一步提高研究成果的有效性和科学性。

