离子选择性电极法测定工业碳酸钠中氯化物的研究
陈魏,王家珍,张及亮,李智,余雅芹
(1.湖北中检检测有限公司,湖北 武汉 430056;2.中国检验认证集团湖北有限公司,湖北 武汉 430022)
0 引言
工业碳酸钠(Na2CO3),又称为纯碱,国际贸易中又名苏打或碱灰。工业碳酸钠是用于玻璃制造的重要化工原料[1]。氯化钠是碳酸钠的主要杂质之一,由于其生产工艺上的原因,或多或少都会含有少量氯化物(以氯化钠计)。而氯化钠是高强度离子晶体,其熔点和沸点分别达到800 ℃和1413 ℃,如果含量太高会影响玻璃的熔融反应过程,造成玻璃的品质下降[2-3],因此必须准确测定工业碳酸钠中的氯化物含量。
目前测定碳酸钠中氯化物的方法主要有离子选择电极法、电位滴定法和汞量法等。国家标准GB/T 210—2022 《工业碳酸钠》对氯化物的测定提供了两种可选方法,即汞量法和电位滴定法[4]。汞量法由于使用到了剧毒化学药品硝酸汞,它对实验人员及生态环境有一定程度的危害,且滴定操作较为繁琐耗时,滴定终点的判断受个人主观影响较大,故该方法的使用仍存在一定的局限性;而电位滴定法的操作同样较为繁琐,在实验过程中,需要记录大量的电位值数据,滴定管很难全程控制每次的滴定体积控制在0.10 mL,且滴定终点需通过计算电位值的突跃来判断,一旦出现偏差,就会对结果的准确性产生不利影响。而离子选择电极法具有操作简单、安全无害、高效准确等优点,可对样品直接进行测定,目前已被广泛的运用于氯化物的测定[5-6]。因此,本文建立离子选择电极法来测定工业碳酸钠中的氯化物含量。
1 实验部分
1.1 方法原理
试样在pH值在5~6之间情况下,用乙酸盐缓冲溶液调节总离子强度,以氯离子选择电极和饱和甘汞电极测量电位。由于电极对溶液中的氯离子有良好的选择性,且试样中氯离子含量的对数值与电极电位存在线性关系,符合能斯特方程,通过测定样品中氯离子的电位值,即可计算出其氯离子浓度。
1.2 主要仪器与试剂
离子计(型号XSJ-216F),测量精度0.01 mV,上海雷磁;氯离子选择电极(型号PCl-1-01)和饱和甘汞电极(型号217),上海雷磁;电子天平(型号AUW120),精度0.0001 g,日本岛津;控温电磁搅拌器(型号GH-09),上海国华。
碳酸钠、硝酸、冰乙酸、硝酸钾均为优级纯,国药集团;基准碳酸钠,主含量为99.95%~100.05%,天津科密欧;水中氯离子溶液标准物质[GBW(E)082683]:1000 μg/mL,北京坛墨质检;实验所用水均为电阻率18.2 MΩ·cm的超纯水。
1.3 实验步骤
1.3.1 标准曲线的配制及测定
用单标移液管吸取水中氯离子溶液标准物质10.00 mL,转移至100 mL容量瓶中,用超纯水稀释至刻度,此溶液为氯离子标准储备溶液,浓度为100 μg/mL。用刻度移液管分别移取0.0、2.5、5.0、10.0、25.0 mL氯离子标准储备溶液和5.0、25.0 mL水中氯离子溶液标准物质至7个50 mL容量瓶中,再分别加入5 mL乙酸盐缓冲溶液(100 g硝酸钾和50 mL乙酸,溶解后用氢氧化钠溶液调节pH值为5~6),用超纯水稀释至刻度,摇匀,即可得到氯离子标准工作溶液,其浓度分别为0、5、10、20、50、100、500 μg/mL。
将上述氯离子标准工作溶液分别转移至100 mL烧杯中,将预热半小时以上的氯离子选择电极和饱和甘汞电极,按照低浓度到高浓度的顺序,依次插入到氯离子标准工作溶液中(需使电极液膜充分浸入)。加入磁力搅拌子,用电磁搅拌器进行匀速搅拌,避免产生的气泡接触到电极。待读数稳定(1 min内电极电位小于0.2 mV)[7]后,分别记录电位值。每次测定前,需用超纯水清洗电极,并用滤纸擦干。以氯离子浓度的对数(logC)为横坐标,以待测溶液的电位值为纵坐标,在半对数坐标系上建立标准曲线。
1.3.2 样品溶液的制备及测定
称取约2 g(精确至0.0001 g)已于270~300 ℃干燥至恒重的样品置于50 mL容量瓶中。加入5 mL硝酸溶液(1+1),并根据样品情况用硝酸溶液(1+1)或氢氧化钠溶液(100 g/L)调节pH值为5~6左右,加入5 mL乙酸盐缓冲溶液,用水稀释至刻度,摇匀。
将制备的上述样品溶液转移至100 mL烧杯中,插入氯离子选择电极和饱和甘汞电极,加入磁力搅拌子,用电磁搅拌器进行匀速搅拌,避免产生的气泡接触到电极。待读数稳定后,记录样品溶液的电位值。注意样品溶液和氯离子标准工作溶液的温差不宜超过1 ℃。根据样品溶液测得的电位值,通过标准曲线方程,计算氯离子含量。
1.3.3 结果计算
氯化物的质量分数(以NaCl计)w,数值以%表示,按下列公示计算:
式中:C为由校准曲线测得样品中的氯离子含量(μg/mL);V为样品溶液定容的体积(mL);1.66为氯离子浓度换算成氯化钠浓度的换算系数;m为样品称样量(g)。
2 结果与讨论
2.1 标准曲线的绘制
根据1.3.1完成氯离子标准工作溶液的测定,每个浓度的标准工作溶液的测试数据详见表1。以氯离子浓度的对数(lgC)为横坐标,以待测溶液的电位值为纵坐标,在半对数坐标系上建立标准曲线,详见图1。曲线方程为:y=-56.47x+177.6,相关系数R=0.9999。从以上数据可以得出,在0~500 μg/mL的浓度范围内,电极对氯离子有良好的响应,并且能够满足各种品级碳酸钠中氯化物的检测需求。
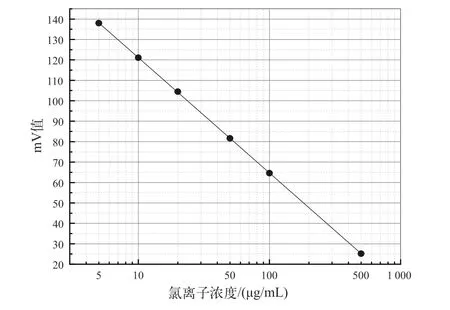
图1 氯离子标准曲线

表1 氯离子标准工作溶液测试数据
2.2 pH值对检测结果的影响
按照1.3.1步骤,配制7组浓度为10 μg/mL的氯离子标准工作溶液,在定容前,用硝酸溶液(1+1)或氢氧化钠溶液(100 g/L)调节上述7个氯离子标准工作溶液的pH值依次为4.0±0.1、5.0±0.1、6.0±0.1、7.0±0.1、8.0±0.1、9.0±0.1和10.0±0.1,然后分别进行测试,每组数据测定6次,以平均值为最终结果,测试数据详见表2。从这些数据可以看出,氯离子在pH值为4~6的范围内变化不大,在pH值为5~6的范围内最接近理论值,而在pH值为8~10的碱性条件下,与实际值则相差较大。因此pH值控制在5~6的范围内最为适宜。

表2 不同pH值的对测试结果的影响(n=6)
2.3 温度对检测结果的影响
按照1.3.1步骤,配制6组浓度为10 μg/mL的氯离子标准工作溶液,在测试前,用控温电磁搅拌器将待测氯离子标准工作溶液的温度维持在15、20、25、30、35、40 ℃,然后分别进行测试,每组数据测定6次,以平均值为最终结果,测试数据详见表3。实验结果表明,温度对测试结果有一定的影响,随着温度的升高,氯离子测试浓度随之升高,因此为了保证结果的准确性,在测定标准溶液和样品时,要保证测量时段温度恒定,前后温差最好控制在±5 ℃范围内,就可以有效抵消由温度变动对结果造成的影响。

表3 不同温度对测试结果的影响(n=6)
2.4 检出限的测定
参考HJ 168—2020 《环境监测分析方法标准制修订技术导则》[8]附录A.1.4离子选择电极法要求,检出限的确定准则为:在没有前处理的情况下,当校准曲线直线部分外延的延长线与通过空白电位且平行于浓度轴的直线相交时,其交点所对应的浓度值即为该离子选择电极法的检出限。称取2 g基准碳酸钠作为空白样品,按照1.3.2的步骤对空白样品平行测定6次,其平均电位值为193.28 mV,将此电位值在标准曲线图上标记,沿该电位点作平行于 x 轴(氯离子浓度)的直线交于曲线直线部分延长线对应的浓度值为0.53 μg/mL,当碳酸钠称样量为2 g时,本方法的检出限为0.0022%。
2.5 精密度和回收率的测定
考虑到样品基准效应,将基准碳酸钠作为空白加标样品,设置3组加标水平,在2 g基准碳酸钠中分别加入1.50、5.00、15.0 mL水中氯离子溶液标准物质(1000 μg/mL),配制成氯离子浓度分别为0.124%、0.415%、1.245%的三组样品,按照1.3.2的步骤对加标样品进行测试,每组样品平行测定6次。得出的精密度和准确度数据详见表4,三组加标样品测定的相对标准偏差在0.99%~2.41%的范围内,加标回收率在96.5%~99.3%的范围内。满足GB/T 27417—2017《合格评定 化学分析方法确认和验证指南》[9]中对精密度和回收率的要求。

表4 配制样品精密度和准确度测试结果
3 结语
本文建立的氯离子选择电极-标准曲线法可以有效测定工业碳酸钠中的氯化物含量,并能够满足各种品级碳酸钠中氯化物的检测需求。同时还对影响实验结果的因素,如pH值和温度对结果的影响进行探讨,并给出了最适条件。另外通过方法学实验表明,本方法特异性强、线性范围宽、检出限低、精密度好、回收率高,为工业碳酸钠中氯化物的测定提供了一种可供选择的技术方法。

