硅胶干燥剂适用范围的探究
李伟伟 杜际更 王志庚 李光跃

摘要: 通过实验验证和理论计算后发现,硅胶通过分子间氢键等作用可以吸附氨气、氯化氢、CO2(或H2CO3)、 SO2(或H2SO3)等分子,所以硅胶不能用于干燥这些气体,只能干燥N2、 O2、 H2、 CH4等气体。在实际教学中,不宜将硅胶简单归为中性干燥剂。
关键词: 硅胶干燥剂; 氨气; 氯化氢; 二氧化硫; 实验探究
文章编号: 10056629(2023)08007304中图分类号: G633.8文献标识码: B
1 问题的提出
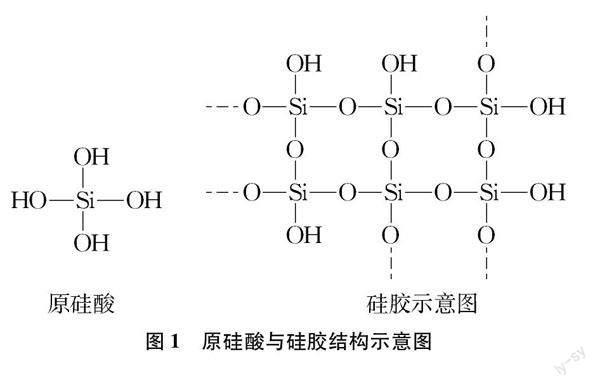
在生产生活中,硅胶可用于干燥N2、空气、氢气、天然气[1]等。按照酸碱性,干燥剂可分为:酸性干燥剂、碱性干燥剂和中性干燥剂[2]。硅胶似乎是中性干燥剂,似乎可以干燥NH3、 HCl、 SO2等。但是从原理来看,硅胶是原硅酸分子三维空间分子间脱水构成的,主体是SiO2,表面有丰富的羟基(见图1)。硅胶之所以可以吸水,是因为硅胶表面的硅羟基可以和水分子间形成分子间氢键,因此可以吸附水,从而起到干燥作用。变色硅胶中含有钴离子,吸附水达到饱和后,变色硅胶中的钴离子变为水合钴离子,从而使蓝色硅胶变为粉红色。在200℃加热粉红色的硅胶一段时间后,硅胶与水分子间氢键断裂,变色硅胶会重新变成蓝色,从而可以重复使用。那么,既然硅胶表面有丰富的羟基,硅胶表面还可能与NH3、 HCl等也形成分子间氢键,可能无法作为NH3、 HCl的干燥剂,已有的文献也没有相关报道。那么实验结果究竟怎样?本课题做了如下的实验探究。
2 实验部分
2.1 硅胶干燥剂适用范围探究——氨气
首先,分别將变色硅胶置于蒸馏水和浓氨水中。变色硅胶在蒸馏水中变为粉红色;在浓氨水中,变色硅胶先变红色,慢慢的变为浅蓝色。这说明,硅胶可以吸附氨水中的NH3或NH3·H2O。
如图2,将氢氧化钙和氯化铵固体混合均匀后,置于试管中加热,将产生的气体通过碱石灰除去水蒸气,然后通过硅胶,靠近入口方向的硅胶颜色变浅(该颜色与浸泡在浓氨水中的硅胶颜色基本一致),湿润的pH试纸没有明显变化,说明产生的NH3没有到达pH试纸,就已被完全吸附。一段时间后,停止加热,取出一小部分硅胶球,放入蒸馏水中,向水中滴加酚酞,溶液变红,说明硅胶对NH3有较强的吸附作用,用蒸馏水脱附后,NH3进入蒸馏水中,溶液呈碱性。所以,由于硅胶对于NH3有较强的吸附作用,硅胶干燥剂不可以干燥NH3。
2.2 硅胶干燥剂适用范围探究——氯化氢
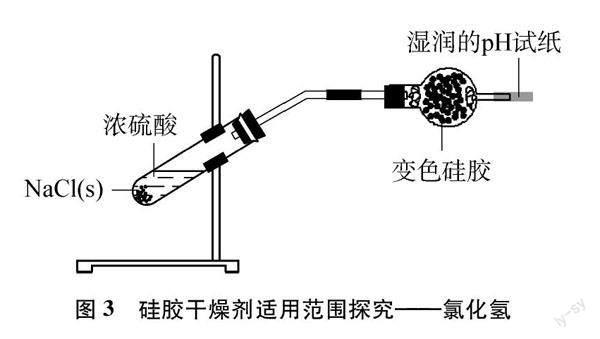
将NaCl固体先用酒精灯火焰灼烧以除去固体组分中的湿存水,待样品冷却后,向NaCl固体中加入浓硫酸,立即产生大量气泡。将产生的气体通入盛有硅胶的球形干燥管中,在干燥管末端放入湿润的pH试纸,前端的硅胶变为浅绿色,湿润的pH试纸无明显变化(见图3)。这说明,产生的HCl气体被硅胶完全吸附,没有逸出到空气中。
将吸附HCl变为浅绿色的硅胶置于试管中。另取蓝色新硅胶置于试管中,加入浓盐酸,硅胶也变为浅绿色,二者颜色基本一致。这说明球形干燥管中的硅胶吸附了HCl。变色硅胶中的钴离子与Cl-形成绿色配合物。
将变为浅绿色的硅胶置于蒸馏水中,变色硅胶逐渐变为黄色,说明硅胶吸附的HCl已经脱附进入水中。取少量上层水溶液,加入硝酸酸化的硝酸银溶液出现白色沉淀。取少量水溶液滴在广泛pH试纸上,试纸变红,说明溶液显酸性。
以上实验说明,硅胶对HCl气体有强烈的吸附作用。HCl是强极性分子,硅胶表面的羟基也有较强极性,二者可能形成分子间氢键或者具有比较强的偶极偶极相互作用,导致硅胶表面可以与HCl分子之间形成比较强的分子间作用力,因而硅胶对HCl有较强的吸附作用。所以,硅胶干燥剂不可以用来干燥HCl气体。
2.3 硅胶干燥剂适用范围探究——二氧化硫
将浓硫酸与硫代硫酸钠固体混合(见图4),Na2S2O3+H2SO4Na2SO4+SO2↑+S↓+H2O;将产生的气体通过盛有变色硅胶的干燥管,变色硅胶变为浅蓝绿色,末端湿润的蓝色石蕊试纸没有明显变化,说明产生的SO2气体已经完全被硅胶球吸附,无法逸出。
取下一部分硅胶球置于蒸馏水中,充分平衡后,取少量水滴在蓝色石蕊试纸上,试纸没有明显变化,说明用蒸馏水不足以使SO2从硅胶上完成脱附。
另取一小部分硅胶球,放在试管内加热,在试管口放湿润的蓝色石蕊试纸,蓝色石蕊试纸变红,说明加热使SO2气体从硅胶球脱附,从而使石蕊试纸变红。
以上实验说明,硅胶对SO2或者H2SO3也有很强的吸附作用,不能用于干燥SO2气体。
2.4 硅胶干燥剂适用范围探究——二氧化碳
如图5,滴有酚酞的碳酸氢钠溶液显浅红色。加热碳酸氢钠固体,将产生的混合气体通过盛有干燥硅胶球的干燥管,硅胶没有明显变化,滴有酚酞的碳酸氢钠溶液逐渐变为无色,说明球形干燥管的末端有CO2气体逸出,即硅胶没有吸附CO2或者只部分吸附了CO2。
为了证明硅胶对二氧化碳气体的吸附情况,继续进行如下实验。将球形干燥管内的硅胶球取出,取部分投入滴有酚酞的碳酸氢钠溶液中,碳酸氢钠溶液退色。这说明:硅胶吸附了二氧化碳,溶于水后,二氧化碳脱附进入碳酸氢钠溶液,使碳酸氢钠溶液退色。将剩余部分的硅胶球置于干燥的试管中加热,将产生的气体通入滴有酚酞的碳酸氢钠溶液中,很快,碳酸氢钠溶液由浅红色变为无色。这同样说明,硅胶对于CO2气体仍然有吸附能力。但是硅胶对CO2的吸附力远小于HCl、 NH3、 SO2,在进行图5的实验时,只能部分吸附二氧化碳。硅胶之所以能部分吸附CO2,很可能是硅胶与CO2形成了分子间氢键Si—OH…OC。由于CO2中心碳原子为sp杂化,而硅胶中硅原子为sp3杂化,所以直线形的CO2分子与硅胶表面配合并不好,导致硅胶对二氧化碳的吸附力相对较小。
3 四种气体在水中的溶解度与在硅胶表面吸附情况对比
从以上实验结果可以看出,硅胶对氨气、氯化氢、二氧化硫三种气体有较强的吸附能力,对二氧化碳吸附力较小(见表1)。这和四种气体在水中的溶解度情况基本类似。这可能是由于水分子中含有羟基—OH,而硅胶表面也含有丰富的羟基,所以这四种气体在水中的溶解度与其在硅胶表面的吸附情况非常相似。氨气、氯化氢、二氧化硫三种气体中,二氧化硫的在水中的溶解度最小,但是被硅胶吸附后,却是三种气体中最难脱附的。硅胶吸附氨气、氯化氢后,用溶剂水就可以将其脱附。而二氧化硫气体被硅胶吸附后,难以用水脱附,必须加热后才能从硅胶表面脱附。所以必须对四种气体在硅胶表面的吸附情况进行理论计算。
4 硅胶与四种气体相互作用的理论计算
在量子化学ORCA软件[4]中,在密度泛函理论(DFT)框架下,使用DFTD/B3LYP/Def2TZVP方法计算了不同气体与硅胶之间的相互作用模式与能量。其中为了简化计算,硅胶固体以四聚原硅酸分子表示。计算结果显示,H2O、 NH3、 HCl均可与硅胶表面的羟基形成氢键(见图6 a~c)。它們在硅胶表面具有相对较强的结合能(见表2),很容易在硅胶表面吸附。由于NH3、 HCl的结合能与H2O相近,因此水洗即可导致这两种气体分子脱附。对于SO2分子来说,其结合能只有-17.47kJ/mol,远小于以上三种分子。但实验证实SO2气体很容易吸附于硅胶上,甚至水洗也不能使其脱附,只有加热才能使SO2从硅胶表面逸出。由此我们猜测,SO2很有可能在硅胶表面与H2O结合生成了H2SO3分子。图6e显示,H2SO3分子同时与硅胶表面的羟基和氧原子形成了三个氢键,其结合能高达-76.63kJ/mol,这可以解释为何SO2吸附于硅胶后很难用水洗脱。非极性CO2与硅胶结合能力最弱,只可以被硅胶部分吸附。虽然H2CO3与硅胶的结合能也达到了-65.65kJ/mol,但是CO2转化为H2CO3的转化率不高,所以CO2的吸附率也就降低了。由以上数据可以看出,气体分子极性大小并非判断它能否被硅胶吸附的唯一标准,与硅胶表面形成的氢键是其稳定吸附的主要原因。
5 结语
硅胶的成分为SiO2·nH2O,硅胶巨大的表面积和表面丰富的羟基使硅胶可以作为性能优良的无毒干燥剂,广泛用于生产和生活中。本文从实验和理论计算两个方面证实:硅胶可以通过分子间氢键吸附NH3、 HCl、SO2、 CO2等气体,所以硅胶不能用于这些气体的干燥。作为气体干燥剂,硅胶只能干燥N2、 O2、 H2、 CH4[5]、空气等不能与硅胶表面形成分子间氢键的气体。在实际的教学中,不能只根据酸碱性而简单地将硅胶归类为中性干燥剂。
参考文献:
[1][5]Jacobs, J. H., et al. The role of carbon dioxide and water in the degradation of zeolite 4A, zeolite 13X and silica gels [J]. New Journal of Chemistry, 2023, (47): 5249~5261.
[2]陆燕海. 对干燥剂选用的一些探讨[J]. 化学教学, 2013, (4): 75~76.
[3]王晶主编. 普通高中教科书·化学·选择性必修2·物质结构与性质[M].北京: 人民教育出版社, 2020: 60.
[4]Neese, F.. Software update: the ORCA program system, version 4.0 [J]. WIRES Computational Molecular Science, 2018, 8(1): 1327.
*河北省十四五规划课题“‘证据推理与模型认知核心素养下高中化学创新实验微课研究”(课题编号:2107001)的阶段性研究成果。

