前列腺癌图像引导放疗中锥形束CT 为合成CT 提供质量保证的可行性研究
张帅楠,田 龙,赵 鑫
(河北北方学院附属第一医院医学影像中心,河北张家口 075000)
0 引言
在基于CT 的前列腺癌(prostate cancer,PCa)图像引导放疗(image guided radiotherapy,IGRT)计划设计中,需将CT 值转换为剂量计算所需的电子密度(electron densities,ED)[1]。相比传统CT 而言,在基于MR 的放疗计划设计中,软组织对比度和靶区勾画精度均得到了显著提升[2-4]。但是,MR 无法提供CT 值和ED,需将MR 数据转换并生成用于剂量计算和获取数字重建放射影像(digital reconstructed radiographs,DRR)的合成CT(synthetic CT,sCT)图像,特别是在单独基于MR 的PCa IGRT 中[5-8]。
以传统CT 作为质量保证(quality assurance,QA)的金标准,sCT 相对CT 的剂量分布Gamma 通过率较高,剂量体积直方图(dose-volume histogram,DVH)差异较小[9]。但以传统CT 作为sCT 的QA 标准后无法实现单独基于MR 的PCa IGRT。常用于分次治疗间靶区位置校准的锥形束CT(cone beam CT,CBCT)可作为一种有效的sCT QA 设备。加速器机载CBCT不同于传统CT,在实现单独基于MR 的PCa IGRT中扮演了重要角色。而且CBCT 图像获取便捷,质量可满足临床鉴别要求。因此,本研究评价利用CBCT 为sCT 提供QA 的可行性,以期实现真正意义上的单独基于MR 的PCa IGRT。
1 资料与方法
1.1 研究对象
本研究分为2 个部分:第1 部分是检验CBCT 设备的性能和建立CBCT 的CT 值-ED 曲线的体外实验,研究对象为KOYOTO KAGAKU PH-4 高精仿真人体模型;第2 部分是验证CBCT 取代CT 成为sCT QA 标准的可行性的临床试验,研究对象为10 例于2021 年6 月至2022 年12 月间在河北北方学院附属第一医院接受诊疗的PCa 患者。患者一般资料:年龄53~57 岁,平均年龄(55.4±2.1)岁;Gleason 评分[10]≤6分的2 例,Gleason 评分为7 分的3 例,Gleason 评分≥8 分的5 例。纳入标准:(1)肿瘤仅适合IGRT 治疗;(2)身体质量指数为18~25 kg/m2;(3)除前列腺特异性抗原外,其他生理、生化指标未见明显异常;(4)接受黄金基准标志物(gold fiducial marker,GFM)置入术。排除标准:(1)前列腺肥大,伴严重钙化;(2)合并直肠息肉或痔疮。本研究通过医学伦理委员会批准,所有患者均签署知情同意书。
1.2 体外实验
体外实验检验CBCT 的CT 值(CT 值CBCT)的长期稳定性并建立CBCT 的CT 值-ED 曲线。(1)使用瓦里安Trilogy 加速器的On-board kV 级CBCT 对模型进行每月1 次共计10 次扫描。CBCT 设置参数:选择pelvis 扫描模式(Full Fan),管电压为100 kVp,管电流为80 mAs,层厚为2.5 mm,视野(field of view,FOV)为25 m×18 cm。(2)使用Philips Big Bore 大孔径CT 对模型进行同步扫描,CT 设置参数:管电压为120 kV,管电流为300 mAs,层厚为3 mm。(3)将CBCT和CT 数据以DICOM 格式传输至影像归档和通信系统(picture archiving and communication system,PACS)并于相同层面进行分析。分别读取10 次扫描2 种图像中不同器官内CT 值的平均值。(4)使用SPSS 19.0软件建立CBCT 与CT 的CT 值之间的函数关系并生成CBCT CT 值-ED 曲线。
1.3 临床试验
1.3.1 GFM 置入和图像获取
患者侧卧,双腿屈曲,双手抱膝,对直肠肛管进行局麻并建立静脉通道。在Philips iU22 彩色多普勒超声诊断仪直肠探头引导下经患者直肠对前列腺成像[11]。采用细针抽吸术(采用5 mL 注射器和18G 针头随超声探头进入直肠,穿透直肠前壁刺入前列腺体)将3 枚IBA Visicoil helical 线性金标志物置入靶区不同层面且间距≥15 mm。
在接受IGRT 前3 d,所有患者接受SIGNAVoyager 1.5T MR 和CT 扫描。MR 设置参数为:采用快速自旋回波(fast spin echo,FSE)序列,层厚为2.5 mm,回波时间(echo time,TE)为96 ms,重复时间(repetition time,TR)为15 000 ms,FOV 为448 mm×314 mm,采集矩阵为640×512,重建矩阵为1 024×1 024,重建体素为0.5 mm×0.5 mm×1.0 mm,带宽为390 Hz,采集时间为7 min,获取T2WI 图像数据。CT 设置参数同体外实验。使用Spectronic Medical MRI Planner 计划系统生成sCT 图像。sCT 用于靶区和危及器官(organ at risk,OAR)的勾画和剂量计算。CT 在临床试验中仅作为QA 的金标准,不用于治疗。首次治疗中的CBCT用于本研究,其他分次治疗中CBCT 联合GFM 用于IGRT。3 种图像均在患者处于相同定位体位且排空膀胱及直肠的情况下获取。IGRT 总剂量为7 600 cGy,分次为38 次,每次200 cGy。
1.3.2 图像处理和比较
使用Eclipse 13.6 软件将sCT、CT 和CBCT 进行基于GFM 的融合配准。将sCT 上的靶区和OAR 轮廓拷贝至CT 和CBCT 图像上后,通过Eclipse 13.6软件读取10 名患者CT 和CBCT 图像上各器官CT值的平均值和标准差,并通过各自的CT 值-ED 曲线转换为剂量分布。分别进行sCT 相对CT 和sCT相对CBCT 图像上的Gamma 通过率和DVH 比较。使用SUNnuclear 公司的SunPatient 软件比较等中心处3 个方向(横断面、冠状面、矢状面)DRR 上剂量分布的Gamma 通过率,其中Gamma 通过率阈值设置为3%/3 mm。2 种图像剂量验证通过点所占百分比为Gamma 通过率。使用DVH 评价靶区和OAR 的剂量指标,包括Dmean、Dmax、Dmin、95%计划靶区(PTV95%)、直肠V50、膀胱V50、耻骨联合V70、股骨头V50、小肠V50。
1.4 统计学分析
采用SPSS 19.0 软件进行统计学分析,符合正态分布的计量资料以表示,组间差异采用配对样本t检验。CT 值CBCT 长期稳定性采用方差分析。函数关系采用一元线性回归分析,相关性分析采用Pearson法。以P<0.05 为差异具有统计学意义。
2 结果
2.1 体外实验
仿真人体模型10 次扫描结果(见表1)显示,各器官的CT 值CBCT 方差比较差异均无统计学意义,满足方差齐性,因此CT 值CBCT 长期稳定性良好。CT 值CBCT和CT 值CT 范围分别为-1 000~1 750 HU 和-1 000~1 500 HU,各器官CT 值CBCT 和CT 值CT 均呈高度正相关,差异均具有统计学意义。一元回归方程为CT 值CBCT=1.110×CT 值CT+3.891,相关系数r为0.999,R2=0.899 8,CT 值CBCT 同CT 值CT 之间具有良好线性,可将CT 的CT 值-ED 曲线转换为CBCT 的CT 值-ED 曲线(如图1 所示)。
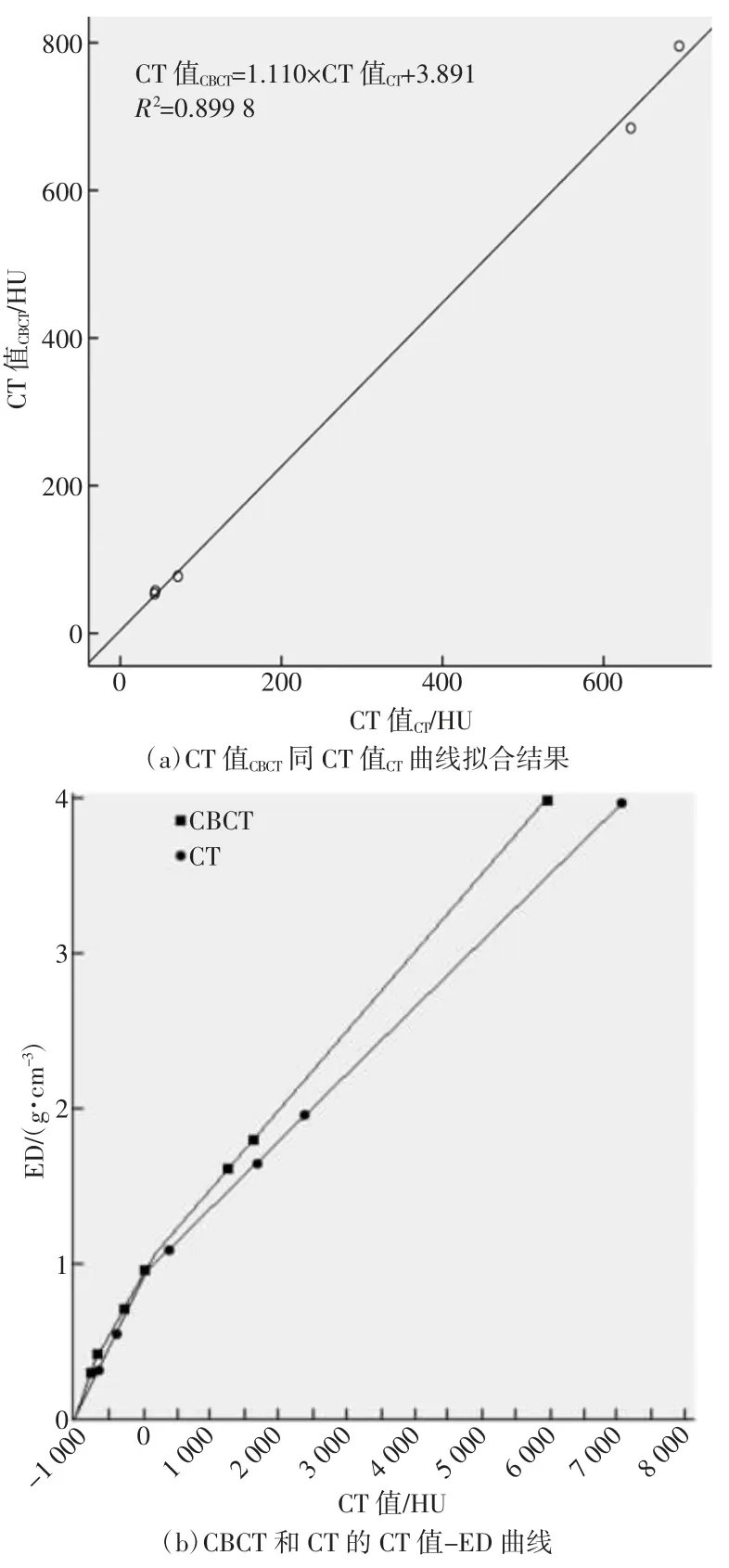
图1 体外实验结果
表1 各器官CT 值CBCT 和CT 值CT 结果()

表1 各器官CT 值CBCT 和CT 值CT 结果()
?
2.2 临床试验
1 号患者3 种图像(如图2 所示)中sCT 相对CT 和sCT 相对CBCT 在横断面、冠状面、矢状面上Gamma 通过率均呈高度正相关(见表2),具有高度一致性,组间差异均具有统计学意义,且差异平均值均小于0.1%,2 组间比较差异可忽略。10 名患者sCT相对CT 和sCT 相对CBCT DVH 各项指标差异平均值均呈高度正相关(见表3),组间差异均具有统计学意义,且差异平均值较小可忽略。

图2 1 号患者的sCT、CT、CBCT 图像
表3 sCT 相对CT 以及sCT 相对CBCT 的DVH 各项指标差异比较()单位:%

表3 sCT 相对CT 以及sCT 相对CBCT 的DVH 各项指标差异比较()单位:%
?
3 讨论
PCa IGRT 中MR 技术在成像质量,即软组织分辨力上具有其他成像技术无法比拟的优势。但MR图像自身无法提供CT 值和CT 值-ED 曲线,因此无法进行剂量计算。一种解决手段是通过基于GFM 或骨骼的MR-CT 图像融合技术,将MR 图像上靶区轮廓和OAR 拷贝至CT 图像上并进行剂量计算[12-13]。该过程无论手动还是自动,均会造成工作量的增加及引入GFM 识别和配准误差,而且重复的扫描也会增加患者额外辐照剂量和经济负担。因此,单独基于MR的PCa IGRT 势在必行,其中基于MR 生成并用于剂量计算的sCT 是重中之重。尽管sCT 已被证明可用于剂量计算,但其QA 程序标准并未确定。目前,利用CT 对sCT 剂量进行验证是唯一手段,但有悖于单独基于MR 的原则,因此亟须开发严格且可行的新QA程序。在放疗科各类大型设备中,CBCT 具有得天独厚的优势,若将CBCT 应用于sCT 剂量的QA 程序中,不仅可在治疗中同时完成靶区位置和剂量验证,也可降低患者额外辐照剂量和经济负担。本研究通过与金标准CT 进行比较,发现CBCT 在sCT 剂量验证中各项差异均较小,可取代CT 为sCT 提供QA。目前国内尚无相关研究,因此本研究为基于MR 生成的sCT 的QA 创建奠定了重要的理论和数据基础,具有一定的临床意义。
通过对本研究各项结果的分析和与其他试验[14-15]的比较,本研究得出以下结论:(1)体外实验中CT 值CBCT 在不同器官中均表现了长期稳定性。本研究应用的是PH-4 高精仿真人体模型,该模型盆腔中各器官与真实人体基本相同。其他试验中应用了不同的模体,也取得了相似的结果。例如,巩汉顺等[14]在不同扫描条件下的CBCT 影像质量及其CT 值长期稳定性分析研究中,应用的是Catphan 504 模体中的CTP 404 模块。结果显示,CBCT 长期稳定性良好,尤其是提高扫描电压和电流后,稳定性显著增加。(2)体外实验中CBCT 的CT 值-ED 曲线随条件改变而不同。本研究计算获取的一元回归方程为:CT 值CBCT=1.110×CT 值CT+3.891,而在宋炳文等[15]针对头颈肿瘤患者的调强剂量计算的快速CBCT CT 值修正方法研究中,却得到CT 值CBCT=1.213 5×CT 值CT+21.08 的方程。本研究认为,导致该差异的原因可能与所使用的模体(即扫描部位)以及CBCT 设置参数有关。因此,不同单位需要根据治疗部位和设备参数建立相应的QA 程序,而不是完全参照已有试验。而且,QA程序的建立必须经历体外实验和临床试验,否则会引入较大误差。另外,宋炳文等[15]研究中数据采集自10 例患者,而本研究数据采集自模体。真实患者在试验过程中不可避免地存在器官运动和充盈度改变的情况,因此存在较大误差,而本研究使用的模体则避免了该误差,因此回归方程更为准确。(3)临床试验中,器官运动和充盈度的改变对结果影响较大。本研究中,各器官DVH 最大差异出现于直肠,其次为膀胱和小肠。尽管试验中已归一了3 种扫描时的定位体位,特别嘱患者排空直肠和膀胱,但仍然无法避免器官运动以及充盈度变化(例如直肠充气)等影响,特别当MR 扫描时间较长时该影响会增大。相比上述器官,其他不易发生位移或无充盈度变化的器官差异明显较小。
总之,本研究通过体外实验证明了CBCT 设备的可靠性并建立了相对科学和准确的CBCT CT 值-ED曲线和剂量学模型,通过临床试验中Gamma 通过率和DVH 数据证明了CBCT 取代金标准CT 为sCT 提供QA 的可行性。严格的体外实验和临床试验为sCT QA 程序的创建提供了重要的方法和理论依据。未来可根据患者和设备特点创建自适应的sCT QA 程序,从而真正实现单独基于MR 的各部位IGRT。但是,本研究依然存在一些不足,包括:(1)患者样本容量较小,需扩大样本容量。(2)临床试验中对GFM 和钙化点的处理不够完善。本研究中仅简单地将其剔除CT 值计算并在原位置取周围组织CT 值平均值进行“填充”。该做法是否对DVH 计算有所影响尚不得知,需在未来试验中深入研究。(3)临床试验的时效性。本研究中MR 和CT 图像获取自放疗前3 d(前后间隔3 h 内),计划完成后于放疗中获取CBCT,该时间段内器官变化未作研究和处理。未来研究中或缩短计划完成时间至1 d,或开发新图像算法有效降低计划拷贝过程中器官变化的影响,或于MR 和CT 扫描后直接进行CBCT 成像,以完成sCT 的QA。

