Al/Fe2O3-RDX纳米复合物的热分解特性
罗庆平,龙新平,聂福德,刘桂香,蒋小华,祝明水
(1.西南科技大学 环境友好能源材料国家重点实验室,四川 绵阳 621010;2.中国工程物理研究院 化工材料研究所,四川 绵阳 621999)
引 言
起爆药是火工品的核心药剂,在军事、民用等方面具有重要作用,是目前炸药研究的热点之一。传统的起爆药如叠氮化铅和斯蒂芬酸铅等,由于含有重金属,环境污染大,其应用受到了很大限制[1-3]。因此,寻找新型绿色环保的起爆药替代物就成为目前起爆药领域研究的关键和热点[4-5]。国内外对绿色环保的起爆药替代物进行了广泛的研究,报道了一些绿色环保的起爆药如四唑类(tetrazoles)及其衍生物(derivatives)[6-11]、呋咱类起爆药[12],但其合成过程复杂,且生产过程产生的废水污染严重。一些纳米复合含能材料(如纳米铝热剂等)在这方面的潜在应用也引起了广泛关注[13-14]。采用纳米复合含能材料则有可能解决这个问题。但目前对绿色环保的纳米起爆药的研究报道较少。
作为纳米含能材料的一种,纳米铝热剂由于具有优异的点火和能量释放特性而逐渐受到了烟火、火工界的广泛重视和研究[15-18]。尽管其具有高能量密度、高热释放速率,但由于其反应不放出气体,不具有爆破性,限制了其在火炸药行业的潜在应用;而RDX等猛炸药的反应放出大量气体,反应对压力敏感,但其能量密度不高,因而将两者结合起来制备出纳米铝热剂/猛炸药复合物,则兼具纳米铝热剂、猛炸药的特性,可能会满足高能起爆药的能量应用特点,而成为一种潜在的、新型的绿色起爆药。
由于起爆药剂对摩擦、撞击、冲击、火花、加热等刺激特别敏感,在生产过程中可能会导致爆炸事故,是火工品生产中最大的固有危险因素。因此,潜在的新型绿色起爆药替代物的安全性研究对其应用具有重要意义。在炸药的安全性评价中,炸药的热性能是其安全性及应用性能的一个重要指标。研究表明[19-21],Al/Fe2O3-RDX纳米复合物具有快速的燃烧转爆轰性能,可作为一类潜在的绿色起爆药,但目前还未对其热性能进行系统评价。因此,本研究制备了潜在的绿色起爆药Al/Fe2O3-RDX纳米复合物,并根据其热分析特征量评价了该纳米复合物的热性能,同时对其热分解反应动力学及热催化机理进行研究,为其应用提供技术支撑。
1 实 验
1.1 材料与仪器
超细RDX由本实验室采用喷射法制备,其粒度约为1~5μm;纳米Fe2O3由本实验室采用溶胶-凝胶法制备,其为多孔结构,粒度约为5~30nm,比表面积为230m2/g,孔体积为0.7956mL/g,平均孔径为11.5nm;纳米Al(40nm钝化Al,活性约为52%),南京埃普瑞纳米材料有限公司;环己烷(分析纯),上海阿拉丁化学试剂公司。
Nova600i型扫描电子显微镜,美国FEI公司;JEM-100CX型透射电子显微镜,日本电子公司;ADSORP型比表面与孔隙度分析仪,美国康塔公司;STA449型综合热分析仪,德国Netzsch公司;KQ200KDB型超声仪器:200W,40kHz。
1.2 Al/Fe2O3-RDX纳米复合物制备
将纳米Al、纳米Fe2O3和超细RDX按一定质量比加入到环己烷中。其中,Al与Fe2O3按两者的铝热反应平衡比Φ为1.1(Al过量)添加[22]:
(1)
式中:nactive Al为铝热反应时活性Al的物质的量(即Al的理论用量),等于反应时需要的钝化纳米Al用量与其活性百分数之积,mol;nFe2O3为铝热反应时Fe2O3的理论物质的量,mol。
样品在超声作用并轻微搅拌下处理3h,直至整个复合物溶液不再有流动感为止,此时为高浓稠溶液。然后将该溶液置于真空干燥箱中,于55℃恒温干燥48h,制得Al/Fe2O3-RDX复合物。由于分散剂环己烷对RDX、纳米Al粉、纳米Fe2O3反应惰性,因此,所制备的Al/Fe2O3-RDX复合物中的Al、Fe2O3颗粒大小及尺寸不变,仍然处于纳米级,故所制备的样品为纳米复合物。图1为Al/Fe2O3纳米铝热剂及Al/Fe2O3-RDX纳米复合物的透射电子显微照片(TEM)。

图1 Al/Fe2O3纳米铝热剂和Al/Fe2O3-RDX纳米复合物的TEM图Fig.1 TEM images of Al/Fe2O3 nanothermite and Al/Fe2O3-RDX nanocomposite
从Al/Fe2O3-RDX纳米复合物的TEM图上可观察到纳米Fe2O3分散在纳米Al粉之间并粘附在纳米Al的球形颗粒上,分散较均匀。此时RDX由于颗粒尺寸太大而不能在TEM图上观察到。作为对照,Al/Fe2O3纳米铝热剂也采用相同的条件制备。
1.3 热性能表征
采用综合热分析仪对所制备的超细RDX、Al/Fe2O3纳米铝热剂、Al/Fe2O3-RDX纳米复合物进行热性能分析。超细RDX的热性能测试条件为:室温至300℃,Al2O3坩埚,N2气氛,流量50mL/min,升温速率分别为2、5、10、20℃/min;Al/Fe2O3纳米铝热剂、Al/Fe2O3-RDX纳米复合物的热分析温度为:室温至900℃,其他测试条件与超细RDX相同。
2 结果与讨论
2.1 Al/Fe2O3-RDX纳米复合物的热性能
将所制备的Al/Fe2O3-RDX纳米复合物在升温速率为10℃/min时进行热性能分析,并与超细RDX、Al/Fe2O3纳米铝热剂进行对比,结果见图2和表1。
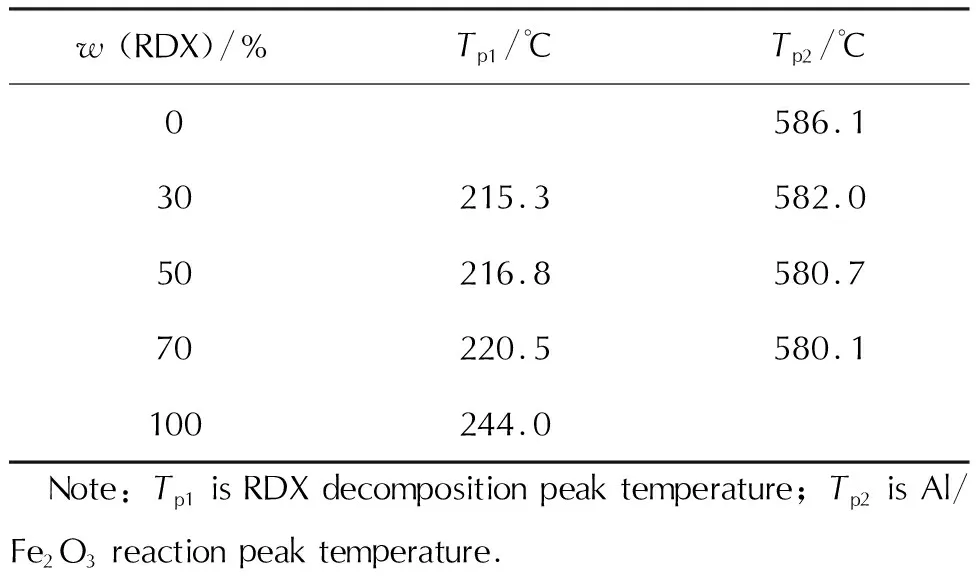
表1 Al/Fe2O3-RDX纳米复合物的DSC特征量Table 1 DSC characteristic values of Al/Fe2O3-RDX nanocomposites
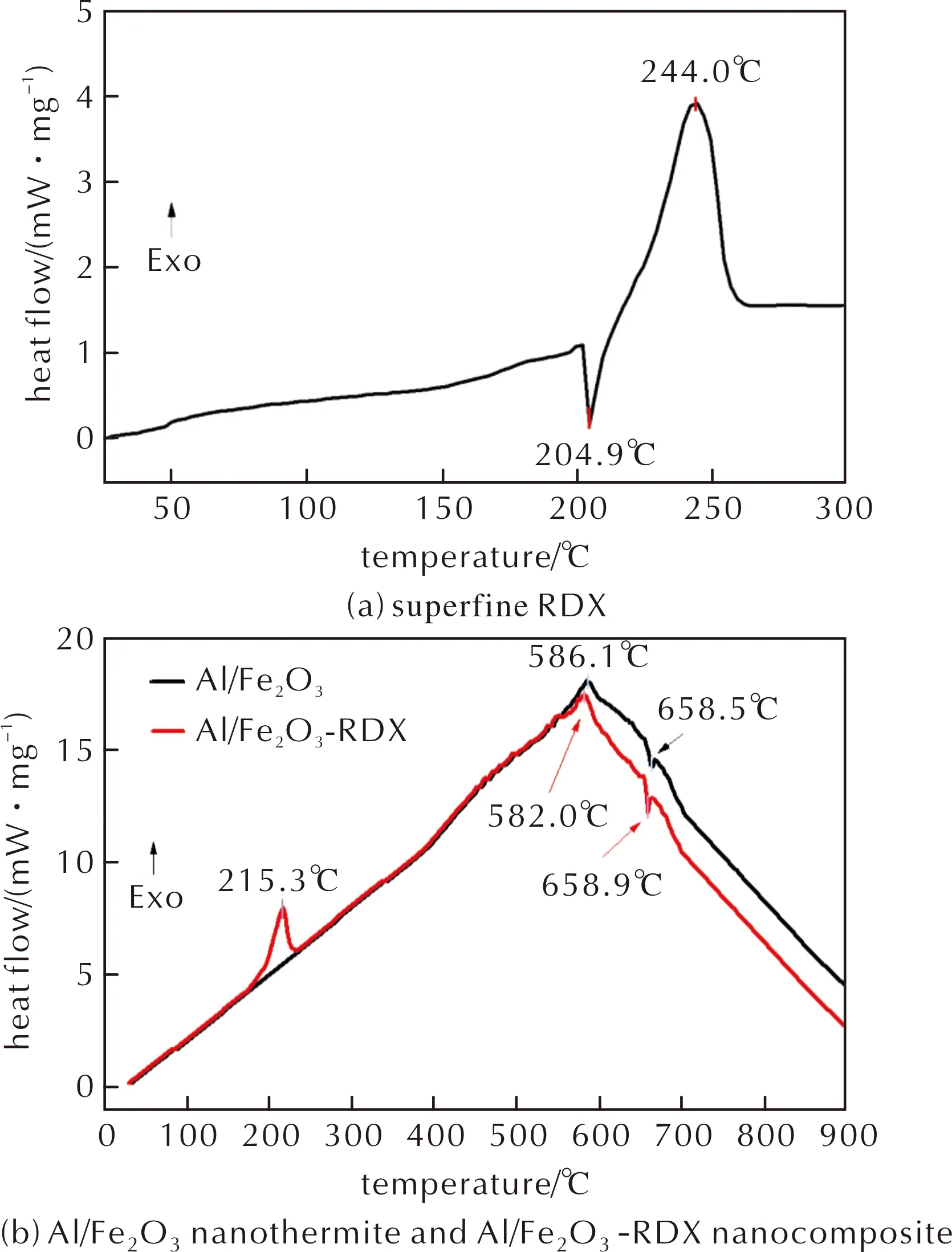
图2 超细RDX, Al/Fe2O3纳米铝热剂和Al/Fe2O3-RDX纳米复合物的DSC曲线Fig.2 DSC curves of superfine RDX, Al/Fe2O3 nanothermite and Al/Fe2O3-RDX nanocomposite
从图2(b)可知,在Al/Fe2O3-RDX纳米复合物的DSC曲线上有两个放热峰,一个吸热峰。第一个放热峰是RDX的分解放热峰,其热分解峰温为215.3℃;第二个是Al/Fe2O3纳米铝热剂发生铝热反应的放热峰,其反应峰值温度约在582℃。在658.5℃的吸热峰应为铝热反应中过剩的纳米Al的熔融吸热峰。在DSC曲线上未发现RDX的熔融吸热峰,这是因为RDX在纳米铝热剂中的纳米Fe2O3的催化作用下,分解反应提前发生,RDX熔融时刻即发生了热分解,导致其熔融吸热峰消失。
从表1可知,随着Al/Fe2O3-RDX纳米复合物中Al/Fe2O3纳米铝热剂含量的增加,RDX的热分解温度降低,这表明Al/Fe2O3纳米铝热剂对RDX的热分解具有较好的催化效果,可有效降低其热分解温度。同时,随着复合物中RDX含量的增加,Al/Fe2O3纳米铝热剂的铝热反应峰温有所降低,这可能和RDX分解产生的气体与纳米铝热剂接触,并对其部分活化有关。
由以上的热性能分析可知,Al/Fe2O3-RDX纳米复合物的起始热分解温度大于200℃,具有较好的热稳定性。由图2可知,由于超细RDX的热分解峰温为244℃,Al/Fe2O3纳米铝热剂的铝热反应峰温为586.1℃,两者的起始热反应温度均大于200℃,故由RDX和纳米铝热剂复合而成的纳米复合物具有200℃以上的起始热分解反应温度,即具有较好的热安定性。尽管纳米复合物的起始热分解温度(热安定性)低于纯RDX,但仍满足LANL关于绿色起爆药标准的热稳定性要求:起爆药的热稳定温度大于200℃[5]。
2.2 Al/Fe2O3-RDX纳米复合物的热反应动力学
利用超细RDX、Al/Fe2O3纳米铝热剂、Al/Fe2O3-RDX纳米复合物在不同升温速率下热分解反应的DSC特征量的不同,对其热性能及热分解反应动力学进行了研究,并比较研究了Al/Fe2O3纳米铝热剂和RDX对彼此热反应性能的影响,其结果见图3和表2。
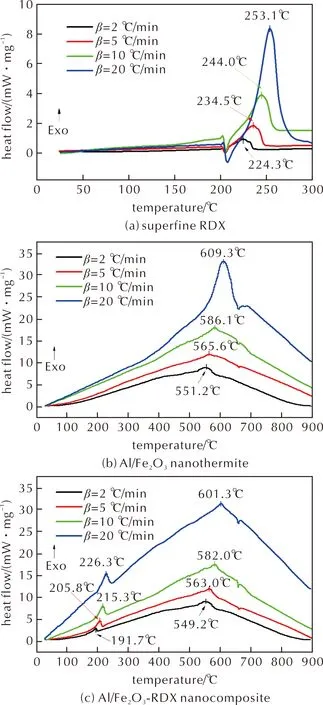
图3 不同升温速率下超细RDX、Al/Fe2O3纳米铝热剂及Al/Fe2O3-RDX纳米复合物的DSC曲线Fig.3 DSC curves of superfine RDX, Al/Fe2O3 nanothermite and Al/Fe2O3-RDX nanocomposite at different heating rates
从图3(a)可知,超细RDX的DSC曲线上存在一个吸热峰和一个放热峰,分别对应于RDX的熔融吸热和分解放热。结合表2可知,随着加热速率的上升,RDX的熔融吸热峰温和分解放热峰温均有所提高。采用微分法(Kissinger 法)对RDX的热分解动力学进行研究[23-25],所得的相关特征值可作为判断RDX分解反应的最可几机理函数形式的主要依据。
Kissinger方程为:
(2)
式中:Ea为表观活化能,J/mol;β为升温速率,K/min;Tp为放热峰温,K;R为气体常数,8.314J/(mol·K);A为指数因子;r为线性相关系数,一般接近1。
将表2中超细RDX的DSC特征值β及Tp1(RDX分解峰温)值代入公式(2)进行线性拟合,便可得到一条直线。从直线斜率求Ea,从截距求Ar,从而得到超细RDX的分解活化能为163.901kJ/mol。同时,根据超细RDX在不同升温速率β下的分解峰温Tp1,用热爆炸临界温度计算公式分别计算了升温速率趋于0时超细RDX的分解峰温Tp0和热爆炸临界温度Tb[26],其结果见表2。超细RDX的热爆炸临界温度为217.15℃,与文献[24]中普通(粗颗粒)RDX的热爆炸临界温度236℃相比,降低了接近19℃。这表明RDX的超细化提高了其反应活性,同时也降低了其热安全性。
从图3(b)和表2可知,Al/Fe2O3纳米铝热剂的DSC曲线上存在一个较大的放热峰和一个吸热峰,分别对应于Al/Fe2O3纳米铝热剂的铝热反应放热和铝热反应后过剩Al的熔融吸热。随着加热速率的上升,纳米铝热剂的铝热反应峰温上升,这与热分析时的温度滞后有关。加热速率越快,温度滞后就越严重,导致所得的铝热反应峰温升高就越明显。采用Kissinger法来对Al/Fe2O3纳米铝热剂的热反应动力学进行研究。将表2中Al/Fe2O3纳米铝热剂的DSC特征值β及Tp2(铝热反应峰温)值代入公式(2)进行线性拟合,便可得到一条直线。从直线斜率求Ea,从而得到Al/Fe2O3纳米铝热剂的铝热反应活化能为208.58kJ/mol。
从图3(c)可知,随着加热温度的上升,在Al/Fe2O3-RDX纳米复合物的DSC曲线上出现了两个放热峰和一个吸热峰。第一个放热峰为RDX的分解放热峰,第二个放热峰为纳米Al与纳米Fe2O3发生铝热反应的放热峰,吸热峰则为纳米铝热剂铝热反应后剩余未反应Al的熔融吸热峰。因此,Al/Fe2O3-RDX纳米复合物在加热时的反应可分为两部分:第一部分为RDX的热分解,第二部分为Al/Fe2O3纳米铝热剂的铝热反应。在DSC曲线上没有出现RDX的熔融吸热峰,这可能与纳米Fe2O3对RDX分解的催化作用有关。
从表2中Al/Fe2O3-RDX纳米复合物的DSC特征值可知,随着升温速率的提高,RDX分解放热峰温Tp1逐渐升高,放热量也逐渐增大。复合物中RDX的分解放热峰温对于升温速率有一定的依赖性[23]。与纯RDX的DSC特征值相比,复合物中RDX的分解峰温大幅下降。这是因为,复合物中的纳米铝热剂改善了RDX的热传导性,使其在热分解过程中更容易达到热平衡。同时,Al/Fe2O3纳米铝热剂中的纳米Fe2O3对复合物中RDX的分解具有催化作用,使得RDX分解反应的活化能下降,降低了RDX的分解反应温度。与超细RDX的热分解反应类似,复合物中Al/Fe2O3纳米铝热剂的铝热反应也对升温速率有一定的依赖性。这表现为纳米复合物中铝热剂的铝热反应温度也随着升温速率的上升而提高。与纯Al/Fe2O3纳米铝热剂DSC分析时的铝热反应相比,在相同升温速率下,其铝热反应温度有一定程度的降低,这可能与分布在纳米铝热剂中的RDX分解所产生的气相与纳米铝热剂接触,并对其部分活(敏)化有关。
采用Kissinger法对Al/Fe2O3-RDX纳米复合物的热反应动力学进行研究,所得的相关特征值可作为判断纳米复合物热反应的机理函数形式的主要依据。将表2中Al/Fe2O3-RDX纳米复合物的β和RDX分解峰温Tp1值、β和Al/Fe2O3纳米铝热剂反应峰温Tp2值分别代入公式(2)进行线性拟合,得到两条直线。从直线斜率、截距分别求得RDX的分解反应活化能为122.271kJ/mol,Ar为7.2467×1012;Al/Fe2O3纳米铝热剂的反应活化能为205.844kJ/mol,Ar为1.277×1012。与超细RDX的分解活化能163.901kJ/mol相比,复合物中RDX的分解活化能下降了41.63kJ/mol,这主要是因为Al/Fe2O3纳米铝热剂加入RDX中,改善了RDX的热传导性,同时纳米铝热剂中的纳米Fe2O3对RDX的分解具有较好的催化作用所致。与纯Al/Fe2O3纳米铝热剂的铝热反应活化能208.58kJ/mol相比,复合物中铝热剂的铝热反应活化能降低了2.736kJ/mol。将所得数据代入公式(2),得到Al/Fe2O3-RDX纳米复合物的热反应动力学微分(Kissinger)方程:

(3)
式中:Tp1为RDX的分解反应峰温,K;Tp2为Al/Fe2O3纳米铝热剂的铝热反应峰温,K;λ为大于0的常数。
从以上的热动力学分析可知,Al/Fe2O3-RDX纳米复合物中Al/Fe2O3纳米铝热剂通过改善RDX的热传导、大幅降低RDX的分解反应活化能来降低RDX的分解反应温度,对RDX的分解反应具有很大的促进作用。这为提高Al/Fe2O3-RDX纳米复合物的燃速,使其获得快速燃烧转爆轰,进而应用于绿色起爆药领域在理论上奠定了基础。
2.3 Al/Fe2O3-RDX纳米复合物的热催化反应机理
从Al/Fe2O3-RDX纳米复合物的热分解反应动力学研究可知,在热分解反应过程中,纳米复合物通过纳米Fe2O3降低RDX的分解反应活化能来大幅降低RDX的分解反应温度,对RDX的热分解反应具有很大的促进作用;而RDX的热分解反应对于Al/Fe2O3-RDX纳米复合物的热分解反应及其燃烧、燃烧转爆轰性能具有重要影响。因此,了解RDX的催化分解反应机理对于理解和改善Al/Fe2O3-RDX纳米复合物的热反应性能和燃烧、燃烧转爆轰性能具有重要意义。
由于纳米Fe2O3中Fe(Ⅲ)具有空轨道,而RDX中硝基官能团中的N原子具有孤对电子,两者之间易于产生配位效应。同时,RDX中N—NO2键的离解能最低(170.1kJ/mol),远低于普通C—H键的离解能(413kJ/mol),在RDX分子结构中活性最高,在外力作用下比其他键更容易断裂。本实验所用纳米Fe2O3为多孔高比表面积材料,存在大量的晶格缺陷,具有较高的反应活性。当纳米Fe2O3中孔隙边缘处的不饱和Fe(Ⅲ)与RDX 接触时,Fe(Ⅲ)与RDX中的硝基N之间很容易形成配位络合物[27-28],从而削弱了RDX中的N—NO2键,使之易于断裂。在受热时,配位络合物中的RDX失去一个硝基官能团,形成一个不稳定的大分子自由基,而Fe2O3中的Fe(Ⅲ)与—NO2结合变为Fe(Ⅱ),形成新的不稳定配位化合物,该配位化合物发生分解放出NO2,使得Fe(Ⅱ)重新变为Fe(Ⅲ);RDX分解反应产生的气相被多孔、高比表面积的氧化铁吸附、反应,同时也会被纳米Al吸附,对纳米Al具有一定的敏化作用,这使得两者所形成的纳米铝热剂的铝热反应温度有一定程度的降低。结合硝胺(RDX,HMX)在燃烧过程所得产物的一些文献[29],可推导出Al/Fe2O3-RDX纳米复合物中RDX可能的热催化分解反应机理如图4所示。
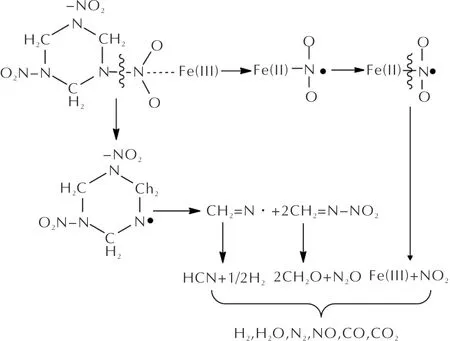
图4 Al/Fe2O3-RDX纳米复合物中RDX热催化分解反应机理Fig.4 Decomposition reaction mechanism of thermal catalysis of RDX in the Al/Fe2O3-RDX nanocomposite
从图4可知,RDX可能的热催化分解反应过程:(1)在纳米Fe2O3的催化作用下,RDX失去—NO2官能团形成大分子自由基,同时生成NO2;(2)紧接着RDX六元杂环的快速协调断裂;(3)产生1mol甲基亚胺自由基(CH2=N·)和2mol甲基硝胺(CH2=N-NO2);(4)接下来不稳定的甲基亚胺自由基离解为HCN和H·,甲基硝胺转变为甲醛(CH2O)和N2O;(5)第1步产生的NO2与HCN发生反应,N2O与甲醛进一步反应生成CO、CO2、N2、H2O和NO等。最终得到产物可能为H2、H2O、N2、NO、CO、CO2[30-31]。故RDX在纳米Fe2O3的催化作用下的热分解反应为:
C3H6O6N6→NO2+2N2O+2CH2O+HCN+H·
(4)
4HCN+5NO2→2H2O+4CO2+9/2N2
(5)
CH2O+N2O→H2O+CO+N2
(6)
从上面的反应式可知,在Al/Fe2O3-RDX纳米复合物的热分解反应过程中,多孔高比表面积的纳米Fe2O3与RDX中N—NO2键的硝基N形成配位络合物,导致RDX中活性N—NO2的断裂,加速了RDX的分解,降低了RDX的分解反应活化能,对纳米复合物的热分解反应起着促进作用,这与纳米复合物的热分解动力学分析结果基本一致。这为Al/Fe2O3-RDX纳米复合物的高燃速、快速燃烧转爆轰奠定了基础,对纳米复合物在起爆药领域的最终应用具有重要意义。
3 结 论
(1)Al/Fe2O3-RDX纳米复合物的起始热反应温度大于200℃,具有良好的热安定性。
(2)由Al/Fe2O3-RDX纳米复合物的热分解反应动力学研究可知,Al/Fe2O3纳米铝热剂通过纳米Fe2O3的催化作用降低RDX的分解反应活化能来降低RDX的热分解反应温度,对RDX的热分解反应具有很大的促进作用。与原料RDX相比,纳米复合物中RDX的分解反应活化能降低了41.63kJ/mol。
(3)在Al/Fe2O3-RDX纳米复合物的热分解过程中,多孔高比表面积的纳米Fe2O3与RDX中N—NO2键的硝基N形成配位络合物,导致RDX中N—NO2的断裂,加速了RDX的分解;RDX的分解产物也对纳米Al具有敏化作用,对纳米复合物的热分解反应起着促进作用,这为Al/Fe2O3-RDX纳米复合物的高燃速、快速燃烧转爆轰在理论上奠定了基础。

