高盐废水同步除硬除硅实验研究
刘松涛,党小梅,贾文瑶,曹 悦,张玉玲,陈传敏
(华北电力大学(保定)环境科学与工程系,河北保定 071003)
高盐废水主要来自煤化工、燃煤脱硫、印染、天然气采集加工以及各类废水回用浓缩等过程,未经处理的高盐废水含有大量无机盐离子(如Na+、K+、Ca2+、Mg2+、Cl-、PO43-等)及COD、SiO2和有机卤素等污染物〔1-4〕。
以脱硫废水、煤化工废水、采矿废水回用及零排放工艺为代表,工业废水零排放工艺一般由预处理、纳滤(NF)/反渗透(RO)浓缩和蒸发结晶3 部分组成〔5-6〕。然而,废水零排放工艺运行中仍存在许多问题,其中以反渗透和蒸发结晶设备的结垢问题最为严重。目前废水中硬度(Ca2+、Mg2+)引起的结垢问题是工业应用的主要问题,常见的成垢化合物包括CaCO3、CaSO4和Mg(OH)2〔7〕。对废水进行酸化以降低碱度可以防止生成Ca2+、Mg2+沉淀物,但酸化处理可能会导致更严重的SiO2结垢问题〔8-9〕。高盐废水中SiO2的主要形态为Sia(单硅酸和二聚硅酸)、Sib(低聚硅酸)和Sic(高聚硅酸及非活性硅)〔10〕。Ming XIE 等〔11〕提出在pH<7 时,废水中的SiO2主要以高聚硅酸[(H2SO3)n]形式存在,高聚硅酸可聚集并沉积在膜表面,部分以单硅酸形式存在的SiO2还可以在膜表面聚合形成无定形的污染层;在废水pH>7 时,SiO2结垢问题同样存在,废水中的SiO2主要以硅酸根离子(SiO32-)形式存在,SiO32-会和废水中的金属阳离子(如Ca2+、Mg2+、Al3+、Fe3+)反应生成金属硅酸盐垢〔12-13〕。硅垢很难从反渗透膜上彻底去除,最终导致废水处理系统性能恶化,如反渗透效率降低和系统运行寿命减少。
为避免膜设备、管道及蒸发结晶器的结垢问题,保证高盐废水零排放工艺长期稳定运行,必须在废水预处理部分对Ca2+、Mg2+和SiO2进行去除。Xin ZHANG 等〔14〕发现Al3+比Fe3+对废水中活性SiO2的去除效果更好,且SiO2的去除效率随Al3+投加量的增加而提升,而Fe3+投加量对SiO2的去除效果影响不大。史元腾等〔15〕讨论了双碱法除硬和除SiO2之间的关联性,同步加入药剂时,SiO2的去除与总硬度的去除是一个矛盾体,SiO2的去除与总硬度的去除呈现相反的趋势;分步加入Ca(OH)2和Na2CO3时,SiO2和总硬度的去除率同时增加,但并未对不同形态硅的去除进行研究。
目前国内外关于废水单独除硬和除硅的研究及应用已相对完善,而对废水中同步除硬和除不同形态硅的研究还相对较少。本研究以高盐废水为研究对象,探究了废水中硬度和不同形态硅的同步去除方法。
1 实验部分
1.1 试剂与仪器
试剂:铝标准溶液、氢氧化钠、碳酸氢钠、六亚甲基四胺、邻苯二酚紫、碳酸钠、氯化镁、偏铝酸钠等,均为分析纯。
仪器:紫外分光光度计T6-1650E(北京普析通用仪器有限责任公司),场发射扫描电子显微镜(SEM,Gemini SEM 300,德国蔡司)等。
1.2 废水水质
为提高废水处理过程中的除硅效率和优化除硅工艺流程,对高盐废水中的SiO2进行了定性及定量分析,根据其存在形态及含量选择分光光度法〔16〕测试。实验用水水质见表1。
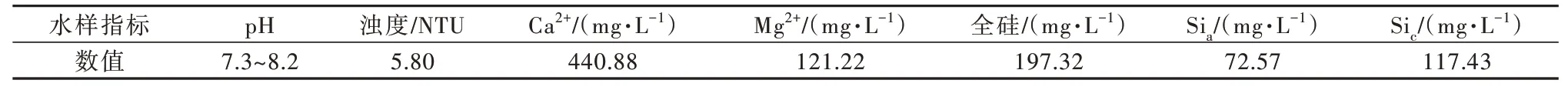
表1 实验用水水质Table 1 Experimental water quality
1.3 实验方法
1.3.1 单独混凝除硬
单独混凝除硬实验于25 ℃下进行,取若干份250 mL 高盐废水置于烧杯中,加入定量药剂,以150 r/min 匀速搅拌20 min,恒温静置1 h 后在液面下2 cm 处移取适量水样;将移取水样经0.45 µm 滤膜过滤后测定Ca2+、Mg2+残留量,每个样品平行测定3次取平均值,计算Ca2+、Mg2+去除率。
1.3.2 单独混凝除硅
前期研究已优选出偏铝酸钠(NaAlO2)为高盐废水的除硅药剂〔16〕。单独混凝除硅实验于25 ℃下进行,取若干份250 mL 高盐废水置于烧杯中,加入定量药剂,立即使用HCl、NaOH 溶液分别调节水样pH至7、8、9、10、11,以150 r/min 匀速搅拌20 min,恒温静置1 h 后在液面下2 cm 处移取适量水样;将移取水样经0.45 µm 滤膜过滤后测定不同形态SiO2的残留量,同时测定加入混凝剂前后Ca2+、Mg2+、Al3+的浓度变化。
1.3.3 混凝同时除硬除硅
混凝同时除硬除硅实验于25 ℃下进行,取若干份250 mL 高盐废水置于烧杯中,分别采用同步加药法和分步加药法处理。同步加药法:同步投加NaOH、Na2CO3和NaAlO2。分步加药法:先向高盐废水中投加NaAlO2,随后取反应后的上清液,再向上清液中投加NaOH 与Na2CO3。加入药剂后,同步加药法和分步加药法的反应溶液均以150 r/min 匀速搅拌20 min,恒温静置1 h 后在液面下2 cm 处移取适量水样,将移取水样经0.45 µm 滤膜过滤后测定Ca2+、Mg2+和不同形态SiO2的残留量。
2 结果与讨论
2.1 高盐废水单独除硬实验
以NaOH 作为pH 调节剂、Na2CO3作为混凝剂,定量考察了加药量分别为0~700 mg/L(NaOH)、0~1 600 mg/L(Na2CO3)对高盐废水中Ca2+、Mg2+的去除效果,并测定水样pH 的变化趋势,结果见图1。

图1 Ca2+、Mg2+浓度和溶液pH 随NaOH、Na2CO3投加量的变化规律Fig. 1 The changes of Ca2+ and Mg2+ concentration and pH with dosage of NaOH and Na2CO3
由图1(a)可知,随NaOH 投加量增加,Ca2+、Mg2+质量浓度均不断降低;当NaOH 投加量为500~700 mg/L 时,Mg2+质量浓度不再发生明显变化,此时Mg2+残留量约为20 mg/L,去除率为83.5%;当NaOH 投加量为700 mg/L 时,Ca2+残留量约为220 mg/L,去除率为50%。由图1(b)可知,随Na2CO3投加量增加,Ca2+质量浓度不断降低;当Na2CO3投加量为1 200~1 600 mg/L 时,Ca2+质量浓度不再发生明显变化,此时Ca2+残留量约为45 mg/L,去除率约为90%;而随Na2CO3投加量从0 增至1 600 mg/L,Mg2+质量浓度略微降低约20 mg/L。这是因为随Na2CO3投加量增加,水样中的CO3
2-会与Ca2+迅速结合生成CaCO3沉淀,使Ca2+质量浓度明显下降;同时水样中的部分CO32-发生水解反应生成HCO3-与OH-,使废水pH 升高,从而去除了少量Mg2+。
由上述除硬分析可知,NaOH 不仅对Mg2+去除效果优异,对Ca2+也有一定去除效果;而Na2CO3对Ca2+、Mg2+的去除具有双面效果。在此基础上,采用正交实验探究复合投加不同比例的NaOH 和Na2CO3对高盐废水硬度的去除规律,原水Ca2+质量浓度为440.88 mg/L,Mg2+质量浓度为121.22 mg/L,pH=8.31,结果见表2。
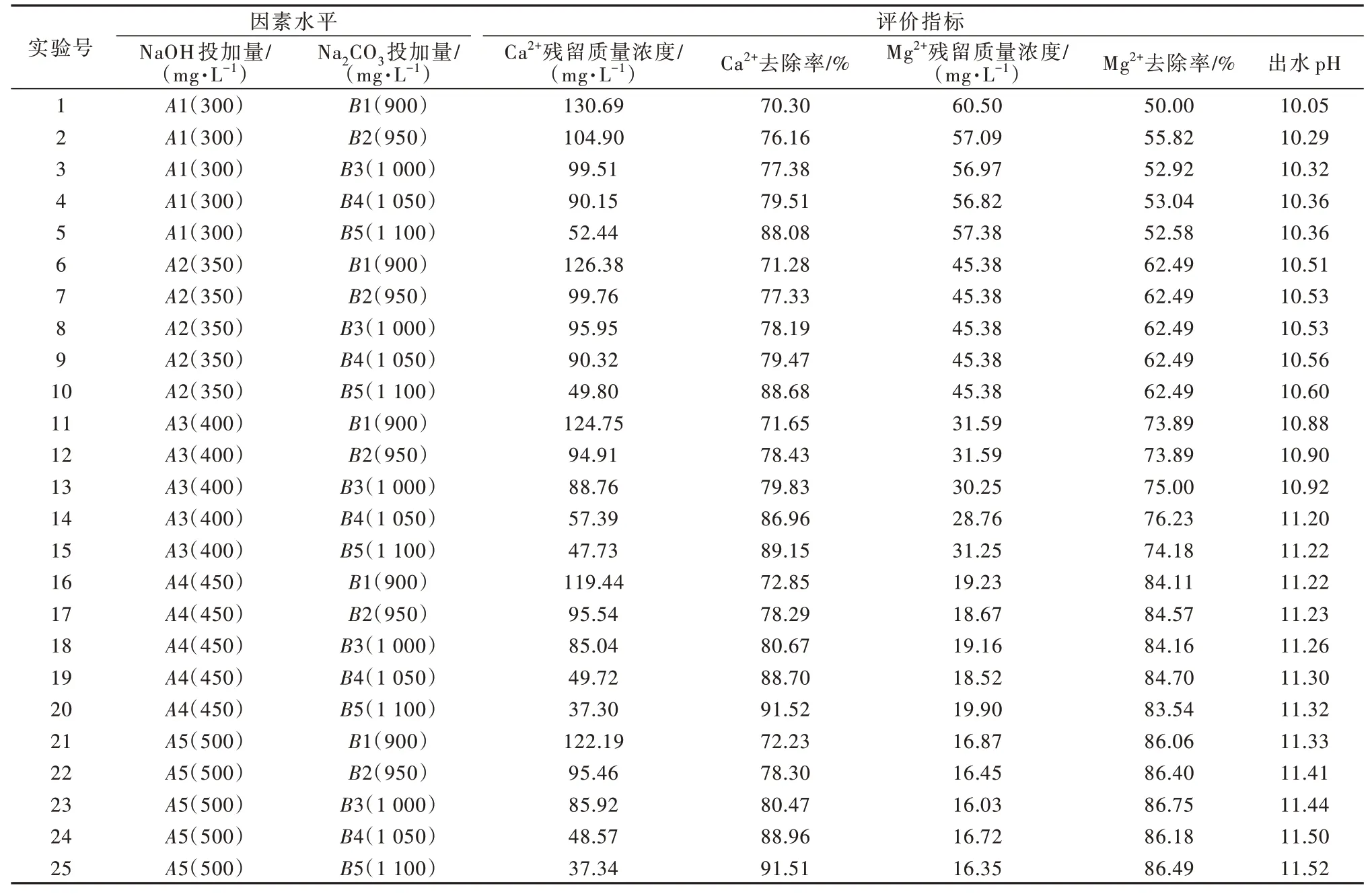
表2 正交实验因素水平及结果Table 2 Orthogonal experimental factor level and results
使用极差分析法分析最佳水平组合和各影响因素的主次顺序,结果见表3。
由表2 和表3 可知,Na2CO3投加量比NaOH 投加量对Ca2+的去除影响更大,去除Ca2+的较佳的实验条件为A4(NaOH 投加量450 mg/L)和B5(Na2CO3投加量1 100 mg/L)。NaOH 投加量比Na2CO3投加量对Mg2+的去除影响更大,去除Mg2+的较佳的实验条件为A5(NaOH 投加量500 mg/L)和B4(Na2CO3投加量1 050 mg/L)。对于本实验,Ca2+残留浓度、Mg2+残留浓度和出水pH 3 个指标均越小越好。由正交实验可知,随着NaOH、Na2CO3投加量增加,Ca2+和Mg2+残留浓度均呈下降趋势,出水pH 呈上升趋势。NaOH投加量直接影响Mg2+残留浓度与出水pH,对Ca2+残留浓度影响不大;Na2CO3投加量直接影响Ca2+残留浓度,而对Mg2+残留浓度和出水pH 影响不大。当NaOH 投加量为450 mg/L 时,Mg2+去除率可达84%左右,残留量不足20 mg/L;而继续增加NaOH 投加量至500 mg/L 时,Mg2+去除率约为86%,基本保持不变,而出水pH 仍会升高。当Na2CO3投加量为1 100 mg/L 时,Ca2+去除率高达约91.5%,Ca2+残留量不足40 mg/L。因此综合考虑,NaOH 最佳投加量为450 mg/L,Na2CO3最佳投加量为1 100 mg/L。
2.2 高盐废水单独除硅实验
本研究考察了在不同pH 操作条件下,NaAlO2混凝剂加入量对高盐废水中不同形态SiO2的去除效果。高盐废水中SiO2的主体形态为Sia和Sic,Sib含量较小,可忽略不计,因此并未对Sib的去除效果进行分析。在pH 为7~11 时,定量考察了NaAlO2投加量(0~1 000 mg/L)对高盐废水中全硅、Sia、Sic的去除效果,同时测定了水样中Ca2+、Mg2+浓度的变化趋势。除硅实验结果见图2。
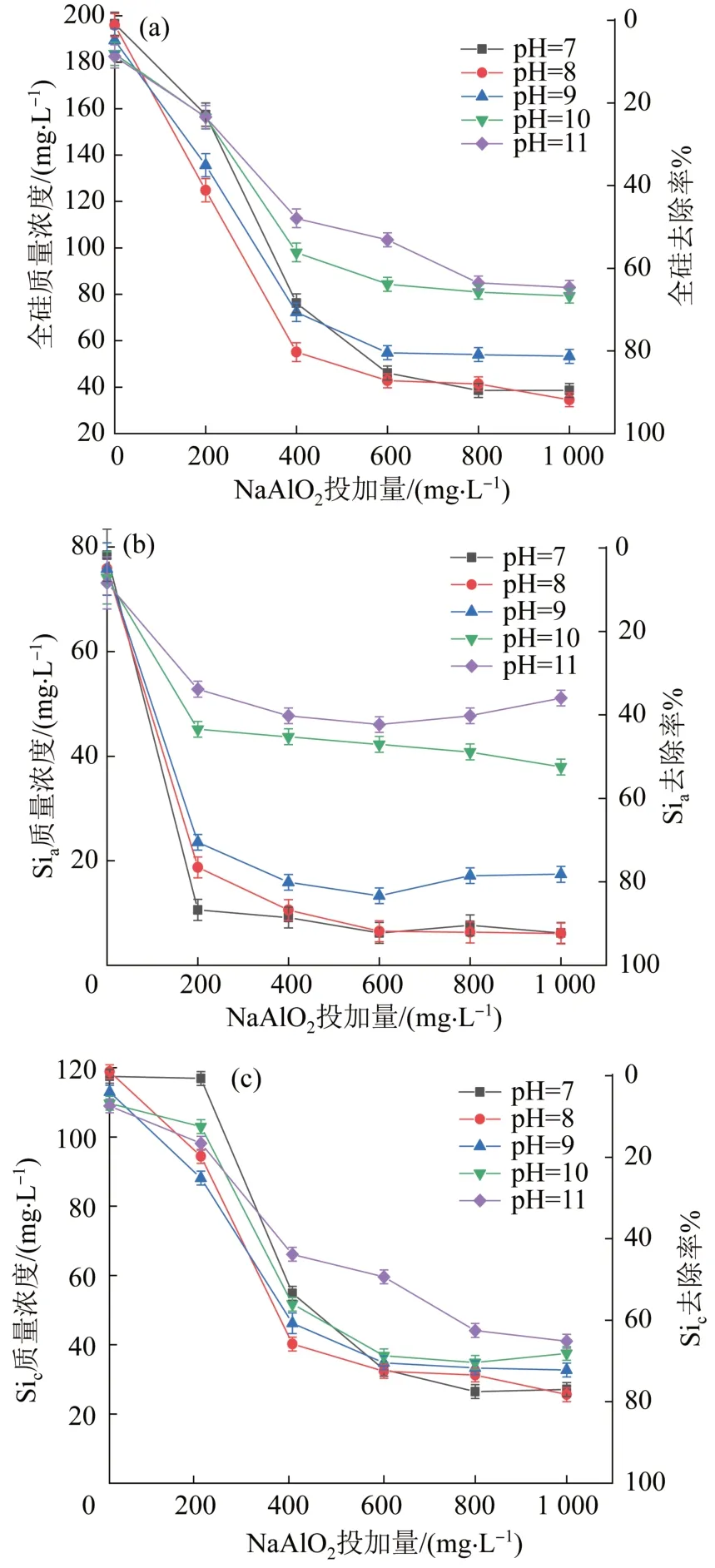
图2 全硅、Sia和Sic浓度及去除率随pH 和NaAlO2投加量的变化规律Fig. 2 The concentration and removal rate of all-silicon,Sia and Sic vary with pH and NaAlO2 dosing
由图2 可知,NaAlO2除硅效果优异,在不同pH条件下,随NaAlO2投加量增加,全硅、Sia(单硅酸和二聚硅酸)、Sic(高聚硅酸及非活性硅)质量浓度均明显降低。在pH 为7、NaAlO2投加量仅为200 mg/L的条件下,Sia去除率高达92%;在pH 为8、NaAlO2投加量为600 mg/L 的条件下,Sia去除率约为92%,Sic去除率约为80%,全硅去除率约为90%,Sia、Sic残留量分别约为5、20 mg/L。
水样中Ca2+、Mg2+质量浓度的变化趋势见图3。
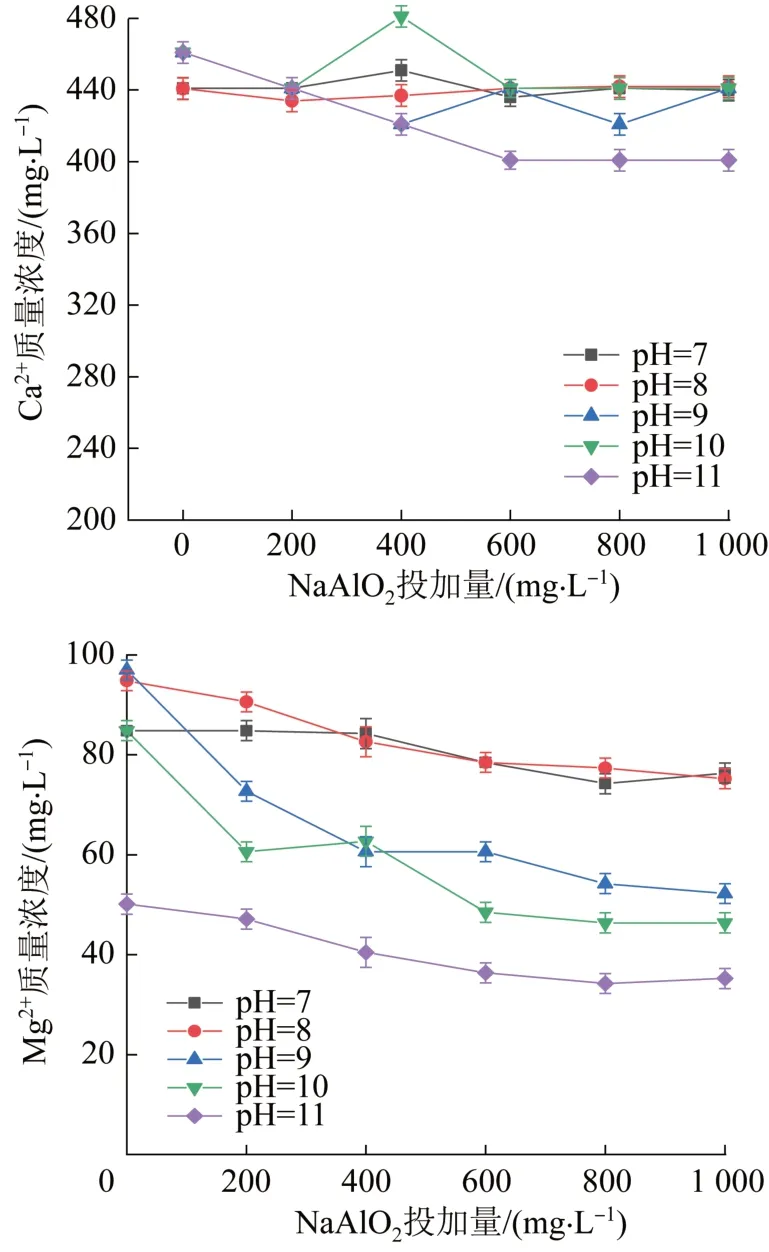
图3 Ca2+和Mg2+浓度随pH 和NaAlO2投加量的变化规律Fig. 3 The concentration of Ca2+ and Mg2+ varies with pH and NaAlO2 dosing
由图3 可知,在不同pH 及NaAlO2投加量下,Ca2+质量浓度基本保持不变,即NaAlO2对Ca2+无明显去除效果。在NaAlO2最佳除硅pH(8)下,随NaAlO2投加量增加,Mg2+质量浓度逐渐降低,并于NaAlO2投加量达到600 mg/L 后趋于稳定,此时Mg2+质量浓度约为80 mg/L,去除率为17.3%,即NaAlO2对Mg2+有少量去除效果。
当使用铝剂除硅时,还需考虑Al3+残留情况。水样中金属离子残留量过高会导致后续反渗透系统出现不溶性金属沉淀,造成膜污染并降低膜通量,从而影响废水处理效率并带来额外的经济损失〔17-18〕。在pH=8 下,水样中Al3+残留量及全硅去除率随NaAlO2投加量的变化趋势见图4。
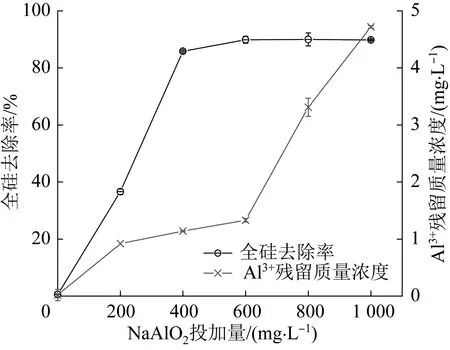
图4 Al3+残留量及全硅去除率随NaAlO2投加量的变化规律Fig. 4 The residual amount of Al3+ and the removal rate of total silicon vary with the dosage of NaAlO2
由图4 可知,在NaAlO2投加量为0~600 mg/L 时,Al3+残留质量浓度缓慢上升;NaAlO2投加量为600 mg/L 时,Al3+残留质量浓度约为1 mg/L,全硅去除率已高达90%;随NaAlO2投加量继续增大,Al3+残留质量浓度急速上升,全硅去除率保持不变。因此确定最佳NaAlO2投加量为600 mg/L。
2.3 同时除硬除硅实验
2.3.1 同步加药法除硬除硅
由高盐废水单独除硬实验与除硅实验可知,最佳除硬条件为投加450 mg/L NaOH 与1 100 mg/L Na2CO3;最佳除硅条件为pH=8、投加600 mg/L NaAlO2。因此,同步加入450 mg/L NaOH、1 100 mg/L Na2CO3、600 mg/L NaAlO2,考察高盐废水中Ca2+、Mg2+、全硅、Sia、Sic的去除效果,结果见表4。
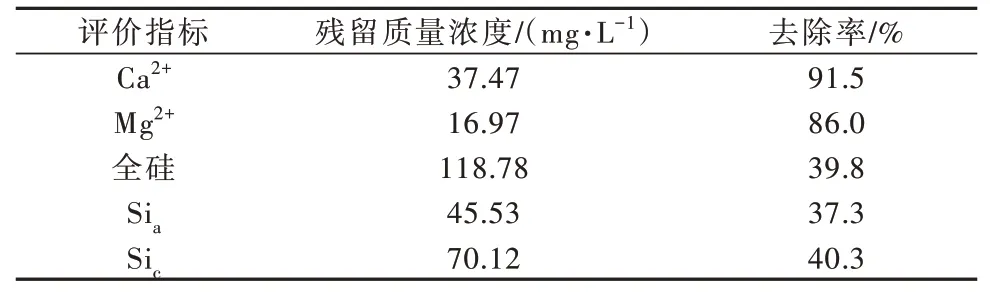
表4 同步加药法除硬除硅实验结果Table 4 Experimental results of hardness and silicon removal by synchronous dosing method
由表4 可知,在同步加药法除硬除硅实验中,Ca2+、Mg2+去除率与高盐废水单独除硬实验结果基本保持一致,去除率分别为91.5%、86.0%;而全硅、Sia、Sic去除率与高盐废水单独除硅实验结果存在较大差异,去除率分别仅为39.8%、37.3%、40.3%。测定水样pH 发现,此时水样pH 已高达11.5,而NaAlO2的最佳除硅pH 为8。为考察除硅效率降低问题,分别将0~1 600 mg/L Na2CO3与600 mg/L NaAlO2同步加入高盐废水水样中,分别测定全硅去除率及水样pH,结果见图5。
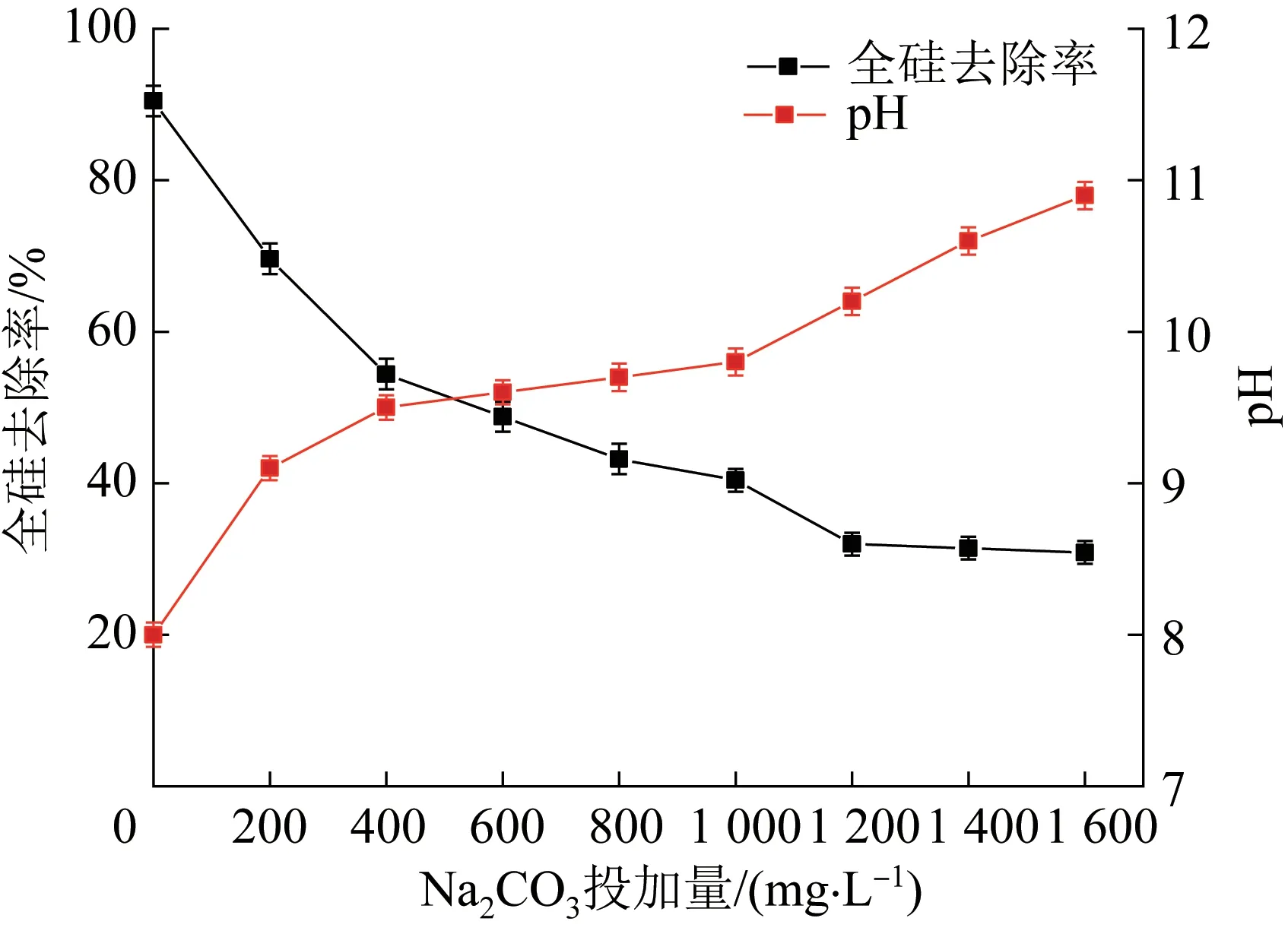
图5 全硅去除率及pH 随Na2CO3投加量的变化规律Fig. 5 The removal rate of total silicon and pH vary with the dosage of Na2CO3
由图5 可知,随着Na2CO3投加量增加,水样pH持续上升,全硅去除率降低。同步加药法中,除硬与除硅相矛盾,加入除硬药剂NaOH、Na2CO3会导致除硅效率降低。
由高盐废水单独除硬和除硅实验可知,使用NaOH、Na2CO3除硬后,水样pH 为11.3;而高盐废水原水pH 为8.3,NaAlO2最佳除硅pH 为8;若先去除高盐废水中的硬度,再去除高盐废水中的SiO2,为达到预期除硅效果,还需要对除硬后的水样进行酸化。因此综合考虑,先去除高盐废水中的SiO2,再去除硬度,即采取分步加药的方法。
2.3.2 分步加药法除硬除硅
先向高盐废水中投加600 mg/L NaAlO2,待沉淀后取上清液,再向上清液中投加450 mg/L NaOH 与1 100 mg/L Na2CO3,分别考察高盐废水中Ca2+、Mg2+、全硅、Sia、Sic的去除效果,结果见表5。

表5 分步加药法除硬除硅实验结果Table 5 Experimental results of hardness and silicon removal by step-by-step dosing method
由表5 可知,在分步加药法除硬除硅实验中,全硅、Sia、Sic去除率与高盐废水单独除硅实验结果基本保持一致,去除率分别为90.1%、95.2%、84.3%;Ca2+、Mg2+去除率分别为91.5%、88.3%,较同步加药除硬除硅实验,Mg2+去除率略有上升。
分别向高盐废水中只加入除硅药剂NaAlO2、同步加入除硬除硅药剂、分步加入除硬除硅药剂,比较3 种不同加药方式对Ca2+、Mg2+及全硅的去除率,结果见图6。
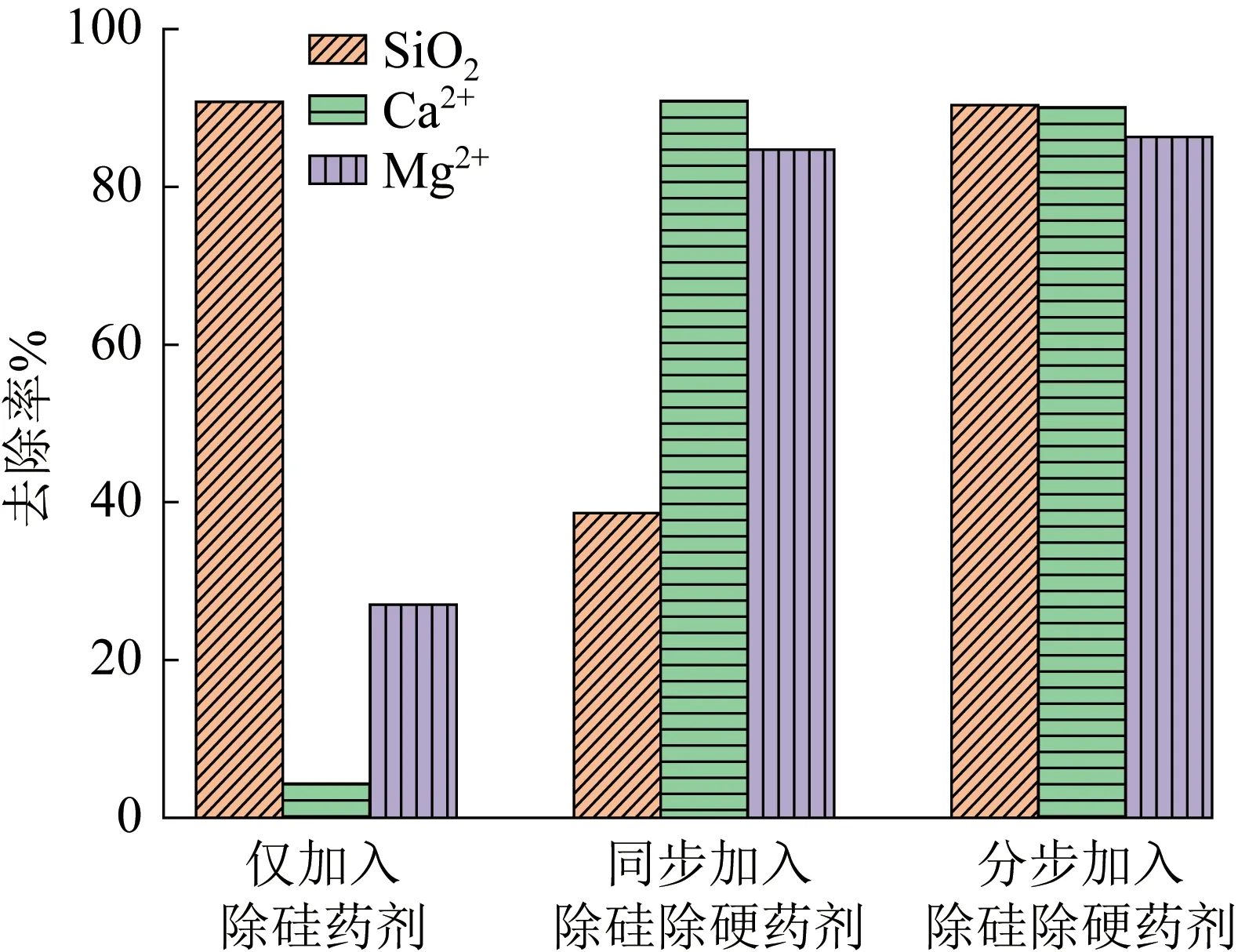
图6 不同加药方式对Ca2+、Mg2+及全硅的去除率Fig. 6 Removal rates of Ca2+,Mg2+ and total silicon in different dosing methods
由图6 可知,仅向高盐废水中加入NaAlO2无法有效去除废水中的Ca2+、Mg2+;同步加药法可有效去除高盐废水中的Ca2+、Mg2+,对SiO2的去除效果较差;而使用分步加药法对Ca2+、Mg2+及SiO2均能高效去除,实现高盐废水同时除硬除硅的目的。这是因为NaAlO2的水解会生成NaOH 和Al(OH)3,Al(OH)3与硅发生反应并生成沉淀从而去除硅。但同步加药法由于加入了NaOH 和Na2CO3,水样pH 增大,抑制了NaAlO2的水解〔19〕,导致全硅去除率降低。
3 混凝产物表征分析
对NaAlO2作为混凝剂形成的沉淀物形貌进行表征分析。将完全反应后的水样用0.45 µm 滤膜快速抽滤后收集滤膜上的沉淀物,置于烘箱中低温加热至完全干燥。采用场发射扫描电镜(SEM)对沉淀物进行表征分析,结果见图7。图7(a)、(b)实验条件为pH=8、NaAlO2投加量为200 mg/L,图7(c)、(d)为pH=8、NaAlO2投加量为600 mg/L,图7(e)、(f)为pH=11、NaAlO2投加量为600 mg/L。

图7 不同反应条件下NaAlO2除硅沉淀物SEMFig. 7 SEM of precipitates of NaAlO2 removing silicon under different reaction conditions
由图7 可知,不同反应条件下的块状沉淀物表面均附着有白色晶体,图7(c)和图7(d)中白色晶体最多,图7(e)和图7(f)中白色晶体最少。结合除硅实验结果,推测块状沉淀物为铝的化合物,而白色晶体为吸附的SiO2。
使用FT-IR 对沉淀物进行分析,结果见图8。

图8 NaAlO2除硅沉淀物FT-IRFig. 8 FT-IR of precipitates of NaAlO2 removing silicon
由图8 可知,所有沉淀物样品均观察到相同的特征吸收峰。3 424 cm-1和1 635 cm-1处出现O—H的特征吸收峰,对应结合水或氢氧化合物基团;1 013 cm-1处出现Si—O 的特征吸收峰,对应SiO2;750 cm-1处出现Al—O 的特征吸收峰,对应Al(OH)3等铝的化合物。在pH 相同的条件下,随NaAlO2投加量增加,Al—O 和Si—O 特征吸收峰透过率逐渐降低,表明随着NaAlO2投加量增加,Al(OH)3等铝的化合物含量不断增加,吸附了更多的SiO2。在NaAlO2投加量相同的条件下,pH 为9 时O—H 和Al—O 特征吸收峰透过率最低,而Si—O 特征吸收峰的透过率却高于pH=8,推测在弱碱性条件下NaAlO2水解生成了更多的[Al(H2O)6]3+、[Al6(OH)14]4+、[Al7(OH)17]4+,而此类高价聚合离子对小分子Sia的去除效果略差于Al(OH)3;当pH 过高时,NaAlO2的水解被抑制,导致除硅效率降低。
4 结论
1)高盐废水单独除硬的最佳实验条件:NaOH、Na2CO3的投加量分别为450、1 100 mg/L,Ca2+、Mg2+去除率分别达到91.5%、83.5%。
2)高盐废水单独除硅的最佳实验条件:pH 为8、NaAlO2投加量为600 mg/L,全硅、Sia、Sic去除率分别约为90%、92%、80%;Al3+残留量较小,约为1 mg/L。
3)同步加药法中Ca2+、Mg2+去除率与单独除硬实验结果保持一致,去除率分别为91.5%、86%;而全硅、Sia、Sic去除率与单独除硅实验结果存在较大差异,去除率分别仅为39.8%、37.3%、40.3%。分步加药法先加入除硅药剂去除SiO2,再加入除硬药剂去除硬度,全硅、Sia和Sic去除率与单独除硅实验结果基本保持一致,去除率分别为90.1%、95.2%、84.3%;Ca2+、Mg2+去除率分别为91.5%和88.3%,Mg2+去除率较单独除硬实验略有上升。

