配合物[Ni(Me3en)(acac)]BPh4合成过程优化的基本思路与初步实施结果
——第10届全国大学生化学实验邀请赛无机及分析化学实验试题合成过程优化的基本思路与初步实施结果
董志强,阮婵姿,张春艳,易波,†,陈欣,†,陈烨超,†,吕银云,许振玲,潘蕊,翁玉华,章文伟,任艳平,*
1厦门大学化学化工学院,化学国家级实验教学示范中心(厦门大学),福建 厦门 361005
2南京大学化学化工学院,化学国家级实验教学示范中心(南京大学),南京 210023
前文[1,2]已经介绍了南京大学为“第10届全国大学生化学实验邀请赛”设计的“无机及分析化学实验试题”,即“配合物[Ni(Me3en)(acac)]BPh4的合成及其溶剂/热致变色行为研究”所富有的教学意义、实验实施过程、实验结果及其拓展问题的探讨内容,其内容概要如图1。
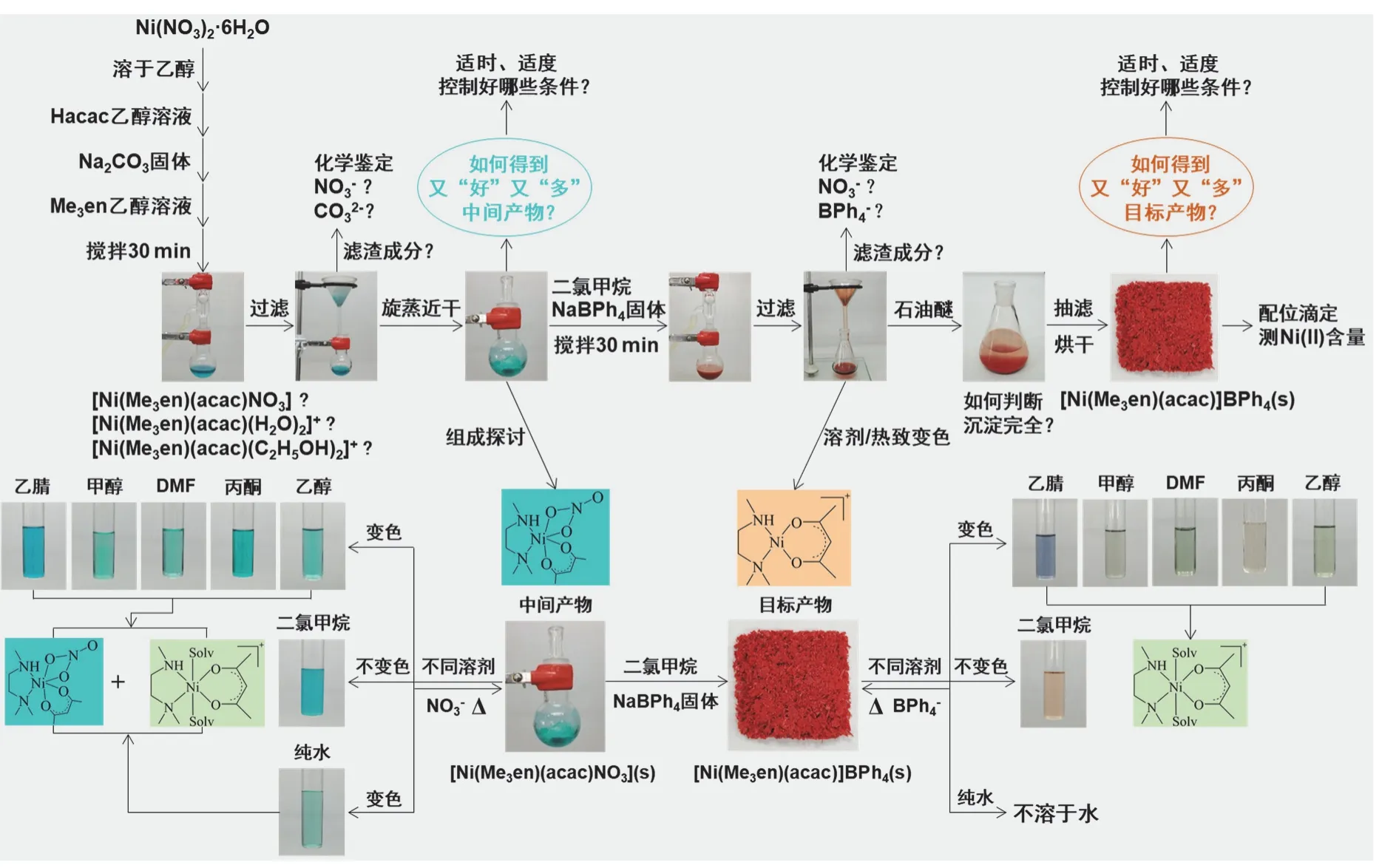
图1 “配合物[Ni(Me3en)(acac)]BPh4的合成及其溶剂/热致变色行为研究”内容概要
本文主要介绍有关配合物[Ni(Me3en)(acac)]BPh4的合成过程优化的基本思路及其初步实施结果等内容。不同合成过程及其初步结果概览如图2所示。
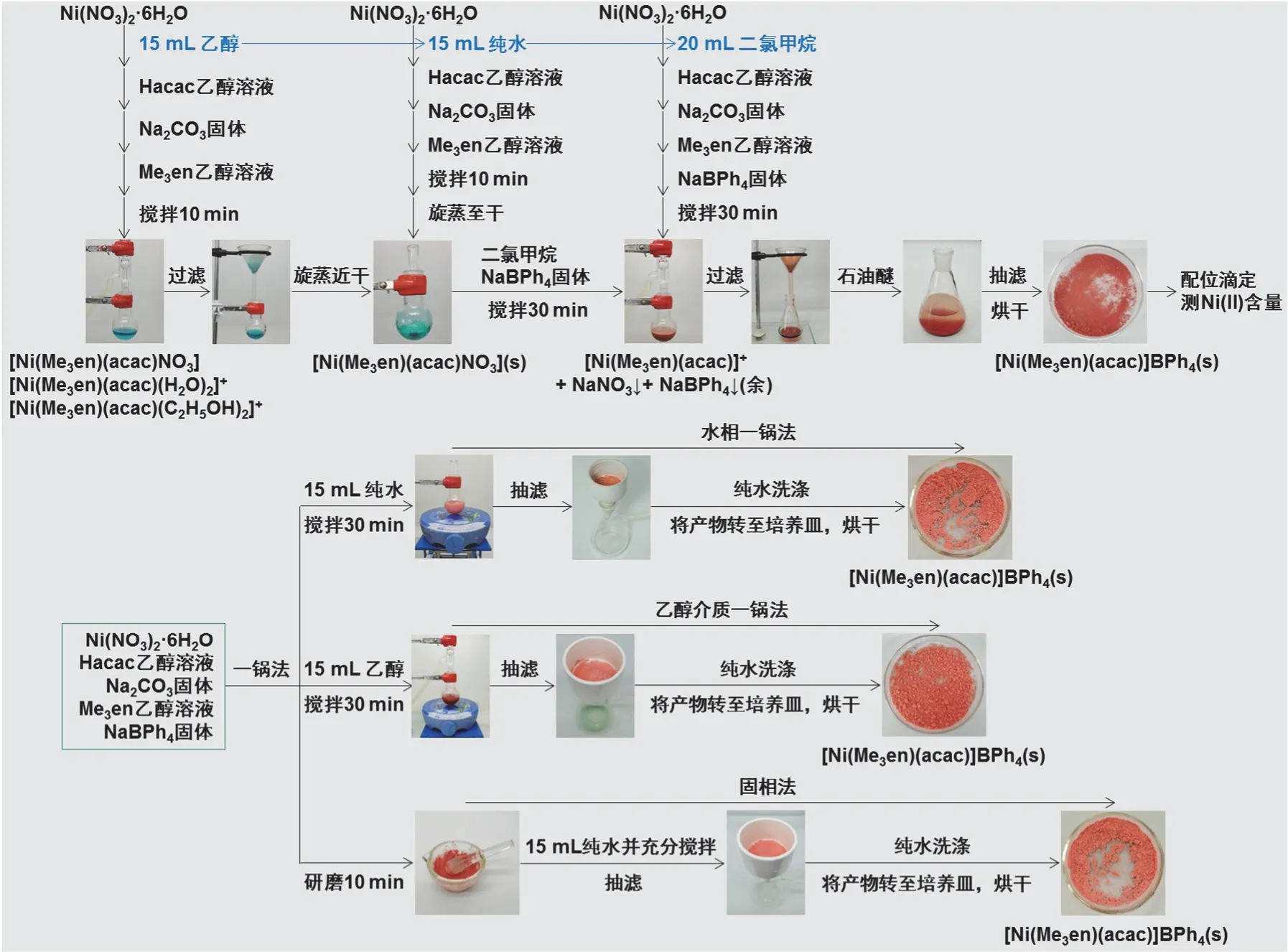
图2 配合物[Ni(Me3en)(acac)]BPh4不同合成过程及其初步结果概览
如前[1]所述,配合物[Ni(Me3en)(acac)]BPh4的合成分为两大步,也称为“乙醇-二氯甲烷+石油醚两步法”,即先在乙醇介质中,由Ni(NO3)2(竞赛题目中强调“称量Ni(NO3)2·6H2O时,用滤纸尽可能将其表面水吸干”)与乙酰丙酮(Hacac)和N,N,N’-三甲基乙二胺(Me3en)以及在Na2CO3存在下得到中间产物[Ni(Me3en)(acac)NO3];再在二氯甲烷介质中,由中间产物[Ni(Me3en)(acac)NO3]与NaBPh4反应并引入不良溶剂石油醚使目标产物[Ni(Me3en)(acac)]BPh4析出,有关合成反应见方程式(1)、(2)和(3)。
在给定的合成原理指导下,已经成功得到目标产物[1,2],即实验事实证明合成原理毋容置疑。根据所给定的合成条件,如反应介质和NaBPh4的引入等以及具体实验过程,结合所学的有关配位化学基础理论知识,引导学生再从理论上分析其合成原理在热力学上的可能性和动力学上的可行性,帮助学生将所学理论知识应用于实践,并通过实践加深对理论知识的理解。
从上述实验原理分析,加速促使反应(3)向右进行的因素有以下三个方面:1) 在得到中间产物后,巧妙转换溶剂,即使用“一举三得”的二氯甲烷作溶剂,既能溶解中间产物,又没有配位能力,还能将目标产物与体系中的杂质有效分离;2) 引入本身没有配位能力,且空间位阻很大的BPh-4阻止了体系中溶剂分子或NO-3配位;3) 更重要的是,对于给定合成体系的Ni2+来说,形成四配位结构的平面正方形配合物比形成六配位八面体结构的配合物能够获得更多的晶体场稳定化能,因此在BPh-4的驱动下,中心金属Ni(II)更趋向于形成配位数为4的平面正方形结构的配离子[Ni(Me3en)(acac)]+。综上所述,在同时满足形成配位数为4和配位数为6的Ni(II)镍配合物的体系中,由于上述三个方面有利因素的共同作用,可以控制体系选择性地定向形成目标产物[Ni(Me3en)(acac)]BPh4。这也是通过控制条件达到精准合成的典型实例。这种有关配合物设计合成的思想方法也是科研中常常用到的。
但对于配合物[Ni(Me3en)(acac)]BPh4的具体合成过程,还有以下疑问或设想:
1)在给定的合成步骤中,特别强调在称取Ni(NO3)2·6H2O固体之时,要用滤纸尽可能将其表面水吸干,为什么?若合成体系中引入了水,对合成结果有什么影响?
2) 如上所述,该配合物成功合成的关键步骤是采用了配位能力很弱的二氯甲烷作为反应介质以及引入了没有配位能力[3],且空间位阻很大的BPh-4阻止了体系中溶剂分子或NO-3配位。既然如此,在反应物量比都不变的条件下,如果直接在二氯甲烷介质中,所有反应物都在“一锅”中反应是否可以得到目标产物呢?
当然,消除这些疑问或证实这些设想的最好方法还是实验事实。下面先来探讨水对合成结果的影响。
为了便于学生直观认识和比较不同合成过程、实验条件、实验现象及实验结果,文中也比较详细地以照片的形式展示了有关配合物[Ni(Me3en)(acac)]BPh4合成的不同过程,旨在培养学生的问题意识和批判性思维能力。
1 用水代替乙醇,即“水-二氯甲烷+石油醚两步法”合成[Ni(Me3en)(acac)]BPh4
首先,我们从理论上分析体系中引入水的几种可能情况:1) 体系中有Na2CO3存在,若体系中引入的水太多,碱性介质可能导致Ni2+水解沉淀,进而导致中间产物的纯度和产率降低;2) 乙酰丙酮能被水分解为乙酸和丙酮[4],也同样导致中间产物的产率降低;3) H2O的配位能力较强,若体系中有大量水存在,导致中间产物可能是有H2O参与配位的配合物[Ni(Me3en)(acac)(H2O)2]NO3,或致使旋蒸除水时间长或难于除尽水而影响后续实验效果。
体系中引入水是否对中间产物的形成有影响?
在反应原料及其量比和其他合成条件都不变的情况下,仅仅用15 mL纯水代替15 mL乙醇,其具体实验过程及实验现象如图3所示。

图3 “水-二氯甲烷+石油醚两步法”合成[Ni(Me3en)(acac)]BPh4实验过程及实验现象
从图3可以看出,用水代替乙醇也能成功得到红色产物,并且表观上来看,所得产物的产率高、晶态好、色泽鲜艳,说明了水对中间产物的形成没有影响,也就是说,Ni(NO3)2·6H2O固体具有很强的吸湿性,所以在称取Ni(NO3)2·6H2O固体时,用滤纸吸干其表面的水,仅仅就是为了称取有效量的Ni(NO3)2·6H2O以防影响产率。
有关合成反应见方程式(4)、(5)和(3)。
用水代替乙醇还具有以下优点:Na2CO3在水中的溶解度大,有利于Na2CO3与Hacac的反应完全,使中间产物的产率可能提高,进而提高了目标产物的产率。同时,用水代替乙醇,反应生成的NaNO3也易溶于水,旋蒸前不需要过滤,溶于水的杂质也不影响后续实验(其杂质能一并在后续过滤时除去),避免由于多次过滤分离而造成物料转移的损失,影响目标产物的产率。
用水代替乙醇后,由于水的沸点较高,旋蒸除水的时间较长。实验结果证实,以水作为介质的合成反应可以在烧杯中进行,反应30 min后,可直接加热蒸发至近干,得到蓝绿色中间产物。这样用水代替乙醇,不仅节约了乙醇,还不需要旋转蒸发仪,同时也减少了相当量的乙醇废液的排放;实验教学成本降低,在一般的无机及普化实验室都可以广泛开展该实验。
2 二氯甲烷介质中“一锅”法合成[Ni(Me3en)(acac)]BPh4
图3的合成实验过程及结果证明水对配合物的合成不仅没有影响,而且用水代替乙醇还有上述诸多优点。在反应物量比都不变的条件下,如果直接在二氯甲烷介质中将所有反应物都一起加入“一锅”中反应是否可以得到目标产物?一起观察图4所示的实验过程及实验现象。
从图4可以看出,在二氯甲烷介质中,所有反应物都放入“一锅”中反应也能成功得到红色产物,产率较高,且产物的晶态和色泽都较好。有关合成反应见方程式(6)和(7)。
在这“一锅”法反应合成中,最终只有红色产物能溶于二氯甲烷,其他杂质如生成的NaNO3以及未反应完全的Na2CO3和反应剩余的NaBPh4都以滤渣形式过滤除去。比较图4与图3可以看出,图4所展示的二氯甲烷介质中的“一锅”法合成反应时间短(共需30 min),且省去了中间产物的过滤分离以及旋蒸等步骤,实验效率大大提高,同时也减少了过滤等造成物料损失而导致目标产物产率降低的几率。二氯甲烷介质中“一锅”法合成[Ni(Me3en)(acac)]BPh4,还省去了15 mL乙醇或纯水溶解Ni(NO3)2,不需要旋蒸分离,也就不需要旋转蒸发仪,实验成本也降低了,同时也减少了废液的排放,在一般无机或普化实验室都可以同时安排多人同时开展实验教学,并使学生有更充足时间试验产物的溶剂/热致变色性质和探讨其变色机理。
通过实验证实:1) 水对中间产物的形成没有影响;2) 也能在二氯甲烷介质中“一锅”法合成得到红色产物。但上述目标产物合成及其后处理过程都要用到二氯甲烷、石油醚等有机溶剂(每个学生完成实验要用近30 mL二氯甲烷和30 mL石油醚),这两种溶剂都有刺激性气味,且沸点还比较低,需要在通风橱中操作,同时排放大量有机废液,存在环保问题和安全隐患,不符合绿色、环保的实验要求。
如上所述,通过采用没有配位能力的二氯甲烷作为反应介质,以及引入没有配位能力且空间位阻很大的过量控制配位数为4的平面正方形结构的配合物[Ni(Me3en)(acac)]BPh4的形成,并借助目标产物溶于二氯甲烷,而体系中生成的杂质NaNO3和反应剩余的NaBPh4都不溶于二氯甲烷,将产物与杂质有效分离。那么,没有配位能力的二氯甲烷是否是必要条件?如果仅从分离的角度来说,鉴于产物难溶于水,而杂质NaNO3等易溶于水,从理论上来说在以水作为介质的“一锅”反应也可以得到目标产物。能否用水代替图4中的二氯甲烷而实现“一锅”法反应合成目标产物,还是通过实验来证实。
3 以水作为介质的“一锅”法合成[Ni(Me3en)(acac)]BPh4
在反应物量比都不变的条件下,直接以水作为介质,将所有反应物都一起加入“一锅”中反应,具体实验过程及实验现象如图5所示。

图5 以水作为介质的“一锅”法合成[Ni(Me3en)(acac)]BPh4实验过程及实验现象
从图5可以看出,以水作为介质,所有反应物都放入“一锅”中反应也能顺利得到红色产物,且产率较高,但产物的晶态和色泽较差,这可能与结晶溶剂及过程有关[5]。有关合成反应见方程式(8)和(9)。
从图5也可以看出,以水作为介质的“一锅”法合成反应时间短;借助产物难溶于水的性质,巧妙将产物与易溶于水的杂质如NaNO3以及未反应完全的Na2CO3和NaBPh4分离,产物合成及其后处理过程都不用有机溶剂,实现绿色化合成,同时实验过程也大大简化。以水作为介质的“一锅”法反应合成得到红色产物,进一步说明图3和图4中用到二氯甲烷的作用主要是溶解中间产物以及分离目标产物与杂质。
4 以乙醇作为介质的“一锅”法合成[Ni(Me3en)(acac)]BPh4
既然用水代替图4中的二氯甲烷的“一锅”法反应也能顺利得到目标产物,并能将产物与杂质有效分离。想必用乙醇代替图4中的二氯甲烷也能实现“一锅”法反应合成目标产物,其具体实验过程及实验现象如图6所示。

图6 以乙醇作为介质的“一锅”法合成[Ni(Me3en)(acac)]BPh4实验过程及实验现象
从图6可以看出,以乙醇作为介质,所有反应物都放入“一锅”中反应也能顺利得到红色产物,产率也较高,但产物的晶体细小、色泽也较差,这可能与结晶溶剂及过程有关[5]。有关合成反应见方程式(10)和(11)。
比较图6与图5所示的以乙醇和水作为介质的“一锅”法反应合成过程,由于产物(微溶于乙醇)及杂质如NaNO3以及未反应完全的Na2CO3都难溶于乙醇,需要用水溶去杂质而达到分离目的,合成过程除用乙醇外也不用其他有机溶剂,基本实现绿色化合成;从图6可以看出,第一次抽滤所得滤液为绿色(与目标产物微溶于乙醇所得溶液的颜色一致,如图6中比色管中溶液颜色),将滤液蒸干得到红色固体,说明目标产物微溶于乙醇并发生颜色变化[2]。
以水和以乙醇作为介质的“一锅”法反应合成都能成功得到红色产物,进一步说明了目标产物的形成主要是由没有配位能力且空间位阻很大的BPh-4控制导向的,与上述所选用的溶剂没有关系。既然如此,能否用固相法合成配合物[Ni(Me3en)(acac)]BPh4?来看图7所示的具体实验过程。
5 固相法合成[Ni(Me3en)(acac)]BPh4
在反应物量比都不变的条件下,将所有反应物都一起加入研钵中,稍加研磨体系就由蓝绿色变为红色。具体实验过程及实验现象如图7所示,有关合成反应见方程式(12)和(13)。
从图7可以看出,将所有反应物按照所给量比关系在室温下混合,稍加研磨体系就由蓝绿色变为红色,说明由BPh-4诱导的平面正方形结构的配合物合成反应是非常快速的。固相法合成过程及其后处理操作简单、方便,实验过程安全、绿色、环保,且实验成本低。但研磨破坏了产物的晶态,所以表观上看,产物的晶态和颜色都不好。如果仅需要研究产物的溶剂/热致变色性质时,可以通过这种捷径来合成目标产物,也借机让学生了解和学习固相合成法[6]。
6 不同合成过程所得产物在二氯甲烷、乙腈中的颜色及其紫外-可见吸收光谱
为了初步证明优化合成过程前后所得产物的一致性,分别以二氯甲烷和乙腈为溶剂,配制浓度分别为1 mg·mL-1和15 mg·mL-1的不同合成过程所得产物溶液各10 mL,其溶液颜色以及分别以二氯甲烷和乙腈溶剂作为参比的UV-Vis吸收光谱如图8所示。
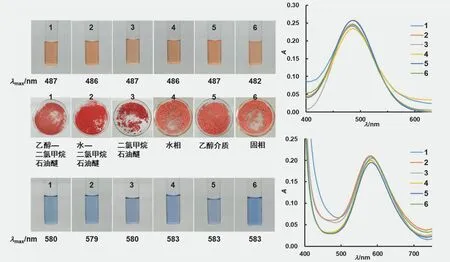
图8 不同合成过程所得产物在二氯甲烷、乙腈中的颜色及其UV-Vis吸收光谱
从图8可以看出,不同合成过程所得产物在二氯甲烷和乙腈中的颜色及其最大吸收波长基本一致,这也初步证明了各产物的组成与结构基本一致,说明不管是哪种形式的“一锅”或固相反应,同时满足形成配位数为6和配位数为4的配合物的条件时,最终都选择性地定向形成配位数为4的平面正方形结构的配合物,进一步说明是控制定向形成配位数为4的平面正方形结构的配合物[Ni(Me3en)(acac)]BPh4的绝对因素。
7 结语
通过实验证实,以水或乙醇为介质或通过固相法合成都能得到目标产物,说明给定的体系尽管同时满足形成配位数为6和配位数为4的配合物的形成条件,但由于具有极大的空间位阻和极弱的配位能力BPh-4的存在,促使反应选择性地定向生成配位数为4 的平面正方形结构的[Ni(Me3en)(acac)]BPh4配合物。以水为介质或固相法合成目标产物,其合成过程简单,不用旋转蒸发仪;全程也不用其他有机溶剂,从源头上控制了有机溶剂的使用,符合绿色、环保实验要求,使该实验项目更具普适性和推广性。
当然,作为教学实验项目,并不是实验过程越简单就越好,因为实验过程既要承载对学生“三基”(基础理论知识、基本思想方法、基本实验技能)和“双意识”(安全意思、环保意识)的教育和培养,更要承载对学生思维和研究能力的培养,要在实验教学过程中不断抛给学生需要思考和解决的问题。对于涉及安全、环保问题的实验项目,有必要课后引导学生去分析和探讨改进或优化实验条件或实验过程的思路和方法,并指导学生付诸于实践,让学生通过实验过程和结果分析、比较和判断改进或优化思路和方法的科学性和可行性,培养学生的分析、认识和判断的能力以及洞察力和创新能力。
另外,基于配合物[Ni(Me3en)(acac)]BPh4其溶剂/热致变色效应,将它与具有层状结构的SAP(saponite,皂石)或高分子聚合物Nafion (一种全氟磺酸聚合物)等材料混合,并经适当处理,可以制得有机溶剂识别材料(固体颗粒物或薄膜)。对于这样有潜在用途的化合物,要产生良好的社会效益和经济效益,就要让学生知道其合成过程应是安全、环保、低廉、高效、快捷的。
总的来说,只有对整个实验原理、实验条件理解到位,才能对原合成过程提出问题,进而引导学生学习思考合成过程优化的思路,即从哪几方面思考优化,选择或优化合成条件的依据是什么等;合成产品,还需要引导学生从哪些方面判断其经济效益和社会效益。针对原合成实验条件或过程中存在的不足进行优化或改进的过程,其实就是一个发现问题、提出问题、分析问题和解决问题的过程,对培养学生的问题意识和好奇心具有重要作用。
鉴于本文篇幅所限,有关配合物[Ni(Me3en)(acac)]BPh4的合成过程的进一步优化条件、结果比较以及改进后的实验项目及其教学意义见后续报道。

