探究二氧化硫性质的实验改进
张子扬 曹曼丽 张秀莲 霍朝晖
摘要: 对人教版教材中探究二氧化硫性质的实验提出改进的实验方案,装置为有机玻璃材质,将多组实验作了整体化设计。优化后实验具有实验现象明显、操作简易、安全可靠、趣味性、绿色化等优点,有助于学生掌握二氧化硫的基本性质。
关键词: 二氧化硫; 实验改进; 实验探究; 有机玻璃材质
文章编号: 1005-6629(2023)09-0071-03 中图分类号: G633.8 文献标识码: B
1 原教材实验分析
《普通高中化学课程标准(2017年版2020年修订)》中明确指出“科学探究与创新意识”是化学学科核心素养之一,要求学生“能从问题和假设出发,依据探究目的设计探究方案,运用化学实验、调查等方法进行实验探究”。
人教版高中化学必修第二册中设置了两个探究SO2性质的实验,分别验证SO2的水溶性、酸碱性及漂白作用。但SO2是一种有毒气体,容易逸出到空气中,危害人体健康,所以并不适合作为演示实验在课堂上操作。其中第一组实验在水下进行,第二组实验要求在通风橱内进行,需要使用明火,两组实验均存在一定的操作难度。
SO2作为一种典型的酸性氧化物,是高中化学课程的重要学习内容,学生通过本节的学习,建立起结构化的元素观,在实验过程中构建证据推理的探究模型,因此本课的实验探究具有重要的地位及作用。本文对教材原实验进行了优化改进,将多组实验作了整体化设计,使实验装置简易化、集成化,同时探究SO2的水溶性、密度、酸碱性、还原性和漂白性等基本性质,以培养学生的证据推理的素养与创新意识,并建立绿色化学的观念。
2 改進后的实验
2.1 实验仪器和试剂
实验装置(20cm×10cm×5cm)、无痕透明胶、磁铁、纸盒、熔胶、针筒、真空采血管、小烧杯、珍珠棉(聚乙烯发泡棉,又称EPE珍珠棉,是一种新型环保的包装材料)、无水Na2SO3、浓硫酸、石蕊试剂、品红溶液、BaCl2溶液、KMnO4溶液、吹风机、陶土网
2.2 实验装置
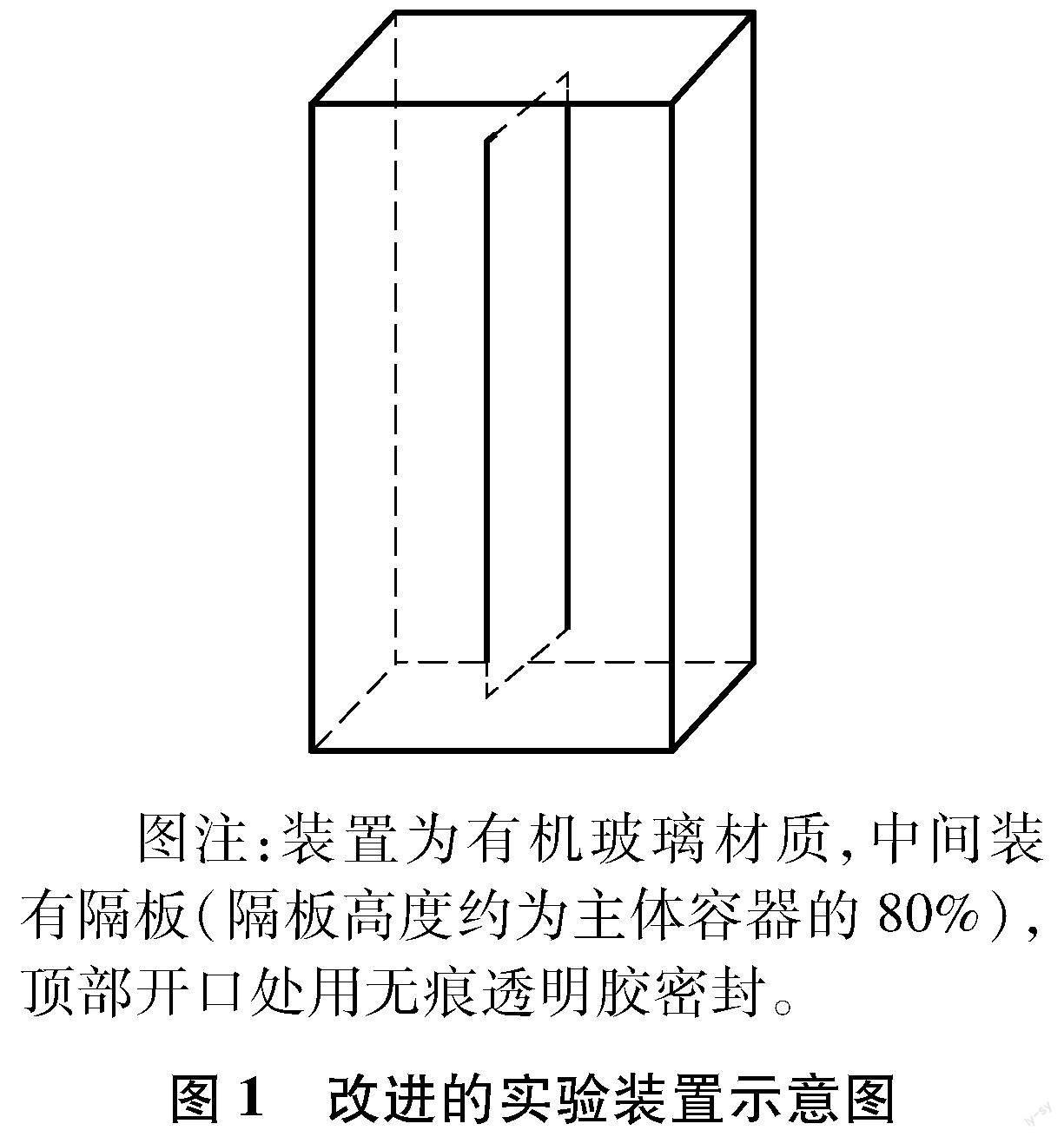
实验装置为有机玻璃材质,具有透光度高、重量轻等优点,整体为六面体,除顶部开放外其余五面均为密封;装置内部中间位置设置隔板,隔板上下悬空,见图1。
2.3 实验准备
实验开始前,将Na2SO3粉末放于纸盒内,纸盒为顶部开口的六面体,将纸盒与一块磁铁用熔胶固定,放置在装置内部,在装置外部用另一块磁铁吸住,由此来控制纸盒(磁铁选用长条形磁铁,长条形磁铁的磁极分布在两端,因此旋转外部磁铁就可以使内部磁铁跟着旋转。但不能选用圆币状磁铁)。
通过旋转装置外部的磁铁来带动装置内部的磁铁,从而使纸盒旋转,进而使Na2SO3粉末落入下方烧杯里的浓硫酸中,产生SO2气体[Na2SO3+H2SO4(浓)SO2↑+Na2SO4+H2O]。通过控制磁铁旋转的幅度,能够控制Na2SO3下落的量,从而控制该反应的速率。
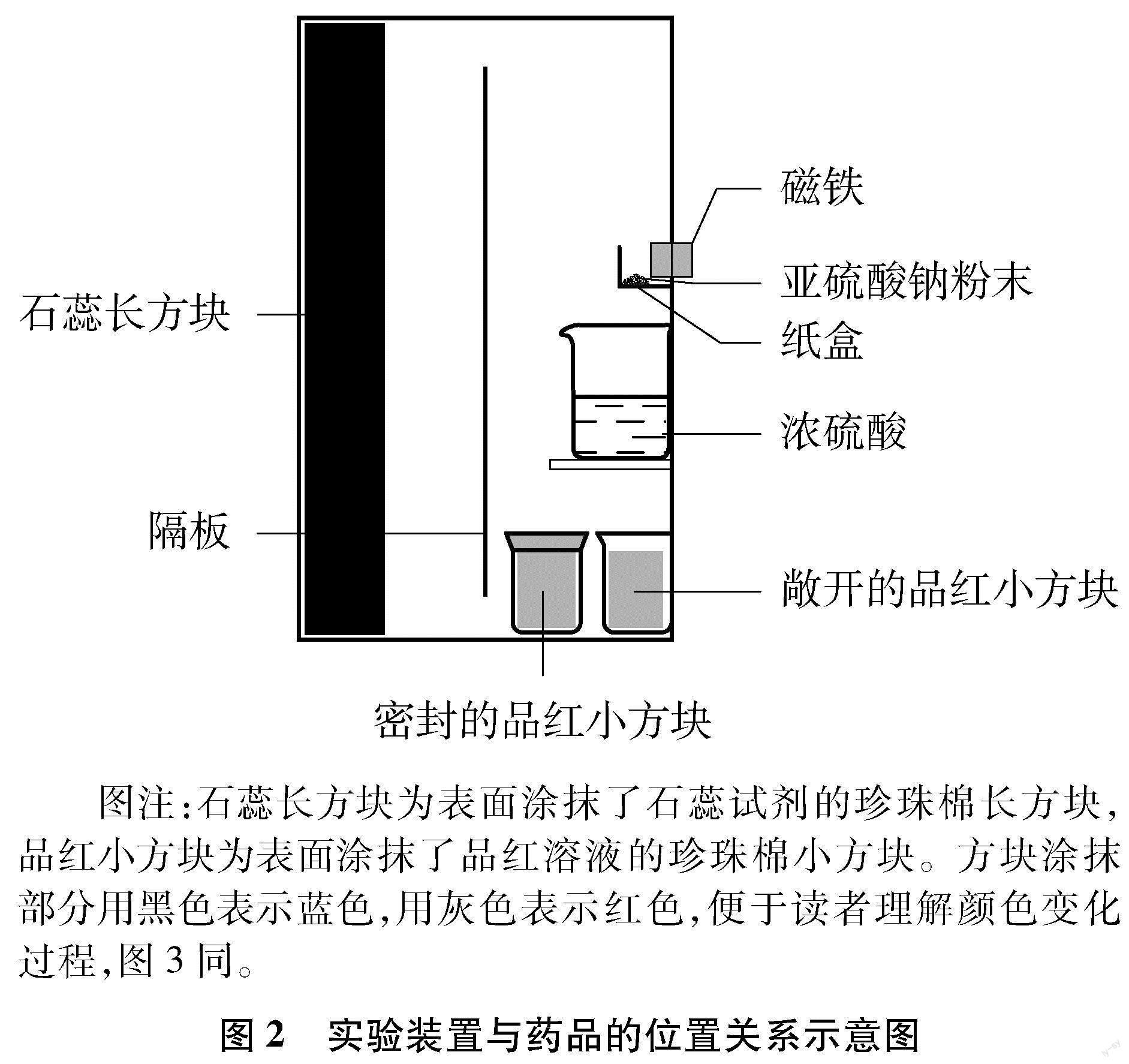
将品红试剂、石蕊试剂分别涂抹在块状珍珠棉的表面(见图2),使试剂附着在珍珠棉表面,便于学生观察。实验中严格控制试剂的涂抹量,保证能够快速地与SO2反应完全,且现象明显。该设计符合绿色、环保的理念。
装置底部的两个小烧杯分别装有涂抹了品红溶液的块状珍珠棉(见图2),其中一个为敞开状态,另一个则经过密封处理,成为一组对照试验,验证SO2的漂白作用。
3 实验演示的讲解
3.1 探究实验的相关知识
在实验探究前,教师可以向学生介绍与探究实验相关的知识,既可以让学生从问题和假设出发,更好地了解实验的目的及意义,又可以拓展化学知识领域,培养“科学态度与社会责任”的化学学科核心素养。在探究实验操作前,教师可以适当地介绍下面几个方面的背景知识[1]。
(1) 熏硫法是一种药材炮制的方法,操作方法为将硫磺放置在药材的上方点燃,使生成的SO2向下沉降,作用于药材,根据硫磺与药材之间的位置关系,可以判断SO2的密度比空气大。
(2) 经过熏硫处理的药材方便储存和运输,有效防止药材被氧化,由此可以判断SO2具有还原性。
(3) 对药材中SO2的残留量,我国有着严格的执行标准(GB2760-2014),所以在上市前,需要经过脱硫处理,具体操作为用流水清洗、用清水浸泡,由此可以判断SO2具有易溶于水的性质。
(4) 部分的纸浆和草帽等制品利用SO2进行漂白,但随着时间的流逝,这些纸张和草帽会逐渐发黄,由此可以判断SO2具有漂白作用,但漂白作用不稳定。
3.2 实验步骤及现象
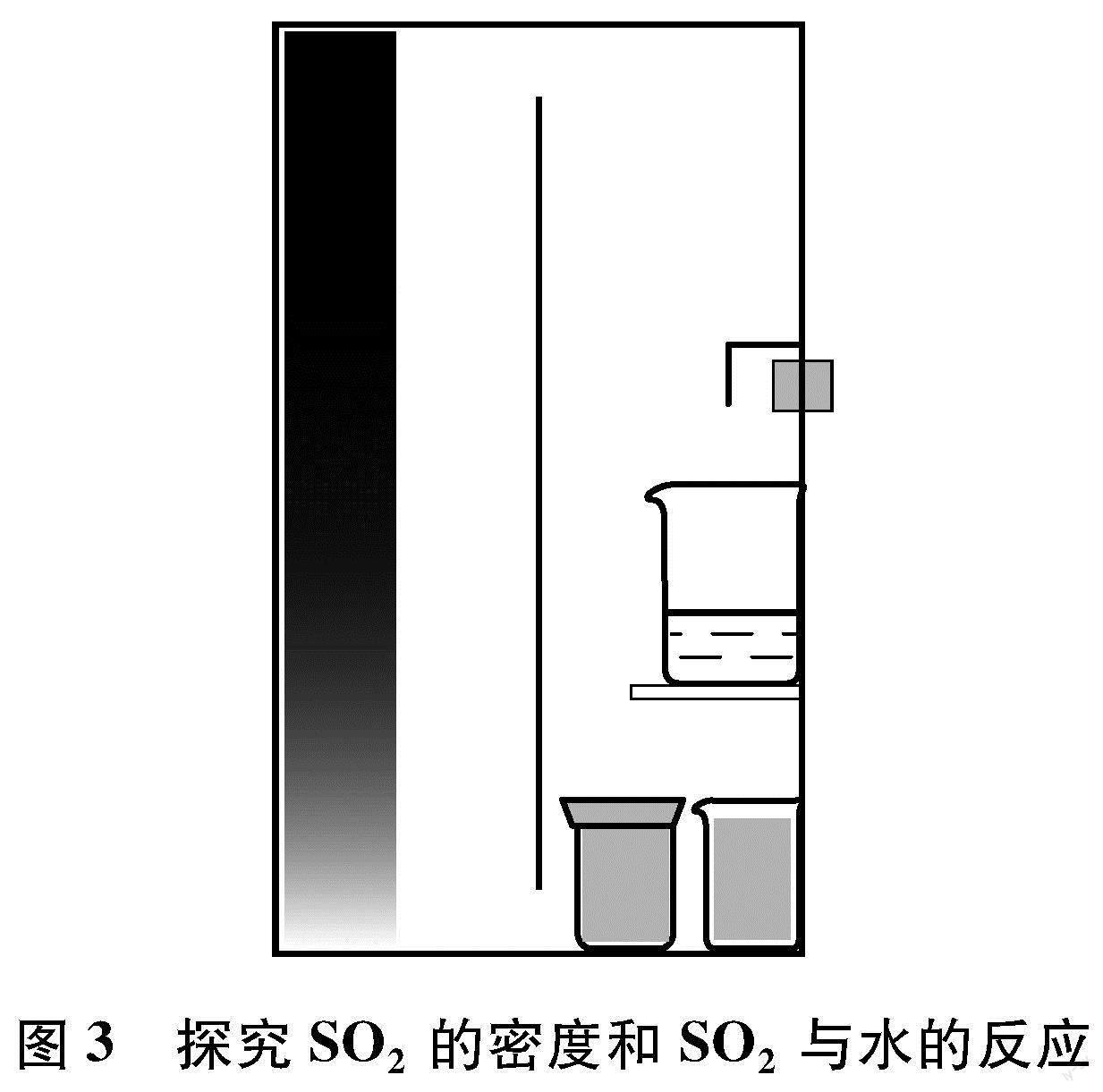
旋转装置外部磁铁,使亚硫酸钠粉末落入浓硫酸溶液中,产生SO2气体,观察装置左侧的石蕊长方块可以发现,其颜色迅速由蓝色变为红色(见图3),证明SO2易溶于水,迅速与石蕊溶液中的水生成酸,从而使石蕊试剂变红。同时,长方块从底部开始变色,说明SO2最先出现在装置的底部,证明SO2的密度比空气大。
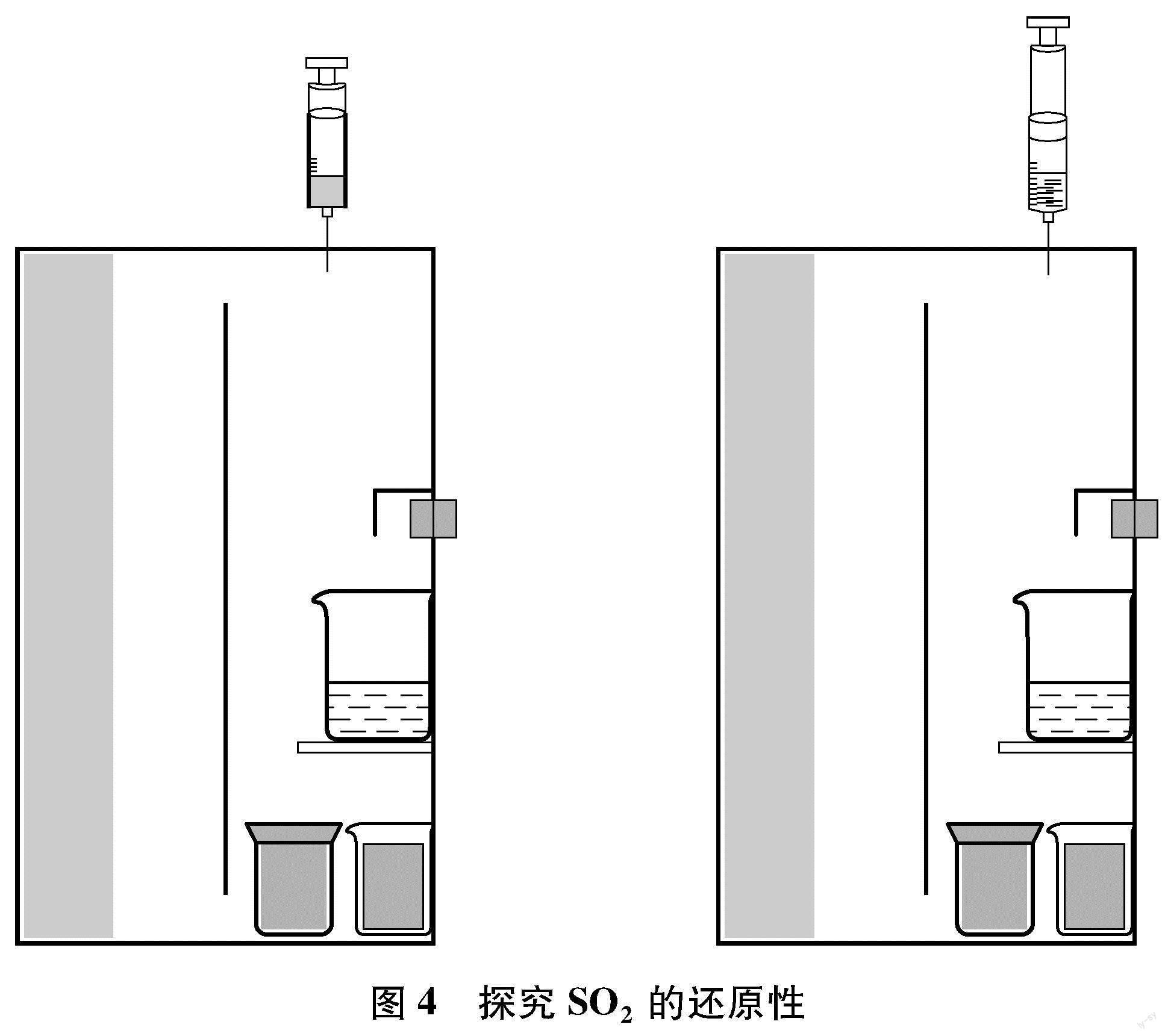
将装有KMnO4溶液的针筒插入装置顶部,从装置内抽取部分气体,发现针筒内KMnO4溶液的颜色逐渐褪去,最后变为无色,见图4。
拔出针筒,将针筒内的溶液注入装有BaCl2溶液的真空采血管中,发现溶液由澄清变得浑浊,说明溶液中含有SO2-4离子,SO2在针筒内的反应体现还原性。
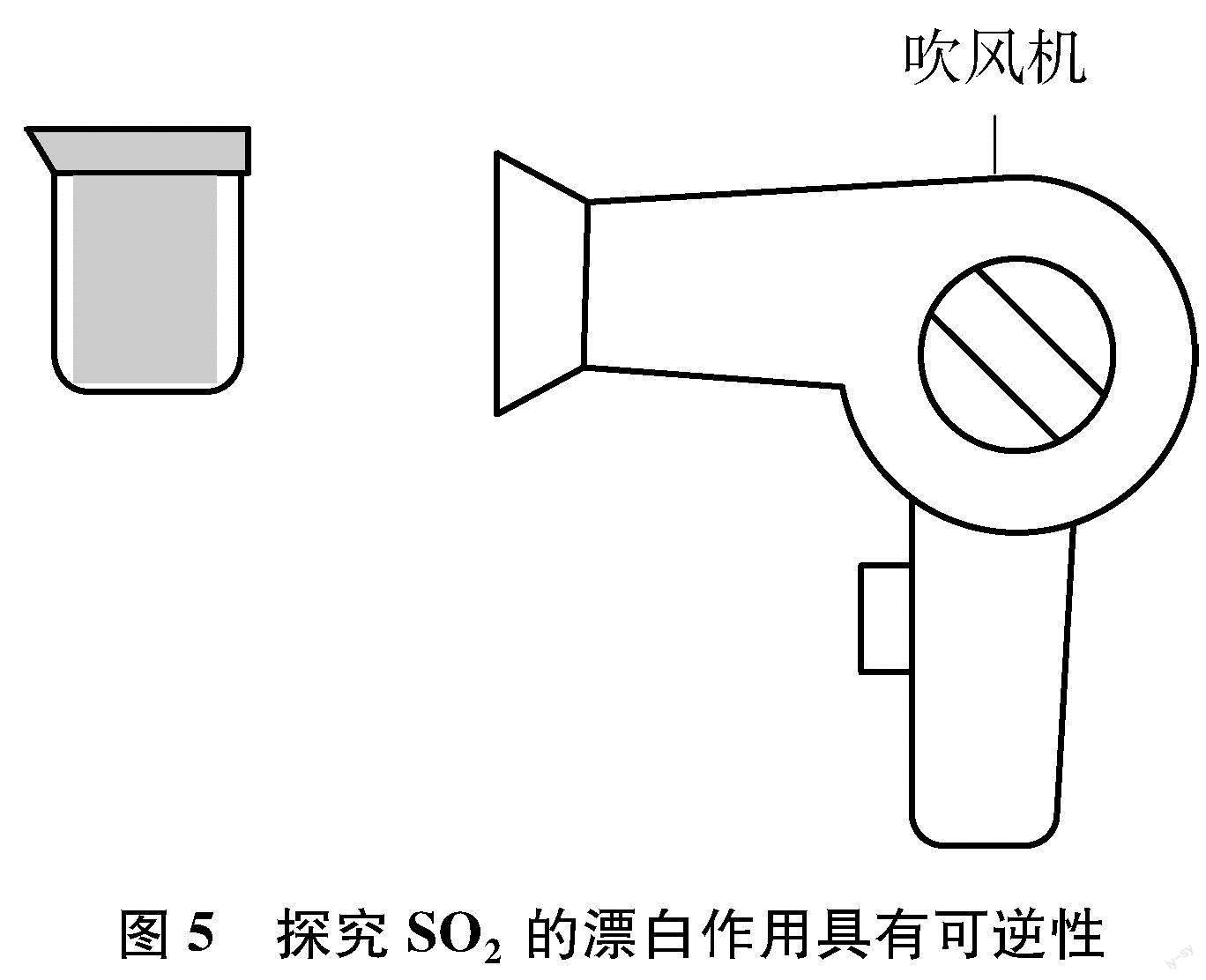
事先准备好经过SO2漂白处理的品红溶液,装入小烧杯中并进行密封处理,利用吹风机进行加热,可以发现品红溶液的颜色恢复了,见图5。
4 实验优点
(1) 实验装置设计巧妙,将多组实验进行整合,不仅有利于教师课堂演示,也便于学生观察实验现象。实验装置的可操作性强,旋转磁铁、利用注射器抽取气体等操作具有趣味性,能激发学生兴趣。如能安排为学生实验,非常有利于培养学生“科学探究与创新意识”的化学学科核心素养。
(2) 实验装置设计严谨,利用质地柔软且粘性强的无痕透明胶进行密封,在制取SO2的过程中,装置内部气压变大,其他的密封方式容易导致气体泄漏,无痕透明胶能够保证装置的气密性良好。在使用针筒抽取装置内气体的操作时,无痕透明胶极具弹性,在针头插入装置时紧紧包裹针头,针头抽出后立即回弹,不会留下针孔,以保证实验过程中不会有SO2逸出到空气中造成环境污染。
(3) 相较于教材原实验,本实验紧扣本章节课题“化工生产中的重要非金属元素”,探究了SO2在工业生产中所体现的常见特性。基于生活化的情景素材,对SO2的性质做出预测和假设,再设置相应的探究实验方案,体现了完整的证据推理过程,同时建立起关于硫元素的认知模型,此过程培养了学生“证据推理与模型认知”的化学学科核心素养[2]。
(4) 在装置内设置了一组对照实验,直接与SO2接触的品红溶液颜色逐渐褪去。在装置外设置另一组经过SO2漂白处理的品红溶液,经过加热处理会恢复原来的颜色,与装置内品红溶液组成第二组对照实验,通过这两组对照实验,帮助学生理解SO2的漂白性和原理。
参考文献:
[1]吴发明, 赵文吉, 姚秋阳, 杨扶德, 刘付松, 吴应贵, 韦中兰. 基于性状特征和有效组分含量的变化综合评价熏硫对党参药材品质的影响[J]. 食品工业科技, 2018,(1): 276~279,292.
[2]石磊, 李德前. 研读课程标准关注教材变化——以“二氧化硫的性质和应用”教学为例[J]. 化学教学, 2020,(8): 43~48.

