LC-MS联合单细胞测序分析探讨参苓白术散治疗原发性骨质疏松症的作用机制
陈伟坚 姜涛 周宜 杨吉勇 刘炜年 王海彬 梁笃 刘文刚*
1. 广州中医药大学第五临床医学院,广东 广州 510095
2. 广东省第二中医院(广东省中医药工程技术研究院),广东 广州 510095
3. 广州市正骨医院,广东 广州 510045
4. 广州中医药大学第一附属医院骨科,广东 广州 510405
原发性骨质疏松症(primary osteoporosis, POP)是一种以骨强度下降、骨微结构破坏为特征的全身性骨骼疾病,是骨形成与骨吸收呈负平衡导致骨重建失衡[1]。POP的防治目标在于通过药物干预和康复治疗维持骨量,减少骨量丢失,并降低骨折风险[2],中药在防治POP中发挥了重要作用[3-4]。
POP归属于中医学“骨萎”的范畴,与脾肾二脏关系最为相关。“参苓白术散”记载于《太平惠民合剂局方》一书中,由“人参、茯苓、白术、白扁豆、桔梗、莲子、砂仁、山药、薏苡仁、甘草”组成,是益气健脾的中医经典名方。现代药理学发现其中药具有调节骨免疫、改善骨密度、抗氧化、抗炎等作用[5]。相关研究发现,其能够改善POP患者骨代谢平衡,但其具体分子机制尚不明确[6-7]。
本研究运用液质联用技术(LC-MS)鉴定参苓白术散的化学成分,通过单细胞转录谱及WGCNA分析筛选POP的细胞亚群及核心靶点,并运用虚拟分子对接验证成分与核心靶点间的活性,挖掘参苓白术散治疗POP的成分及作用机制。
1 材料和方法
1.1 LC-MS鉴定参苓白术散化学成分
1.1.1参苓白术散溶液制备[8]:称取党参 20 g、茯苓 20 g、白术 30 g、白扁豆 10 g、桔梗 10 g、莲子 10 g、砂仁 10 g、山药 10 g、薏苡仁 10 g、甘草 10 g,加水煎煮2次,浓缩并定容至250 mL,用正丁醇萃取中药煎液并减压浓缩,取2 mL样品加入甲醇溶液,振荡混匀后离心10 min,取上清液用于后续LC-MS检测。
1.1.2色谱条件[9]:采用Thermo Vanquish超高效液相系统,色谱柱:ACQUITY UPLC®HSS T3,设定流速:0.25 mL/min,柱温:40 ℃。正离子模式:流动相为 0.1 %甲酸乙腈和甲酸。负离子模式:流动相为乙腈和5 mmol/L甲酸铵水,并进行梯度洗脱。
1.1.3质谱条件[10]:采用Thermo Q Exactive质谱检测器,分别设定正、负离子喷雾电压为3.50 kV和-2.50 kV,采集信号前10离子进行二级裂解,同时采用动态排除杂乱无关的MS/MS信息。
1.1.4化学成分鉴定:根据分子量误差≤30 ppm对鉴定物进行筛选,结合人类代谢组数据库(human metabolome database, HMDB)、METLIN、Massbank、LipidMaps以及mzClound数据库确认注释获得参苓白术散的化学成分[11]。
1.2 参苓白术散潜在作用靶点筛选
从PubChem数据库获取参苓白术散化学成分结构式,并导入Swiss Target Prediction得到潜在作用靶点。
1.3 POP靶点获取
在GEO数据库中下载与POP相关的基因芯片数据,利用bioconductor R软件进行背景矫正、归一化和表达值计算,并利用limma R软件计算两组间的差异表达基因,设定调整后P值<0.05,表达变化幅度≥2倍(∣log2FC∣≥1.00)为筛选DEGs的标准。
1.4 加权基因共表达(WGCNA)网络构建
将POP-DEGs表达矩阵数据利用WGCNA R软件构建POP-WGCNA网络。通过无标度网络计算出最佳的软阈值β,之后通过β次幂运算构建邻接矩阵。随后建立拓扑重叠矩阵(topological overlap matrix,TOM)为基本元素构造层次聚类树。采用动态混合切割法进行模块划分、合并以及绘制基因树状图。模块划分后,计算每个模块的特征向量 (module eigengene,ME),关联POP患者及正常人的临床性状,使用皮尔逊相关系数计算ME与样本临床性状的相关程度,将与POP相关程度最高的模块定义为枢纽模块。
1.5 POP单细胞测序数据分析
1.5.1单细胞测序数据预处理:在GEO数据库下载与POP相关的单细胞测序数据,利用Limma、Seurat、Dplyr和Magrittr R软件过滤低丰度数据。设定Seurat对质量控制的筛选条件为:基因表达>3个细胞,基因数200 ~10 000细胞,线粒体基因百分比<20 %。
1.5.2细胞注释和标记基因筛选:对数据进行主成分(PCA)分析,取前16个PCs进行tSNE以及UMAP聚类分析,设定分辨率为0.2。根据标记基因表达情况注释细胞簇群,并使用DESeq2和wilcox计算各细胞簇群间的DEGs。
1.6 参苓白术散治疗靶点在POP细胞簇群中的分布
借助Venn R软件将药物作用靶点与POP-DEGs以及WGCNA-枢纽基因进行交互映射,输出共表达VENN图,并利用Seurat软件对共同基因在不同细胞簇中的表达进行展示。应用STRING数据库构建共同靶点互作网络(protein-protein interaction,PPI),进行拓扑分析以筛选关键靶点。
1.7 GO/KEGG富集分析
利用Bioconductor、clusterProfiler R软件对核心靶点进行基因本体论(gene ontology, GO)和 KEGG(Kyoto encyclopedia of genes and genomes)信号通路分析,进一步探讨核心靶点的潜在作用机制。
1.8 分子对接虚拟筛选
从Pubchem数据库下载药物化学成分,并从PDB数据库下载核心蛋白结构域。借助Discovery Studio 2019的Libdock模块来完成虚拟筛选。根据虚拟对接结果选择LibDockScore值最大的化合物分别与核心蛋白结构域进行半柔性分子对接,运行AutoDock-Vina进行结合能计算以及分子对接结果展示,以评价生物信息分析预测的可靠性。
2 结果
2.1 参苓白术散化学成分鉴定及作用靶点筛选
根据LC-MS正、负离子模式中化合物的质核比,保留时间及峰面积等,结合化合物质谱图,最终鉴定得到148个化合物,联合文献检索结果,共筛选得到10个参苓白术散化学成分,见表1,并预测得到潜在作用靶点414个。

表1 参苓白术散10个化学物的LC-MS测量参数Table 1 LC-MS parameters of 10 components of Shenling Baizhu San
2.2 POP差异表达基因
得到与POP相关的转录谱数据集GSE35958,包括POP患者5例和健康成人4例,筛选得到843个DEGs,其中包括581个上调DEGs及262个下调DEGs。
2.3 WGCNA分析
WGCNA分析发现,最佳软阈值(β)为9,尺度独立性为0.9(图1A),构建网络分层聚类树和共表达模块(图1B、C)。并将所有基因划分成25个模块,其中MEbrown共表达模块与POP显著负相关(r=-0.97,P<0.05),包含1 976个潜在基因,说明MEbrown共表达模块中可能存在POP枢纽基因。最后,构建枢纽基因在各模块中的表达变化热图(图1D)。

注:A:最佳软阈值;B:差异表达基因聚类树;C:25大模块与POP相互关系;D:基因在各模块中的表达变化热图。图1 WGCNA分析Fig.1 WGCNA analysis
2.4 POP单细胞转录谱异质性分析
选取POP-scRNA-seq数据集(GSE147287)为研究对象,其中包括1例POP患者和1例骨性关节炎患者的骨髓细胞,共获得21 464个细胞以及12 002个相关基因(图2A)。设定PC=16,以及分辨率为0.20后(图2B),分别进行TSNE以及UMAP降维聚类分群后,将整合后的细胞分为14个cluster (图2C、D)。并根据已知的人类细胞标记基因进行细胞注释,发现POP中骨髓血样本中包括骨髓细胞、组织干细胞、巨噬细胞、BM细胞、红细胞、单核细胞、T细胞、B细胞、前CD34-B细胞、前CD34+B细胞(图3 A、B)。

注:A:细胞分布情况;B:分辨率筛选;C:TSNE聚类分群分布;D:UMAP聚类分群分布。图2 POP单细胞测序数据预处理Fig.2 Single-cell sequencing data pre-processing of POP
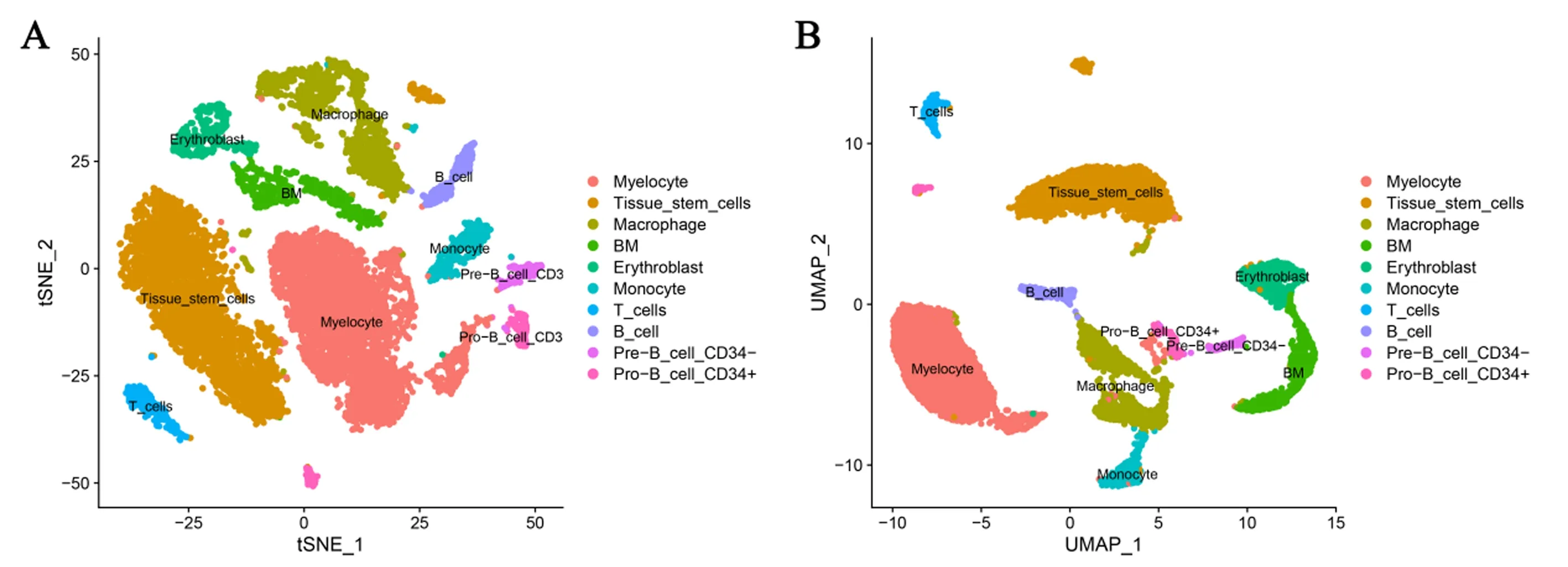
注:A:细胞注释后的tSNE图;B:细胞注释后的UMAP图。图3 POP单细胞注释分群Fig.3 Single-cell annotation clustering of POP
2.5 参苓白术散治疗POP核心交集基因分布
联合414个药物作用靶点以及843个POP-DEGs和1 976个WGCNA-枢纽基因分析,共得到52个药物治疗POP的靶点(图4A),以P<0.05,∣log2FC∣≥0.50为筛选标准得到37个DEGs,根据度值大小得到19个核心基因(图4B)。

注:A:参苓白术散-POP-WGCNA交集基因韦恩图;B:核心靶点PPI网络。图4 参苓白术散- POP -WGCNA交集基因分布Fig.4 The distribution of Shenling Baizhu San-POP-WGCNA intersection gene
2.6 核心基因的富集分析
对19个POP核心靶点进行富集分析发现,发现其GO主要富集在细胞对氧化应激的反应、衰老、细胞对非生物刺激的反应等。而KEGG主要富集在细胞衰老、内分泌抵抗、凋亡、破骨细胞分化、MAPK等。
2.7 虚拟分子对接验证
核心蛋白选择度值前4位以及2个共同靶点,即TP53、AKT1、JUN、BCL2L1、BAX、RPL27A,与鉴定得到的药物成分进行虚拟对接发现,TP53、JUN、BCL2L1、BAX与α-倒捻子素,AKT1与芹菜素,RPL27A与姜黄醇结合最好(图5)。并进一步发现JUN、BAX与α-倒捻子素,AKT1与芹菜素,RPL27A与姜黄醇形成的对接复合体结合能均<-6.7 kcal/mol,RMSD值均<2.00,说明以上复合体能够形成稳定的对接模型。见表2,图6。

图5 虚拟分子对接筛选Fig.5 Virtual molecule docking screening

图6 分子对接模型Fig.6 Molecular docking models

表2 分子对接结果Table 2 The results of molecular docking
3 讨论
目前对POP的治疗主要以抑制骨吸收为主,能有效稳定骨微结构、降低骨折发生率,但不能逆转已破坏的骨微结构[12]。中医从肾虚论治骨质疏松症较多,然而肾主骨的功能强弱依赖于脾的后天滋养[13]。参苓白术散是益气健脾的经典名方,能影响内分泌调节骨代谢和免疫功能,并能通过肠-微生物-内分泌-骨轴影响钙磷吸收[14-15]。
本研究中借助LC-MS鉴定得到10种参苓白术散的化学成分,包括了α-倒捻子素、芹菜素、白术内酯III等。目前多项研究发现,以上成分能通过NF-κB和MAPK信号传导抑制炎症性骨吸收,且能激活Wnt/β-catenin信号传导促进成骨分化改善骨形成,调节骨代谢稳态延缓POP的发展[16-20]。
联合参苓白术散成分靶点,POP-DEGs以及WGCNA-枢纽基因分析得到19个核心靶点,包括TP53、AKT1、JUN、BCL2L1、BAX和RPL27A等。Wang等[21]研究发现,AKT1激活能促进间充质干细胞成骨分化;BCL2L1是抗凋亡基因,能抑制成骨细胞凋亡并增加骨体积和强度[22];促凋亡蛋白Bax能促进成骨细胞凋亡,加速骨破坏[23]。此外,发现以上靶点可能参与了细胞衰老、细胞凋亡、破骨细胞分化等信号通路。细胞衰老在骨微环境中不断积累并分泌促炎衰老相关分泌表型[24],作用于成骨细胞抑制骨形成,作用于破骨细胞促进骨吸收,作用于间充质干细胞使其向脂肪细胞分化[25]。此外,破骨细胞分化及活性是造成OP骨量丢失和骨破坏的重要因素[26]。本研究发现POP中存在多种免疫细胞,包括巨噬细胞、单核细胞、T细胞、B细胞等,研究表明免疫细胞可通过直接细胞-细胞接触或旁分泌机制,影响骨质流失和骨修复[27]。因此,参苓白术散可能通过调控免疫细胞与骨细胞的相互作用治疗POP。
综上所述,参苓白术散可从多成分、多靶点及多细胞水平治疗POP,为参苓白术散治疗POP提供了理论依据。然而,本研究并没有开展相应化学成分的实验验证,后期将进一步开展基础实验进行探索。

