关注催化剂的三个考查点
杜敏敏
(山东省枣庄市第一中学)
催化剂是在化学反应过程中能改变化学反应速率而不改变化学平衡,且本身的质量和化学性质在化学反应前后都没有发生改变的物质.催化剂逐渐成为考试的热点和难点,主要考查催化剂的判断、催化剂对化学反应的影响,如化学反应的热效应、反应物的转化率、化学平衡的移动等.
1 考查催化剂的判断
近年来,对化学反应历程的考查成为考试的热点.大多数化学反应都需要催化剂,催化剂参与了化学反应,因此结合化学反应历程示意图判断出催化剂成为一个考点.要求学生能从复杂的化学反应历程中找出催化剂.
例1在一定条件下,反应物和生成物的相对能量与反应历程如图1所示.下列说法错误的是( ).

图1
A.E1-E4=E2-E5
B.Cl(g)为历程Ⅱ的催化剂
C.相同条件下,历程Ⅰ、Ⅱ中O3的平衡转化率相同
D.两个反应历程中速率最快的一步反应的ΔH=(E3-E2)kJ•mol-1
分析由图可知,Cl(g)是历程Ⅱ的催化剂,催化剂不能改变反应的反应热,则历程Ⅰ、Ⅱ的反应热相等,即E1-E4=E2-E5,选项A、B说法正确.催化剂不能改变反应的始态和终态,不能改变反应物的平衡转化率,即相同条件下,历程Ⅰ、Ⅱ中O3的平衡转化率相等,选项C说法正确.由图可知,历程Ⅱ中的第二步反应活化能小于第一步反应的活化能,反应的活化能越低,反应速率越快,则历程Ⅰ、Ⅱ中速率最快的一步反应的焓变为(E2-E3)kJ•mol-1,选项D 说法错误.答案为D.
2 考查催化剂对化学反应速率和化学平衡的影响
化学反应中催化剂可以降低反应的活化能,加快化学反应速率,但对化学平衡没有影响.试题对化学反应的反应热和反应物的转化率考查较多.
例2利用反应2CO(g)+SO2(g)⇌2CO2(g)+S(l) ΔH<0可实现从燃煤烟气中回收硫.向3个容积相同的恒容密闭容器中通入2 mol CO(g)和1 mol SO2(g)发生反应,反应体系的总压强随时间的变化如图2所示.下列说法错误的是( ).

图2
A.与实验a相比,实验b改变的条件是加入催化剂
B.使用催化剂可以降低反应的活化能,增大活化分子百分数,反应速率加快
C.使用高效率催化剂,可提高单位时间内S 的产率
D.相应条件下实验a、b、c的平衡常数:Ka=Kb<Kc
分析由题意可知,反应为放热反应,3个反应容器的容积相同且恒容,反应物起始量相同,实验a、b起始压强相同,说明反应温度相同,实验b达到平衡快,反应速率大,但两者平衡状态相同,说明实验b使用了催化剂,选项A 说法正确.一般使用催化剂可以降低反应的活化能,部分分子变为活化分子,则活化分子百分数增大,活化分子有效碰撞的概率增大,化学反应速率加快,选项B 说法正确.使用高效率催化剂,能降低反应的活化能,加快反应速率,可提高单位时间内S的产率,选项C 说法正确.平衡常数只受温度影响,根据分析可知,实验a、b反应温度相同,则Ka=Kb.反应ΔH<0,说明该反应是放热反应,升高温度,平衡逆向移动,平衡常数减小,实验c温度比实验a、b高,则Ka=Kb>Kc,选项D 说法错误.答案为D.

催化剂对化学反应速率的影响:降低了反应的活化能,加快化学反应速率,提高单位时间内的产率.催化剂对化学平衡没有影响,因此不能改变反应的焓变,不能改变反应物的转化率.
3 考查催化剂的使用条件
催化剂的使用是有条件的,不同条件下催化剂的催化效率不同,即使是同一催化剂在不同条件下催化效率也不相同.因此,有的试题就要求通过比较催化剂对反应物转化率的影响选择适宜的条件.
例3煤和石油等化石燃料燃烧产生的NOx是大气中氮氧化物的主要来源.选择性催化还原脱硝技术是控制尾部烟气中NOx排放的最成熟有效的技术之一.在相同时间内,3种催化剂条件下,NO 的转化率、NO2的浓度随温度的变化如图3所示.空速(规定的条件下,单位时间、单位体积催化剂处理的气体量)的大小直接决定了烟气在催化剂表面的停留时间和装置的烟气处理能力.催化剂能够适应较大的空速,就可以在保证足够高的脱硝效率的前提下提高催化剂处理烟气的能力.相同时间内,Mn CeZr催化剂在不同空速下NO 的转化率随温度的变化如图4所示.
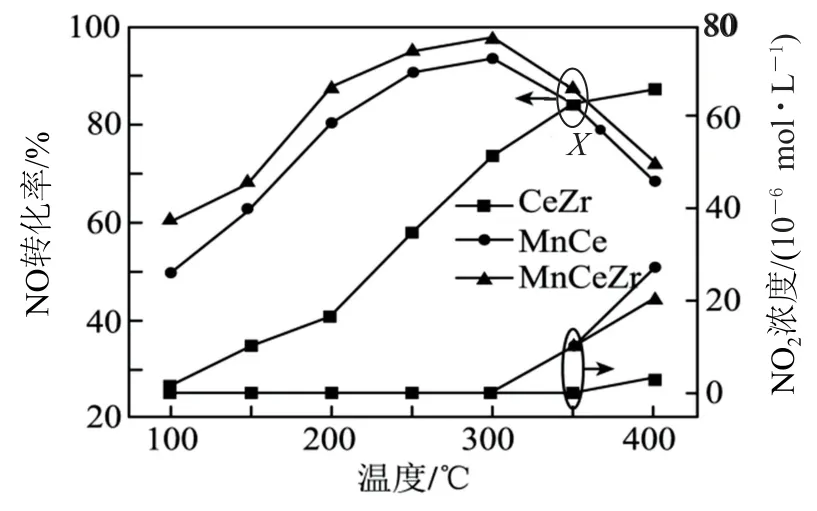
图3 催化剂脱硝活性曲线(O2 含量3%)

图4 空速对脱硝过程影响(O2 含量3%)
(1)根据图3和图4分析,选取工业脱硝的最佳反应条件为________.350~400 ℃产生较多NO2的原因为_________.
(2)通过改善催化剂的结构特性可以使脱硝效率得到提升.较低温度下,Mn CeZr催化剂的脱硝效率远高于CeZr催化剂,说明主要是_________(填元素符号)的存在改善了催化剂的低温活性.在Mn Ce催化剂催化下,X点的正反应速率________(填“>”“<”或“=”)逆反应速率,说明理由:_________.
分析(1)结合图3 可知,温度为300 ℃、Mn CeZr作催化剂时,NO 的转化率最高.根据图4及题干信息“催化剂能够适应较大的空速,就可以在保证足够高的脱硝效率的前提下提高催化剂处理烟气的能力”可知,空速30 000 h-1时NO 的转化率足够高,故选取工业脱硝的最佳反应条件为Mn CeZr作催化剂、300 ℃、空速30 000 h-1.350~400 ℃产生较多NO2的原因是在较高温度下,Mn CeZr、Mn Ce催化活性均下降,反应速率减慢,随着脱硝效率的下降,没有参加反应的NO 逐渐被氧化成了NO2.
(2)较低温度下,Mn CeZr作催化剂的脱硝效率远高于CeZr作催化剂的脱硝效率,说明主要是Mn的存在改善了催化剂的低温活性.在Mn Ce催化下,X点的正反应速率>逆反应速率,其理由为平衡是可逆反应所能达到的最大限度,相同温度下,X点时NO的转化率不是最大的(Mn CeZr作催化剂时NO 的转化率更大),所以X点时反应没有达到平衡,反应仍在正向进行,即正反应速率大于逆反应速率.
总之,化学课程要求学生能从微观层面和模型认知角度分析解决化学问题,分析催化剂在化学反应机理和化学反应过程中对化学反应的影响体现了这一理念,解题时要理解催化剂的本质,分析模型和图像,找出催化剂对物质变化和对化学反应的影响.
(完)

