追根溯源,突破Kc、Kp及Kx计算问题
王志刚
(陕西省西安市长安一中)
研究近年高考化学试题可以发现,化学平衡常数计算类试题,考查形式多样、考查手段灵活,尤其是结合图形、图表进行的考查,较好地测试了学生分析问题、解决问题的能力,具有较高的区分度,是化学平衡考查中的热点与难点.本文分类剖析近年高考试题中化学平衡常数计算类问题,追根溯源,以探寻该问题的有效备考思路与突破办法.
1 浓度平衡常数(Kc)的计算
例1(2019全国Ⅲ卷28,节选)近年来,随着聚酯工业的快速发展,Cl2的需求量和HCl的产出量也随之迅速增长.因此,将HCl转化为Cl2的技术成为科学研究的热点.Deacon 发明的直接氧化法为4HCl(g)+O2(g)⇌2Cl2(g)+2H2O(g).图1为刚性容器中,进料浓度比c(HCl)∶c(O2)分别等于1∶1、4∶1、7∶1时HCl平衡转化率随温度变化的关系.可知反应平衡常数K(300 ℃)______K(400 ℃)(填“大于”或“小于”).设HCl初始浓度为c0,根据进料浓度比c(HCl)∶c(O2)=1∶1的数据计算K(400 ℃)=______(列出计算式).
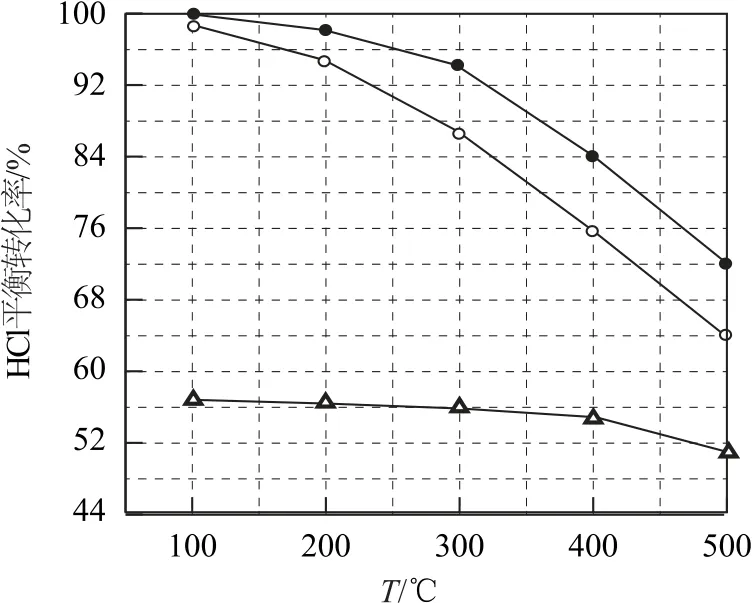
图1
分析研究图像可以推知,4HCl(g)+O2(g)⇌2Cl2(g)+2H2O(g)为放热放应(ΔH<0),故K(300 ℃)大于K(400 ℃).在温度相同时c(HCl)与c(O2)的比值越大,HCl的平衡转化率越小,由图像可知最上面的曲线表示进料浓度比c(HCl)∶c(O2)=1∶1时HCl的转化率.400 ℃时,HCl的转化率为84%.列出三段式如下:
拓展(2018全国Ⅱ卷27,节选)CH4-CO2催化重整不仅可以得到合成气(CO 和H2),还对温室气体的减排具有重要意义.CH4-CO2催化重整反应为CH4(g)+CO2(g)⇌2CO(g)+2H2(g) ΔH=+247 kJ•mol-1.某温度下,在容积为2 L的容器中加入2molCH4、1molCO2以及催化剂进行重整反应,达到平衡时CO2的转化率是50%,其平衡常数为_________mol2•L-2.
答案1/3.
备考启示2018年全国卷Ⅱ卷理综第27题关于Kc的计算,就是“三段式法”的直接运用.此题计算时要注意两点:1)要明确CH4-CO2催化重整反应属于反应前后气体体积改变的反应,计算平衡常数时用的数据是各组分的平衡浓度而不是物质的量.2)由计算结果可以推知,除非是反应前后气体体积不变的反应,否则计算得出的平衡常数都是有单位的.
2 压强平衡常数(Kp)的计算
压强平衡常数(Kp)是研究气体平衡时的一个重要物理量,其在中学化学考试中的考查应用,最早出现于化学奥林匹克竞赛试题中.高考试题中对压强平衡常数计算的考查,多以图形、图表的方式展现,考查考生的“证据推理与模型认知、变化观念与平衡思想”化学核心素养,具有较高的区分度.对于Kp的计算问题,是近年高考平衡常数计算中的热点与难点,需要我们深入研究,发现解题规律与方法,以帮助学生高效备考.
例2(2019年全国Ⅱ卷27,节选)某温度下,等物质的量的碘和环戊烯()在刚性容器内发生反应[(g)+I2(g)⇌(g)+2HI(g)],起始总压为105Pa,平衡时总压增加了20%,该反应的平衡常数Kp=______Pa.(分压=总压×各组分物质的量分数)
分析在刚性恒容容器中,,令a=105Pa,设平衡时转化的环戊烯的压强为x.
备考启示与传统定义法计算分压平衡常数相比较,此题直接用分压法计算Kp有如下优点:1)不用进行烦琐的各组分分压计算,根据压强比等于物质的量之比,直接用分压进行计算,计算过程简捷.2)尤其是对于反应前后气体体积改变的反应,计算时不会因反应后总压发生改变而犯低级错误(即依旧用原压强进行了计算),学生计算出错率明显降低.
拓展1(2023年湖北卷19,节选)纳米碗C40H10是一种奇特的碗状共轭体系.1200K 时,假定体系内只有反应C40H12(g)⇌C40H10(g)+H2(g)发生,反应过程中压强恒定为p0(即C40H12的初始压强),平衡转化率为α,该反应的平衡常数Kp为____(用平衡分压代替平衡浓度计算,分压=总压×物质的量分数).
装置为恒压装置,通过“三段式”法,用Kp进行计算.设开始时C40H12物质的量为1mol.
备考启示“恒压”装置,只能先用物质的量分数算出各组分分压,再按照定义进行计算,而“恒容”装置,才可以用分压直接进行简化计算.
拓展2(2023年全国卷乙卷28,节选)硫酸亚铁在工农业生产中有许多用途,如可用作农药防治小麦黑穗病,制造磁性氧化铁、铁催化剂等.
(3)将FeSO4置入抽空的刚性容器中,升高温度发生分解反应:
平衡时p(SO3)-T的关系如图2所示.660K 时,该反应的平衡总压p总=_________kPa、平衡常数Kp(I)=________(kPa)2.Kp(Ⅰ)随反应温度升高而________(填“增大”“减小”或“不变”).
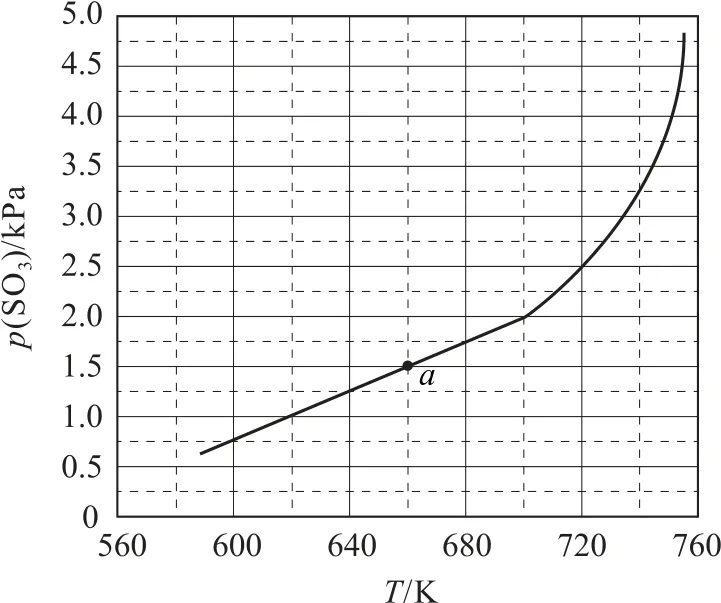
图2
(4)提高温度,上述容器中进一步发生反应:
平衡时p(O2)=______[用p(SO3)、p(SO2)表示].在929 K 时,p总=84.6kPa、p(SO3)=35.7kPa,p(SO2)=______kPa,Kp(Ⅱ)=______kPa(列计算式).
(3)由图可知p(SO3)=1.5kPa,根据反应2FeSO4(s)=Fe2O3(s)+SO2(g)+SO3(g)计算可得p(SO2)=1.5kPa,故p总=3.0kPa,
升高温度,p(SO3)分压增大,p(SO2)分压也增大,故Kp(Ⅰ)随反应温度升高而增大.(4)上述容器中仅发生反应(Ⅰ)时,p(SO2)=p(SO3),进一步发生反应(Ⅱ),则有p(SO2)-2p(O2)=p(SO3)+2p(O2),故.
由于p(SO3)=35.7 kPa,p总=84.6 kPa=p(SO2)+p(SO3)+p(O2)=p(SO2)+p(SO3)+],所以p(SO2)=46.26kPa,p(O2)=2.64kPa.故.
备考启示2023年全国乙卷对Kp的考查,既有继承性,又有创新性,考生易错点有:1)没有找出仅发生反应(Ⅰ)时,p(SO2)=p(SO3)的关系式而导致计算无从下手.在考场上,学生由于紧张,不能快速找出等量关系,导致计算出现问题.2)计算平衡常数时,由于没有找出p总=p(SO2)+p(SO3)+p(O2)的合理关系,导致p(SO2)、p(O2)没有算出来,进而无法计算Kp.因此,在复习备考中,学生在重视基本解题方法训练的同时,还要辅之以开放性、创新性解题方式的训练.
3 物质的量分数平衡常数(Kx)的计算
Kx指的是物质的量分数平衡常数,对于反应mA(g)+nB(g)⇌pC(g)+qD(g),则有.自2015年全国Ⅰ卷第28题开始,涉及与Kx计算有关的试题多与速率方程式结合在一起进行考查.自人教版选择性必修1«化学反应原理»介绍了基元反应之后,通过K与k正、k逆的关系设计问题,则是近年高考化学试题的另一个热点与难点.下面结合2015年高考试题中Kx计算问题,分析近年高考平衡常数计算与k正、k逆相结合的考查方式,以进一步增强学生在平衡常数计算方面的备考能力.
例3(2015年全国Ⅰ卷28,节选)碘及其化合物在合成杀菌剂、药物等方面具有广泛用途.Bodensteins研究了下列反应:2HI(g)⇌H2(g)+I2(g),在716K 时,气体混合物中碘化氢的物质的量分数X(HI)与反应时间t的关系如表1所示.
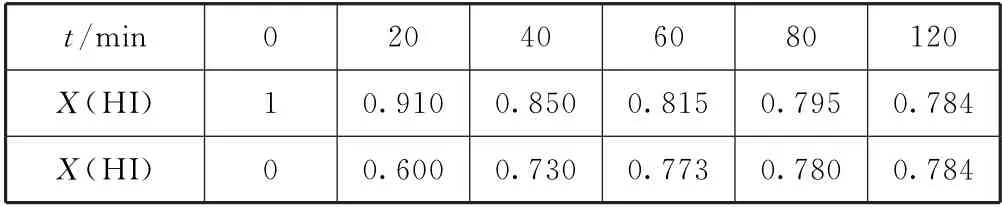
表1
①根据上述实验结果,该反应的平衡常数Kx的计算式为_________.
②上述反应中,正反应速率为v正=k正x2(HI),逆反应速率为v逆=k逆x(H2)x(I2),其中k正、k逆为速率常数,则k逆为_________(以Kx和k正表示).
分析①结合表格数据,可以发现反应无论是由正向建立还是由逆向建立,在120 min时,反应均达到了平衡,利用“三段式”法可以快速计算出物质的量分数平衡常数(Kx).
备考启示2015年的这道高考题,尽管难度小、简单易做,但该题设置的问题,尤其是利用v正=v逆推导平衡常数(K)与速率常数(k正、k逆)关系的考查思路与考查视角,对2024年化学平衡常数的复习备考,具有非常好的启迪作用.复习备考中,首先要做到“面面俱到”,然后做到“重点突破”,这是复习备考的根本原则.
拓展(2018 年全国Ⅲ卷28,节选)三氯氢硅(SiHCl3)是制备硅烷、多晶硅的重要原料.对于反应2SiHCl3(g)⇌SiH2Cl2(g)+SiCl4(g),采用大孔弱碱性阴离子交换树脂催化剂,在323 K 和343 K 时SiHCl3的转化率随时间变化的结果如图3所示.
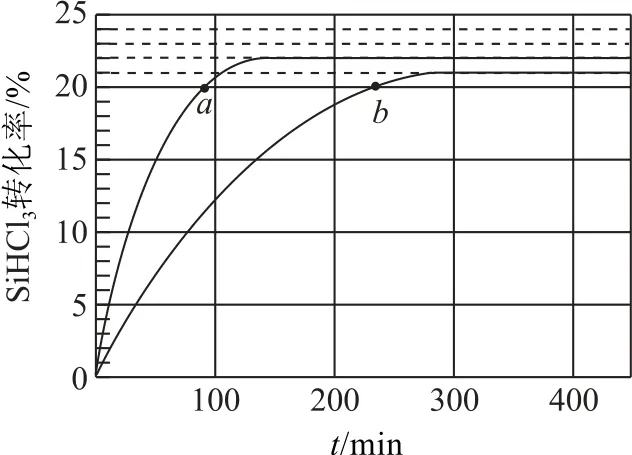
图3
①343K 时反应的平衡转化率α=______%,平衡常数K343K=_________(保留2位小数).
②反应速率v=v正-v逆=k正x2(SiHCl3)-k逆x(SiH2Cl2),k正、k逆分别为正、逆向反应速率常数,x为物质的量分数,计算a处=_________(保留1位小数).
分析①由“先拐先平,数值大”,可判断出a点所在曲线温度为343K,分析可知该温度下平衡转化率为22%,可取1mol•L-1的SiHCl3发生如下反应:
②中巧妙地运用平衡状态时,v正=v逆,推导得出.结合a处转化率为20%,列出“三段式法”进行计算:
备考启示平衡常数计算备考时的一般解题思路可以总结为“写”“列”“算”.
1)写:写出方程式;
2)列:列出三段式;
3)算:算出Kc、Kp或Kx.
通过对化学平衡常数计算问题追根溯源式研究,不难发现,高考试题不仅具有继承性,而且具有创新性,稳中求新、稳中求变是高考试题的永恒追求.在化学平衡常数计算问题的复习备考中,抓住根本(用好三段式法),精准备考(深研Kp相关计算),琢磨真题(体会继承性),洞察方向(把握创新性),定可取得事半功倍的复习效果.
(完)

