他达拉非片有区分力的溶出度检查方法的建立及溶出曲线相似性评价
潘瑞雪,江玉娟,许 敏,王 莉,袁倩倩,高 超,崔 阳,刘 杰
(山东明仁福瑞达制药股份有限公司 山东省骨科疼痛类药物工程研究中心,山东 济南 250104)
他达拉非是磷酸二酯酶(PDE5)的选择性抑制剂,用于治疗男性勃起功能障碍及勃起功能障碍合并良性前列腺增生的症状和体征,与其他同类药物相比,他达拉非具有选择性高、半衰期长、耐受性好等优点[1-2]。他达拉非片原研公司为美国礼来,2002年11月在欧盟15个成员国获准上市;2003年11月获美国FDA批准上市,2004年12月获批进口中国[3]。
近年,仿制药质量和疗效一致性评价工作不断推进。本研究以国家药品监督管理局公布的参比制剂目录为依据,选定由礼来公司生产的希爱力作为参比制剂,仿制了规格为20 mg的他达拉非片。参考国家颁布的相关指导原则[4-5],通过桨法研究他达拉非片在不同pH介质中的溶出行为,建立了他达拉非片具有区分力的溶出度检查法,以期为后续仿制药一致性评价提供参考。
1 仪器与材料
1.1 仪器
LC-2040C 3D型高效液相色谱仪(日本岛津公司);Logan 812A-12型智能溶出仪(美国LOGAN公司);XPE205型电子天平(梅特勒-托利多公司);ZWY-111B型恒温培养振荡器(上海智诚)。
1.2 药品与试剂
他达拉非对照品(E P 标准物质,批号:2.0);他达拉非原料药(山东海佑福瑞达制药有限公司,批号:20170908);他达拉非自制片(山东明仁福瑞达制药股份有限公司,批号:20041601,20051801,20051901);他达拉非参比制剂(美国礼来公司,商品名希爱力,批号:D189502);十二烷基硫酸钠(SDS,西陇科学,化学纯)。
2 方法与结果
2.1 色谱条件
采用高效液相色谱法(HPLC)检测他达拉非溶解度及他达拉非片溶出度。色谱柱:Agilent Zorbax SB-C8柱(4.6 mm×150 mm,3.5 µm);流动相:甲醇-水(65:35);检测波长:225 nm;流速:1.0 ml/min;进样量20 μl。
2.2 溶出介质配制
0.2 %SDS水溶液:精密称取SDS 2.0 g,加水适量溶解,并用水稀释至1000 ml,摇匀。
0.2 %SDS盐酸溶液(pH 1.2):精密量取盐酸7.65 ml,加水适量稀释,加入SDS 2.0 g,用水溶解并稀释至1000 ml,摇匀。
0.2 %SDS醋酸盐缓冲液(pH 4.5):精密量取2 mol/L醋酸溶液(取冰醋酸120.0 g或114 ml,用水稀释至1000 ml)14 ml,加入醋酸钠2.99 g,加水适量使溶解,加入SDS 2.0 g,用水溶解并稀释至1000 ml,摇匀。
0.2 %SDS磷酸盐缓冲液(pH 6.8):取0.2 mol/L磷酸二氢钠溶液(取磷酸二氢钠24 g,用水溶解并稀释至1000 ml,摇匀)250 ml与0.2 mol/L氢氧化钠溶液(取8.00 g氢氧化钠,用水溶解并稀释至1000 ml,摇匀)112.0 ml,混合,加水适量稀释,加入SDS 2.0 g,用水溶解并稀释至1000 ml,摇匀。
2.3 溶液的配制
2.3.1 对照品溶液 取他达拉非对照品约25 mg,精密称定,置于100 ml量瓶中,加50 %乙腈溶液适量,超声30 min使他达拉非完全溶解,用50 %乙腈溶液稀释至刻度,摇匀,作为他达拉非对照品储备液;精密量取他达拉非对照品储备液适量,分别用4种溶出介质稀释配制成每1 ml中约含他达拉非2 µg的对照品溶液。
2.3.2 线性溶液 精密称取他达拉非对照品约20 mg,置100 ml量瓶中,加50 %乙腈溶液适量,振摇使他达拉非完全溶解,用50 %乙腈稀释至刻度,摇匀,作为他达拉非对照品贮备液;精密量取对照品储备液1,2,3,5,7 ml至50 ml量瓶中,分别用2.2项下溶出介质稀释至刻度,即得线性1~线性5溶液,浓度约为4,8,16,20,28 μg/ml。
2.3.3 不同pH值溶液的配制
pH 1.2水溶液:取盐酸7.65 ml,加水稀释至1000 ml。
pH 2.0水溶液:取盐酸1.17 ml,加水稀释至1000 ml。
pH 3.8水溶液:取2 mol/L醋酸溶液22.6 ml与醋酸钠0.67 g,加水溶解并稀释至1000 ml。
pH 4.5水溶液:取2 mol/L醋酸溶液14.0 ml与醋酸钠2.99 g,加水溶解并稀释至1000 ml。
pH 5.5水溶液:取2 mol/L醋酸溶液3.0 ml与醋酸钠5.98 g,加水溶解并稀释至1000 ml。
pH 6.0水溶液:取0.2 mol/L磷酸二氢钠溶液250 ml与0.2 mol/L氢氧化钠溶液28 ml,加水稀释至1000 ml。
pH 6.8水溶液:取0.2 mol/L磷酸二氢钠溶液250 ml与0.2 mol/L氢氧化钠溶液112 ml,加水稀释至1000 ml。
pH 8.0水溶液:取0.2 mol/L磷酸二氢钠溶液250 ml与0.2 mol/L氢氧化钠溶液230.5 ml,加水稀释至1000 ml。
2.3.4 不同pH值0.2 %SDS溶液的制备 分别按2.3.3项下方法制备不同pH溶液,加入SDS 2 g,溶解,即得不同pH值0.2 %SDS溶液。
2.4 溶出曲线测定方法
采用桨法,溶出介质体积为1000 ml,转速为每分钟50转,分别于5,10,15,20,30,45,60,90 min时,取出溶出液5 ml,滤过,作为供试品溶液,并即时补充相同温度、相同体积的溶出介质。取上述溶液,按2.1项下色谱条件进样测定,绘制溶出曲线。
2.5 溶解度的测定
2.5.1 不同pH值溶液中溶解度的测定 取过量的他达拉非原料药,置50 ml量瓶中,精密加入pH 1.2,pH 2.0,pH 3.8,pH 4.5,pH 5.5,pH 6.0,pH 6.8,pH 8.0溶液及水各25 ml,置恒温振荡器中,37 ℃下振摇24 h,过滤,取续滤液,按2.1项下色谱条件进样测定,采用外标法计算他达拉非溶解度。结果显示,他达拉非为水难溶性药物,且无pH依赖性,水作为溶出介质无区分能力。结果见表1。

表1 他达拉非在不同pH溶液及水中溶解度
2.5.2 不同浓度SDS溶液中溶解度的测定 取过量的他达拉非原料药,置50 ml量瓶中,精密加入0.1 %,0.15 %,0.20 %,0.25 %,0.30 %,0.35 %,0.40 %,0.45 %,0.50 %,0.55 %SDS溶液各25 ml,置恒温振荡器中,37 ℃下振摇24 h,过滤,取续滤液,按2.1项下色谱条件进样测定,采用外标法计算他达拉非溶解度。结果显示,他达拉非溶解度与介质中SDS浓度基本呈正比,且在0.2 %SDS中的溶解度与他达拉非片在1000 ml溶出介质中完全溶出时的浓度(20 μg/ml)基本一致,说明本品在0.2 %及以上浓度SDS溶液中可达到完全溶出。结果见表2。

表2 他达拉非在不同浓度SDS溶液中的溶解度
2.5.3 不同pH值0.2 %SDS溶液中溶解度的测定 取过量他达拉非原料药,置50 ml量瓶中,精密加入含0.2 %SDS的pH 1.2、pH 2.0、pH 3.8、pH 4.5、pH 5.5、pH 6.0、pH 6.8、pH 8.0介质和水各25 ml,置恒温振荡器中,37 ℃下振摇24 h,过滤,取续滤液,按2.1项下色谱条件进样测定,采用外标法计算他达拉非溶解度。结果见表3。
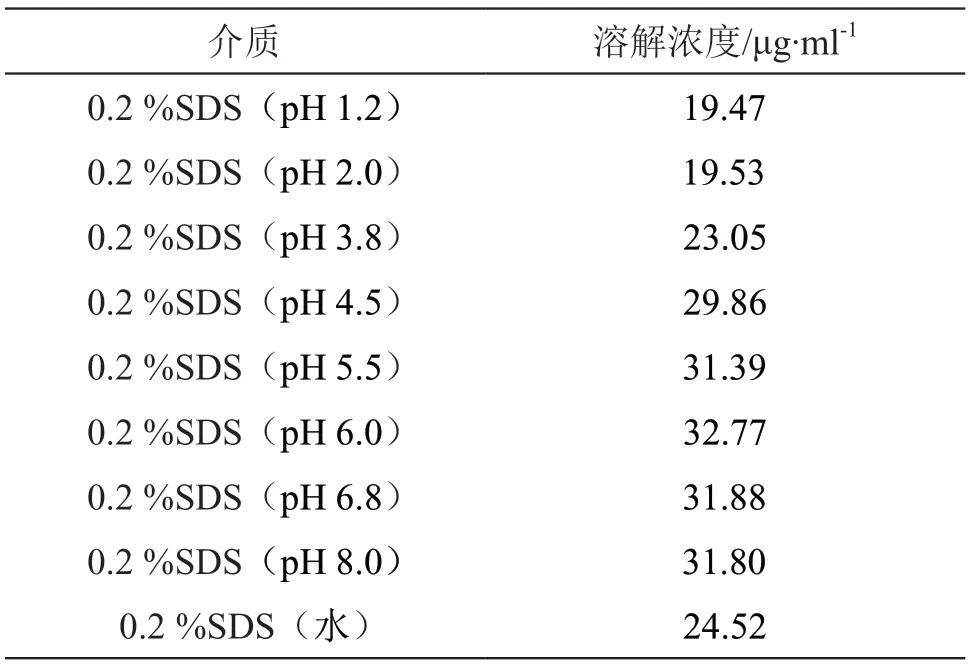
表3 他达拉非在不同pH值0.2 %SDS溶液中溶解度
SDS浓度为0.2 %时,不同pH溶液中的溶解度无明显的pH依赖性。参照普通口服固体制剂溶出度试验技术指导原则[5-6]、他达拉非片进口注册标准及美国药典(USP41)溶出数据库中的内容,选择2.2项下0.2 %SDS盐酸溶液(pH 1.2)、0.2 %SDS醋酸盐缓冲液(pH 4.5)、0.2 %SDS磷酸盐缓冲液(pH 6.8)和0.2 %SDS水溶液4种介质进行筛选。
2.6 溶出度测定方法学验证
2.6.1 专属性试验 称取按处方比例配制的空白辅料约33 mg,置100 ml量瓶中,分别加2.2项下4种溶出介质适量,振摇,并用相应的溶出介质稀释至刻度,摇匀,滤过,作为空白辅料溶液。
精密量取空白辅料溶液、4种溶出介质、2 µg/ml他达拉非对照品溶液各20 μl,按2.1项下色谱条件进样测定,结果显示4种溶出介质及空白辅料均不干扰溶出度测定。色谱图见图1~3。
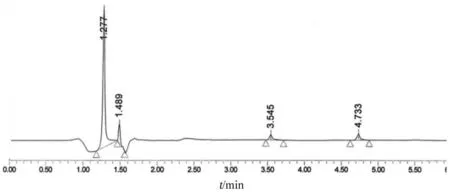
图1 溶出介质(0.2 %SDS水溶液)色谱图
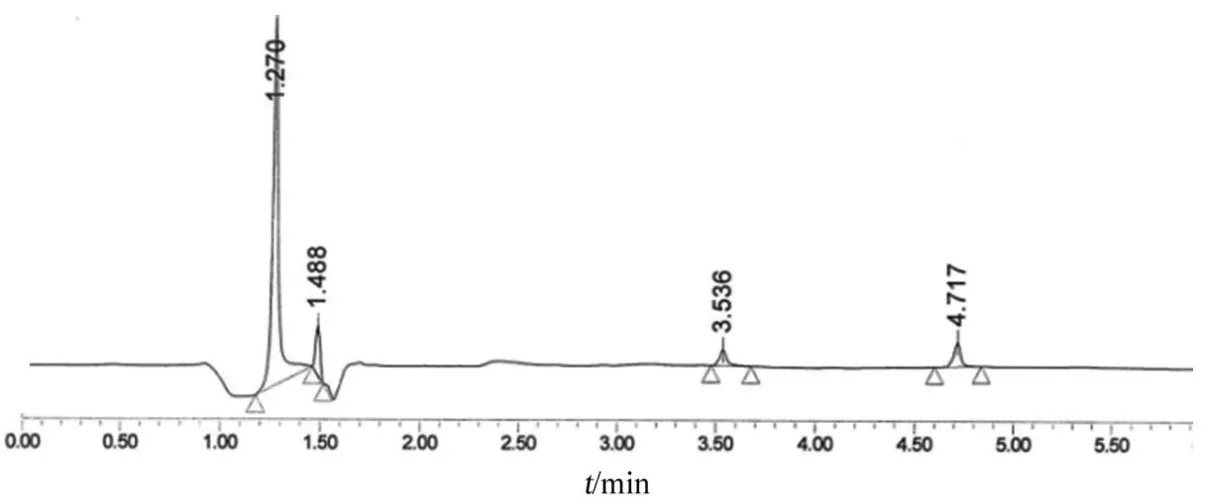
图2 空白辅料溶液(以0.2 %SDS水溶液配制)色谱图
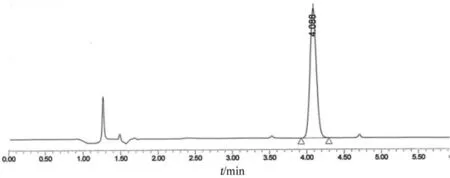
图3 对照品溶液(以0.2 %SDS水溶液配制)色谱图
2.6.2 线性试验 取2.3.2项下线性溶液,按2.1项下色谱条件进样测定,以浓度(C,μg/ml)对峰面积(A)进行线性回归,结果见表4。由表4可见,他达拉非在4种溶出介质中线性关系良好。
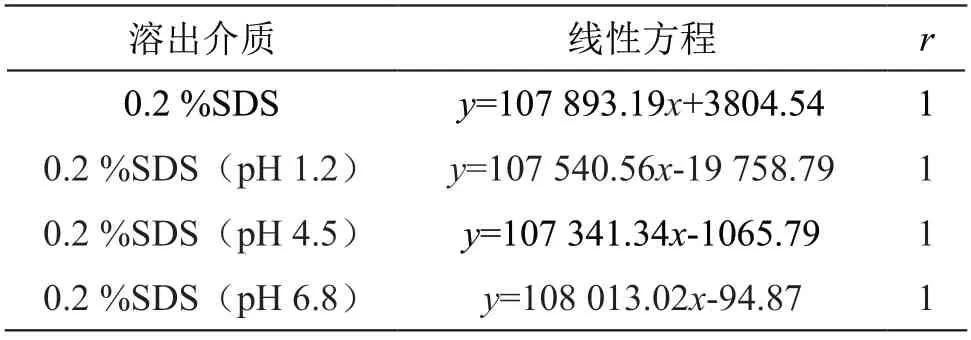
表4 线性关系
2.6.3 定量限 取2.3.2 项下线性溶液1(浓度约为4 μg/ml),分别用4种溶出介质依次逐级稀释,按2.1项下色谱条件进样测定,以信噪比为10计算定量限。结果显示,他达拉非在0.2 %SDS盐酸溶液(pH 1.2)、0.2 %SDS醋酸盐缓冲液(pH 4.5)、0.2 %SDS磷酸盐缓冲液(pH 6.8)和0.2 %SDS水溶液中的定量限分别为0.2431,0.1616,0.1135,0.1926 μg/ml。
2.6.4 精密度试验 取2.3.2 项下线性溶液4(浓度约为20 μg/ml)为对照品溶液,按2.1项下色谱条件进样测定,连续进样6次,记录色谱图。结果显示,4种溶出介质配制的对照品溶液连续进样6次峰面积的RSD依次1.4 %,0.1 %,0.2 %,0.1 %,均小于2.0 %,说明仪器的精密度良好。
2.6.5 回收率试验 取他达拉非对照品约50 mg,置100 ml量瓶中,用50 %乙腈溶液溶解并稀释至刻度,摇匀,作为回收率贮备液。称取处方量空白辅料,置25 ml量瓶中,加入回收率贮备液0.3 ml(30 %浓度水平)、0.5 ml(50 %浓度水平)、0.8 ml(80 %浓度水平)、1.0 ml(100 %浓度水平),分别用4种溶出介质稀释至刻度,每个浓度平行配制3份,取续滤液作为回收率试验供试品溶液。按2.1项下色谱条件进样测定,记录色谱图,以测得量与加入量计算回收率。结果显示,方法准确度良好,见表5。

表5 回收率试验结果
2.6.6 溶液稳定性试验 取分别以2.2项下4种溶出介质配制的浓度为20 μg/ml他达拉非对照品溶液及2.6.5项下加样浓度水平为100 %的回收率试验供试品溶液,室温放置,分别于0,2,4,6,8,12 h时按2.1项下色谱条件进样测定,记录色谱图。随着时间的增加,各样品溶液峰面积RSD均在2 %以内,表明各样品溶液至少在12 h内稳定。
以上溶出度测定方法学验证指标均满足要求,提示建立的溶出度测定方法可行。
2.7 参比制剂溶出曲线的测定
取他达拉非片参比制剂(批号:D189502),分别考察于不同溶出介质[0.2 %SDS盐酸溶液(pH 1.2)、0.2 %SDS醋酸盐缓冲液(pH 4.5)、0.2 %SDS磷酸盐缓冲液(pH 6.8)和0.2 %SDS水溶液]中溶出曲线,结果见图4。他达拉非片参比制剂(批号:D189502)在4种溶出介质中,30 min溶出率均能达到85 %,无拐点和突释,表明溶出介质具有较强的区分能力,且不会过度区分,适用于评价参比制剂和自制片的一致性[6]。
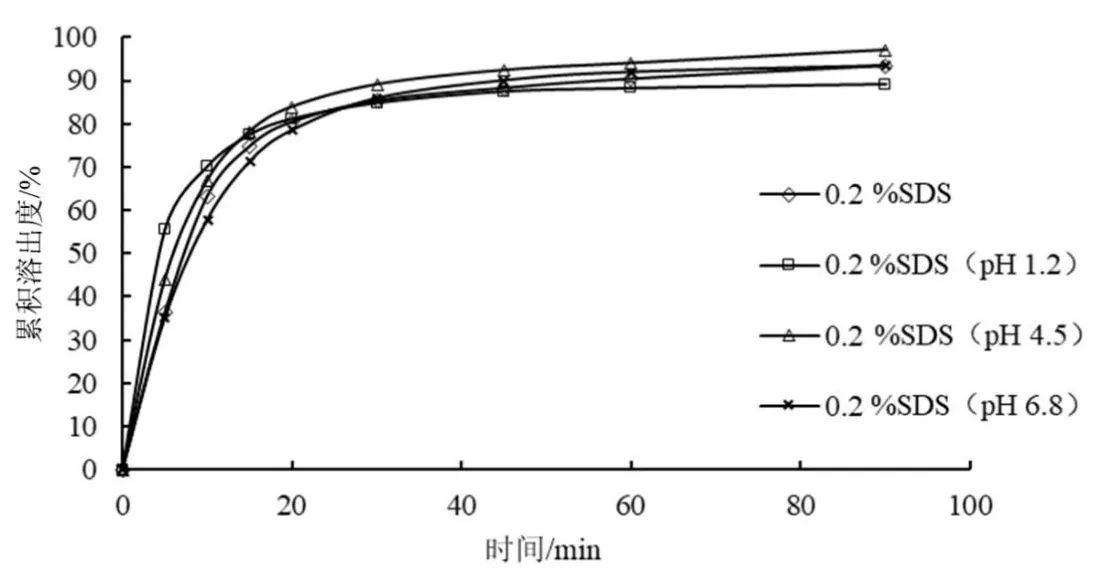
图4 参比制剂在不同溶出介质中的溶出曲线(n=12)
2.8 溶出曲线相似性评价
采用相似因子(ƒ2)法比较参比制剂和自制片溶出曲线的相似性:若50≤ƒ2≤100,可认为2条溶出曲线相似,计二者的溶出量平均差异<10 %。比较不同处方自制片与参比制剂在4种溶出介质[0.2 %SDS盐酸溶液(pH 1.2)、0.2 %SDS醋酸盐缓冲液(pH 4.5)、0.2 %SDS磷酸盐缓冲液(pH 6.8)和0.2 %SDS水溶液]中溶出曲线的ƒ2值,结果见表6。由表6可见,参比制剂和自制他达拉非片在4种溶出介质中的溶出曲线间的ƒ2值均大于50,表明自制他达拉非片具有与参比制剂相似的溶出特性。
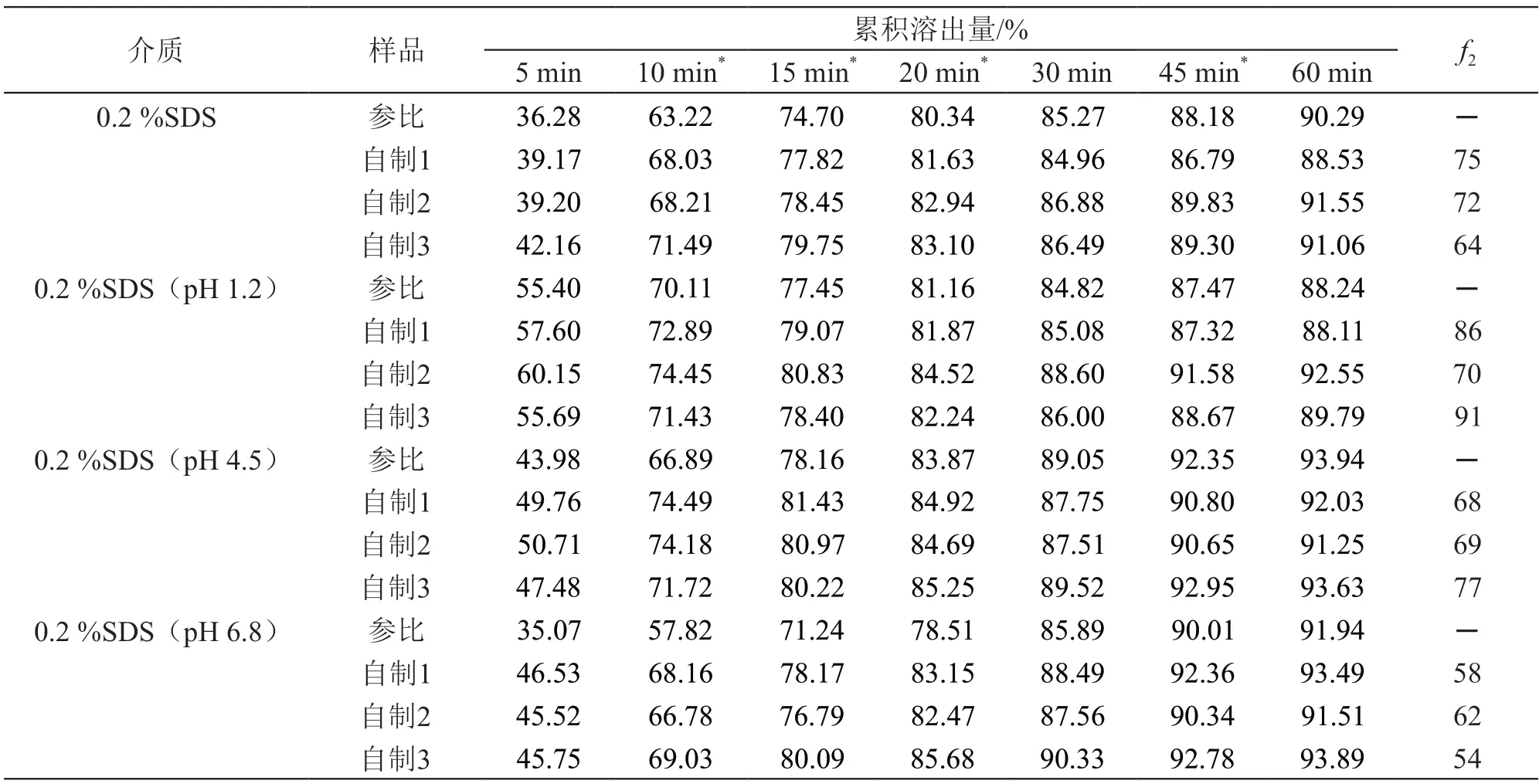
表6 自制他达拉非片在不同溶出介质中的溶出曲线对比
3 讨论
他达拉非为水难溶性药物,且无pH依赖性,水作为溶出介质无法满足漏槽条件且无区分能力。通过溶解度试验结果可知,他达拉非溶解度与溶剂中SDS浓度基本成正比,但当SDS浓度浓度过大时,他达拉非片呈快速溶出状态,满足漏槽条件但基本无区分力。本研究最终确定在溶出介质中加入0.2 %SDS可使溶出条件更具有区分力。参考指导原则推荐的溶出条件,最终筛选得到具有区分力的4种不同的溶出介质。
他达拉非片进口药品注册标准中溶出度定量检测方法为UV法,采用吸光度的一阶导数法计算他达拉非溶出量,计算过程比较复杂;美国药典USP43中溶出度测定方法为HPLC法,但流动相为甲醇-水(50:50),黏度较大,极易损伤色谱柱,且主成分出峰时间较晚,分析时间较长。本研究所用液相色谱条件可使他达拉非快速出峰且峰形良好,溶剂及辅料峰均不干扰测定,能较大程度提高检测效率,同时采用标准曲线法进行定量计算,即使供试品溶液浓度范围波动较大也能保证计算结果的准确性。此外,本研究对他达拉非在不同溶出介质中的溶出度定量测定方法进行了验证,本方法专属性、准确度、精密度良好,且在最低与最高溶出度范围内,他达拉非浓度与峰面积呈良好的线性关系,各项试验结果均符合规定。最终确定本方法用于测定他达拉非溶出度准确可靠。
溶出曲线相似性评价结果表明,自制片与参比制剂在各溶出介质中的溶出行为基本相似,为仿制药一致性评价提供了试验依据。

