双黄连口服液不同精制工艺对比评价研究*
白璐 惠志立 崔春利 史亚军 刘红波 刘航 刘文豪
(1.西安市第一医院,陕西 西安 710002;2.西安医心演绎医疗科技有限公司,陕西 西安 710301;3.陕西中医药大学/陕西省中药基础与新药研究重点实验室,陕西 西安 712046;4.陕西中医药大学附属医院,陕西 咸阳 712000)
以水煎服的中药汤剂,是中医临床用药的主要形式,也充分体现出中药水提液临床应用的普遍性与重要性。“溶液环境”是指溶液体系所具有的黏度、pH、离子强度、电解质成分等特征性质[1-2]。中药水提液因为溶媒水、极性大、溶出成分多样,使得水提液环境复杂。正如双黄连口服液在提取过程中,不仅提取出了对疾病有治疗作用的有效成分,如黄芩苷、绿原酸等;一些易溶于水的杂质和无效成分也随之被提取出来,如多糖、蛋白质等大分子物质。为了确保药物有效成分的溶出度,提高药物疗效,水提醇沉法[3-4]、微滤法[5-11]、絮凝法[12-15]、高速离心法[16-17]均在中药水提液精制中被探索研究。本文以双黄连口服水提液为实验体系,基于“溶液环境”与药物有效成分密切关系,通过研究双黄连口服液三种不同精制工艺,比较其物化参数、指标性成分黄芩苷的含量和其大分子去除率,从而得出双黄连口服液的最佳精制工艺,以期为复杂“溶液环境”的中药水提液的精制提供实验基础。
1 仪器与试药
1.1仪器 KQ-400KDE型高功率数控超声波清洗器(昆山市超声仪器有限公司);AL204电子天平(梅特勒-托利多仪器上海有限公司);UPR系列超纯水器(四川优普超纯科技有限公司);Agilent 1260高效液相色谱(美国);实验室用LNG-CM-101膜分离机(上海朗极膜分离设备工程有限公司);DDS-307电导率仪(上海精密科学仪器有限公司);PHSJ-4F实验室用pH计(上海仪电科学仪器股份有限公司);DV-I+黏度计(美国BROOKFIELD公司);WGZ-3.3A浊度计(上海昕瑞仪器仪表有限公司)。
1.2试药 黄芩、金银花和连翘3味药材饮片均购自西安兴盛德中药饮片有限责任公司,经王继涛高级实验师鉴定均符合《中国药典》2020年版一部规定。黄芩苷标准物质(批号:110715-201318)来源于中国食品药品检定研究院。牛血清白蛋白(BSA);考马斯亮蓝G-250;甲醇为色谱纯,其余试剂均为分析纯。
2 方法
2.1双黄连口服液水提液的制备 按处方比例,分别取金银花375 g,黄芩375 g,连翘750 g,称取各味药的1/15。黄芩煎煮3次,第一次加入14倍水,煎煮2 h;第二次加12倍水,煎煮1 h;第三次加12倍水煎煮1 h。分别用四层纱布滤过,合并滤液。金银花、连翘先温浸30 min,煎煮两次,第一次14倍水,煎煮1.5 h;第二次12倍水,煎煮1.5 h。四层纱布滤过,合并滤液。将两次滤液合并,调整成浓度为0.04 g·mL-1(以生药量计,下同)的水提液,待用。
2.2精制操作工艺
2.2.1微滤法 取双黄连水提液500 mL,过孔径为0.08 μm的无机陶瓷膜,收集滤液,调整成0.04 g·mL-1,待用。
2.2.2醇沉法 取1 L双黄连水提液平均分成四等份,不断搅拌并缓慢加入250 mL、375 mL、583 mL、1000 mL的95%分析乙醇(慢加快搅),分别使含醇量达到50%、60%、70%、80%,静置24 h,滤过,挥至无醇味后,调整成0.04生药g·mL-1,待用。
2.2.3絮凝法 取三等份双黄连水提液,每份500 mL,加入配置好的壳聚糖絮凝液,使壳聚糖含量达10%、20%、30%,静置24 h,滤过,挥至无酸味后,调整成0.04生药g·mL-1,待用。
2.3物化参数的测定 分别取双黄连口服液水提液及精制液适量,均通过恒温水浴恒温至25 ℃,分别以已校正精密pH计测定pH值;以电导率仪测定电导率值;以浊度计测定浊度;依据《中国药典》2020年版四部通则0633黏度测定法第三法中(3)转子型旋转黏度计以BROOKFIELD黏度计测定水提液及各纯化法所得精制液流体的相对黏度。
2.4高分子物质的测定 分取2.1项下双黄连口服液水提液及2.2项下各精制液适量,采用考马斯亮蓝G-250比色法测定蛋白质含量[18];采用《中国药典》2020年版四部通则2202鞣质含量测定法测定鞣质含量[19];采用高锰酸钾滴定法测定酶解前的还原糖量及酶水解和酸水解后还原糖量,依据公式计算:淀粉含量=酶水解和酸水解后还原糖量-酶解前的还原糖量[20];果胶含量测定利用果胶酸钙不溶于水的特性,向含果胶溶液中加入沉淀剂,使果胶形成果胶酸钙沉淀,测定果胶酸钙量并换算成果胶量[21]。
2.5黄芩苷含量测定[22-25]
2.5.1色谱条件 以十八垸基硅烷键合硅胶为填充剂;甲醇-水-磷酸(47∶53∶0.1)为流动相,检测波长为280 nm。理论板数按黄芩苷峰计算应不低于2500。
2.5.2对照品溶液的制备 取黄芩苷对照品适量,精密称定,加甲醇制成每1 mL含0.064 mg黄芩苷的溶液,即得。
2.5.3供试品溶液的制备 分别取各方法精制样液25 mL,摇匀,精密吸取1 mL,置于50 mL量瓶中,加70%乙醇约45 mL,超声处理30 min,放至室温,加70%乙醇定容至刻度,摇匀,滤过,取续滤液,精密量取5 mL,加甲醇稀释至10 mL,摇匀,0.45 μm微孔滤膜过滤,备用。
2.6相关性统计分析方法 采用R语言3.4.3软件和IBM SPSS Statistics 19.0软件分别进行性分析,分别对pH、浊度、黏度、电导率、蛋白质含量、鞣质含量、淀粉含量、果胶含量及黄芩苷含量进行正态性检验。R语言构建目标数据集,然后批量求解,*表示P<0.1,*表示P<0.05,**表示P<0.01,***表示P<0.001。
3 结果
3.1物化参数测定 结果与原液相比较,唯独微滤液pH显著上升,醇沉液的pH随着加入醇量的增大变化不明显,絮凝液的pH随着絮凝剂浓度变化,其中20%絮凝液的pH最大,30%絮凝液次之;浊度微滤液的浊度显著下降,醇沉液的浊度随着醇量的增多先减小后增大,其中60%醇沉液浊度下降最多,随絮凝液浓度增大浊度增加,10%絮凝液浊度最小;三种精制液的黏度变化不大,微滤液的黏度下降最为明显,醇沉液的黏度基本随加入醇量的增大而增大;电导率与原液相比较,微滤液的电导率下降最明显,醇沉液的电导率随加入醇量的增多而减小,絮凝液的电导率随加入絮凝剂的增多而增大。结果见表1。
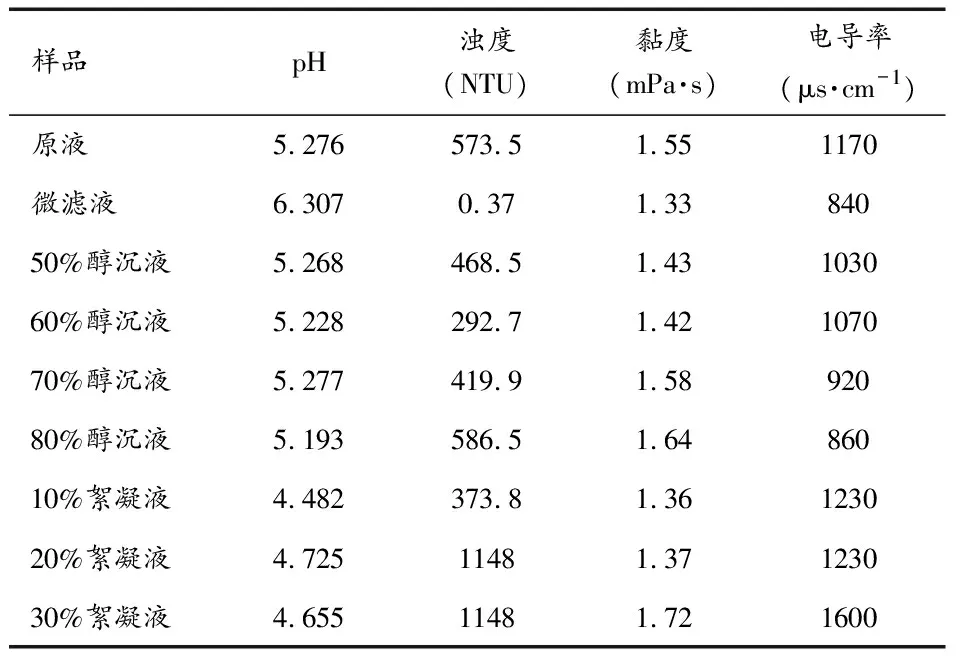
表1 物化参数测定结果
3.2高分子测定结果 通过数据比较分析,从四种高分子去除总体70%醇沉液>微滤液>50%醇沉液>80%醇沉液>10%絮凝液>30%絮凝液>60%醇沉液>20%絮凝液,结果见表2。
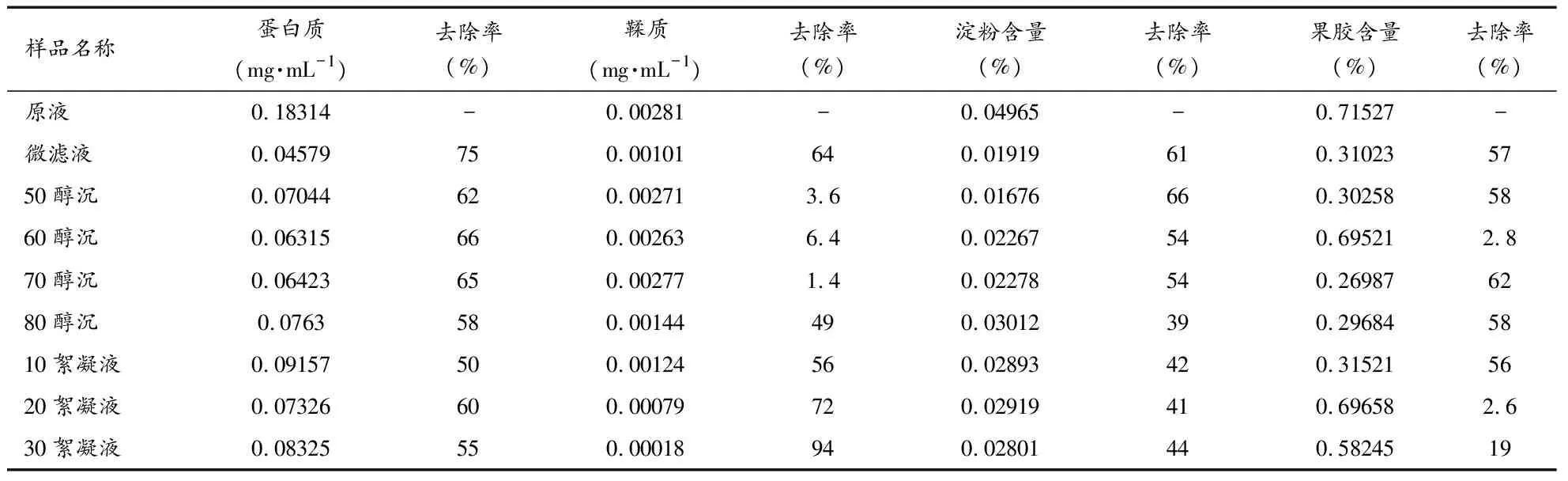
表2 高分子含量测定结果
3.3黄芩苷含量测定结果
3.3.1线性关系考察 分别精密吸取3.4.1对照品溶液2、4、6、8、10μL注入高效液相色谱仪,按选定的色谱条件进行测定,记录色谱图及峰面积。以峰面积的积分值定量,以峰面积积分值Y为纵坐标,进样量X(μg)为横坐标,绘制标准曲线,并进行回归分析,黄芩苷的回归方程为:Y=301.1X+27.678,r=0.9997。结果表明,黄芩苷的进样量在0.128~0.64 mg范围内具有良好的线性关系。
3.3.2精密度实验 精密吸取标准品溶液10 mL,连续进样5次,测得黄芩苷峰面积积分值的RSD值为0.38%,结果表明该仪器精密度良好。
3.3.3稳定性实验 取标准品溶液,依法分别于0、2、4、6、8、12 h测定,测得黄芩苷峰面积积分值的RSD值为1.99%,表明供试品溶液在12 h内稳定性良好。
3.3.4重复性实验 取微滤液5份,分别按2.5.3项下供试品溶液制备方法制成5份供试品溶液,以2.5.1项下色谱条件测定,测得黄芩苷质量浓度分别为1.145、1.138、1.147、1.135、1.142 mg·mL-1,RSD值为0.43%,表明该方法重复性良好。
3.3.5回收率实验 取微滤液10 mL,6份,分别加入一定量的黄芩苷对照品,按照供试品溶液的制备方法制备供试品溶液,按上述色谱条件及测定方法进行测定,计算回收率,平均回收率为96.51%,RSD值为1.42%。表明黄芩苷回收率良好,结果见表3。
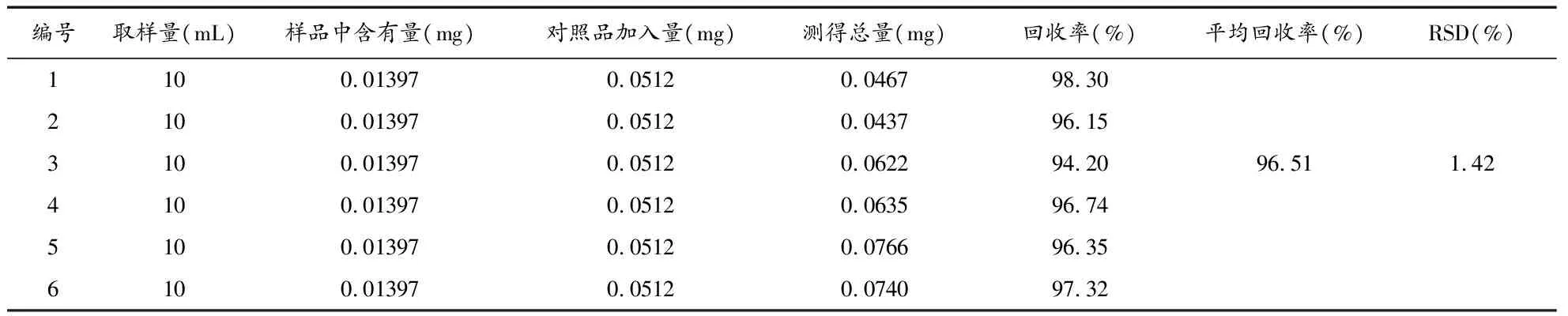
表3 回收率试验测定结果(n=6)
3.3.6样品含量测定 分别取供试品溶液,进样10 μL,在给定的色谱条件下,测定黄芩苷的峰面积,由对应的线性方程计算其含量,结果见表4。
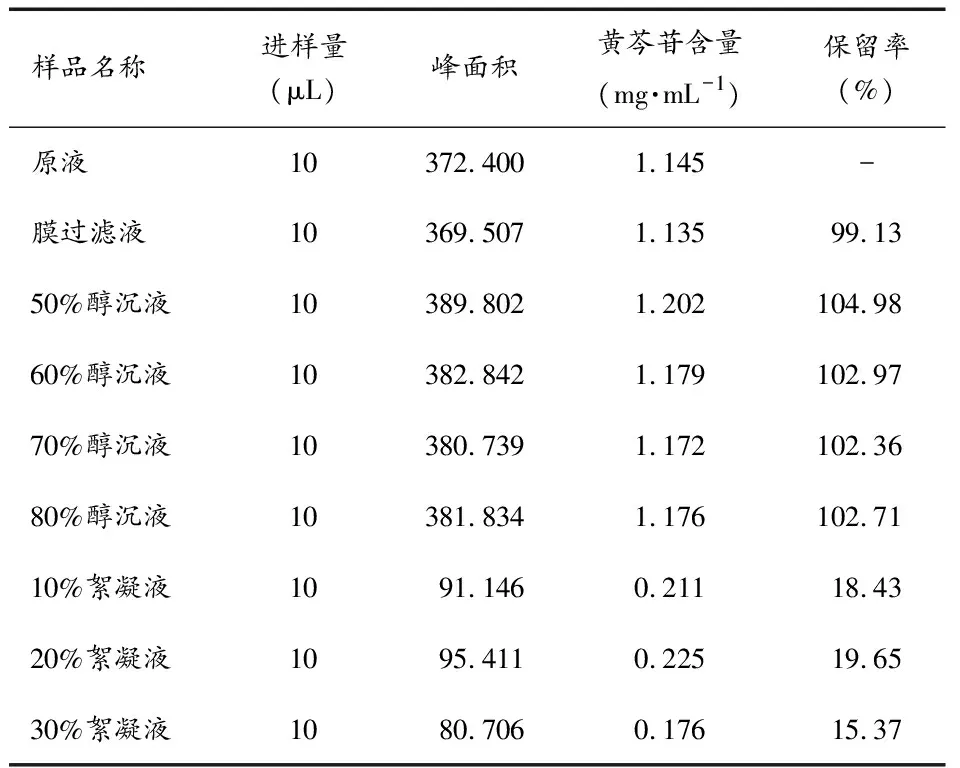
表4 黄芩苷含量测定结果
由表4结果显示,膜过滤液黄芩苷含量略有下降,可能是过滤时黄芩苷随杂质一起被滤过所致;醇沉液黄芩苷含量反而略有上升,这可能与黄芩苷的溶解度密切相关,表明黄芩苷在50%~80%的醇液中溶解度会增大,其中50%醇沉液黄芩苷含量最高,60%醇沉液、70%醇沉液、80%醇沉液的黄芩苷含量相近。絮凝液黄芩苷含量大幅下降,其中20%絮凝液黄芩苷含量较10%絮凝液、30%絮凝液高。由此可见,对于双黄连口服液最不理想的精制方法为絮凝法。
3.6相关性分析结果
3.6.1不同精制工艺“高分子含量-物化参数”“物化参数之间”“高分子含量之间”相关性分析结果 通过分析,物化参数与高分子含量之间均没有相关性。物化参数之间结果显示:pH与浊度呈显著负相关(P<0.05);pH与电导率呈显著负相关(P<0.05);浊度与电导率呈显著正相关(P<0.05)。高分子之间相关结果显示:蛋白质含量与淀粉含量呈极显著正相关(P<0.001)。见图1。
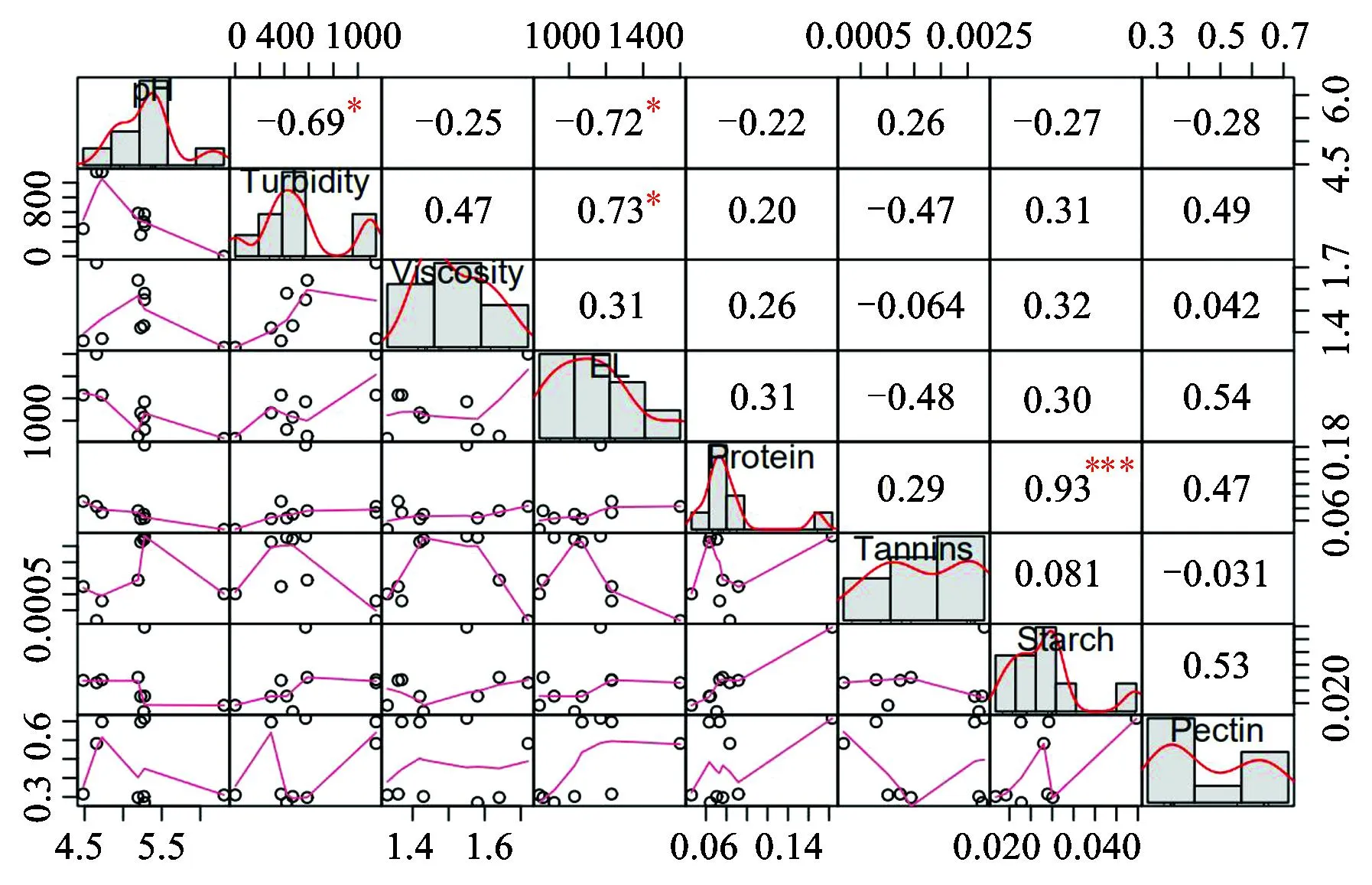
注:图中方框中数字表示两个比较样本相关值;*表示显著程度(*P<0.05,***P<0.001);Turbidity表示浊度;Viscosity表示黏度;EL为 electrical conductivity缩写,表示电导率;Protein表示蛋白质;Tannins表示鞣质;Starch表示淀粉;Pectin表示果胶
3.6.2不同精制工艺“黄芩苷含量-物化参数”相关性分析结果 相关性结果显示:pH与黄芩苷含量呈显著正相关(P<0.05);浊度与黄芩苷含量呈负相关(P<0.1),黏度与黄芩苷含量没有相关性;电导率与黄芩苷含量呈显著负相关(P<0.05)。见图2。

注:图中方框中数字表示两个比较样本相关值;*与#表示显著程度(*P<0.05,#P<0.1);Turbidity表示浊度;Viscosity表示黏度;EL为 electrical conductivity缩写,表示电导率;Baicalin表示黄芩苷
3.6.3不同精制工艺“黄芩苷含量-高分子含量”相关性分析结果 高分子含量中仅鞣质含量与黄芩苷含量呈显著相关(*P<0.05),蛋白质含量、淀粉含量、果胶含量均与黄芩苷含量没有相关性。见图3。
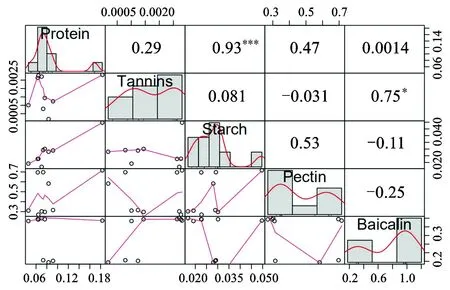
注:图中方框中数字表示两个比较样本相关值;*表示显著程度(*P<0.05);Protein表示蛋白质;Tannins表示鞣质;Starch表示淀粉;Pectin表示果胶
从以上相关性结果可以看出,采用不同精制工艺测得的黄芩苷含量与pH、鞣质含量呈正相关;与浊度、电导率呈负相关。相关性较好,说明不同精制工艺对双黄连口服液有效成分黄芩苷含量有显著影响。
4 讨论
中药复方水提液是一个极其复杂的化学体系,对水提液精制方法应建立在能去除杂质,最大程度的保留有效成分,同时还要考虑其经济性、实用性。基于中药复方水提液的特点,膜分离技术在中医药领域的应用彰显优势。郭立玮等[26]在20多年前分析论证了21世纪中药植物药深加工与现代膜分离技术相结合的研究开发思路,之后很多研究者开展了符合国际规范的中药或复方的膜分离技术探究。孙立霞等[27]采用KBT-ZTC絮凝澄清法、酶解法、微滤法、酶解-微滤法及絮凝澄清-微滤法澄清参玉口服液,研究结果证实絮凝澄清-微滤法为最佳方法。高红宁等[28]通过比较分析枳实、苦参和金银花澄清前后固形物、性状、膜通量、指标成分等指标,研究证实微滤法对中药水提液起到较好的澄清除杂效果。不仅如此,微滤法也被应用到中药挥发油的分离,韩志峰[29]以常见的九种含油水体进行优化探究,旨在推进微滤在挥发油淋领域的应用。朱华旭等[30]探讨了膜分离技术在中药废弃物有效组分资源化的原理、方法与应用实践,比较系统描述了膜技术在中药废弃物的提取、分离、浓缩、纯化工程的应用前景,论述了膜技术在中药资源产业化过程中的适宜性和可行性。
本文以双黄连口服液为例,实验结果显示,采用醇沉法略高保留了有效成分,但其存在耗醇量大、乙醇回收率低、耗能大、醇沉后的药液进行浓缩相对较慢、成本较高、危险性较大的缺点。絮凝法中絮凝剂在凝结过程中不仅去除了杂质,还去除了一些小分子有效成分,导致其有效成分大幅含量降低。膜过滤法其有效成分含量介于醇沉法和絮凝法之间,但物化参数结果显示膜过滤法能更大程度的去除杂质,保证药液澄明度和稳定性。综合考虑,膜微滤法应用于中药复方水提液的精制效果最佳。
双黄连口服液不同精制工艺研究中,从相关分析性结果看,在物化参数相关性结果中提示pH值浊度、电导率测定具有较大意义,而黏度测定意义不大。高分子含量相关性分析结果提示,鞣质测定对处方中黄芩苷含量具有显著影响,果胶测定意义不大,处方中蛋白质含量与淀粉含量具极显著正相关性,今后评价时应予以重点关注。

