量子化学计算白藜芦醇与芝麻酚在油脂中的抗氧化协同作用
高伟洪 曲潇笛 姚云平 李昌模
(天津科技大学食品科学与工程学院,天津 300457)
近年来,随着生活水平的提高,食用油脂的安全问题受到关注与重视[1-2]。脂质过氧化与许多外在因素有关,例如辐射、金属离子和光照。脂类氧化不仅会在食品中产生令人不快的酸败味,还会在烹饪和加工后形成有害的氧化产物,从而降低营养质量和安全性[3]。人工合成的抗氧化剂虽对油脂的抗氧化效果显著,但因具有潜在毒性,过量使用有一定致癌作用[4]。安全、高效、绿色的天然抗氧化剂开发已成为当今食品科学研究领域的重点和发展趋势[5-6]。
白藜芦醇和芝麻酚是天然的酚类物质,具有抗自由基、抗氧化等生理活性,作为抗氧化剂添加到油脂中能明显降低油脂的氧化、劣变[7-12]。Huang等[13]发现白藜芦醇与芝麻酚对高油酸花生油能起到协同保护作用,并对脂肪酸的异构化有明显抑制作用。虽然白藜芦醇与芝麻酚在油脂保护方面具有明显的协同作用,但协同机理尚不清楚,且二者对油脂中自由基清除的相关报道较少。随着计算科学的发展,量子化学模拟技术在学术和工业研究领域发挥着重要作用。与传统的试验方法相比,量子化学模拟可以从化学动力学角度揭示化学反应的机理[14-15]。Tang等[16]利用量子化学观察到不同烷基链长的抗氧化剂对橄榄油的影响,其中极性抗氧剂表现出良好的抗氧化性和相对适宜的迁移性。
研究拟将去除天然抗氧化剂的葵花籽油作为基质,研究白藜芦醇和芝麻酚之间的相互作用。通过自由基分析和量子计算相结合的方法,深入研究白藜芦醇与芝麻酚在葵花籽油中的协同抗氧化行为,以期为脂溶性抗氧化剂的协同作用提供依据。
1 材料与方法
1.1 材料与仪器
1.1.1 材料与试剂
葵花籽油:市售;
芝麻酚、白藜芦醇:纯度98%,上海阿拉丁生化科技股份有限公司;
1,1-二苯基-2-三硝基苯肼(DPPH):纯度99%,西亚化学科技有限公司;
其他试剂均为国产分析纯。
1.1.2 主要仪器设备
烘箱:DH-101-1BY型,天津市中环电炉股份有限公司;
紫外—可见光分光光度计:Evolution 300型,北京瑞利分析仪器有限公司;
高效液相色谱仪:LC-20AT型,日本岛津公司;
油脂氧化稳定仪:892型,瑞士万通公司。
1.2 方法
1.2.1 葵花籽油的纯化 100 g硅胶中加入150 mL浓盐酸进行酸化,然后水洗至中性,于110 ℃烘箱中活化6 h,加入50 g活性炭,搅拌均匀,加入100 g葵花籽油,200 mL正己烷,超声、搅拌2 h,抽滤、50 ℃旋蒸,置于-18 ℃贮藏备用。
1.2.2 自由基检测 将油样于180 ℃加热5 h,每隔1 h取样,将50 μL氧化的油样与4 mL 6 μmol/L的DPPH—乙醇溶液涡旋混合,暗处反应30 min,利用紫外—可见光分光光度计测定517 nm处的吸光度。
1.2.3 氢过氧化物的检测 将油样于60 ℃加热5 d,每24 h取样一次。取40 mg样品,加入5 mL正己烷,加入5 mL脂肪酶缓冲液(A液:取1.78 g磷酸氢二钠溶于100 mL水,B液;取0.78 g磷酸二氢钠溶于100 mL水;将100 mg脂肪酶溶于49 mL A液与51 mL B液的混合液体中),涡旋15 min,静置后取上层清液,重复3次,合并有机相,氮气吹干后用正己烷定容至1 mL,过0.45 μm微孔有机滤膜,待进样。
液相条件:色谱柱为Inertsil SIL 100A(5 μm,4.6 mm×250 mm),柱温40 ℃,检测波长234 nm,等度洗脱,流速2 mL/min,流动相为正己烷∶异丙醇∶冰乙酸(V正己烷∶V异丙醇∶V冰乙酸为100∶1∶0.1);进样量为20 μL。
1.2.4 诱导期测量 使用Rancimat 892油脂氧化稳定仪测量诱导期(IP),取3.0 g油脂样品于仪器专用测量管中,加入60 mL蒸馏水。仪器温度为110 ℃,空气流量为20 L/min。按式(1)、式(2)分别计算抗氧化保护系数和协同效应。
PF=IP′/IPC,
(1)
SE=EE/(E1+E2),
(2)
式中:
PF——抗氧化保护系数;
IP′——加入抗氧化剂的油脂氧化诱导时间,h;
IPC——未添加抗氧化剂的油脂氧化诱导时间,h;
SE——协同效应(SE>1为协同作用,SE<1为拮抗作用[17]);
EE——组合抗氧化剂的试验值减去空白油样的试验值,h;
E1、E2——单一抗氧化剂的试验值减去空白油样的试验值,h。
1.2.5 抗氧化剂检测
(1) 芝麻酚检测:取2.0 g样品和4 mL甲醇置于10 mL试管中,涡流混匀3 min,超声15 min,4 ℃、5 000 r/min离心15 min,将上清液转移到10 mL试管中,萃取过程重复3次(每次3 mL甲醇),合并提取溶剂,氮气吹干,复溶1 mL,并使用0.22 μm微孔有机滤膜过滤待进样。
色谱条件:色谱柱为ZORBAX Eclipse Plus C18柱;流动相为含5%乙酸乙酯的甲醇—水(V甲醇∶V水=7∶3);柱温30 ℃;等度洗脱;流速0.8 mL/min;检测波长298 nm;进样体积20 μL。
(2) 白藜芦醇检测:取2.0 g样品和4 mL甲醇置于10 mL试管中,涡流混匀3 min,超声15 min,4 ℃、5 000 r/min离心15 min,将上清液转移到20 mL试管中,萃取过程重复3次(每次3 mL甲醇),合并提取溶剂,氮气吹干,复溶1 mL,并使用0.22 μm微孔有机滤膜过滤待进样。
色谱条件:色谱柱为ZORBAX Eclipse Plus C18柱;柱温35 ℃;进样量10 μL;流动相A为水;流动相B为甲醇。梯度洗脱程序:0~5 min,60% B;5~11 min,90% B;11~15 min,100% B。检测波长306 nm;温度35 ℃,流速1 mL/min,进样量10 μL。
1.2.6 量子化学计算 利用第一性原理的从头计算方法,采用密度泛函理论(DFT)进行计算。在B3LYP/6-311G(d,p)基础上计算,利用过渡态(TST)理论公式进行动力学常数计算。TST理论公式:
(3)
式中:
σ——反应路径简并度,一般为1;
kB——玻尔兹曼常数;
ΔG——标准态的活化能(过渡态与反应物的能量差值);
T——反应温度,℃;
h——普朗克常量;
R——理想气体常数。
1.2.7 数据处理 所有数据为3次平行测量的平均值,用平均值±标准差表示。采用Origin 2019软件作图, Gaussian09软件进行相关的量子计算。
2 结果与分析
2.1 油脂高温氧化下的自由基变化
由图1可知,分别添加100 mg/kg白藜芦醇和芝麻酚至葵花籽油中,氧化2 h时,抑制油脂氧化产生的自由基效果为白藜芦醇>芝麻酚。相比于空白组,白藜芦醇将自由基含量从0.21 mol/L下降到0.08 mol/L,减少了61.9%。加热至3 h后,油样中自由基含量趋于一致,且无显著差异,与Lee等[18]的研究结果一致。所有样品在氧化3 h后表现出相似的自由基含量,这与抗氧化剂的种类无关,可能是由于加入抗氧化剂后油脂残留的脂自由基所导致的。白藜芦醇具有较强的清除自由基能力可能归因于它不仅能起到供氢的作用,且在供氢后白藜芦醇自由基能与脂肪酸自由基结合,影响其空间结构,增大了异构化的能垒,从而防止异构化的作用[19],进而间接影响自由基含量。

图1 白藜芦醇与芝麻酚对自由基的抑制影响
2.2 氢过氧化物含量变化
根据已知的脂质链式反应,油脂在形成烷基自由基后,易与三线态氧(3O2)反应,产生过氧自由基,过氧自由基通过抽氢形成氢过氧化物,通过对氢过氧化物的分析可知过氧自由基的变化。由图2可知,60 ℃下,未添加酚类抗氧化剂的葵花籽油在加热后的第4天氢过氧化物含量最高。添加100 mg/kg的白藜芦醇和芝麻酚,其氢过氧化物含量分别从32 mg/g下降至16,5 mg/g。白藜芦醇和芝麻酚均能抑制已鉴定的氢过氧化物的形成。根据已提出的自由基介导机制,可以推测自由基清除剂可能通过阻止氧化过程中的过氧自由基的形成来抑制氢过氧化物的形成。

图2 60 ℃下氢过氧化物含量变化
2.3 油脂热稳定性分析
当白藜芦醇和芝麻酚添加量从100 mg/kg提高到2 000 mg/kg时,能够显著增加葵花籽油的氧化诱导时间,且二者添加量为1 400 mg/kg时,氧化诱导时间分别达(3.60±0.09),(8.32±0.48) h,相比于空白油样分别延长了4.1,11.2倍,PF值最高。通过表1可知,白藜芦醇和芝麻酚能起到协同作用的最佳添加量分别为1 400,200 mg/kg。与空白组相比,氧化诱导时间延长了9.18倍;与单独添加芝麻酚相比,氧化诱导时间增加了3倍;与单独添加白藜芦醇相比,氧化诱导时间增加了1.89倍,说明二者按照一定配比添加到葵花籽油中,对亚油酸体系的氧化诱导时间的延长有更好的效果。
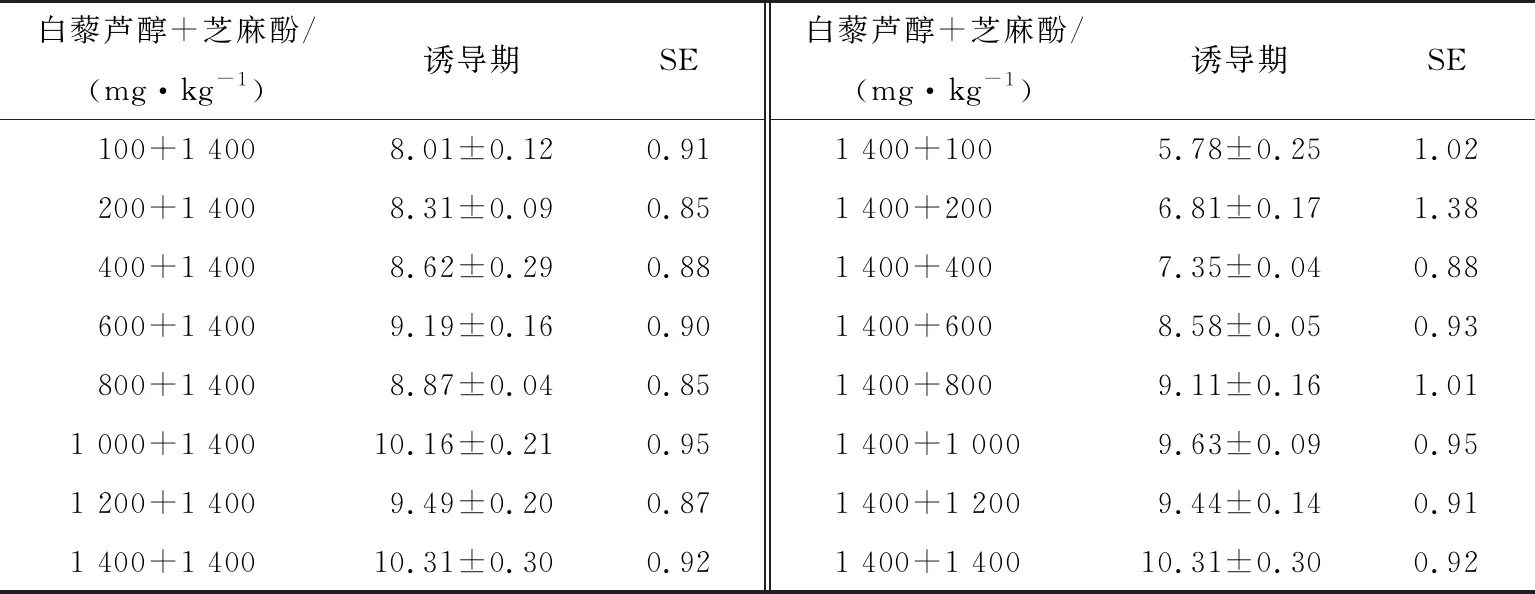
表1 白藜芦醇与芝麻酚混合作用对葵花籽油氧化诱导时间的影响
2.4 组合抗氧化剂的降解
白藜芦醇和芝麻酚于180 ℃下加热7 h,其含量与降解速度变化分别如图3、图4所示。
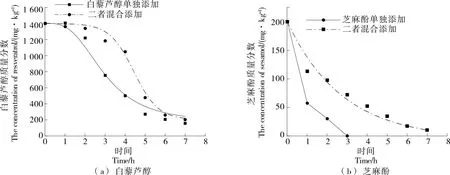
图3 白藜芦醇和芝麻酚于180 ℃下的降解曲线

图4 白藜芦醇和芝麻酚于180 ℃下的降解速度变化曲线
由图3可知,单独添加,白藜芦醇添加量随加热时间的延长呈下降趋势,对比混合添加,白藜芦醇添加量在加热时间≤3 h时,其含量一直保持在相对稳定的状态,3 h后其含量开始下降。由图4可知,白藜芦醇消耗速度最快的时间为2.5 h,混合添加时消耗速度最快的时间为4.5 h。与单独添加相比,芝麻酚的加入延缓了白藜芦醇的消耗,一方面是前期白藜芦醇的消耗量较少,其消耗速度明显减缓。由此推测:① 芝麻酚与白藜芦醇同时存在时,芝麻酚先参与抗氧化;② 二者前期都有一定的消耗,但是前期白藜芦醇失去一个H后,能够接受芝麻酚提供的H,导致白藜芦醇的降解速度变得缓慢。
单独添加芝麻酚时,其在3 h内消耗殆尽,且诱导期数据也表明添加200 mg/kg的芝麻酚可以在2.2 h内保证油的稳定性。混合添加时,加热时间为3 h时,芝麻酚的拨云见日一分数为75 mg/kg,到加热第7 h时,芝麻酚剩余10 mg/kg。白藜芦醇的加入,能够延长芝麻酚的保护时间,可能是因为白藜芦醇能够对芝麻酚起到再生作用。
2.5 协同抗氧化机理分析
2.5.1 反应活性位点的确定 量子化学分子轨道理论认为,最高占据轨道(HOMO)和最低空轨道(LUMO)分布直观地显示了抗氧化剂的主要活性中心,这些参数可以直观地表达抗自由基活性相关的重要参数,HOMO的形状决定了自由基攻击的位置[20]。
由图5可知,芝麻酚的HOMO定位于苯酚环和亚甲基二氧基位置,白藜芦醇的HOMO定位于除间位的羟基以外的整个分子中。由图6可知,羟基的键解离能相比于其他位置的碳氢键要低112.97~138.07 kJ/mol,因此二者的活性位点位于羟基基团附近。在脂质环境中,酚类抗氧化剂的羟基基团在热力学上优先选择H原子转移机制[21],进而阻止油脂氧化中的链传播。所以这二者更是一种通过供H的方式来实现其动态平衡。

图5 白藜芦醇和芝麻酚的最高占据轨道
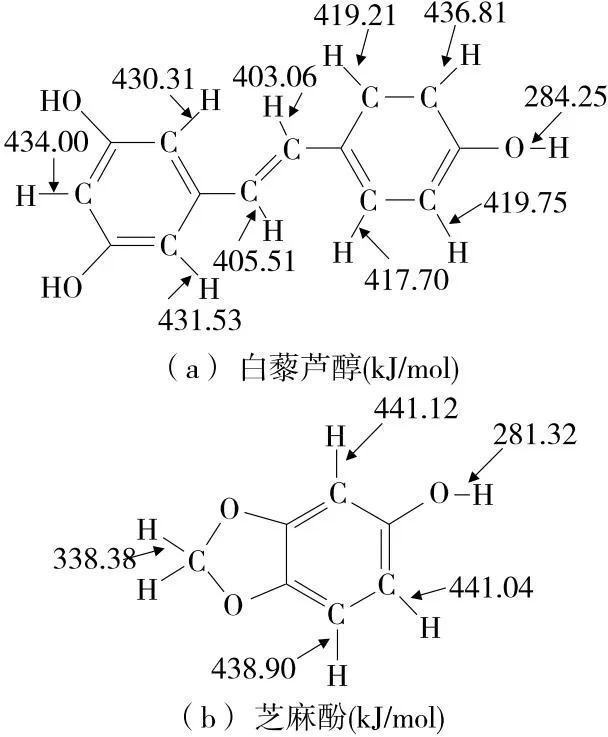
图6 白藜芦醇和芝麻酚的键解离能
2.5.2 白藜芦醇与芝麻酚之间的H转移 由图7可知,白藜芦醇向芝麻酚自由基供H的能垒为17.66 kJ/mol,芝麻酚向白藜芦醇自由基供H的能垒为12.93 kJ/mol,这两种反应均可自发进行,表明白藜芦醇与芝麻酚之间存在一种反应平衡。相比之下,自由基更容易夺取芝麻酚中的H。虽然芝麻酚的能垒比白藜芦醇的低4.73 kJ/mol,但当芝麻酚添加量较少时,白藜芦醇才能与芝麻酚发生协同作用。当芝麻酚添加量>400 mg/kg时,芝麻酚向白藜芦醇自由基供H占据整个体系中的主导反应,所以二者发生拮抗作用,与表1结果一致。

图7 白藜芦醇和芝麻酚之间的反应路径
反应动力学常数是描述化学反应速率的重要参数。利用TST理论公式对白藜芦醇与芝麻酚之间的供H反应分别进行动力学常数计算,其中白藜芦醇向芝麻酚自由基供H的反应速率常数为8.682×1010mol/(L·s),芝麻酚供H给白藜芦醇的反应速率常数为3.040×1011mol/(L·s),芝麻酚供H给白藜芦醇的速率更快,与二者混合添加时白藜芦醇在前期的降解消耗较慢相对应。随着降解时间的延长,芝麻酚一方面保护葵花籽油,另一方面保护白藜芦醇,导致其含量不断下降,向白藜芦醇供H反应速率下降,打破了互相供H的局面,特别是加热4.5 h时,白藜芦醇的消耗速度最快,反应后期更倾向于白藜芦醇供H给芝麻酚自由基,导致芝麻酚再生。
3 结论
试验表明,白藜芦醇和芝麻酚对葵花籽油中的总自由基和过氧自由基分别有最佳抑制效果。当白藜芦醇和芝麻酚添加量分别为1 400,200 mg/kg时具有最佳抗氧化性,诱导期达到(6.81±0.17) h,为空白组的9.2倍。反应后期,反应平衡更倾向于白藜芦醇向芝麻酚自由基供氢,从而间接地保护了芝麻酚。后续可从抑制不同自由基的作用与抗氧化剂之间相互作用相结合进一步阐明协同抗氧化性的研究机制。

