光催化水还原4-氯硝基苯制备4,4′-二氯氧化偶氮苯
王海军,李明昊,仇 铭,任运来,田欣哲
(1.陕西科技大学 轻工科学与工程学院,陕西 西安 710021;2.河南农业大学 理学院,河南 郑州 450002)
0 前言
4,4′-二氯氧化偶氮苯是1种重要的有机物,在染料、指示剂和液晶材料等方面有着较多的用途[1-3]。该化合物主要通过4-氯硝基苯的还原来合成。反应中使用的还原剂通常为锌粉[4-5]、硼氢化钠[6-7]、甲醛[8]、氢硅烷[9]、二甲基亚砜[10]等。其中锌粉或硼氢化钠还原法不但使用了高成本的还原剂,而且会产生氧化锌或氧化硼污染物[4-7]。甲醛、氢硅烷或二甲基亚砜还原法通常需要使用复杂的催化剂,而且也会产生污染物[8-10]。近年来,化学界发展了很多以氢气或异丙醇为还原剂的方法。例如,文献[11]使用单原子钴催化剂,实现了氢气对硝基苯的还原,得到氧化偶氮苯类化合物。文献[12]使用四羟基二硼催化剂,实现了以异丙醇为还原剂的硝基苯还原。文献[13]制备了1种氮掺杂介孔碳催化剂,并用于以异丙醇为还原剂的硝基苯还原。此外,化学家们也为这类反应发展了多种光催化的方法。文献[14]制备了CQDs/ZnIn2S4纳米复合材料,并以该材料为催化剂,实现了光照条件下的硝基苯还原。文献[15]在光照条件下,完成了硝基苯向氧化偶氮苯的转化反应。
与上面的还原剂相比,水更为清洁易得。因此本研究引入光促进的方式,以水为还原剂,实现了4-氯硝基苯的还原,为4,4′-二氯氧化偶氮苯的合成提供了一种清洁经济的方法。
1 实验部分
1.1 试剂和仪器
主要试剂:蒸馏水(细胞培养级,从麦克林试剂公司购买)、4-氯硝基苯(纯度:99%)、1,4-二氧六环(纯度:>99%)、乙腈(分析纯)、N,N-二甲基甲酰胺(分析纯)、二甲基亚砜(分析纯)、四氯化碳(分析纯)、甲苯(分析纯)、环己烷(分析纯)、四氢呋喃(分析纯)。
主要仪器:核磁共振仪 (400 MHz);气相色谱仪(Thermo Trace 1610);气相色谱-质谱联用仪(Shimadzu QP2020NX);小型光反应仪(光功率可在0~100 W内调节)。
1.2 实验过程
反应操作及后处理过程:把3 mL 1,4-二氧六环、5 mL 蒸馏水、0.5 mmol 4-氯硝基苯加入到反应管(材质为石英)中,并用氮气把管中的空气置换三次。用螺帽封严反应管后,在各表注的条件下进行光照反应(所有反应实验温度为20 ℃)。反应时间到达后,向反应液中加入15 mL水。使用15 mL环己烷萃取3次。利用旋转蒸发仪,把合并的萃取液浓缩至约5 mL。
利用气相色谱内标法确定转化率和产率,具体过程如下:向浓缩液中加入0.5 mmol内标物联苯后,对浓缩液取样,将样品注入气相色谱进行分析。分别根据下面的公式计算出原料4-氯硝基苯的转化率及目标产物4,4′-二氯氧化偶氮苯的产率。
转化率=f×ns×Ai÷As÷na×100%,
其中:f为内标物联苯与原料4-氯硝基苯间的相对物质的量校正因子;ns为内标物的物质的量;Ai为未反应4-氯硝基苯的色谱峰面积;As为内标物的色谱峰面积;na为4-氯硝基苯的物质的量。
产率=f×ns×Ai÷As÷na×100%,
其中:f为内标物联苯与产物4,4′-二氯氧化偶氮苯间的相对物质的量校正因子;ns为内标物的物质的量;Ai为产物4,4′-二氯氧化偶氮苯的色谱峰面积;As为内标物的色谱峰面积;na为原料4-氯硝基苯的加入量(物质的量)÷2。
相对物质的量校正因子f的计算。称取0.5 mmol左右的内标物和0.5 mmol左右的标准品(4-氯硝基苯或4,4′-二氯氧化偶氮苯),并放入样品瓶中,加入5 mL二氯甲烷,并摇晃至均相。将样品注入气相色谱进行分析。根据下面的公式计算出相对物质的量校正因子:
f=(As×ni)÷(Ai×ns),
其是:f为相对物质的量校正因子;As为内标物的峰面积;ni为标准品的物质的量;Ai为标准品的峰面积;ns为内标物的物质的量。
气相色谱定量分析条件:TG—5SILMS毛细管柱 (30 m×0.32 mm),氢火焰离子化检测器,气化室温度280 ℃,初始柱温60 ℃,柱升温速率8.8 ℃/min,最高柱温180 ℃,载气流速35 mL/min。
为了确定目标产物,对产物进行了分离提纯,具体过程如下:按照上述反应操作及后处理过程,做1组平行实验,得到浓缩的萃取液。利用柱层析的方法(填料:200-300目硅胶,洗脱液:石油醚和乙酸乙酯体积比为10∶1),对浓缩萃取液中的产物进行分离提纯。得到的4,4′-二氯氧化偶氮苯[16-17]是橙色固体,熔点为153~156 ℃。1H NMR(400 MHz,CDCl3):δ=8.25(d,J=9.0 Hz,2H),8.16(d,J=8.9 Hz,2H),7.48(d,J= 9.0 Hz,2H),7.45(d,J=8.9 Hz,2H),这与标准样品的1H NMR数据吻合。13C NMR (100 MHz,DMSO-d6):δ=146.2,142.2,138.1,135.3,129.0,127.1,123.7,这与标准样品的13C NMR数据吻合。质谱数据(m/z):[M+]=266.1,这与标准样品的质谱数据吻合。
2 结果与讨论
反应的基本原理被列于图1a中。在光照下,水中的氧提供电子和氢正离子,把4-氯硝基苯还原为4,4′-二氯氧化偶氮苯。与以前的方法(图1b)相比,该反应方法不需要添加任何催化剂,不需要加热,这使得该方法更加清洁和低成本。

图1 本文报道反应原理及特点
2.1 不同溶剂对反应的影响
考察了不同溶剂对反应的影响,结果见表1。值得说明的是,在大部分条件下,底物的转化率都大于目标产物的产率,这主要归因于副产物的生成。当以二氯化碳或四氯化碳为溶剂时,不但没有得到4,4′-二氯氧化偶氮苯产物,而且几乎没有检测到其他产物(表1,序号1~2)。当以环己烷为溶剂时,4-氯硝基苯的转化率为18%,没有检测到目标产物,但有4,4′-二氯偶氮苯及一些未知结构的副产物生成(表1,序号3)。甲苯也不适合用作该反应的溶剂,当以它为溶剂时,仅检测到4-氯苯胺等少量副产物(表1,序号4)。当以四氢呋喃为溶剂时,底物几乎完全转化,目标产物的产率为74%,同时有苯胺和4,4′-二氯偶氮苯副产物生成,产率分别是12%和14%(表1,序号5)。N,N-二甲基甲酰胺也是有效的溶剂,以该化合物为溶剂的反应给出80%产率的目标产物(表1,序号6)。从这些结果可以看出,在筛选的溶剂中,1,4-二氧六环最为有效,在使用该溶剂的情况下,目标产物的产率高达92%(表1,序号7)。值得注意的是,水能够与四氢呋喃、N,N-二甲基甲酰胺或1,4-二氧六环很好地互溶,反应能够有效进行。而水与表1中的其它溶剂难以互溶,则反应不能顺利进行。这些现象说明水与所使用有机溶剂的充分互溶是反应顺利进行的关键。
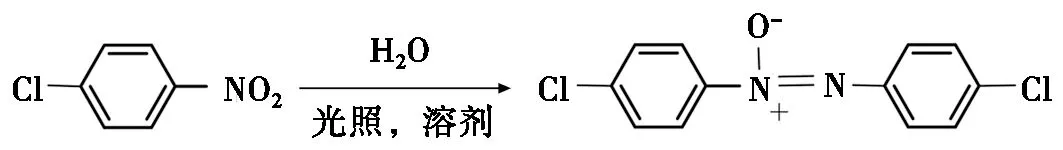
表1 不同溶剂对反应的影响[a]
2.2 不同量的水对反应的影响
考察了不同加入量的水对反应的影响,结果见表2。在不加水的情况下,几乎没有目标产物生成(表2,序号1),这说明水在反应中起到至关重要的作用。当水和1,4-二氧六环的体积比为1∶3时,目标产物的产率为46%(表2,序号2)。随着水和1,4-二氧六环的体积比增大到5∶3,目标产物的产率增大到92%(表2,序号4)。继续增大水的比例,目标产物的产率会降低(表2,序号5)。在无1,4-二氧六环的情况下,反应不能进行(表2,序号6),这主要归因于在纯水中底物不能有效溶解。另外,上述结果也说明:水和1,4-二氧六环的最佳体积比为5∶3。

表2 不同量的水对反应的影响[a]
2.3 不同波长的光对反应的影响
考察了不同光波条件下的反应结果(见表3)。当光的波长为320 nm时,4-氯硝基苯的转化率为100%,4,4′-二氯氧化偶氮苯的产率为81%(表3,序号1),同时得到7%的4,4′-二氯偶氮苯副产物。增大光的波长到365 nm时,4-氯硝基苯也得以完全转化。与320 nm的情况相比,副产物明显减少,因此目标产物的产率得以显著增长(表3,序号2)。在使用420 nm波长的光时,底物转化率和目标产物产率都会明显下降(表3,序号3),分别为46%和44%。继续增大光的波长到520 nm时,反应很难进行,仅5%的底物得以转化(表3,序号5)。上述结果也表明365 nm波长的光是最佳条件。

表3 不同波长的光对反应的影响[a]
2.4 不同功率的光对反应的影响
考察不同功率光条件下的结果。当光的功率为100 W时,4-氯硝基苯能够完全转化(表4,序号1),目标产物的产率为83%。随着光的功率从100 W降低到75 W,底物依然能够转化完全;但副产物减少了,4,4′-二氯氧化偶氮苯的选择性增大了,造成4,4′-二氯氧化偶氮苯的产率提高到92%(表4,序号2)。在75 W基础上继续降低光的功率,底物的转化率和目标产物的产率都会一直降低(表4,序号3~6)。例如,在使用10 W的光源时,反应很慢,仅得到15%产率的4,4′-二氯氧化偶氮苯。这主要归因于:当减小光的功率时,一定时间内反应物接收的光子数会变少,自然减慢了反应速度[14-15]。此外,还考察了无光照条件下的反应,结果表明:无光照条件下反应不能进行(表4,序号7)。即使升温到60 ℃,也没有检测到产物的生成(表4,序号8)。这说明该反应是个光促进的反应。

表4 不同功率的光对反应的影响[a]
2.5 不同底物对反应的影响
考察了不同结构底物对反应的影响。在考察的底物中,仅4-氯硝基苯的反应能够产生高产率的目标产物(表5,序号1)。硝基苯和4-氟硝基苯的反应分别给出23%和26%产率的目标产物(表5,序号2和3),同时有多种未知的副产物生成。当以4-甲氧基硝基苯和4-氰基硝基苯为底物时,目标产物的产率很低(表5,序号4和5)。硝基萘和硝基环己烷不但转化率低,而且目标产物的产率也很低,仅分别为3%和2%(表5,序号6和7)。还考察了溶剂、反应时间等多种条件的改变对序号2~7中反应的影响。结果表明:表5中的反应条件是最优条件。试图通过改变溶剂、反应时间、光的波长等多种反应条件,来控制反应生成其他产物(例如4,4′-二氯偶氮苯、4-氯苯胺等还原产物)。但无论怎么改变反应条件,这些还原产物的选择性一直很低。
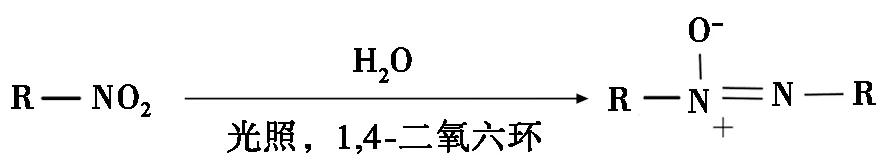
表5 不同底物对反应的影响[a]
2.6 反应机理的研究
图2列出了同位素标记实验结果。在使用H218O的情况下,利用气相色谱-质谱联用仪对气体产物进行检测,发现有18O2气体生成。这说明在反应的过程中,水分子中的氧失去电子转化为氧气;同时说明水分子充当还原剂的作用。在大部分反应中,能够检测到自由基形成的物质。例如在表1(序号4)条件下,会得到由苄基自由基偶联生成的1,2-二苯基乙烷产物。根据文献报道[14,18-26]及上述结果,可以推测该反应经历了自由基反应过程。如图3所示,根据文献报道[20],4-氯硝基苯吸收光能,能形成硝基的三线态双自由基中间体。然后双自由基中间体从水分子中夺取2个氢原子,再脱水生成亚硝基化合物[20];同时水分子转变为羟基自由基。接着亚硝基化合物在光照条件下连续从水中夺取氢原子,转化为羟胺中间体。亚硝基化合物与羟胺中间体反应,脱去一分子水,得到目标产物。
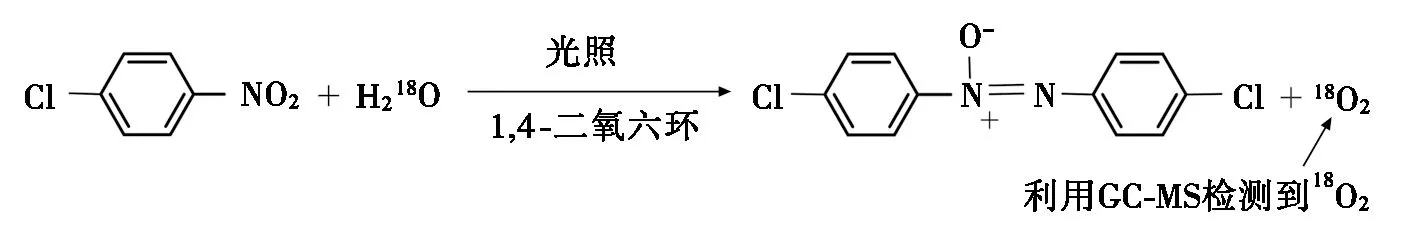
图2 同位素标记实验
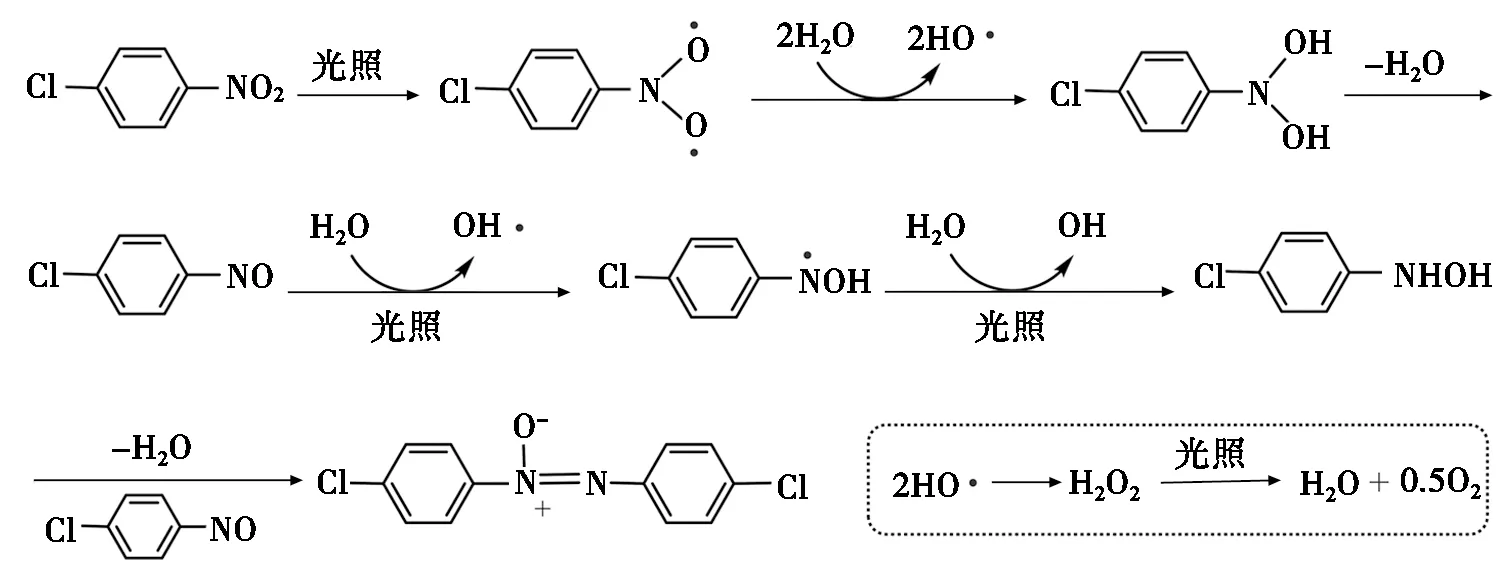
图3 水还原4-氯硝基苯反应机理路径
3 结论
(1)以便宜无毒的水为还原剂,实现了4-氯硝基苯向4,4′-二氯氧化偶氮苯的转化。与以前的工艺相比,本文中的方法避免了污染性还原剂的使用。
(2)考察了不同溶剂、不同量的水、不同波长的光、不同功率的光对反应的影响。结果表明水与所使用有机溶剂的充分互溶是反应顺利进行的关键。反应的最佳条件为:1,4-二氧六环作为溶剂,光的功率为75 W,光的波长为365 nm。在最佳条件下,考察一系列硝基化合物的反应。结果表明仅4-氯硝基苯的反应能够给出高产率的目标产物,产率达到92%。
(3)利用同位素标记实验考察了水的作用,结果表明:水分子发挥还原作用后,生成了无污染的氧气。反应可能经历自由基机理,4-氯硝基苯首先吸收光能,并经历亚硝基和羟胺中间体的形成,得到目标产物。

