戈舍瑞林联合戊酸雌二醇对子宫内膜异位症术后患者疼痛程度、性激素水平的影响
李志言
濮阳市妇幼保健院(河南 濮阳 457000)
子宫内膜异位症是指子宫内膜组织生长在子宫腔、子宫肌层以外部位,且异位内膜可侵犯盆腔脏器、壁腹膜等其他部位,其发病率为15%,临床表现为月经不规律、痛经、慢性盆腔痛[1]。若未及时治疗可引发不孕,腹腔镜手术可清除病灶,促进机体排卵,但部分病灶难以完全清除,术后需予以药物治疗,以此降低复发风险,但长期应用单一药物治疗可能会出现围绝经期症状,因而需采用多种药物联合治疗方案。戊酸雌二醇可增强子宫内膜容受性,改善子宫内膜异位症患者围绝经期症状,提升其生活质量[2]。戈舍瑞林属于促性腺激素释放激素,可拮抗雌激素,缓解子宫内膜异位症临床症状,抑制局部病灶部位细胞增生,降低炎性、氧化应激反应水平,改善病灶部位血液动力学[3-4]。目前子宫内膜异位症患者术后联合应用戈舍瑞林、戊酸雌二醇的疗效尚未完全明确,基于此,本研究主要观察其临床疗效,并分析其对患者疼痛程度、性激素、氧化应激水平的影响,为临床治疗提供参考依据。
1 资料与方法
1.1一般资料 选取2019年1月至2021年1月于本院行子宫内膜异位症术患者80例为研究对象,依据术后治疗方案分为单一组40例、联合组40例。
单一组:年龄27~38(32.25±1.75)岁,病程1~5(3.26±0.52)年,体重指数19~24(21.63±0.72)kg/m2。
联合组:年龄27~39(33.01±1.92)岁,病程1~6(3.32±0.61)年,体重指数19~25(21.85±0.85)kg/m2。两组一般资料比较,差异无统计学意义(P>0.05),具有可比性。本研究经本院伦理委员会批准。
1.2纳入与排除标准 纳入标准:符合子宫内膜异位症诊断标准[5];单侧囊肿者;符合腹腔镜手术要求者;首次确诊者;签署知情同意书者。排除标准:合并其他妇科疾病者;自身免疫功能异常者;既往接受子宫、单侧或双侧卵巢切除术者;近半年有性激素使用史者。
1.3方法 子宫内膜异位症手术(腹腔镜手术)由同一个手术小组完成:在月经结束后3~7 d行腹腔镜手术,肚脐上方1 cm处作穿刺口,腹腔镜放入其中,使用探头探查盆腔,切除病灶,使用双极电凝剥离盆腔粘连部分。使用0.9%生理盐水(1 L)反复冲洗盆腔。单一组于术后第2 d口服戊酸雌二醇(浙江仙琚制药股份有限公司,国药准字H20020299,规格:1mg),1mg/d,连续口服21 d后停药7 d(第1个月),然后开始第2、3个月用药,用药方法、剂量同第1个月。联合组予以戈舍瑞林(英国AstraZeneca UK Limited,国药准字HJ20160260,规格:3.6mg/支)+戊酸雌二醇治疗,戊酸雌二醇治疗方法同单一组,同时于术后第1 d注射戈舍瑞林,间隔28 d再次注射1支。两组连续治疗3个月。
1.4观察指标 (1)临床疗效[6]:显效:术后药物维持过程中月经恢复正常,痛经、腹痛等临床症状明显改善;有效:术后药物维持过程中月经恢复正常,痛经、腹痛等临床症状有改善趋势;无效:不符合上述标准。总有效率为显效、有效比例之和。(2)比较两组治疗前、治疗1个月、3个月后性激素水平:分别于治疗前、治疗1个月、3个月后月经周期第2 d采集空腹静脉血6mL,3500r/min离心10min分离血清,采用ELISA法检测血清雌二醇(E2)、卵泡刺激素(FSH)、促黄体生成素(LH)、性激素结合球蛋白(SHBG)水平,广州奥瑞达生物提供检测试剂盒。(3)比较两组治疗前、治疗1个月、3个月后血清学指标:分别于治疗前、治疗1个月、3个月后采集空腹静脉血6mL,相同条件下分离血清待测。采用ELISA法检测血清血管内皮生长因子(VEGF)、胰岛素样生长因子-1(IGF-1)水平,上海酶联生物提供VEGF检测试剂盒,美国R&D公司提供IGF-1检测试剂盒。采用化学发光法检测血清血栓素B2(TXB2)水平,上海科培瑞生物提供检测试剂盒。(4)比较两组治疗前、治疗1个月、3个月后氧化应激水平:采用试剂盒检测血清活性氧簇(ROS)、维生素E(VE)、超氧化物歧化酶(SOD)水平,美国R&D公司提供检测试剂盒。(5)比较两组治疗前、治疗1个月、3个月后视觉模拟评分法(VAS)、Kupperman评分,采用VAS评分评估疼痛程度[7]:总分为10分,分值越高表明疼痛程度越严重。采用Kupperman评分评估临床症状严重程度[8]:包括潮热出汗、泌尿系统刺激、阴道不适、失眠、感觉异常,总分为51分,分值越高表明症状越严重。(6)复发情况:术后随访1年,统计两组复发情况:a、术后症状缓解,但3个月后出现盆腔阳性体征或达到术前水平;b、术后B超复查显示出现新病灶;c、排除其他疾病情况下,血清糖类抗原125(CA125)水平下降后又升高,若满足其中任何一项即可判定为复发。

2 结果
2.1两组临床疗效比较 单一组:显效21例、有效9例、无效10例;联合组:显效24例、有效13例、无效3例。联合组总有效率92.50%(37/40)高于单一组75.00%(30/40)(χ2=4.501,P=0.034)。
2.2两组VAS、Kupperman评分比较 治疗前两组VAS、Kupperman评分比较,差异无统计学意义(P>0.05)。治疗1个月、3个月后两组VAS、Kupperman评分低于治疗前,且联合组低于单一组(P<0.05),见表1。

表1 两组VAS、Kupperman评分比较分)
2.3两组性激素水平比较 治疗前两组性激素水平比较,差异无统计学意义(P>0.05)。治疗1个月、3个月后两组E2、FSH、LH水平低于治疗前,SHBG水平高于治疗前,且联合组改善幅度大于单一组(P<0.05),见表2。
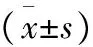
表2 两组性激素水平比较
2.4两组血清学指标比较 治疗前两组血清学指标比较,差异无统计学意义(P>0.05)。治疗1个月、3个月后两组VEGF、IGF-1、TXB2水平低于治疗前,且联合组低于单一组(P<0.05),见表3。
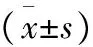
表3 两组血清学指标比较
2.5两组氧化应激水平比较 治疗前两组氧化应激水平比较,差异无统计学意义(P>0.05)。治疗1个月、3个月后联合组ROS水平低于单一组,VE、SOD水平高于单一组(P<0.05),见表4。
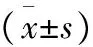
表4 两组氧化应激水平比较
2.6复发情况 随访1年后,联合组失访4例、单一组失访5例。联合组术后复发率8.33%(3/36)低于单一组28.57%(10/35)(χ2=4.860,P=0.027)。
3 讨论
子宫内膜异位症可引起异位内膜腺体反复增殖、坏死,影响卵巢皮质内分泌状态,引起雌激素水平升高,其病因与免疫、遗传、内分泌有关[9]。目前子宫内膜异位症尚缺乏根治手段,临床以去除病灶、减少复发、促进生育为治疗原则,首选治疗方案为腹腔镜手术联合药物治疗。
戊酸雌二醇可改善子宫内膜异位症患者盆腔疼痛程度,缓解围绝经期症状,提高妊娠率[10]。戈舍瑞林可缓解患者疼痛,有效控制雌激素水平,抑制异位内膜增殖、促性腺激素分泌,增强机体抗氧化能力,并可减轻子宫内膜损伤[11]。本研究结果显示,联合组总有效率高于单一组,提示子宫内膜异位症患者术后联合应用戈舍瑞林、戊酸雌二醇可提高临床疗效。戊酸雌二醇可改善子宫内膜异位症临床症状;戈舍瑞林可改善卵巢功能、盆腔微环境,促进盆腔解剖结构恢复正常,其与戊酸雌二醇联合使用可发挥协同作用,提高治疗效果。E2、FSH、LH、SHBG水平变化可反映性激素水平状态,其水平异常表明性腺功能、卵巢可能发育不全、生殖功能减退等[12]。本研究结果显示治疗后联合组E2、FSH、LH水平低于单一组,SHBG水平高于单一组,表明联合治疗对性激素水平的调节作用更佳。分析其原因可能为戊酸雌二醇可调节雌激素、卵巢轴功能,促进女性生殖器官发育;戈舍瑞林可调节机体内分泌,降低促黄体生成激素、雌激素生成量,抑制内膜异位组织生长,并可通过下丘脑垂体,促使异位子宫内膜病灶退化,促进内膜组织修复[13]。
血管生成与子宫内膜异位增生过程有关,VEGF、IGF-1、TXB2属于血管生成相关因子,可为异位子宫内膜提供营养,促进子宫内膜异位症病情进展[14]。本研究结果显示,治疗后联合组VEGF、IGF-1、TXB2水平低于单一组,提示联合治疗可降低血清VEGF、IGF-1、TXB2水平,进一步抑制子宫内膜异位症新生血管形成。这可能与戈舍瑞林抑制血管新生相关信号通路有关,可促进炎性反应物质代谢,改善局部血管收缩、舒张,减轻病灶部位炎性反应,加之戊酸雌二醇可促进相关激素水平恢复,进而形成良性循环,有助于防止术后复发。氧化应激与子宫内膜异位症发生发展密切相关,ROS属于有氧代谢产物,其水平升高致使细胞氧化损伤;VE属于非酶类抗氧化物,可促使机体免受自由基损害;SOD属于酶类抗氧化物,可抑制氧自由基对细胞的损害[15]。本研究结果显示,治疗后联合组ROS水平低于单一组,VE、SOD水平高于单一组,表明联合治疗可降低机体氧化应激水平,可能为其发挥治疗作用的机制之一。分析其原因可能为戈舍瑞林可改变子宫内膜基质细胞,直接侵袭异位病灶细胞,促进细胞外基质降解,改变血管内皮通透性,降低巨噬细胞活性,致使异位内膜细胞逃脱免疫监视,进一步发挥抗氧化作用。同时本研究发现联合治疗后VAS、Kupperman评分降低,并可降低复发率,提示联合治疗可减轻病情严重程度、疼痛程度,减少复发情况发生。
综上所述,子宫内膜异位症患者术后采取戈舍瑞林联合戊酸雌二醇治疗方案,可提高临床疗效,快速缓解其临床症状,减轻疼痛程度,降低性激素水平,抑制新生血管形成,改善氧化应激状态。

