Ni/γ-Al2O3 催化剂的2-MF 气相加氢合成2-MTHF 性能研究
方姿予, 张 炜, 谈立美, 种思颖, 张雅静, 王康军
(沈阳化工大学 化学工程学院, 辽宁 沈阳 110142)
随着化石资源日益枯竭, 生物质合成化学品和燃料受到广泛关注.2-甲基四氢呋喃(2-MTHF)是一种生物质衍生物, 可作生物燃料、 溶剂和化学中间体[1].作为生物燃料, 2-MTHF 可单独使用, 也可与其他燃料混合使用, 其能量密度略低于汽油, 但比重高于汽油, 等体积下能达到和汽油相似的里程[2].更重要的是, 2-MTHF 与汽油可以在任意比下互溶,在汽油中的体积混合比例可超过60%都不会影响发动机性能, 无腐蚀性, 能在现有燃烧设施中直接应用, 极具市场潜力[3].2-MTHF 沸点适中(80.2 ℃), 疏水(20 ℃, 14 g/100 g H2O), 具有较强的路易斯碱性,在格氏、 锂化、 偶联以及两相反应中作溶剂, 产物选择性高, 且其无遗传毒性、 无致突变性, 是新型环保溶剂[4-5].近年来, 2-MTHF 市场供不应求, 价格居高不下, 开发绿色低成本生产路线非常必要.2-MTHF 主要合成路线包括乙酰丙酸法、 内酯法、 糠醛法[6].其中, 糠醛法因其原料成本低、 来源广泛的优势受到研究者关注.
以糠醛(FUR)为原料加氢制备2-MTHF 有一步法和两步法两种路线.一步法即FUR 在一个反应器或者两段反应器中加氢合成2-MTHF, Dong 等[7]采用铜钯双固体催化剂使糠醛在常压下一步转化得2-MTHF, 收率97.1%, 该方法避免了高压、 减少了产物分离成本.两步法是指两个反应器中步完成两个过程: (1) FUR 在Cu-Cr 或者Cu/SiO2催化剂上转化为中间品2-甲基呋喃(2-MF)/糠醇(FFA); (2) 2-MF/FFA 在其他催化剂上转化为2-MTHF.其中, 两步法中经2-MF 转化为2-MTHF 为常用生产路线.目前, 工业上2-MF 转化为2-MTHF 采用液相加氢工艺, Pd 或Ni 作为催化剂.Pd 催化剂对于呋喃环上C=C 双键加氢性能优于Ni 催化剂, 但催化剂成本高.李增杰等[8]采用液相加氢工艺, 考察了2-MF在Ni/Al2O3催化剂上生成2-MTHF 的性能, 在3 MPa、 150 ℃下, 25% NiO 负载量催化剂上, 2-MF 转化率为99.4%, 2-MTHF 的选择性为97.1%,连续使用8 次, 性能稳定, 具备工业化前景.液相加氢工艺条件由于较高的反应压力和温度对设备要求较高, 且固体催化剂在溶剂中呈浆状, 使用后催化剂分离困难[9].相比之下, 2-MF 气相加氢转化为2-MTHF 工艺能克服上述问题.Biswas 等[10]研究了贵金属及碱金属催化剂Ba/Cu/Cr、 Cu/Cr/Ni/Zn/Fe、Cu-Ru/C、 Pt/C 和Pd/C上2-MF 加氢性能, 结果表明在反应温度较低为125 ℃时, Pd/C 催化剂对生成2-MTHF 具有较好的催化活性, 收率达98%; 而其他4 种催化剂对呋喃的开环反应均具有较高的活性, 反应的主要产物为2-戊酮, 而在较高反应温度250 ℃下, 所有催化剂催化加氢得到的主要产品均为2-戊酮.林涛等[11]研究了Pd/C、 Pt/C 和Ru/C 贵金属催化剂催化2-MF 加氢气固相反应性能, 在反应温度为100 ℃、 反应压力为3.0 MPa, 质量空速为0.48 h-1及和H2与2-MF 的物质的量比为20∶1的条件下, Pd/C 活性高、 稳定性好, 稳定运行100 h,2-MTHF 收率在99.9%, 而Pt/C、 Ru/C 催化剂活性随着时间增长逐渐下降, 原因是表面活性位被覆盖造成的.Ding 等[12]采用溶胶-凝胶法制备了Ni/SiO2催化剂, 在反应温度为180 ℃、 反应压力为1.6 MPa及H2/2-MF 摩尔比为10.7 反应条件下, 当Ni 负载量为25%时, 2-MF 的转化率达98.0%, 2-MTHF 选择性达86.8%, 催化剂稳定性不足, 反应8 h 内转化率逐渐降低.王英文等[13]采用蒸氨法制备了Ni/SiO2催化剂, 反应温度160 ℃, 压力1.6 MPa, LHSV(每克催化剂每小时处理2-MF 的质量)为1.6 h-1, 2-MTHF 收率为95.3%, 反应15 h 后催化性能开始降低.除了活性组分、 制备方法、 反应条件, 催化剂的载体性质特别是表面酸性也会影响催化性能.催化剂中的酸性位, 特别是路易斯酸性位具有亲电性, 易与2-MF 中的O 原子键合, 促进反应物在催化剂表面吸附[14].Liu 等[15]研究了1 MPa、 180 ℃, Ni/SiO2、Ni/Al2O3和Ni/CeO2催化剂上2-MF 加氢生成2-MTHF 的反应性能, 研究结果表明2-MF 气相加氢制2-MTHF 反应中需提供适量的酸性来提高反应性能, Ni/Al2O3催化剂上2-MF 的转化率较低(81.3%), Ni/CeO2催化剂上2-MTHF 的选择性较低(75.3%), Ni/SiO2催化剂性能最佳.γ-Al2O3是一种亚稳晶体形式, 具有较高表面积、 一定的孔容, 成本较低且来源广泛, 常用作催化剂载体, 与SiO2载体不同,γ-Al2O3表面具有路易斯酸性(Al3+离子)和Brønsted (OH-离子)位点, 以及路易斯碱性位点(O2-离子)[16].因此, 本研究制备了Ni/γ-Al2O3催化剂, 考察Ni 含量、焙烧温度和反应条件对2-MF 气相加氢制2-MTHF 的性能的影响规律, 并优化了反应条件,考察了催化剂的稳定性.15% Ni/Al2O3-400 在100~120 ℃、压力在1.6 或2 MPa、WHSV=2.7 h-1、H2/2-MF=6.4 的条件下, 催化上2-MTHF 的收率均在97%以上, 催化剂能稳定运行40 h, 高于目前文献报道2-MF 在Ni 基催化剂上气相加氢制备2-MTHF的性能.
1 实验部分
1.1 催化剂的制备
采用等体积浸渍法制备Ni/γ-Al2O3催化剂.将氧化铝(国药集团)破碎至粒径0.900~0.450 mm,500 ℃焙烧4 h 后进行浸渍.将六水合硝酸镍(国药集团)加入去离子水中, 搅拌至完全溶解, 缓慢加入需要质量载体, 搅拌均匀, 浸渍12 h, 接下来在120 ℃干燥12 h 后于马弗炉中焙烧4 h.分别制备了NiO质量分数为5%、10%、15%、20%的NiO/γ-Al2O3催化剂(命名为x% Ni/Al2O3-y,x%表示NiO 质量分数,y代表焙烧温度).
1.2 催化剂结构表征
采用康塔Autosorb-iQ-C 型全自动物理化学吸附仪进行比表面积和孔结构测定.测试前将催化剂在300 ℃真空脱气处理3 h, 在-196 ℃液氮温度下等温吸附脱附.粉末X 射线衍射(XRD)在布鲁克D8 Advance X 射线衍射仪上进行, Cu 靶Kα 线, 管电压为40 kV, 管电流为40 mA, 扫描范围10°~80°.采用康塔ChemBET Pulsar TPR/TPD 自动化学吸附仪进行氢气程序升温还原(H2-TPR)测试.0.05 g 催化剂装入U 型管中, 在He 气氛下于400 ℃处理30 min, 冷却至50 ℃, 通入10% H2-N2标准混合气, 以10 ℃/min 的速率升温至900 ℃, 用热导检测器(TCD)记录信号.采用上述相同设备进行氨气程序升温脱附(NH3-TPD)测试.0.2 g 催化剂装入U 型管中, 在He 气氛下于550 ℃处理30 min, 温度降至50 ℃, 通入NH3/Ar 吸附1 h, He 吹扫1 h, 最后升温至550 ℃, 用热导检测器记录信号.采用X 射线光电子能谱(XPS, ThermoES CaLAB 250 Al 靶)表征催化剂的表面化学状态.采用日本日立公司H-7650 型透射电子显微镜(TEM), 通过超声波分散乙醇中的催化剂悬浮液滴在铜网上, 晾干后进行观察和拍照.通过H2脉冲吸附法进行催化剂的H2化学吸附, Ni 分散基于H∶Nisurface=1∶1 的化学计量计算, 每个镍原子表面积为6.5×10-20m2, 计算金属表面积和镍分散度[17].
1.3 催化剂的活性评价
在固定床反应装置上进行Ni/γ-Al2O3催化剂性能评价.将焙烧后催化剂在15 MPa 压片, 破碎过筛,取粒径0.900~0.450 mm 颗粒1 g, 装入反应管中部,两端以石英砂填料固定.通入氢氮混合气(N2/H2=4), 以5 ℃/min 速率升温至600 ℃, 还原4 h.2-MF由高压微量进样泵进样, H2流量由质量流量计控制.在100 ℃、1.6 MPa、WHSV=2.7 h-1、H2/2-MF=6.4的条件下进行催化加氢反应.采用SP-3420A 气相色谱对产物进行定量分析.KB-1 色谱柱, 柱温程序升温, 范围为50~250 ℃, 进样器为250 ℃, FID 检测器为270 ℃.通过面积修正归一化法进行定量分析.
2 结果与讨论
2.1 催化剂的性能评价
Ni/γ-Al2O3催化剂的2-MF 气相加氢性能在高压固定床管式反应器进行.在1.6 MPa, 100 ℃, Ni/γ-Al2O3催化剂的2-MF 气相加氢性能见表1.2-MF在Ni/γ-Al2O3催化剂作用下加氢, 呋喃环上C=C键加氢生成主要产物为2-MTHF, 呋喃环上C—O键断裂再加氢会生成副产物2-戊酮(2-PN)、2-戊醇(2-PL)、戊醇(1-PL).根据文献, 产物2-MTHF 中C—O 键按照路线1 断裂, 会生成副产物1-PL; 按照路线2 断裂, 会相继生成2-PN 和2-PL[18].由图1、表1 可知, 产物中2-PL 的选择性均高于1-PL, 表明C—O 键主要按照路线2 断裂, 这是因为线路2 中C—O 比路线1 中C—O 断裂需要较小的能量势垒,因此2-PL 选择性高[19].反应过程中2-PN 的选择性较小, 表明由2-PN 加氢变成2-PL 反应速率较快.反应中, 不同分子在一定条件下还会缩合、 加氢或分子间重排生成较高碳数分子(C10以上)副产物,包含2-(四氢糠氧基)四氢吡喃、 2-(12-十四炔氧基)四氢吡喃、 2-(糠氧基)四氢吡喃等.

图1 2-MF 加氢生成2-MTHF 的反应途径[17]Fig.1 Reaction pathway of hydrogenation of 2-MF to 2-MTHF[17]

表1 催化剂的2-MF 加氢反应性能aTable 1 2-MF Hydrogenation performance of catalystsa
由表1 数据可见, 500 ℃焙烧制备的Ni/γ-Al2O3催化剂, 随着Ni 负载量的增大, 2-MF 的转化率呈现先增大后减小的趋势, 2-MTHF 的选择性逐渐降低.其中, 5%Ni/Al2O3-500 催化剂上2-MF 的转化率只有50.5%, 但是选择性可达97.5%, 这表明反应活性位较少时催化剂活性不高, 加氢能力较弱, 这种情况下2-MF 转化率较低[20].20%Ni/Al2O3-500 催化剂上的2-MF 转化率、2-MTHF 选择性均低于15%Ni/Al2O3-500 催化剂, 可能是因为较大Ni 负载量会导致Ni 分散性变差、Ni 颗粒尺寸增大, 从而降低催化活性[21].焙烧温度同样影响催化剂性能,15%Ni/γ-Al2O3催化剂在300、400 ℃焙烧, 催化剂的活性较高, 2-MF 转化率均达到99.8%; 升高焙烧温度, 2-MF 转化率逐渐下降.与我们报道的溶胶-凝胶和蒸氨法制备的Ni/SiO2催化剂相比[12-13], Ni/γ-Al2O3对于2-MF 加氢活性高且2-MTHF 选择性高,性能有较大提升, 这可能与载体性质有关, 将结合催化剂结构表征结果进行讨论.
2.2 催化剂的表征
2.2.1 Ni/γ-Al2O3催化剂的物相
γ-Al2O3载体、焙烧和还原后催化剂的XRD 谱图见图2.在焙烧后催化的XRD 谱图中, 2θ=37.4°、45.5°和67.3°处的衍射峰归因于γ-Al2O3的衍射峰,2θ=43.3°和62.9°处的衍射峰归因于NiO[22].在还原后催化剂的XRD 谱图中, 2θ=44.6°、51.5°和76.6°处的衍射峰归因于Ni 的衍射峰[23], 分别对应Ni 的(111)、(200)和(220) 晶面(JCPDS, 04-0850), 这是NiO 还原后生成Ni.催化剂中也可能存在未还原NiO, 其在2θ=37.2°和43.3°的衍射峰与γ-Al2O3的色散峰重叠, 从而在XRD 上无法确认NiO 是否完全还原为Ni.Ni 负载量由5%变化到20%, 还原后催化剂中Ni 的衍射峰强度逐渐增大, 表明Ni 的晶粒尺寸在增大.图2(b)中, 10%Ni/γ-Al2O3-500 催化剂的Ni 衍射峰比其他催化剂上要尖锐, 可能是NiO 的衍射峰与γ-Al2O3色散叠加所致.根据谢乐公式计算Ni 晶粒尺寸.15%Ni 负载量的催化剂, 焙烧温度越高, 还原后催化剂中Ni 的衍射峰强度越高, 峰形越尖锐, 在600 ℃焙烧的催化剂,γ-Al2O3衍射峰强度也上升, 表明焙烧温度升高会导致晶粒尺寸增大.文献中报道NiO 较容易与γ-Al2O3发生固相反应, 生成NiAl2O4尖晶石相[24], 但从XRD 谱图中, 很难确定是否存在NiAl2O4尖晶石相, 这归因于两个方面: 一方面, NiAl2O4的衍射峰与γ-Al2O3峰位置因重叠难以区分; 另一方面, 即使生成NiAl2O4相, 如果NiAl2O4含量较低, XRD 也无法检测到, 还需要进一步借助其它表征来确定.15%Ni/γ-Al2O3-300 和15%Ni/γ-Al2O3-400 催化剂上Ni 晶粒尺寸较小, Ni 金属面积最大[25], 这可能其催化活性较高的原因之一.
图3 为还原后不同负载量的Ni/γ-Al2O3催化剂的TEM 图.从图3 中观察到, 还原后Ni 颗粒分布均匀, Ni 颗粒尺寸随着Ni 负载量的增加而增大, Ni负载量为10%和15%的催化剂中Ni 颗粒尺寸接近,为8 nm 左右; Ni 负载量为20%的催化剂Ni 颗粒尺寸明显变大, 尺寸较多集中在12 nm 左右.在还原后的催化剂HRTEM 图像中晶格间距为0.20 nm的条纹像对应Ni (111)晶面.同时还发现NiO 的条纹像, 这可能有两个原因, 一个是NiO 与γ-Al2O3载体相互作用较强难以还原, 二是在样品测试中Ni 重新被氧化变成NiO.TEM 的表征结果表明: Ni 负载量较高会导致Ni 颗粒聚集从而颗粒尺寸较大[26-27].
图4 为催化剂Ni 2p3/2XPS 谱图, 峰拟合结果总结于表2 中.结合能在851 eV 左右的峰对应Ni0的特征峰, 结合能在854.5 eV 左右的峰对应NiO中Ni2+的特征峰, 860.1 eV 左右的峰为Ni2+的卫星峰[28].15%Ni/Al2O3-300、15%Ni/Al2O3-400 与15%-Ni/Al2O3-600 催化剂中Ni2+的特征峰逐渐向高结合能方向移动, 这可能有两种归因: 一是高温焙烧的催化剂表面存在少量NiAl2O4, 在还原过程中NiAl2O4相没有被还原成Ni, 文献报道NiAl2O4中Ni2+的 2p3/2的特征峰在856.2 eV; 二是催化剂的Ni 物种和载体之间的相互作用增强[29].

图4 Ni/γ-Al2O3 催化剂还原后XPS 图Fig.4 XPS Diagram of Ni/γ-Al2O3 catalysts after reduction

表2 N/iγ-Al2O3 催化剂还原状态XPS 数据Table 2 XPS Data of reduction state of Ni/γ-Al2O3 catalysts
表2 总结了各个催化剂的表面元素组成.可以看出, 20%Ni/Al2O3-500 和15%Ni/Al2O3-600 催化剂中可能存在较多NiAl2O4物种.文献报道, 在450 ℃煅烧的Ni/Al2O3催化剂中的所有表面Ni 都形成NiAl2O4物种, 直到单层饱和完成, 超过该阈值覆盖范围, 过量的Ni 原子开始在镍-氧化铝界面上形成NiO 物种[30], 使催化剂活性降低.为了进一步明确催化剂表面Ni 活性位情况, 采用H2脉冲法表征催化剂Ni 的分散度及Ni 金属面积, 结果见表3.结果表明在300、400 ℃焙烧, 负载量为15%的催化剂具有较大的Ni 金属面积, 这是其性能良好的原因;600 ℃焙烧的负载量为15%的催化剂Ni 金属面积小.结合表1 催化剂性能, 可以看出催化剂的活性与Ni 的金属面积相关, Ni 金属面积越大, 催化剂活性越高.

表3 Ni/γ-Al2O3 催化剂的织构性质Table 3 Textural properties of Ni/γ-Al2O3 catalysts
2.2.2 Ni/γ-Al2O3催化剂的比表面积、 孔径和孔容
采用BJH 法分析平均孔径结果见表3, 催化剂孔径均主要集中分布在5~7 nm 范围之间, 表明催化剂均具有介孔结构[31].从表3 中可以看到, 随着催化中Ni 负载量的增加, Ni/γ-Al2O3催化剂的比表面积和孔容呈逐渐减小的趋势.比表面积下降可能是由于载体γ-Al2O3中的孔隙填充了Ni 物种, 堵塞了孔道, 从而降低比表面积和孔体积.Ni 负载量越大,覆盖载体表面越多, 比表面积和孔容下降是合理的[8].催化剂的比表面积随着焙烧温度的升高而减小, 可能是由于氧化铝载体的一些小孔隙的破坏所致[32].15%Ni/Al2O3-400 催化剂BJH 平均孔径最大.孔径大, 有利于反应物和产物扩散, 减少内扩散过程对反应的影响, 进而减少一些副反应发生, 这可能是该催化剂上2-MTHF 选择性能较好的原因之一.
2.2.3 Ni/γ-Al2O3催化剂的H2-TPR
不同催化剂的 H2-TPR 见图5, 分峰结果总结在表4 中.Ni/γ-Al2O3催化剂在400~800 ℃的范围内存在3 个明显的还原峰.研究表明, 400~500 ℃左右的还原峰(α峰)归因于与Al2O3载体相互作用较弱的NiO 颗粒或者是分散较好的小的NiO 颗粒的还原; 500~600 ℃左右的还原峰(β峰)归因于与Al2O3载体相互作用较强的NiO 颗粒或者是较大的NiO 颗粒的还原[33]; 在600~800 ℃左右的还原峰(γ峰)可能是催化剂中少量的 NiAl2O4的还原峰.随着Ni 负载量的增加,α峰的峰顶温度向较低的温度移动, 表明较高的金属负载诱导了具有较弱金属-载体相互作用的分散NiO 物种的形成[34].随着焙烧温度升高, 还原峰位置逐渐向高温移动, 这归因于NiO 晶粒尺寸变大/金属-载体相互作用增强, 这与XRD 表征结果一致.15%Ni/Al2O3-600 催化剂上γ峰比例最大, 这是在高温焙烧条件下Ni2+进入Al2O3表面的四面体或八面体空位, 形成NiAl2O4尖晶石物种, 而NiAl2O4比NiO 难以还原, 所以高温还原峰位向高温偏移.形成NiAl2O4尖晶石物种,Ni 会向着催化剂体相内扩散, 导致载体表面Ni 物种的减少, 从而导致催化剂反应活性降低[35-36].

图5 Ni/γ-Al2O3 催化剂的H2-TPR 图Fig.5 H2-TPR Profiles of Ni/γ-Al2O3 catalysts

表4 催化剂还原峰温度及峰面积分布Table 4 Reduction temperature and peak area distribution of different catalysts
2.2.4 Ni/γ-Al2O3催化剂的NH3-TPD
采用NH3-TPD 表征方法测定催化剂表面酸位点的数量和强度.Ni/γ-Al2O3催化剂的NH3-TPD 见图6.如图所示, 各催化剂均在160 ℃左右出现第一个明显的NH3脱附峰, 归属于催化剂表面弱酸中心;在 500~750 ℃出现第二个NH3脱附峰, 表明催化剂表面存在强酸中心.可以看出, 载体γ-Al2O3只有弱酸中心, 随着负载Ni 量逐渐增大, 催化剂的弱酸性中心逐渐向低温方向发生偏移, 表明催化剂的弱酸中心强度减弱, 这可能是金属Ni 组分覆盖、阻断、调和Al2O3载体上的酸性位所致[37].对NH3-TPD 曲线进行面积积分, 得到催化剂表面酸量与不同表面酸性中心的比例, 结果见表5.焙烧温度升高, 还原后催化剂的弱酸中心和强酸中心都向低温移动, 表明表面酸性强度降低, 这是焙烧温度的升高导致催化剂脱水程度的提高, Al2O3发生了二羟基化反应,消除了Brønsted 酸位, 酸度逐渐降低[38].15%Ni/Al2O3-400 催化剂总酸量较大, 酸性强度适中, 在加氢反应中, 适当数量的酸位有利于吸附和活化具有吸电子基团的反应物, 存在适量酸性位特别是与金属Ni 活性位位置邻近的酸性位, 会因Ni 与酸性位的协同作用提高催化剂的活性[39].

图6 Ni/γ-Al2O3 催化剂的NH3-TPD 图Fig.6 NH3-TPD Curves of Ni/γ-Al2O3 catalysts
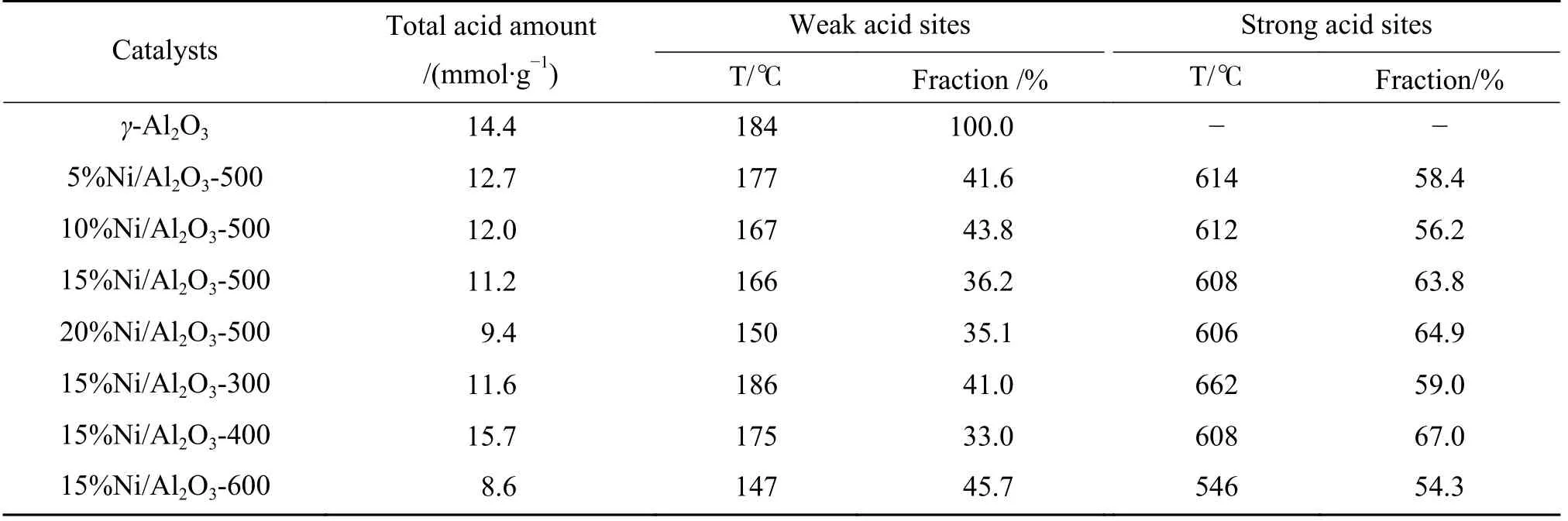
表5 NH3 脱附峰温度及峰面积分布Table 5 NH3 Desorption peak temperature and peak area distribution
2.2.5 反应条件对Ni/γ-Al2O3催化剂性能的影响
由表6 可见, 1.6 MPa、70 ℃, 15%Ni/Al2O3-400催化剂上2-MF 转化率只有91.2%, 随着反应温度的升高, 2-MF 的转化率增大, 2-MTHF 的选择性先增后减, 副产物2-PL 的选择性随着反应上升而增大, 这表明温度是影响2-MTHF 开环生成副产物的主要因素.反应温度为100 ℃, 在压力为0.8~2 MPa下, 催化剂活性都很高, 2-MF 转化率大于99%; 压力在0.4 MPa, 催化剂活性受到明显影响, 2-MF 转化率不足50%.一般来说, 在加氢过程中, 较高的压力有利于高反应速率也有利于化学平衡.在本研究中, 2-MF 的转化率随压力的增加而增加, 2-MTHF的选择性略增, 表明压力对催化剂的活性影响较大,对选择性影响小.压力为2.0 MPa, 温度100 ℃时,15%Ni/Al2O3-400 的催化性能最优, 2-MF 转化率为99.8%, 2-MTHF 选择性为98.0%.反应在100~120 ℃,压力在1.6~2.0 MPa, 催化上2-MTHF 的选择性均在97%以上, 表明催化剂性能良好.与文献中蒸氨法制备的Ni/SiO2催化剂相比[13], 浸渍法制备的Ni/Al2O3催化剂活性高, 最佳反应温度相对低, 避免高温导致C—O 键断裂生成副产物[40-41], 提高了2-MTHF 的选择性, 这可能与载体表面酸性有关,Al2O3作为载体酸量较多.

表6 不同反应条件下2-MF 加氢反应性能aTable 6 Hydrogenation performance of 2-MF under different reaction conditionsa
2.2.6 Ni/γ-Al2O3催化剂的稳定性
在2 MPa、100 ℃、WHSV=2.7 h-1、H2/2-MF=6.4 条件下, 对15%Ni/Al2O3-400 催化剂进行40 h活性评价, 结果见图7.催化剂可以稳定连续反应40 h,2-MF 转化率大于99.0%, 2-MTHF 的选择性高于98.0%, 说明催化剂的稳定性较好, 比本实验组前期研究的Ni/SiO2催化剂性能、稳定性都明显提高[13].制备不同批次催化剂进行考察, 仍得到较好的催化性能, 重复性良好.

图7 15%Ni/Al2O3-400 催化剂的稳定性Fig.7 Stability test of 15%Ni/Al2O3-400
3 结论
采用浸渍法制备了Ni/γ-Al2O3催化剂, 用于2-MF 气相加氢合成2-MTHF 反应.研究结果表明, 随着催化剂 Ni 负载量的增加, 2-MF 的转化率先增加后减小, 这与Ni 金属分散度、面积、晶粒尺寸有关,Ni 金属分散度及面积越大、 晶粒尺寸越小, 催化剂活性越高.焙烧温度升高, 催化剂Ni 金属面积减小、晶粒尺寸增大, 酸性减弱.催化剂的孔结构、酸性和反应温度是影响2-MTHF 选择性的主要原因, 平均孔径大有利于减少内扩散的影响从而抑制副反应,提高2-MTHF 选择性; 总酸量较大, 酸性强度适中,适当的负载量与焙烧温度会因Ni 与酸性位的协同作用提高催化剂的活性; 反应温度上升导致呋喃环C—O 断裂再加氢生成2-PL 和1-PL, 降低2-MTHF选择性.结果表明, 在反应温度100~120 ℃, 反应压力1.6~2 MPa 时, 15%Ni/Al2O3-400 的催化性能最优, 2-MTHF 的收率均在97%以上, 催化剂活性可稳定40 h.未来研究应改进Ni/γ-Al2O3制备工艺, 提高Ni 金属面积, 优化孔结构, 调控酸性, 将提升Ni/γ-Al2O3催化剂工业应用潜力.

