山东省临沭县鸭疫里默氏杆菌分离鉴定及生物特性分析
杨希川
(临沭县动物疫病预防控制中心,山东临沭 276700)
鸭疫里默氏杆菌病是一种由鸭疫里默氏杆菌(Riemerellaanatipestifer,RA)感染水禽(鸭、鹅等)和鸟类引起的细菌性传染病,广泛流行于世界各地,发病率和死亡率均较高。卫生条件差、营养不良、环境突变等引起的应激反应常导致易感动物感染RA。被RA 感染的动物常表现流鼻涕、咳嗽、鼻窦炎、腹泻和神经症状,病死动物以纤维素性心包炎、脑膜炎、肝周炎、卵管炎和气囊炎为主要病理特征。RA 血清型较多,目前世界上已至少发现21 种[1],国内至少流行13 种[2]。由于不同血清型之间缺乏交叉保护,疫苗保护效力有限,抗生素仍然是治疗RA 感染的常用方法。然而,由于抗生素滥用导致RA 耐药性加剧,加之临床上RA 常与其他病原微生物混合感染,均给鸭疫里默氏杆菌病治疗增加了难度。
近年来,山东省临沭县某些鸭鹅养殖场户鸭疫里默氏杆菌病频发,造成一定经济损失。2023年5—6 月,从临沭县8 家鸭鹅养殖场户采集疑似鸭疫里默氏杆菌病病死动物的心血、脑和肝脏等组织样本,进行RA 分离鉴定和血清型分型,并对RA 耐药性及致病性进行了评估,以期为鸭疫里默氏杆菌病治疗和防控提供参考。
1 材料与方法
1.1 病料与试验动物
从山东省临沭县8 家鸭鹅养殖场户采集疑似感染RA 的病死鸭鹅心血、脑和肝脏等组织病料,每只动物病料计为1 份,共40 份。未免疫7 日龄健康雏鸭20 只,购自临沭县金兴养鸭专业合作社。
1.2 主要试剂和质控菌株
胰酪大豆胨液体培养基(TSB)、巧克力琼脂培养基、麦康凯培养基(MAC),购自青岛海博生物技术有限公司;抗菌药物药敏纸片(共16 种)、微量生化鉴定管,购自杭州微生物试剂有限公司;新生犊牛血清,购自江苏科晶生物科技有限公司;Goldview 核酸染料、革兰氏染液,购自北京万佳首化生物科技有限公司;DL 2 000 DNA Marker,2×TaqPCR Master Mix,TIANamp Bacteria DNA kit、DNA 胶回收试剂盒,购自天根生化科技(北京)有限公司;RA 1~13、16 血清型阳性血清,购自中国农业科学院哈尔滨兽医研究所;质控菌株大肠埃希菌(CMCC(B)44102),购自中国兽医药品监察所。
1.3 引物设计与合成
参考文献[3] 设计16S rRNA 基因通用引物: 上游引物27F:5'-AGAGTTTGATCATGGCTCAG-3'; 下游引物1492R:5'-TACGGTTACCTTGTTACGACTT-3'。扩增产物长度约1 450 bp,引物由生工生物工程(上海)股份有限公司合成。
1.4 分离培养
将病料无菌划线接种于巧克力琼脂培养基,37 ℃培养24 h;挑取边缘整齐、半透明、表面光滑湿润的露滴状菌落分别接种于巧克力琼脂培养基和MAC,置于37 ℃、5% CO2恒温培养箱中培养24~48 h,观察菌落形态;选取单个菌落接种于TSB(含5%新生犊牛血清),取纯培养菌液进行革兰氏染色,利用生物学显微镜观察,记录菌体形态、染色特性。
1.5 生化鉴定
参照《常见细菌系统鉴定手册》[4],挑取纯化培养的分离菌接种于生化鉴定管,置于37 ℃、5%CO2恒温培养箱中培养24~48 h,对照手册判定生化特性。
1.6 PCR 鉴定
吸取纯培养液1~5 mL, 采用TIANamp Bacteria DNA kit 提取总DNA,使用16S rRNA 基因通用引物进行PCR 鉴定。PCR 反应体系(25.0 μL):2×TaqPCR Master Mix 12.5 μL,上、下游引物(10 μmol/L)各1.0 μL,菌液2.0 μL,ddH2O 补至总反应体积25.0 μL。PCR 反应条件:95 ℃ 8 min;93 ℃ 25 s,54 ℃ 40 s,72 ℃ 50 s,共37 个循环;72 ℃ 10 min。将PCR 产物胶回收后,送至生工生物工程(上海)股份有限公司测序。利用BLAST 软件与NCBI 公布的15 株RA 参考菌株进行同源性比对,并用MegAlign 绘制系统发育进化树。
1.7 血清型分型
参考文献[5]方法,采用玻片凝集法进行RA血清分型。同时设各血清型阳性菌株为阳性对照,以PBS 和大肠杆菌为空白对照和阴性对照。3 min内RA 凝集抗原与相应血清型血清出现颗粒状凝集者判为阳性,否则判为阴性。
1.8 药敏试验
参照美国临床和实验室标准化协会(CLSI)推荐的K-B 法进行16 种抗菌药敏感性检测。以大肠埃希菌CMCC(B)44102 为质控菌株,按照CLSI—2017 年版标准判断抗菌药敏感、中介和耐药。
1.9 动物回归试验
随机选取1、2、11 血清型RA 各1 株,接种于含有5%犊牛血清的TSB 液体培养基中进行增菌培养。取培养好的菌液进行10 倍倍比稀释,每个稀释度菌液各取100 μL均匀涂布于绵羊血平板,37 ℃厌氧培养24 h 后进行活菌计数,计算菌液浓度,配制浓度为1×109CFU/mL 的菌液作为RA 攻毒菌液。将20 只未免疫7 日龄健康雏鸭随机分为1 个对照组和3 个试验组,5 只/组。试验组雏鸭分别腿部肌肉注射1、2、11 血清型RA 菌液,0.5 mL/只,对照组注射等量生理盐水。注射完毕后分组饲养,连续7 d 每日观察雏鸭发病情况。
2 结果
2.1 分离培养
将病料分别接种于巧克力琼脂培养基和MAC,结果有12 份病料在巧克力琼脂培养基表面出现边缘整齐、半透明、表面光滑湿润的露滴状菌落(图1-A),而MAC 未见菌落生长。革兰氏染色镜检,可见两端钝圆、单个或成对排列的革兰阴性短小杆菌(图1-B)。

图1 分离菌株菌落形态及革兰氏染色镜检结果
2.2 生化鉴定
将12 株纯培养分离菌分别接种于微量生化鉴定管。结果(表1)显示,所有分离菌生化反应结果均与RA 一致。结合培养特性、菌体形态和生化反应结果,初步判定12 株分离菌均为RA,分别命名为LS-RA01~12。

表1 分离菌生化鉴定结果
2.3 PCR 鉴定
随机选取5 株分离菌进行PCR 扩增。结果(图2)显示,均获得长度约为1 450 bp 的PCR 扩增产物。将分离菌株16S rRNA 基因测序结果与NCBI数据库公布的15 株RA 参考菌株进行核苷酸同源性比对,发现核苷酸同源性达98.6%~99.9%。系统进化树(图3)显示,5 株分离菌株与15 株RA 参考菌株亲缘性较近,其中,LS-RA02、LS-RA011与LS-RA05 株亲缘性相近,LS-RA07 与LS-RA08株亲缘性相近。结合分离菌的培养特性、生化试验特性及16S rRNA 基因测序结果,证实这5 株分离菌均为RA。
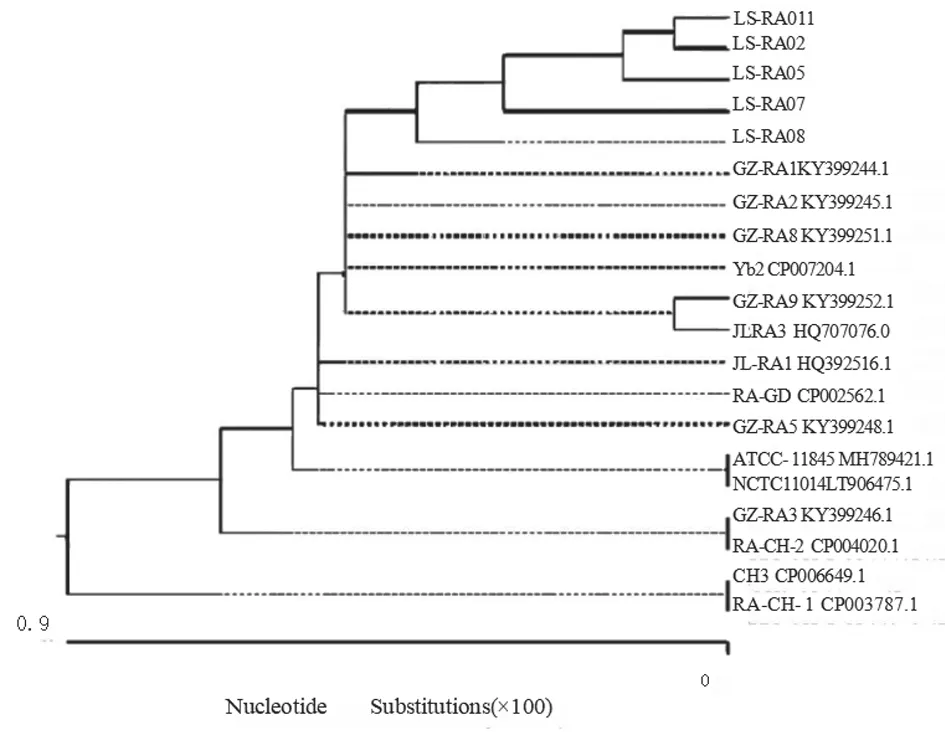
图3 系统进化树
2.4 血清型鉴定
采用玻片凝集法对12 株分离菌进行血清型分型。 结果显示:LS-RA01~05、LS-RA08、LS-RA09 为血清1 型, 共7 株;LS-RA06、LSRA07 为血清2 型,共2 株;LS-RA10~12 为血清11 型,共3 株。
2.5 药敏试验
采用K-B 纸片扩散法对12 株RA 进行药敏试验。结果(表2)显示,所有菌株均对丁胺卡那、庆大霉素、新霉素和阿莫西林耐药,对头孢他啶、头孢曲松、头孢氨苄敏感;对复方新诺明、氨苄西林、氟苯尼考、四环素、多西环素、恩诺沙星、诺氟沙星、阿米卡星、红霉素的耐药率为25.00%~58.33%。

表2 药敏试验结果
2.6 动物回归试验
攻毒8 h 后,3 个试验组雏鸭均表现精神萎靡、缩颈、不愿走动、食欲减退;24 h 后,均出现神经症状、眼鼻分泌物增多、腹泻,其中血清2 型试验组有1 只雏鸭死亡;48 h 后,血清1 型、2 型、11型试验组分别有2、4、2 只雏鸭死亡,死亡率为40%(8/20),56 h 后,3 个试验组所有雏鸭均死亡。对照组雏鸭未见发病。剖检(图4)可见:病死雏鸭心包膜增厚、出血,表面附着纤维素性渗出物;肝脏肿大、质脆、散在分布点状结节和纤维素性薄膜、肝周炎;脑膜水肿增厚、充血。临床症状及病理变化与临床发病鸭一致。

图4 对照组和试验组雏鸭临床症状及病理变化
3 讨论
RA 是一种有荚膜、不形成芽孢、无内孔、不能运动的革兰氏阴性杆状细菌,属于黄杆菌科里默氏杆菌属,可以通过呼吸道和皮肤伤口水平传播,也可垂直传播[6]。由于当前多种病原微生物混合感染的情况非常普遍,加之临床症状、病理变化相似甚至相同,临床上区分RA 与其他病原体(大肠杆菌、沙门氏菌和多杀性巴氏杆菌)感染十分困难,因此对病原微生物进行实验室检测很有必要。值得注意的是,已有研究[7]报道,不同来源RA 的生化特性存在部分差异,绝大部分RA 不发酵碳水化合物,仅少数菌株可发酵葡萄糖、果糖和麦芽糖等,而本研究中12 株RA 生化特性一致,具体原因需要进一步研究分析。
本研究采用细菌培养、生化试验和16S rRNA方法对疑似感染RA 鸭鹅的40 份病料进行了病原学检测,检出12 株RA。结果提示,近年来临沭县部分鸭鹅养殖场持续流行的以流鼻涕、咳嗽、鼻窦炎、腹泻和神经症状(如斜颈、头部震颤和跛行)等为特征的疫病可能与RA 感染有关,也可能存在与其他病原继发或者混合感染的情况。Lyu等[8]报道,山东省鸭疫里默氏杆菌病总体流行率为16.76%(171/1 020),低于本研究结果,这可能与抽样数量、采样部位以及不同地区等因素有关。丹麦RA分离率为90%[9],印度鸭疫里默氏杆菌病患病率为40%,死亡率为75%[10],说明部分国家和地区RA感染较为严重,且流行率差别较大。
细菌血清型鉴定有助于疫苗开发和应用,提高疫病防治效果。RA 的血清学分型鉴定方法主要有试管凝集试验和玻片凝集试验[11]。RA 血清型复杂,本研究利用玻片凝集法对12 株分离菌株进行血清分型鉴定,发现血清1 型占比最高(58.33%),说明血清1 型为临沭县RA 流行的优势血清型。受病料来源局限,未检出其他血清型,但不排除当地存在其他血清型流行。吕泽昊等[12]报道,山东省部分地区RA 流行菌株大多为血清1、2、6 和7 型。吴彩艳等[13]研究发现,广东省存在RA 分离株血清1、2、3、5、6、7、8、10 型流行,其中以1 型为优势血清型。在迄今为止报道的21 种RA 血清型中,我国已经分离鉴定了13 种,其中血清型1和2 是引起鸭疫里默氏杆菌病暴发最常见的病原体[14]。国外也流行多种RA 血清型[8]:丹麦大多数RA 为血清4 型;血清1 型是匈牙利最常见的RA血清型,占菌株总数的64.5%;越南RA 血清型10占多数。由此可见,国内外RA 血清型流行种类较多,血清1 型为优势血清型,应重点关注。此外,一个地区RA 的血清型会随气候、季节变化,并且存在高比例、不可分型的RA 菌株[15]。因此,建议定期监测本地区RA 流行情况,根据其流行菌株选择合适疫苗进行防控。
RA 对氨基糖苷类、大环内酯类、头孢菌素类等多种抗生素具有天然耐药性,是一种多重耐药细菌[16]。用抗生素防治RA 感染同时也增加了耐药菌株的出现和传播。从RA 耐药性来看,不同地区、时间分离的RA 耐药性差异较大[17]。Éva 等[18]报道,匈牙利大多数RA 对氟苯尼考、氨苄西林、青霉素、磺胺甲恶唑-甲氧苄啶和大观霉素敏感,而对四环素、氟甲喹、链霉素和红霉素的耐药率相对较高,且根据菌株的地理来源,耐药模式显示出一些变化。本研究对12 株RA 进行耐药性检测发现,所有菌株对丁胺卡那、庆大霉素、新霉素和阿莫西林耐药,而对头孢他啶、头孢曲松、头孢氨苄敏感,与朱元军等[19]和王庆云等[20]报道基本一致,而与吕泽昊等[21]、陈栋等[22]和朱玲玲等[23]报道有所不同,这可能与菌株的生物特性、养殖环境和药物使用习惯等密切相关。已有研究[5]表明,细菌的耐药性与生物被膜的形成有关。因此,在使用抗菌药防治RA 感染前应结合药敏试验结果选用敏感药物,从而提高药物防治成效。
在动物回归试验中,3 种血清型RA 感染雏鸭后,临床症状和病理变化与临床自然感染RA 鸭表现一致,均具有眼鼻分泌物增多、头颈歪斜、抽搐和运动障碍等症状,剖检可见明显的纤维素性心包炎、肝周炎和气囊炎,最终攻毒组雏鸭全部死亡,说明3 种血清型RA 对雏鸭均具有较强的致病力,提示当地鸭疫里默氏杆菌病死亡率较高可能与流行菌株毒力较强有关。
4 结论
临沭县RA 感染较普遍,主要流行血清1 型,同时也存在血清2、11型。RA流行菌株致病力较强,对常用抗菌药的耐药情况不容乐观。建议加强定期病原学监测和耐药性分析,结合本地菌株生物学特性针对性选择疫苗和抗菌药防治,以提高RA 防控效果。

