加速度记录仪定量化评价安神健脑方对早期帕金森患者睡眠障碍的疗效
刘 云, 潘卫东, 方正龙, 支惠萍
(上海中医药大学附属曙光医院神经内科,上海 201203)
帕金森病(Parkinson’s disease,PD)是一种常见的中老年神经系统变性疾病,主要临床表现为静止性震颤、运动迟缓、肌强直、姿势步态异常等。近年来,随着对 PD患者非运动症状研究的逐步深入,开始较多地关注 PD相关的睡眠障碍[1,2]。中医药在本病的治疗中虽不处于主导地位,但其在延缓疾病过程,提高西药疗效、减轻毒副作用,提高患者的生存质量方面可能具有意义。2009年6月~2010年9月,我们对收治的 65例伴有睡眠障碍的早期 PD患者选用中药安神健脑方治疗并结合加速度记录仪进行定量分析[3-5],以期探讨中医药参与治疗早期 PD患者睡眠障碍的疗效评定,现汇总如下。
1 资料与方法
1.1 一般资料 入选 2009年6月~2010年9月于上海中医药大学附属曙光医院神经内科门诊及病房就诊的早期 PD(Hoehn– Yahr分期 1~2期)患者65例。所有患者均由专科医师按照推荐的原发性PD的诊断标准[6]进行诊断。①认知损害、痴呆、精神疾病等;②其他原因引起的 PD综合征及 PD叠加综合征;③患有疼痛性疾病、药物或酒精成瘾者;④睡眠呼吸暂停综合征;⑤其他可能影响睡眠的疾病,如慢性阻塞性肺病、冠心病、心绞痛、卒中等。将33例患者入选治疗组,男 21例,女 12例;年龄 49~78岁,平均年龄(68.6±9.2)岁;病程 0.5~5.5年,平均病程(3.62±2.31)年;Hoehn-Yahr评分(1.8±1.2)分;PD统一量表(UPDRS)评分(28.8±16.2)分;左旋多巴制剂的平均使用剂量 (368.2±203.9)mg/d。对照组 32例,男 19例,女 13例;年龄 49~79岁,平均年龄(67.1±10.1)岁;病程 0.5~5年,平均病程(3.6±2.3)年;Hoehn-Yahr评分(1.7±1.5)分;UPDRS评分(29.5±14.3)分;左旋多巴制剂的平均使用剂量 (362.7±205.1)mg/d。全部 PD患者均经头颅 CT和(或)MRI检查。
1.2 方法
1.2.1 全部患者均进行记录、神经系统检查及量表评分。病史记录包括年龄、性别、病程、疾病程度、治疗用药及用量,有无家族史及有无合并其他疾病等。病情评价采用 Hoehn– Yahr分期。PD睡眠质量调查采用 PD睡眠量表(PDSS)[7]。在治疗前后各评定1次。该量表包含 15个 PD睡眠障碍的相关问题,每一项的评分自 0分(症状极严重且持续)~10分(无症状)。
1.2.2 将便携式加速度微电脑记录仪(Micro-Mini-Motion Ambulatory Monitoring Inc,Ardsley,New YorK)带于患者手腕,在用药前 1周和治疗最后 1周(第 6周)用患者日记记录脱下、与戴上的时间。收取后,经电脑软件分析相关数据:生理节律(biorhythm,BIO);睡眠效率(sleep efficiency,SE)(%);入睡延迟(sleep latency,SL)(m in);最低 5 h活动量(least active 5 h,L5)(次)[8,9]。
1.3 治疗用药 两组患者均参照中国 PD治疗指南(第 2版)的用药指导原则[10]给予规范治疗。治疗组在治疗(左旋多巴或卡左双多巴控释片)的基础上加用安神健脑方:天麻、钩藤、郁金、姜黄、僵蚕、石菖蒲、三七、夜交藤、酸枣仁,水煎剂,每日 200 mL,与酉时(17:00~19:00)及亥时(21:00~23:00)分两次服用。对照组仅根据病情调整多巴制剂的用量及用法。整个疗程观察时间为 6周。
1.4 统计学处理 采用 SAS 6.12统计分析软件进行统计分析。所有的统计检验均采用双侧检验,不同治疗组各次访视的计量资料将采用(±s)进行统计描述。两组治疗前后的变化采用 ANOVA分析和Wilcoxon秩和检验进行比较。两组治疗前后的变化采用 χ2检验或非参数检验。P<0.05为差异有统计学意义。
2 结 果
2.1 一般情况 试验结束时,脱落 4例,原因是胃脘不适(治疗组 2例)或同时服用了多巴胺受体激动剂(治疗组和对照组各 1例)。两组患者在年龄、性别、病程、疾病程度以及左旋多巴制剂治疗剂量方面比较,差异无显著统计学意义 (P>0.05)。服药前,两组患者间的 SL、SE及 L5相近,差异无显著统计学意义 (P>0.05),见表1。
表1 治疗组与对照组患者治疗前一般情况比较[例,(±s)]
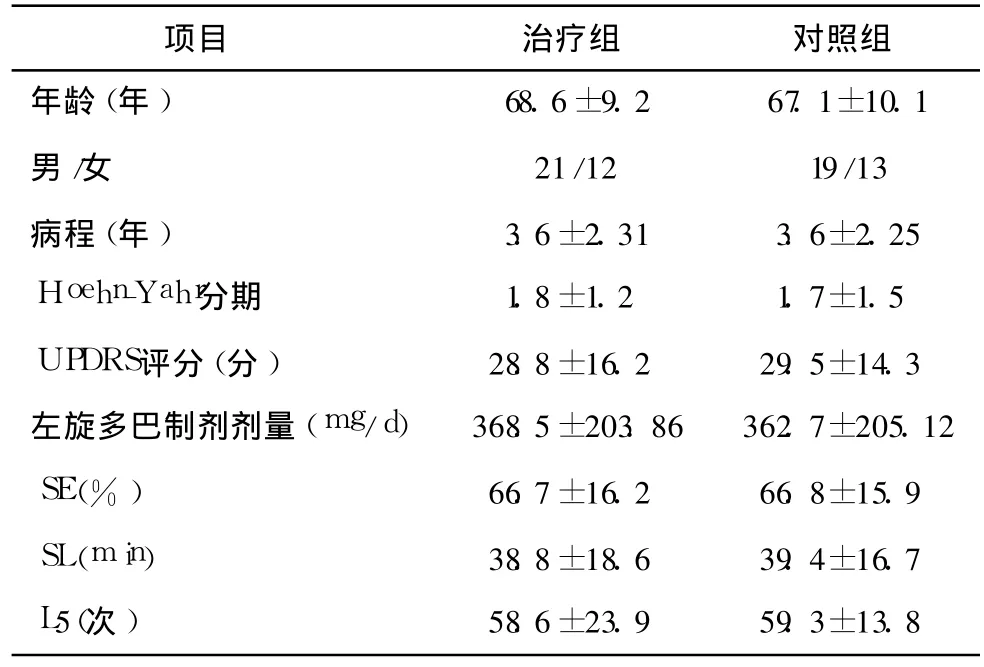
表1 治疗组与对照组患者治疗前一般情况比较[例,(±s)]
项目 治疗组 对照组年龄(年) 68.6±9.2 67.1±10.1男/女 21/12 19/13病程(年) 3.6±2.31 3.6±2.25 Hoehn-Yahr分期 1.8±1.2 1.7±1.5 UPDRS评分(分) 28.8±16.2 29.5±14.3左旋多巴制剂剂量(mg/d) 368.5±203.86 362.7±205.12 SE(%) 66.7±16.2 66.8±15.9 SL(m in) 38.8±18.6 39.4±16.7 L5(次) 58.6±23.9 59.3±13.8
2.2 安神健脑方治疗前后 PDSS评分 除 PDSS的第 4、7、9、11与 12外 ,治疗后 ,患者的 PDSS其他各项评分较治疗前有明显改善(P<0.05)。安神健脑方治疗后,患者的 PDSS总分较治疗前获得明显改善,与对照组相比,改善程度差别有显著统计学意义(P<0.05),见表2。
2.3 安神健脑方治疗前后加速度记录仪分析
2.3.1 日常活动与 BIO改变情况:伴有睡眠障碍的PD患者服药前夜间活动量较多,BIO较差;在加服安神健脑方后有所改善,而对照组无相应改善,见图 1。
2.3.2 SE、SL、L5与服药前相比,安神健脑方组患者服药后 SE明显提高,而对照组未见明显改善,差异有显著统计学意义(P<0.05);安神健脑方组入睡时间明显缩短,而对照组未见明显改善,差异有显著统计学意义(P<0.05);安神健脑方组 L5明显减低,而对照组未见明显改善,差异有显著统计学意义(P<0.05或 P<0.01),见图 2。
表2 患者治疗前后 PD睡眠量表评分比较(±s)
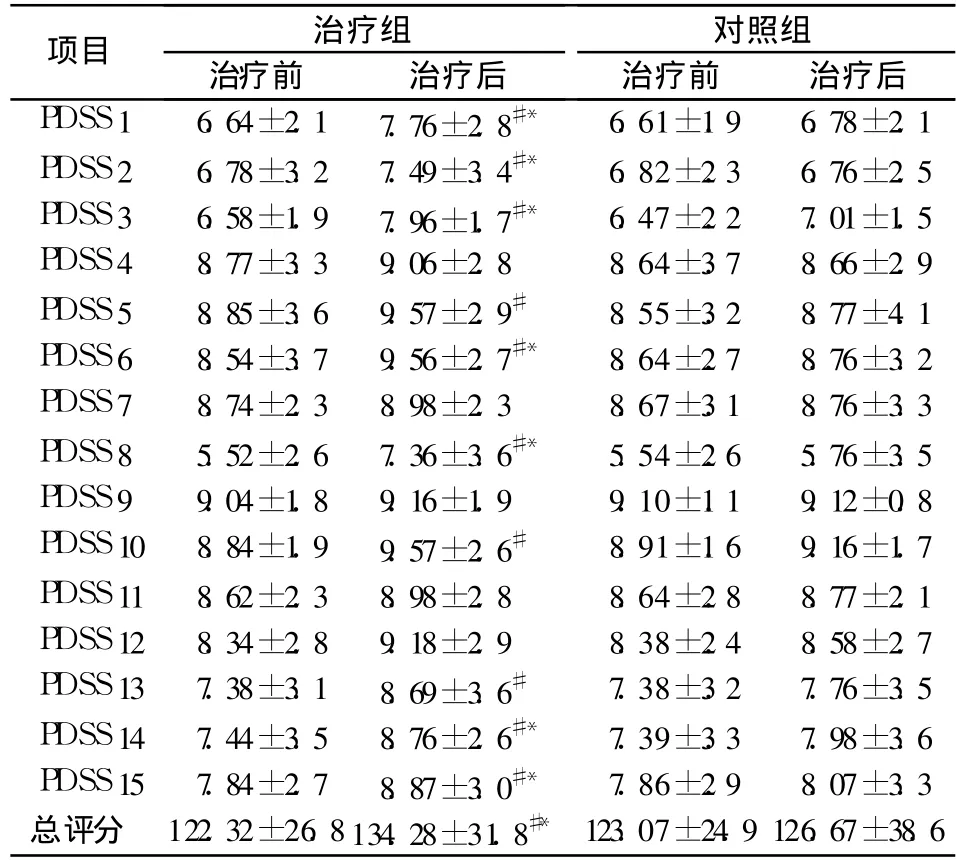
表2 患者治疗前后 PD睡眠量表评分比较(±s)
注:治疗组患者治疗后评分与治疗前比较,#P<0.05;治疗组治疗后与对照组治疗后比较,*P<0.05。
项目 治疗组 对照组治疗前 治疗后 治疗前 治疗后PDSS 1 6.64±2.1 7.76±2.8#* 6.61±1.9 6.78±2.1 PDSS 2 6.78±3.2 7.49±3.4#* 6.82±2.3 6.76±2.5 PDSS 3 6.58±1.9 7.96±1.7#* 6.47±2.2 7.01±1.5 PDSS 4 8.77±3.3 9.06±2.8 8.64±3.7 8.66±2.9 PDSS 5 8.85±3.6 9.57±2.9# 8.55±3.2 8.77±4.1 PDSS 6 8.54±3.7 9.56±2.7#* 8.64±2.7 8.76±3.2 PDSS 7 8.74±2.3 8.98±2.3 8.67±3.1 8.76±3.3 PDSS 8 5.52±2.6 7.36±3.6#* 5.54±2.6 5.76±3.5 PDSS 9 9.04±1.8 9.16±1.9 9.10±1.1 9.12±0.8 PDSS 10 8.84±1.9 9.57±2.6# 8.91±1.6 9.16±1.7 PDSS 11 8.62±2.3 8.98±2.8 8.64±2.8 8.77±2.1 PDSS 12 8.34±2.8 9.18±2.9 8.38±2.4 8.58±2.7 PDSS 13 7.38±3.1 8.69±3.6# 7.38±3.2 7.76±3.5 PDSS 14 7.44±3.5 8.76±2.6#* 7.39±3.3 7.98±3.6 PDSS 15 7.84±2.7 8.87±3.0#* 7.86±2.9 8.07±3.3总评分 122.32±26.8134.28±31.8#*123.07±24.9 126.67±38.6
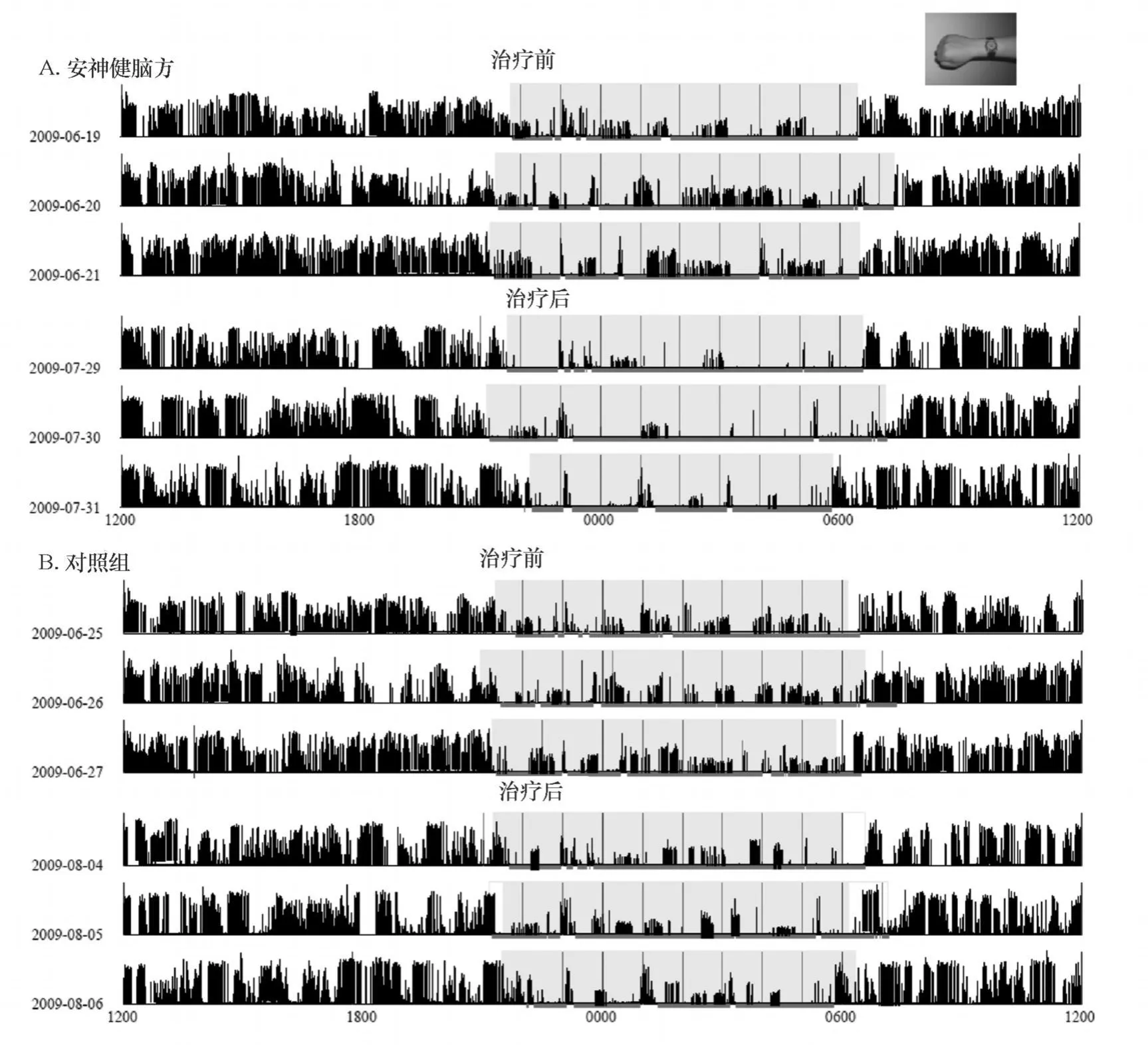
图1 治疗组和对照组患者治疗前后的昼间活动量的变化
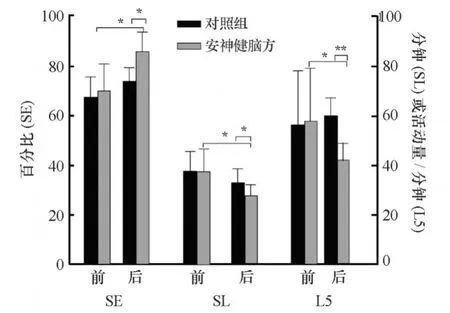
图2 中药治疗前后睡眠参数的变化
3 讨 论
随着世界人口的老龄化,与年龄密切相关的 PD的发病率日益增高。而 PD相关的睡眠障碍早在Pakinson的论著中就有记载[11]。Pal等[12]报道 67%~88%的 PD患者存在睡眠障碍。有学者对早期 PD患者进行睡眠调查,发现早期 PD患者睡眠障碍的发生率为 66%(35/53)。研究表明,PD患者的睡眠障碍主要包括失眠、不宁腿综合征和周期性肢动症[10]。其中,入睡困难和夜间频繁觉醒是 PD睡眠障碍最早和最常见的表现形式,由于觉醒次数显著增加,导致睡眠片段化。
目前认为 PD患者睡眠障碍的发生机制与以下几个方面有关[13]:①疾病导致睡眠中枢结构和递质异常,如中脑黑质 -纹状体多巴胺系统与行为觉醒有关,去甲肾上腺素、乙酰胆碱与脑电觉醒(脑电波去同步化)有关。②老化和抑郁对睡眠的影响,因为老年人本身存在着与增龄有关的睡眠能力下降。PD伴抑郁也参与了睡眠障碍发生与发展的过程。③运动障碍对睡眠的影响,运动缓慢及强直减少了睡眠中肢体活动和翻身动作,导致不适感和觉醒次数增加;RLS、周期性肢体运动障碍、震颤或药物诱发的肌阵挛均可产生唤醒。④治疗药物对睡眠的影响,如多巴制剂、多巴胺受体激动剂和抗胆碱能药物均可破坏睡眠。
睡眠障碍严重影响患者的生活质量。目前西医主要通过调整多巴制剂,加用多巴胺受体激动剂或抑制剂,必要时选用短效镇静安眠药物等进行治疗[10]。由于 PD患者多为中老年,睡眠障碍发生后均需长期服用镇静催眠药物,因此较易产生药物依赖、出现认知功能障碍等不良反应。而中医药在以往的临床观察与实验研究中,已被证明对 PD患者的震颤、肢体僵硬、便秘等有改善作用,并可推迟服用左旋多巴的时间、减少服药剂量及不良反应[14]。因此,本研究试图探讨中医药对早期 PD患者睡眠障碍的干预程度,以期在一定程度上达到改善 PD患者夜间睡眠障碍等症状,减少药物毒不良反应。
中医对睡眠的阐述已有二千余年,早在《黄帝内经》就有记载,主要通过阴阳、营卫气血学说对“寤寐”进行了比较深刻、朴素的阐述与治疗。传统的中医理论认为,无论是治疗颤证还是治疗不寐均从辨证论治开始。尤其对治疗睡眠障碍,或补益心脾,养血安神;或滋阴清热,交通心肾;或清心化痰,重镇安神;或益气镇惊,安神定志;或消食导滞,和胃安神等。本研究从文献统计的治疗 PD常用中药中,用辩证结合辨病的方法,结合现代药理研究,选取中药天麻 、钩藤 、姜黄 、僵蚕 、三七 、郁金 、石菖蒲 、夜交藤 、酸枣仁等组成安神健脑方以安神健脑定颤,治疗 PD早期伴睡眠障碍的患者。结果表明,治疗组患者的PDSS评分与对照组比较具有显著性差异。各单项中,PD患者夜间总体睡眠质量(PDSS 1)、入睡时间(PDSS 2)、睡眠维持时间(PDSS 3)、运动症状(PDSS 5)、精神状况 (PDSS 7)、夜尿情况 (PDSS 8)、震颤(PDSS 13)、醒后精神状况及白天过度嗜睡(PDSS 14和 PDSS 15)等在两组间的差异具有显著统计学意义。说明中医中药的参与,不仅能改善患者夜间总体睡眠质量,还能部分改善患者的其他相关症状,如运动症状、夜尿、精神状况以及白天过度嗜睡等。本组药方,多入心、肝、脾经。其中天麻、钩藤具有熄风定惊、清热平肝的功能,《药性论》谓天麻“治……,语多恍惚,多惊失志”;郁金、石菖蒲能解郁开窍,安心神,《本草汇言》:“郁金清气化坛散瘀血之药也,其性轻扬,能散郁滞,顺逆气,上达高巅,……”;僵蚕亦具熄风解痉作用;夜交藤、枣仁养心安神,《本草正义》记载夜交藤“治夜少安寐”。现代药理研究表明[15],天麻苷具有镇静作用,正常人服用天麻素或天麻苷元后多数有嗜睡感,脑电图 α波指数降低,天麻的镇静催眠作用可能与其降低脑内羟色胺的含量有关;钩藤对小鼠有明显的镇静作用;钩藤生物碱还能调节脑内 5-羟色胺代谢紊乱,对抑郁症有治疗作用。郁金能明显延长戊巴比妥钠和水合氯醛所致的小鼠睡眠时间,提高阈下催眠剂量戊巴比妥钠的小鼠入睡率。而石菖蒲水提物和去油水煎剂具有镇静作用,能使小鼠的自发活动显著减少。研究表明:石菖蒲挥发性成分的镇静作用更强。石菖蒲油能使实验动物的自发活动减少,肌张力降低,触觉和听觉能力降低。其中所含的 α-细辛脑有明显的镇静作用,其强度与持续时间与氯丙嗪相似。僵蚕具有催眠与抗惊厥作用。僵蚕醇浸出液,在小鼠皮下、腹腔注射或灌服及兔静脉注射均有催眠作用。脑电图观察显示,酸枣仁灌胃给药,可使睡眠总时间和慢波睡眠时间增加,觉醒睡眠显著减少,表现为慢波睡眠阶段高幅慢波增多,波幅增大,频率变慢。夜交藤的煎剂灌胃对大鼠的多导图显示,总睡眠时间延长,主要是慢波睡眠时相延长,异相睡眠时相缩短。此外,三七的镇静催眠作用主要是因为其地上部分含人参二皂甙较多,能起到中枢抑制的作用,从而达到镇静、安定与改善睡眠等功能。同时,三七皂甙 E1可显著减少小鼠的自发活动使动物安静,延长硫喷妥钠的睡眠时间。因此,无论从中医传统理论还是现代药理研究,本组中药的参与治疗对早期 PD患者伴有的睡眠障碍确能起到一定的积极作用。进一步证实了中医药的参与既能改善 PD患者的运动症状,又能改善其非运动症状,从而明显改善 PD患者的生活质量。
通过对 PDSS评分量表的分析,早期 PD患者幻觉、尿失禁的发生率非常低,治疗组 3.0%(1/33)、6.1%(2/33);对照组 3.1%(1/32)、6.25%(2/32)。可能与运动症状较轻、服多巴药物剂量较小有关[16]。
运动障碍对 PD患者的睡眠影响比较大。临床主要通过 PDSS量表进行评定,该表以问卷的方式采集,主观相对因素较多,存在患者表述不清,理解差异等问题。近年来有学者使用加速度治疗仪对 PD的运动与非运动症状进行相关研究[17]。本研究试图利用记录运动的仪器—加速度记录仪来客观地分析患者夜间睡眠中的运动障碍,如不安腿、震颤、夜间翻身次数,以期寻找更有效的治疗方法。本研究显示加速度记录仪携带方便,能比较客观地记录患者的运动情况、睡眠状况,值得临床推广应用。结合PDSS评分量表,我们还发现因震颤、夜间翻身次数、肢体痉挛疼痛而影响睡眠的发生率,在治疗组及对照组分别为 24.24%(8/33)、25%(8/32);15.15%(5/33)、12.5(4/32);3.03%(1/33)、3.12%(1/32),低于中晚期 PD患者的发生率[7],提示早期 PD患者的运动症状较轻,尚处于多巴胺治疗的“蜜月期”,运动症状并非影响早期 PD患者睡眠的主要因素。
根据中医理论,失眠的产生是由于阳不交阴。因此选择在酉时(17:00~19:00)以及亥时(21:00~23:00)[18]各服用中药服用 100 mL。以期能更好地调整阴阳及人的睡眠 -觉醒周期规律,提高中药治疗的有效率。传统的中医理论认为酉时阴气渐盛,阳气渐衰,又称“阳收之时”。而亥时为阳藏阴收之际,此时服药则能助阳入阴。
中医中药具有整体综合调节和不良反应小的特点而在治疗本疾病中有独特优势。本研究表明:中医中药参与治疗早期 PD伴睡眠障碍,在一定程度上确能起到改善 PD患者生活质量,防止白天过度嗜睡,进而稳定病情,提高整体治疗效果的作用。但由于样本量偏小,可信度受到一定的影响,因此,应进一步开展多中心随机双盲的临床观察,减少随意性。同时对伴有睡眠障碍的 PD患者在积极治疗的同时,可适时指导其建立良好的睡眠习惯,保证良好的睡眠环境,疏解焦虑紧张的情绪。睡前避免刺激,勿长时间看电视、书报或聊天等;床褥不宜太软,以免翻身困难;卧室内放置尿壶、便盆等。另外加速度记录仪对患者夜间身体的活动量与睡眠状态进行了客观的记录,但它们之间是否存在必然的关联尚需要进一步验证,可以通过身体活动的参数与多导睡眠仪同步评价患者的睡眠,并且考察两者的关联性以进一步明确加速度记录仪评价睡眠障碍的可靠性与准确性,也是本研究小组下一步研究内容之一。
[1]刘姝,陈彪,蔡彦宁,等.帕金森病患者的睡眠异常[J].中华神经科杂志,2006,39:193-195.
[2]何远宏,朱迎慧,刘柳,等.帕金森病患者睡眠障碍临床分析[J].中国实用神经疾病杂志,2008,11:29-30.
[3]潘卫东,元唯安,方正龙,等.增效安神止颤 2号方对帕金森病运动与非运动症状疗效评价[J].上海中医药大学学报,2009,4:29-34.
[4]潘卫东,方正龙,刘云,等.身体活动的幂型自相关指数定量化反映帕金森病的程度[J].中国临床神经科学,2010,18:257-262.
[5]PanW,OhashiK,Yamamoto Y,etal.Power-law temporalautocorrelation ofactivity reflectsseverity of parkinsonism[J].Mov Disord,2007,22:1308-1313.
[6]蒋雨平,丁正同,邬剑军,等.原发性帕金森病的诊断标准(2005年)[J].中国临床神经科学,2005,14:40.
[7]Chaudhuri KR,Pal S,DiMarco A,et al.The Parkinson’s diseasesleep scale:a new instrument for assessing sleep and nocturnal disability in Parkinson’s disease[J].JNeurol Neurosurg Psychiatry,2002,73:629-635.
[8]潘卫东,郭伸,刘云,方正龙,等.养血清脑颗粒改善帕金森病睡眠障碍疗效评价[J].上海中医药大学学报,2010,4:38-41.
[9]Comella CL,Morrissey M,Janko K.Nocturnal activity with nighttime pergolide in Parkinson disease:a controlled study using actigraphy[J].Neurology,2005,64:1450-1451.
[10]中华医学会神经病学分会帕金森病及运动障碍学组.中国帕金森病治疗指南(第 2版)[J].中华神经科杂志,2009,42:352-355.
[11]Pakinsong J.An essay on the shaking palsy[J].JNeurop Psychiatry Clin Neurosci,2002,14:2223-2236.
[12]Pal PK,Thennarasu K,Fleming J,et al.Noctumal sleep disturbances and daytime in patients with parkinson’s disease and in their caregivers[J].Parkinsonism Relat Disord,2004,10:157-168.
[13]赵忠新,黄流清.帕金森病的睡眠障碍[J].老年医学与保健,2006,12:205-207.
[14]刘毅,李如奎.止颤汤治疗帕金森病临床观察[J].山西中医,2002,18:16-17.
[15]周金黄,王建华.中药药理与临床研究进展[M].3版.北京:军事医学科学出版社,1995:295-301.
[16]李琳,刘振国,干静,等.早期帕金森病患者睡眠障碍分析[J].中国现代疾病杂志,2008,8:176-180.
[17]潘卫东,元唯安,方正龙,等.增效安神止颤 2号方对帕金森病运动与非运动症状疗效评价[J].上海中医药大学学报,2009,4:29-34.
[18]郁青萍,高翔.辨时治疗失眠 50例[J].中医药学刊,2006,24:763.

