电极材料Li4Ti5O12制备方法研究进展
刘浩文,刘针邑,唐定国
(中南民族大学化学与材料科学学院催化材料科学湖北省重点实验室,湖北武汉 430074)
锂离子电池具有电压高、能量密度大、循环寿命长、无环境污染等特点,自从20世纪90年代由Sony公司引入市场以来,已广泛应用于移动电话、笔记本电脑、小型摄像机等便携式电子设备中。而且,作为电源更新换代产品,锂离子电池还将在电动汽车、卫星及航天等领域得到广泛应用。
锂离子电池多采用碳素材料作为负极。碳负极材料一般具有石墨的层状结构,可以嵌入/脱嵌锂,和正极材料一起构成电池。由于碳电极与金属锂的电极电位相近,在充电过程中电解液将发生还原分解反应并在碳电极表面形成固体-电解质界面(SEI),消耗电解液并恶化电极性能。而且,在电池过充电状况下,碳电极表面可能析出金属锂而形成枝晶造成短路,给电池带来极大的安全隐患。基于高电化学性能和高安全性的考虑,负极材料的研究除了碳之外,还有硅负极、硫化物、锡基合金等,但这些材料还无法获得理想效果。这时,“零应变”钛酸盐材料Li4Ti5O12逐渐成为研究的热点。Li4Ti5O12在1.55 V电压下的较高放电容量和稳定的循环性能,使它可以作为负极与LiMn2O4、LiCoO3、LiNiO2等4 V正极材料组装成2.5 V锂离子电池[1],与5 V正极LiCoPO4组装成3.5 V锂离子电池[2],或与3.5 V正极LiFePO4组装成2 V锂离子电池[3]。
1 电极材料Li4Ti5O12的特点
Li4Ti5O12(也写作Li4/3Ti5/3O4)为白色物质,在空气中能稳定存在。Li4Ti5O12为尖晶石结构,具有与 LiMn2O4相似的“(A)[B2]O4”结构,空间群为Fd3m,其中 O2-离子构成 FCC点阵,位于32e的位置,部分Li+位于8a的四面体间隙中,同时部分Li+和Ti4+位于16d的八面体间隙中,其结构式可写为[Li]8a[Li1/3Ti5/3]16d[O4]32e,晶格常数a=0.836 nm。充电过程中,结构变化如下[4]:

参与反应的Li+嵌入到Li4Ti5O12的晶格中时占据16c位置,且原来位于8a的Li+也迁移到16c位置,最后所有16c位置都被Li+占据,反应产物Li7Ti5O12为淡蓝色。
研究发现,在Li+嵌入或脱嵌过程中,Li4Ti5O12的晶型不发生变化,晶胞参数a在0.836 nm和0.837 nm之间变化,体积变化小于1%,因此被称为“零应变”材料[4]。这具有重要意义,能够避免充放电循环中由于电极材料的膨胀收缩而导致的结构破坏,从而提高电极的循环性能和使用寿命,减慢循环过程中电池容量衰减的速度,使Li4Ti5O12具有比碳电极更优良的电化学性能。
Li4Ti5O12相对于金属锂的电极电位为1.55 V,理论比容量为175mAh/g,实际比容量约为150~160mAh/g[5]。由于Li4Ti5O12电极的工作电压较高,因此在锂离子电池充放电过程中,有机电解液将不会在较低的电压(<0.8 Vvs.Li+/Li)下发生还原分解,提高了电池的循环性能和安全性[6]。在25℃下,Li4Ti5O12的化学扩散系数为2×10-8cm2/s,比锂在碳负极材料中的扩散系数约高一个数量级,使其能以较大电流快速地充放电[7]。同时,Li4Ti5O12在全充电状态下有良好的热稳定性、较小的吸湿性及稳定的充放电平台,使它成为下一代锂离子电池的候选负极材料[6]。
2 电极材料Li4Ti5O12的合成方法
2.1 高温固相合成法
高温固相合成法技术成熟,操作简单,对设备要求低,适用于大规模生产,因此在很多研究中通过高温固相反应合成Li4Ti5O12。Li4Ti5O12的高温固相合成工艺与其他金属复合氧化物的合成工艺类似,通常以LiOH·H2O或Li2CO3与TiO2为原料,通过高温(800~1 000℃)、长时间(24 h以上)的热处理制备产物。常用的表征手段包括热失重(TG)分析和X射线衍射图谱(XRD)分析。一般按一定物质的量比例[如n(Li)∶n(Ti)=4∶5]将LiOH·H2O和TiO2分散在有机溶剂或水中,在高温下除去溶剂,然后在空气气氛中800~1 000℃烧结3~24 h,自然冷却后球磨得到理想的尖晶石结构Li4Ti5O12。Izquierdo[8]在对锂钛氧化合物系列的制备研究中发现Li4Ti5O12的尖晶石结构可耐受的最高焙烧温度为(1 015±5)℃。超过这个温度,它就会分解为Li2TiO3和Li2Ti3O7的混合相。
在高温固相反应中,反应温度、反应时间、原料比例以及混料工艺均是影响Li4Ti5O12材料性能的重要因素。高玲等[9]以LiOH和TiO2粉体为原料,分别在600、700、800、900℃下加热12 h制备得到了钛酸锂。经分析发现,600℃时反应不完全,产物中含有大量TiO2;700℃以上时反应比较完全,产物为Li4Ti5O12,XRD分析与标准图谱有很好的对应性。因此,高温固相法合成钛酸锂的温度应在700℃以上。通常,为了保证产物结晶性和反应较快地进行,反应温度一般控制在800~1 000℃之间。Li等[10]将LiOH和TiO2的混合物在800℃下加热2 h合成了Li4Ti5O12,然后考察后续热处理不同时间对产物性能的影响。研究发现,虽然经600℃热处理不同时间(0、2、8、12 h)后产物的晶体结构未发生明显的变化,但其电化学性能有较大的改变。测试表明,8 h的热处理可以很好地改善钛酸锂材料的形貌、动力学过程和锂离子扩散系数,从而提高了倍率性能。高温固相反应中使用的原料通常是固体粉末,一般按照化学计量比[11](Li与Ti摩尔比为4∶5)称取一定质量的反应物混合后经过高温反应得到Li4Ti5O12,产物具有较好的电化学性能。但考虑到锂盐在高温下容易挥发,阮艳莉等[12]将锂盐过量8%,然后经高温固相反应制备出晶型很好的钛酸盐产物。杨建文等[13]经过研究认为,当锂钛摩尔比为0.84时产物具有最优性能。Li等[10]在研究中也采用这一比例制备了Li4Ti5O12。混料工艺可以影响原料均匀程度,从而影响产物的纯度和电化学性能。目前,混料工艺一般分为三种:普通混合[10]、研磨混合[12]和球磨混合[9]。高剑等[11]研究了研磨和球磨方式混合反应物对产物性能的影响,结果表明,球磨混合原料的方法制备出的Li4Ti5O12颗粒更均匀,具有更好的电化学性能。阮艳莉等[12]在研究中发现,以研磨方式混合原料时加入适量的溶剂,可以很好地分散混合反应物,提高固相反应速率,在较短的时间内合成纯相的Li4Ti5O12。
高温固相反应工艺简单,易于实现工业化生产,但缺点也是显而易见的。如:粉体原料需要长时间的研磨混合,混合均匀程度有限,扩散过程难以顺利进行;要求较高的热处理温度和较长的热处理时间,能耗大;产物非常坚硬,很难将其磨成制作电极需要的粉末;材料电化学性能不易控制,等等。
2.2 溶胶-凝胶法
由于固相反应受到合成条件的影响,可能导致材料不均匀,粒径分布过宽,性能不易控制等弊病,通常可采用溶胶-凝胶法避免上述情况的发生,提高材料的均匀性。溶胶-凝胶法一般将金属有机化合物和无机化合物经溶液-溶胶-凝胶过程而固化,再经热处理得到氧化物和其他化合物,通常采用草酸、酒石酸、丙烯酸、柠檬酸等作为螯合剂,不仅可以使原料在原子级水平均匀混合,而且保持产物粒径在纳米范围内。经过溶胶-凝胶过程的反应前驱体在较低温度下焙烧就可得到结晶良好的材料,烧结时间也比固相反应法短,且成分容易控制,适合制备多组分材料,也是制备纳米级Li4Ti5O12的主要方法。
溶胶-凝胶法制备Li4Ti5O12的典型步骤如图1所示[14]。溶胶-凝胶法制备Li4Ti5O12的可能形成过程为:钛酸丁酯的醇溶液在有水存在时缓慢水解,首先生成Ti(OH)4,然后发生失水缩聚和失醇缩聚形成凝胶;前驱体在高温加热时氢氧化钛发生分解生成TiO2,然后和锂盐LiOOCCH3分解得到的Li2O或Li2CO3反应生成Li4Ti5O12。在图1所示的步骤中,钛酸丁酯水解形成Ti(OH)4的同时,锂盐在溶液中可以和钛盐在原子级水平相互分散,所以在前驱体中锂钛二者均匀存在,减少了高温反应中离子迁移,故而可以有效地降低反应的温度。

溶胶-凝胶法制备Li4Ti5O12采用的钛源通常是钛酸丁酯
Ti(OC4H9)4[15-19]或其他有机钛盐[20-21]。高剑等[22]选择无机钛盐TiCl4作为钛源,发展了一种新颖的油包水体系的溶胶-凝胶技术,形成了球形前驱体,使最终得到的产物为球形,具有较高的振实密度和良好的电化学性能。Hao等采用草酸[17]、柠檬酸[18]和三乙醇胺[19]作为螯合剂通过溶胶-凝胶法制备了纳米Li4Ti5O12。研究发现,这样制备的Li4Ti5O12材料形貌规则,粒径分布较窄,平均粒径分别为200 nm[17]和500 nm[18],三乙醇胺的加入量不同时,粒径在223~105 nm[19]之间变化。同时,材料具有很好的电化学性能,初始放电容量高达167~171mAh/g。王斌等[15]专门研究了溶胶-凝胶法后续处理中焙烧温度对材料性能的影响。他以钛酸丁酯和醋酸锂为原料,考察了600、700、800、900℃处理得到的材料的性能。研究发现:随着焙烧温度的增加,Li4Ti5O12晶粒的尺寸不断长大,电极材料的电化学循环性能趋于平稳,但是比容量却不断下降。800℃焙烧的样品比容量最高,且表现出良好的循环性能。随着焙烧温度的升高,晶粒尺寸的长大及分布变宽,可能是导致其容量下降的原因。贺慧等[16]的研究表明,合成温度低于650℃时会有杂质TiO2存在,而在800℃以上时则可得到单相Li4Ti5O12,与王斌的结论相符。Hao[17,19]和高剑等[22]亦得到相似的结果。所以,溶胶-凝胶法制备Li4Ti5O12时的焙烧温度一般在800℃以下,比高温固相法所需温度低,且反应迅速完全。除了常规的溶胶-凝胶法研究外,Jiang等[21]将溶胶-凝胶过程和模板方法相结合,将含有钛锂的前驱体凝胶包覆在碳微球表面,然后经过高温处理,成功地制备了Li4Ti5O12材料。这样制备的Li4Ti5O12具有空心球结构,比粉体材料具有更高的比容量和更好的倍率性能,这是因为空心球的薄壁结构减少了锂离子的迁移距离,增加了和电解液的接触面积,从而提高了放电性能。Kim等[20]采用溶胶-凝胶法,在850℃下制备了Li4Ti5O12,然后使用高能球磨工艺处理产物。最终产物是晶型很好的纳米微晶,循环性能良好,初始放电容量高达173mAh/g。
2.3 水热合成法(溶剂热合成法)
水热合成法也是制备电极材料较常见的湿法合成法,但水热法合成Li4Ti5O12的研究却少有报道。一般来说,水热合成法具有以下优点:(1)在相对较低的温度下合成具有晶体结构的材料;(2)反应条件多变可调;(3)产物组成均匀,物相和微结构一致,粒径分布较窄;(4)设备比较简单,操作不复杂。
Li等采用超声-水热法成功地在强碱溶液中制备了钛酸纳米管前驱体[23],经过离子交换和低温焙烧制备了形状可控、电化学性能优良的Li4Ti5O12纳米管/纳米线[24]。首先,将锐钛矿TiO2分散在高浓度NaOH溶液中,超声波处理一定时间后将分散液转移到水热反应釜中,在120~170℃下反应24 h至数天,然后洗涤沉淀并进行酸处理得到钛酸纳米管,再将钛酸纳米管和LiOH溶液进行水热处理以进行锂离子交换,产物进一步低温焙烧后得到最终产物Li4Ti5O12纳米管/纳米线。反应温度、pH值等离子交换条件和焙烧温度与时间会影响产物的形貌和性能,研究结果表明水热合成法制备的材料在电荷转移阻抗及动力学数据方面比传统高温固相法制得的材料有一定程度的改善。另外,Li等[25]将LiOH和四丁基钛酸酯分散在乙醇中在140℃下反应24 h,通过溶剂热法合成了钛酸锂。XRD研究发现产物的结晶度不高,主要晶型为Li4Ti5O12和Li2Ti3O7。结论表明,原料中锂钛摩尔比会影响产物的颗粒大小和结晶度,稳定的晶体结构将有助于材料保持良好的循环性能。
2.4 高能球磨法
高能球磨法是新近发展起来的一种化学合成方法,可以提高原料混合的效率,产物结晶度高。作为一种新技术,它具有明显降低反应活化能、细化晶粒、极大提高粉末活性和改善颗粒分布均匀性的特点,同时可以促进固态离子扩散,诱发低温化学反应。因此,高能球磨法是一种节能、高效的材料制备技术,也被应用到合成Li4Ti5O12的研究中。
Yu等[26]以化学计量比的锐钛矿TiO2和Li2CO3为原料,添加一定质量的酚醛树脂,通过高能球磨法制备分散均匀的前驱体,然后经高温处理可以制得Li4Ti5O12。Kim等[20]以钛酸异丁酯和LiOH为原料,通过溶胶-凝胶方法制备前驱体,并喷雾干燥经高温处理得到Li4Ti5O12。然后,将所得产物经过高能球磨,研究发现,无论XRD谱线的强度还是尖锐程度,在高能球磨处理之后都变强了,说明产物经过高能球磨处理后,结晶度有一定程度的提高。
2.5 微波法
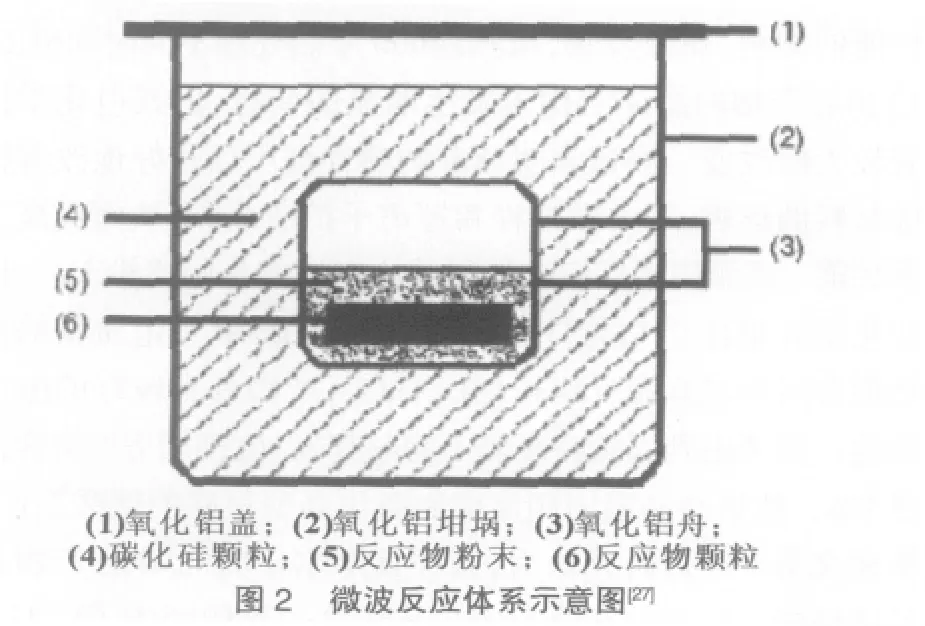
微波技术用于制备电极材料从本质上也是高温固相反应,但与传统的高温固相反应相比,微波加热具有节约能源、合成速度快、加热均匀等特点,因此越来越受到人们的重视。微波法已被广泛用于制备正极材料,可以快速有效地使固相反应进行并且降低反应温度。现在,微波法也被用于制备钛酸锂负极材料。Yang等[27]利用微波法首次合成了一系列锂钛氧化合物,如 Li4Ti5O12、Li2Ti3O7、Li2TiO3和 LiTiO2。产物 Li4Ti5O12具有很好的性能,初始放电容量为150mAh/g,放电平台为1.56 V。按照化学计量比混合原料Li2CO3和TiO2,置于氧化铝坩埚,用碳化硅作为微波吸收材料,并将热量转移至原料发生化学反应,生成Li4Ti5O12。因为反应有CO2气体放出,所以要控制微波加热功率,以保证最终产物的形貌特征。典型的微波反应体系如图2所示。
2.6 喷雾干燥法
喷雾干燥法将原料溶液雾化,然后在高温干燥气流中迅速失水得到产物,常用于制备具有一定形貌的细微粒子,它的优点是产物形貌均一,粒径分布窄。喷雾干燥法也可用于制备Li4Ti5O12负极材料。KiyoshiNakahara等[28]将LiOH和TiO2的混合物经喷雾干燥处理,得到分散性良好的细微粒子,再经高温处理即得到Li4Ti5O12,平均粒径仅有0.7μm。产物具有优良的倍率放电性能和循环特性,1C循环100次放电容量保持了99%,即使10C下也能保持86%。如果在50℃下10C循环100次,放电容量保持率为96%。Wen等[29]采用喷雾干燥法得到了多孔球形Li4Ti5O12。他们将Li2CO3、TiO2和一定量PVB用乙醇混合,球磨得到浆液,然后喷雾干燥得到球形前驱体。经过高温处理,则得到多孔球形Li4Ti5O12。
2.7 燃烧法
燃烧法是一种制备Li4Ti5O12的新方法,它的优点在于经济性高,产物粒径可以小至纳米级别。Raja等[30]将一定量的Ti(OCH3)4溶解在70%的HNO3溶液里,然后将其和LiNO3溶液150℃下在热板上混合,并在混合物中加入适量L-丙氨酸,最终得到凝胶。将所得凝胶燃烧,并经800℃高温处理得到最终产物。研究发现,在凝胶燃烧过程中,丙氨酸将成为合成Li4Ti5O12所需的能量来源,即463℃以上可能发生了Li4Ti5O12合成反应。用这种方法合成的Li4Ti5O12平均粒径为40~80 nm。结论表明,燃烧法不仅比较经济,而且可以得到纳米级产物。
2.8 其他合成方法
除了以上合成方法,研究者也采用了其他一些方法合成Li4Ti5O12。比如,电合成法[31]采用钛金属制备纳米钛酸锂前驱体,简单易行,等等。
3 结束语
作为一种“零应变”电极材料,Li4Ti5O12受到越来越多的重视,是锂离子电池负极材料的研究热点之一。它具有优良的电化学性能,尤其是循环性能使其在动力电源方面的应用空间十分广泛,可满足电动汽车或混合动力汽车对电源的一些特殊要求。
[1]OHZUKU T,HIRAL T.Thermal gravimetric studies ofmanganese dioxide[J].Electrochim ica Acta,1982,27:1049-1053.
[2]OKADA S,SAWA S,EGASHIRA M,et al.Cathode properties of phospho-olivine LiMPO4for lithium secondary batteries[J].Journal of Power Sources,2001,97-98:430-432.
[3]RAVET N,CHOUNINARD Y,MAGNAN JF,et al.Electroactivity of natural and synthetic triphylite[J].Journal of Power Sources,2001,97-98:503-550.
[4]OHZUKU T,UEDA A,YAMAMOTO N.Zero-strain insertionmaterial of Li[Li1/3Ti5/3]O4for rechargeable lithium cells[J].Journal of the Electrochem ical Society,1995,142:1431-1435.
[5]吴宇平,戴晓兵,马军旗,等.锂离子电池——应用与实践[M].北京:化学工业出版社,2004:120-124.
[6]唐致远,武鹏,杨景雁,等.电极材料Li4Ti5O12的研究进展[J].电池,2007,37(1):73-75.
[7]唐致远,薛建军,刘春燕,等.锂离子在石墨负极材料中扩散系数的测定[J].物理化学学报,2001,17(5):285-288.
[8]IZQUIERDO G,WEST A R.Phase equilibria in the system Li2OTiO2[J].Materials Research Bulletin,1980,15(11):1655-1660.
[9]高玲,仇卫华,赵海雷.合成温度对Li4Ti5O12电化学性能的影响[J].电池,2004,34(5):351-352.
[10]LIY,ZHAO H L,TIAN Z H,et al.Heat treatment effect on electrochemicalpropertiesof spinel Li4Ti5O12[J].Rare Metals,2008,27(2):165-169.
[11]高剑,姜长印,应皆荣,等.Li4Ti5O12的合成及性能研究[J].电源技术,2006,130(5):362-365.
[12]阮艳莉,唐致远,彭庆文.尖晶石型Li4Ti5O12电极材料的合成与电化学性能研究[J].无机材料学报,2006,21(4):873-879.
[13]杨建文,钟晖,钟海云,等.Li4Ti5O12的合成及其影响因素[J].中南大学学报:自然科学版,2005,36(1):55-59.
[14]SHEN C,ZHANG X,ZHOU Y,etal.Preparation and characterization of nanocrystalline Li4Ti5O12by sol-gelmethod[J].Materials Chem istry and Physics,2002,78:437-441.
[15]王斌,瞿美臻,林浩强,等.煅烧温度对Li4Ti5O12的电化学性能的影响[J].合成化学,2006,14(6):631-633.
[16]贺慧,程璇,张颖.锂离子电池负极材料Li4Ti5O12的结构和性能[J].材料研究学报,2007,21(1):82-86.
[17]HAO Y J,LAIQ Y,LU JZ,etal.Synthesisand characterization of spinel Li4Ti5O12anode material by oxalic acid-assisted sol-gel method[J].Journalof Power Sources,2006,158:1358-1364.
[18]HAO Y J,LAIQ Y,LIU D Q,etal.Synthesisby citric acid sol-gel method and electrochem ical properties of Li4Ti5O12anodematerial for lithium-ion battery[J].Materials Chemistry and Physics,2005,94:382-387.
[19]HAO Y J,LAIQ Y,XU Z H,et al.Synthesis by TEA sol-gel method and electrochem ical properties of Li4Ti5O12anodematerial for lithium-ion battery[J].Solid State Ionics,2005,176:1201-1206.
[20]KIMH J,OHLMH,SONW K,etal.A novel synthesismethod and electrochem ical characteristics of lithium titanium oxide as anode material for high power device[J].IEEE Conference Proceeding,2006(6):464-467.
[21]JIANG CH,YONG Z,HONMA I,etal.Preparation and rate capability of Li4Ti5O12hollow-sphere anode materia[J].Journal of Power Sources,2007,166:514-518.
[22]高剑,姜长印,应皆荣,等.锂离子电池负极材料球形Li4Ti5O12的合成及性能研究[J].无机材料学报,2007,22(1):176-1780.
[23]LIJR,TANG Z L,ZHANG Z G.H-titanate nanotube:a novel lithium intercalation hostwith large capacity and high rate capability[J].Electrochem istry Communications,2005,7:62-67.
[24]LIJR,TANG Z L,ZHANG ZG.Controllable formation and electrochemical properties of one-dimensional nanostructured spinel Li4Ti5O12[J].Electrochem istry Communications,2005,7:894-899.
[25]LIY,ZHAOH L,TIAN ZH,etal.Solvothermal synthesis and electrochem ical characterization of amorphous lithium titanate materials[J].Journalof Alloysand Compounds,2008,455:471-474.
[26]YU H Y,ZHANG X F,JALBOUT A F,etal.High-rate characteristics of novel anode Li4Ti5O12-polyacene materials for Li-ion secondary batteries[J].Electrochimica Acta,2008,53:4200-4204.
[27]YANG L H,DONG C,GUO J.Hybrid microwave synthesis and characterization of the compounds in the Li-Ti-O system[J].Journalof Power Sources,2008,175:575-580.
[28]KIYOSHIN,RYOSUKE N,TOMOKO M,et al.Preparation of particulate Li4Ti5O12having excellent characteristics as an electrode active material for power storage cells[J].Journal of Power Sources,2003,117:131-136.
[29]WEN Z Y,GU Z H,HUANG SH,et al.Research on spray-dried lithium titanate as electrodematerials for lithium ion batteries[J].Journalof Power Sources,2005,146:670-673.
[30]RAJA MW,MAHANTY S,KUNDU M,et al.Synthesis of nanocrystalline Li4Ti5O12by a novel aqueous combustion technique[J].Journalof A lloy and Compounds,2009,468:258-262.
[31]朱传高,朱其永,魏亦军,等.纳米Li4Ti5O12前驱体的电合成及其溶胶-凝胶过程[J].化学世界,2005,8:453-457.

