吸入一氧化氮在小儿心脏术后肺动脉高压的临床应用
周智恩,孙小圣,严善秀,冯 君,何伦德,王道庄,邓硕曾
肺动脉高压(pulmonary hypertension,PH)是左向右分流型先天性心脏病(先心病)最常见的严重并发症之一,重症患者手术预后差,国外报道重度PH患者总的一年生存率为 88%[1]。而一氧化氮(NO)被认为是较理想的肺血管扩张剂,但目前国内仍未普及应用。我们的研究旨在评价吸入 NO对先心病合并重度 PH患儿体外循环(extracorporeal circulation,ECC)术后的作用。
1 资料与方法
1.1 研究对象 2007年8月至 2009年8月我们共收治先心病伴 PH患儿 205例,占同期小儿先心病手术例数的 35.4%,按小儿肺动脉高压分度:肺动脉收缩压 30~40mm Hg为轻度,41~70 mm Hg为中度,>70mm Hg为重度[2]。其中术前 PH重度 50例,中度 58例,轻度 97例。未做心导管检查仅超声心动图检查存在 PH 125例。50例术前合并重度PH患儿中有 32例术后肺动脉压下降不明显接受 NO吸入治疗。其中男 20例、女 12例,年龄 4个月~12岁(4.8±2.8)岁,体重 4.4~36(14.1±6.5)kg。手术种类包括室间隔缺损(VSD)修补术12例,动脉导管直视闭合术 8例,完全性心内膜垫缺损(TECD)修补术 5例,右室双出口(DORV)矫治术 3例,完全性肺静脉异位引流矫治术、大动脉错位调转术各 2例。所有患儿均在静脉复合麻醉 ECC下进行,采用膜肺氧合,术中超滤。ECC时间 75~210(98±30)min,主动脉阻断时间 15~160(75±18)min,术后患儿均返 ICU监护。
1.2 吸入 NO的入选标准 必须同时具备以下四条:①术后平均肺动脉压(mPAP)≥25 mm Hg(1mm Hg=0.133KPa),跨肺压(TGP)≥15mm Hg,肺血管阻力指数(PVRI)≥3U/m2[3];②给予肌松、镇静、止痛、吸入高浓度氧,适宜的过度通气和碱中毒,静脉用血管扩张剂等常规治疗无效;③术后患儿循环稳定为先决条件,保证研究指标的稳定性;④在监测期间避免快速输注液体和大剂量调整血管活性药,尽可能保证呼吸参数的一致性,以减少除试验用药外其他因素对血流动力学和呼吸功能的干扰。剔除标准为:研究前出现以下任一并发症,包括:急性左心衰、心内仍存在残余分流、肺静脉梗阻、严重心律失常、胸腔积液。
1.3 吸入 NO及监测方法 采用带有 NO/二氧化氮(NO2)传递和监测系统的西门子 300A呼吸机输送和持续监测 NO、NO2峰值浓度,利用 AVL OMNL血气分析仪进行分析和测定高铁血红蛋白(MetHb)浓度。NO为北京氧气厂制造,以 10 ppm作为起始浓度,每 30 min增加 2 ppm,一般最大不超过 20 ppm,连续监测心率(HR)、平均动脉压(mSAP)、mPAP、中心静脉压(CVP)、肺毛细血管楔压(PCWP),利用 FICK法测定心输出量,根据公式计算心脏指数 (CI)、肺血管阻力 (PVR)、体血管阻力(SVR)、体肺血管阻力指数比(Rp/Rs)。动脉二氧化碳分压(PaCO2)、动脉血氧分压(PaO2)、动脉血氧饱和度(SaO2)、PaO2与吸入氧浓度(FiO2)之比(PaO2/FiO2)和呼吸指数(RI)等指标。
1.4 统计学分析 采用 SPSS 11.5统计软件分析,参数均以均数±标准差(±s)表示,各组均数采用配对 t检验,P<0.05为有统计学意义。
2 结 果
2.1 术后患儿一般情况 32例接受 NO吸入治疗患儿全部有效。吸入 NO 32~335 h,平均(66.4±21.3)h,NO浓度为 10~25 ppm。6例治疗期间曾发生 PH危象,积极治疗后好转。3例在撤离呼吸机后仍需面罩吸入 NO。全组死亡 3例(1例 VSD吸痰诱发 PH危象死亡,1例 TECD和 1例 DORV因术后多器官功能衰竭死亡)。
2.2 吸入 NO前、后血流动力学和呼吸功能指标的变化 血流动力学指标结果显示,吸入 NO 24 h后mPAP、PVR、Rp/Rs显著下降,体循环指标 HR、CI、SVR变化不明显。呼吸功能指标显示,吸入 NO 24 h后 PaO2/FiO2、SaO2显著升高。见表1。
表1 NO治疗前、后血流动力学和呼吸功能的变化 (±s)
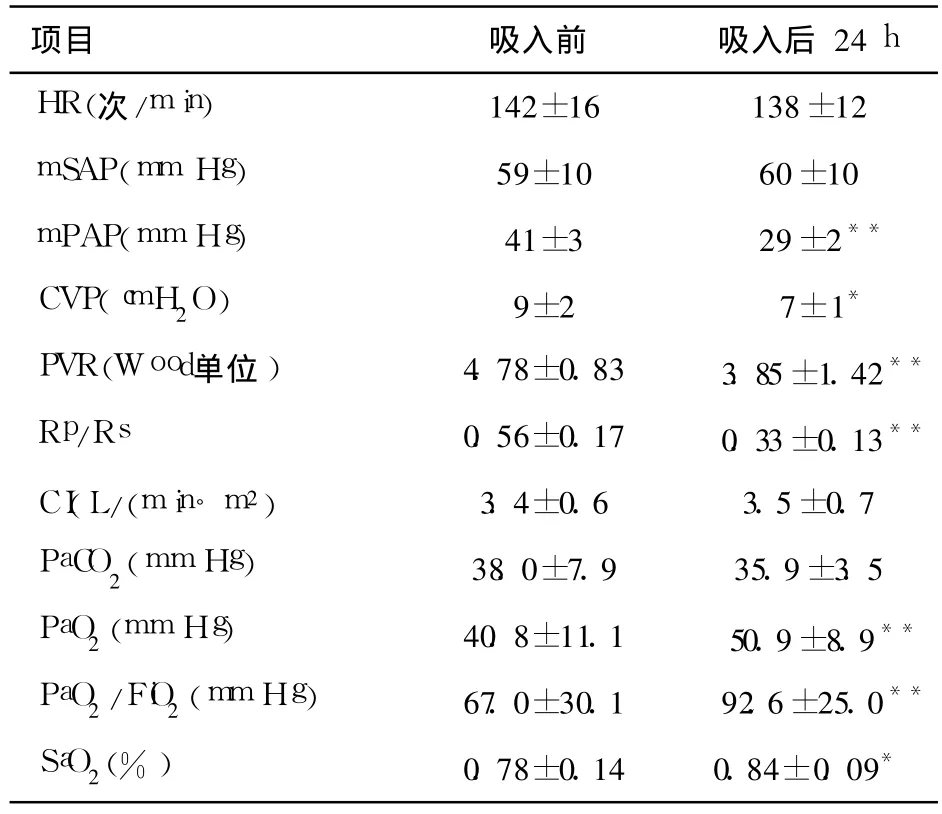
表1 NO治疗前、后血流动力学和呼吸功能的变化 (±s)
注:与 NO吸入前比较*P<0.05,**P<0.01
HR(次/Min) 142±16 138±12 mSAP(mm Hg) 59±10 60±10 mPAP(mm Hg) 41±3 29±2**CVP(cmH2O) 9±2 7±1*PVR(Wood单位) 4.78±0.83 3.85±1.42**Rp/Rs 0.56±0.17 0.33±0.13**CI(L/(Min· m2) 3.4±0.6 3.5±0.7 PaCO2(mm Hg) 38.0±7.9 35.9±3.5 PaO2(mm Hg) 40.8±11.1 50.9±8.9**PaO2/FiO2(mm Hg) 67.0±30.1 92.6±25.0**SaO2(%) 0.78±0.14 0.84±0.09*
2.3 监测 NO2、MetHb情况 所有患儿 NO治疗期间监测NO2浓度均 <5 ppm,最高浓度1.2 ppm,平均(0.5±0.4)ppm,MetHb均在 3%以下,平均(1.5±0.5)%。
3 讨 论
由于小儿代偿能力低下,先心病异常的血流动力学可严重影响其呼吸功能和肺血管发育,大量左向右分流导致肺充血,易诱发肺部感染,使肺血管压力和阻力增高;持续肺动脉高压又加重患儿心力衰竭,呼吸困难,形成恶性循环[4]。此外,长时间 ECC所致肺血管内皮功能障碍是引起术后早期肺血管阻力增高的主要原因[5]。因此合并有 PH的心内畸形矫治术后的早期,肺动脉压仍维持较高水平,并对该类疾病的预后有重要影响,成为制约该类手术早期成功率的重要因素之一[6]。所以,先心病合并 PH患儿围术期血流动力学的管理重点是降低肺动脉压及肺循环阻力并维护心功能。
NO是一种内皮细胞衍生的体液因子,由 L-精氨酸经 NO合酶催化而成,当吸入 NO进入肺泡腔后,通过升高毛细血管平滑肌细胞内的环磷酸鸟苷(cGMP)引起肺血管平滑肌舒张,随后扩散至血管腔内与血红蛋白结合而被灭活,因其具有可吸入性,选择性舒张通气性肺泡壁的微小血管以及 cGMP的半衰期短暂等优点,目前作为选择性肺血管扩张剂在心外科得到广泛的应用[7]。
我们通过吸入疗法来补充外源性 NO,从而降低 PVR。结果显示,吸入 NO可显著降低 mPAP、PVR和 Rp/Rs;同时显著升高 SaO2、PaO2和 PaO2/FiO2,而 HR、SVR、mSAP、PaCO2无变化 。提示吸入NO通过降低 PVR来改善肺血流灌注和氧合功能,对体循环、通气功能无影响。同时我们观察到,绝大多数患儿吸入低浓度 NO(10~25 ppm)即可产生较好的治疗效果,对 NO反应不好者,继续增加 NO并不能提高疗效。所以我们主张应用 NO时应尽量以产生临床疗效的最低浓度维持。一部分患儿对 NO吸入呈依赖性,提示 NO治疗存在一定的个体差异。这与 Miller等[8]研究结果相似。
NO治疗期间应密切监测毒副作用,虽然低浓度 NO(<40 ppm)本身毒性不强,但 NO气体与氧反应生成的 NO2却有很强的毒性,气道中 NO2浓度过高可与肺水结合形成亚硝酸盐和硝酸盐,引起严重的肺损伤,一般认为呼吸环路中 NO2浓度不应超过5 ppm[9]。本组监测到 NO2的最高浓度为 1.3 ppm。NO入血后与 Hb结合,最终形成 MetHb,MetHb无法结合氧,可造成 Hb携氧能力下降。婴幼儿由于存在 MetHb还原酶发育不全,更需要严密监测。本组监测 MetHb浓度均在正常范围。
总之,我们认为,对于先心病 ECC术后难治的反应性 PH或 PH危象患儿,若常规治疗无效,可通过 NO吸入治疗。NO是一种有效、安全、理想的肺血管扩张剂。
[1]Humbert M,Sibon O,Chaouat A,et al.Pulmonary arterial hypertension in France results from a national registry[J].Am J Respir Crit Care Med,2006,173(9):1023-1030.
[2]李少民,王丽娜,张莉,等.先天性心脏病合并肺动脉高压的诊断及外科治疗 [J].中国胸心血管外科临床杂志,2006,13(60):434-436.
[3]徐卓明,苏肇伉,陈玲,等.先天性心脏病术后肺动脉高压的一氧化氮吸入治疗[J].中华胸心血管外科杂志,2001,17(2):74-76.
[4]周智恩,孙小圣,严善秀,等.婴幼儿体外循环手术后呼吸功能衰竭的危险因素分析 [J].中国体外循环杂志.2009,7(3):129-131.
[5]Wynne R,Botti M.Postoperative pulmonary dysfunction in adultsafter cardiac surgery with cardiopulmonary bypass:clinical significance and implications for practice[J].Am JCrit Care,2004,13(5):384-393.
[6]Brown KL,Ridout DA,Goldman AP,eta l.Risk factors for long intensive care unitstay after cardiopulmonary bypass in children[J].Crit Care Med,2003,31(1):28-33.
[7]SteudelW,Hurford WE,ZapolWM.Inhaled nitric oxide:basic biology and clinical applications[J].Anesthesiology,1999,91(4):1090-1121.
[8]Miller OI,Celemajer DS,Deanfield JE,et al.Very-low-dose inhaled nitric oxide:aselective pulmonary vasodilator after operations for congenitalheartdisease[J].JThorac Cardivasc Surg,1994,108(3):487-494.
[9]Foubert L,Fleming B,Latimer R,et al.Safety guidelines for use of nitric oxide[J].Lancet,1992,339(8809):1615-1616.

