TiO2纳米管负载铂催化剂催化完全氧化甲醛*
何运兵,纪红兵
(中山大学化学与化学工程学院化工系,广东 广州 510275)
TiO2纳米管负载铂催化剂催化完全氧化甲醛*
何运兵,纪红兵
(中山大学化学与化学工程学院化工系,广东 广州 510275)
采用阳极氧化法制备了管径均匀、排列规整的TiO2纳米管阵,负载Pt之后直接用于动态条件下60 mg/m3甲醛的催化氧化脱除.实验结果表明在空速为60000 h-1以及100℃条件下,该纳米管催化剂对甲醛转化率高达98%,并且100%转化为二氧化碳和水.采用SEM、XRD和TPR对TiO2纳米管及纳米管催化剂进行了分析.结果表明TiO2纳米管管径约为130 nm,经过450℃煅烧2 h后由无定形转化成锐钛矿型,负载质量分数为1%的Pt不会改变纳米管的晶型,但是出现了氧化铂的晶相峰,表明Pt在纳米管上没有得到充分的分散,进而说明有望通过进一步提高Pt在纳米管上的超微分散以提高其催化性能;Pt负载在纳米管上使得催化剂表面活性氧物种增多,同时导致Ti—O键减弱,晶格氧的流动性有所增加,进而促进了纳米管表面氧的活性.通过本文的研究我们得出:1%Pt/TiO2在温和条件下对甲醛催化氧化反应具有良好的催化效果,有望通过进一步的研究,实现在更为温和的条件下对室内甲醛的完全催化氧化脱除.
铂;二氧化钛纳米管;甲醛;催化氧化
甲醛是室内最严重的污染物之一,对人体多种器官(肝、神经系统、免疫系统、生殖系统等)都有损害,己被 WHO确定为致癌和致畸形物质[1-2].随着室内甲醛等污染问题的日益突出,对其相应的控制与治理也越来越受到人们的重视.目前市场上已经出现多种空气净化器,但绝大部分主要都是采用吸附方式对空气中的甲醛等进行消除,而吸附技术受吸附剂失活与再生以及吸附容量的限制[3-4].催化氧化是一种很有应用前景的甲醛脱除技术,能在温和条件下将甲醛氧化为无毒的二氧化碳和水,不仅降低了室内空气中甲醛等VOCs的治理成本,而且避免了二次污染.因此开发温和条件下对甲醛氧化具有良好催化活性的材料成为研究热点[5-8].
2001年Gong及其合作者[9]首次报道采用HF水溶液作为电解液制备了长500 nm排列规整的TiO2纳米管.这种材料不但具有规整的结构同时还具有很大的内部表面积,煅烧之后形成整齐的晶体,非常有利于界面之间的电子传递.与纳米TiO2粉末相比,TiO2纳米管具有更强的吸附能力和良好的选择性,尤其是在管中加入更小的无机、有机、金属或磁性纳米粒子组装成复合纳米材料,可大大改善TiO2的催化性能[10].因而对阳极氧化法制备排列规整的TiO2纳米管的研究逐渐成为研究热点.现在 TiO2纳米管主要应用于光催化[11-12]、太阳能电池[1315]、气 敏 传 感 材 料[16-17]、超 级 电 容 器 等 领域[18-19].但尚未见到将贵金属修饰后的纳米管催化剂直接用于温和条件下室内污染空气治理的报道.本文采用电化学方法制备TiO2纳米管,负载1%Pt(质量分数,下文同)之后直接用于催化氧化脱除体积分数为百万分之一级别的甲醛.采用SEM对阳极氧化法制备的TiO2纳米管的形貌进行表征,采用XRD对煅烧前后以及负载Pt之后的纳米管的晶型进行表征,同时采用TPR对负载Pt前后催化剂表面氧的还原情况进行考察.希望通过本研究,设计出合适的纳米管催化剂,直接用于空气净化器之中,最终为室内甲醛等VOCs温和条件下的完全脱除提供技术支持.
1 实验部分
1.1 实验主要原料及仪器
试剂:氯铂酸(AR,Alfa Aesar公司);甲醛溶液(AR,湖北大学化工厂);乙二醇(AR,江苏永华精细化学品公司);金属钛片(99.9%,宝鸡钛业股份有限公司).
仪器:恒温循环器(HX-1050,北京博医康实验仪器公司);稳压电源(WJ20001D,佛山威捷电子设备制造厂);气相色谱(GC7890II,上海天美科学仪器有限公司);吸附仪(TP5000,天津先权科技开发有限公司).
1.2 实验方法
1.2.1 TiO2纳米管催化剂的制备
采用阳极氧化法来制备二氧化钛纳米管.一个典型的反应条件为:电解液的主体组分为乙二醇,加入0.3%的NH4F以及2%的H2O,在60 V的电压下反应42 h,可以得到管径约为130 nm、管长为200 μm的TiO2纳米管阵.

图1 阳极氧化法制备TiO2纳米管装置图
取1 g TiO2粉末或纳米管分散到50 m L去离子水中,70℃水浴加热磁力搅拌下,向悬浮液中缓慢滴加5 m L 1.0×10-2mol/L的氯铂酸水溶液,继续搅拌1 h,加入NaOH溶液控制悬浮液的p H=8,然后向其中滴加过量的35%~37%的甲醛溶液,滴加完毕继续搅拌2 h,之后于80℃下旋转蒸发脱除悬浮液中的水分,将粉末置于110℃烘箱中干燥3 h,最后放入450℃马弗炉中煅烧2 h,待催化剂自然冷却后置于干燥器中备用.
1.2.2 TPR测试
催化剂程序升温还原(TPR)测试是在天津先权科技开发有限公司的TP5000型多用吸附仪上进行的.样品装载量为50 mg,在氮气流中(30 m L/min)升温至120℃,吹扫30 min脱除水分,然后冷却至室温,待基线稳定后,切入H2和N2体积比为1∶9的混合气体,以10℃/min升温速率进行程序升温还原.进入热导池检测器之前用分子筛脱除混合气中的水分.
1.2.3 反应性能测试
通过一内径为7 mm的石英管固定床反应器对纳米管催化剂在甲醛氧化反应中的催化性能进行测试.反应气体组成为一路N2作为载气通过鼓泡装置产生甲醛气体,氧气O2体积分数为10%,另一路气N2作为稀释气体,通过质量流量计来调节各气路气体流量使得甲醛浓度为60 mg/m3,总流量为100 m L/min.反应尾气中甲醛的量采用酚试剂吸收后在紫外-可见分光光度计上测量,CO2的测量采用气相色谱来进行,采用TDX01填充柱,柱后接一甲烷转化炉,将尾气中的CO2转化为甲烷进行间接测定.
2 结果与讨论
2.1 甲醛在纳米管催化剂上的氧化
图2给出了在甲醛浓度60 mg/m3,O2体积百分数10%,气体总流量100 m L/min,空速60000 h-1的反应条件下,甲醛在催化剂1%Pt/TiO2-NT上的转化率随温度的变化.在常温时对甲醛的转化率为78%.随着温度的升高,甲醛转化率增大.当反应温度升高到100℃时,转化率达到了98%.而当温度高于150℃时,尾气中已经几乎检测不到甲醛气体了,即转化率达到100%.
在室温下和100℃的条件下,分别对进气中甲醛和CO2的含量进行测试,然后待甲醛转化达到稳态后,再测定反应尾气中甲醛和CO2的含量.催化氧化转化为CO2的转化率根据尾气中CO2增加量占甲醛减少量的百分比来表示,即y=ΔCO2/ΔHCHO×100%.实验测定结果见表1.

图2 甲醛在1%Pt/TiO2-NT催化剂上的氧化反应

表1 甲醛在1%Pt/TiO2-NT上催化氧化转化为CO2的转化率
进气中甲醛的浓度均为61.5 mg/m3,CO2的浓度均为4.8 mg/m3.在常温、空速为60000 h-1的反应条件下,出口处的甲醛浓度分别为13.3 mg/m3,CO2的浓度为42.2 mg/m3,这表明在反应中有48.2 mg/m3的甲醛被催化氧化,同时有37.4 mg/m3的CO2生成,催化氧化转化为CO2的转化率为77.6%,即反应还生成其他产物,没有发生完全催化氧化.而在100℃、其他条件相同的情况下,出口处甲醛浓度为1.2 mg/m3,CO2浓度为67.6 mg/m3,转化为CO2的转化率为100%,即100℃下转化的甲醛被完全氧化成了水和二氧化碳.
2.2 TiO2纳米管的X-射线衍射
采用XRD对煅烧之前、450℃煅烧以及负载1%Pt之后的纳米管进行测试,测试结果如图3所示.
从图3中可以看出,阳极氧化法制备出的TiO2纳米管为无定形结构,这与文献[20-21]中报道的结论一致.经过450℃煅烧后,无定形的TiO2纳米管转换成为锐钛矿晶型.负载1%Pt之后,锐钛矿型的TiO2纳米管的晶相结构没有发生变化,但是出现了新的晶相结构,在2θ为29.018°、31.661°、和33.820°出现了新的晶相衍射峰,分别对应于氧化铂的(110)、(002)和(101)晶面.说明Pt在纳米管上没有得到充分的分散,还存有进一步提高分散度的空间.

图3 TiO2纳米管的XRD分析
2.3 TiO2纳米管的微观形貌
采用扫描电镜对阳极氧化法制备的TiO2纳米管的形貌进行表征,如图4所示.阳极氧化法制备出的纳米管为排列规整、管径均匀的管阵结构,管径大约130 nm,管长可达到200μm以上.经过煅烧以及负载Pt之后,管阵结构会出现少许的损坏,但整体上仍然是管阵结构.

图4 TiO2纳米管的扫描电镜图
2.4 TiO2纳米管的程序升温还原实验
为了考察Pt的负载对TiO2纳米管催化性能的影响,分别对TiO2纳米管和1%Pt/TiO2-NT进行了程序升温还原(TPR)实验.测试结果如图5所示.从图5可以看出,TiO2纳米管的还原温度很高,超过650℃,但是负载Pt之后,在75℃和493℃附近有两个耗氢峰.75℃处耗氢峰对应于氧化铂Pt Ox还原为金属Pt所消耗的氢气,而493℃处的峰属于TiO2纳米管表面氧还原时的氢气消耗峰.这些结果说明Pt的负载减弱了二氧化钛的Ti—O键,丰富了催化剂表面氧物种,增加了催化剂晶格氧的流动性,进而促进了纳米管表面氧的活性,此即Pt/TiO2-NT具良好催化活性的一个重要原因.
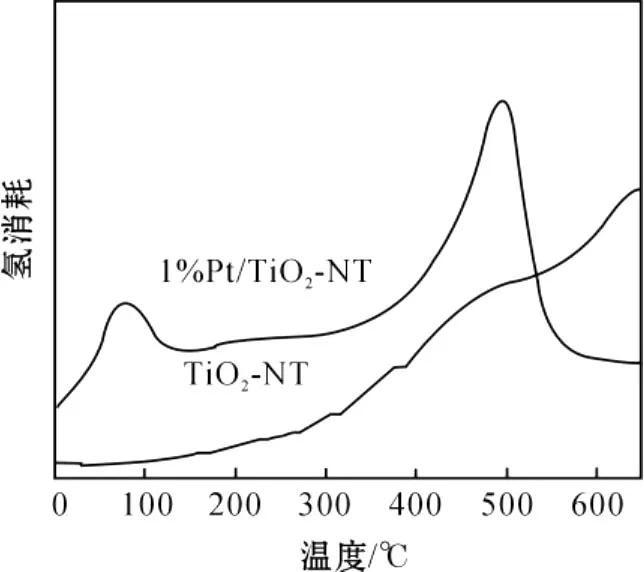
图5 Pt/TiO2-NT和TiO2纳米管在H 2中的TPR谱图
3 结 论
(1)Pt负载于TiO2纳米管而形成的催化剂在温和条件下对甲醛催化氧化反应具有良好的催化效果.对于60 mg/m3的甲醛气体,空速为60000 h-1以及100℃条件下,该纳米管催化剂对甲醛转化率高达98%,并且100%转化为二氧化碳和水,即实现了对甲醛的完全催化氧化.有望通过进一步的研究,实现在更为温和的条件下对室内甲醛的完全催化氧化脱除.为此本文为开发TiO2纳米管催化剂在室内空气治理上的应用提供了一个参考.
(2)采用本文中阳极氧化法实验条件下制备出的TiO2纳米管管径约为130 nm,管长可达200 μm,且为无定形的,经过450℃煅烧2 h之后转化为锐钛矿型.在纳米管上负载Pt之后不会改变其晶型,但在TiO2纳米管上出现了氧化铂的晶相峰,说明Pt在纳米管上没有得到充分的分散,因此有望通过进一步的研究,将Pt高度均匀地分散到TiO2纳米管上进一步提高其催化性能.
(3)TiO2纳米管的特殊管阵结构有利于甲醛与催化剂的活性位接触,此即纳米管催化剂表现出良好催化活性原因之一.此外,TPR表征结果表明在TiO2纳米管负载Pt之后,载体TiO2表面氧的还原温度下降了,催化剂表面活性氧更加丰富了,说明贵金属与载体的相互作用导致Ti—O键减弱,晶格氧的流动性有所增加,此即Pt/TiO2具良好催化活性的另一重要原因.
[1]JONES A P.Indoor air quality and health[J].Atmospheric Environment,1999,33(28):4535-4564.
[2]何运兵,纪红兵,王乐夫.室内甲醛催化氧化脱除的研究进展[J].化工进展,2007,26(8):1104-1109.
[3]HAYASHI A,FUJIMOTO Y,OGAWA Y,et al.Adsorption of gaseous formaldehyde and carboxylic acids by ammonium-ion-exchanged α-zirconium phosphate[J].Journal of Colloid and Interface Science,2005,283(1):57-63.
[4]RONG H Q,RYU Z Y,ZHENG J T,et al.Effect of air oxidation of rayon-based activated carbon fibers on the adsorption behavior for formaldehyde[J].Carbon,2002,40(13):2291-2300.
[5]ZHANG C B,HE H,TANAKA K.Catalytic performance and mechanism of a Pt/TiO2catalyst for the oxidation of formaldehyde at room temperature[J].Applied Catalysis B,2006,65(1-2):37-43.
[6]唐幸福,黄秀敏,邵建军,等.氧化锰八面体分子筛纳米棒的合成及其催化甲醛低温氧化性能[J].催化学报,2006,27(2):97-99.
[7]SEKINE Y.Oxidation decomposition of formaldehyde by metal oxides at room temperature[J].Atmospheric Environment,2002,36(35):5543-5547.
[8]何运兵,纪红兵.温和条件下甲醛在Pt/TiO2上催化氧化反应的原位漫反射红外光谱研究[J].催化学报,2010,31(2):171-175.
[9]GONG D W,GRIMES C A,VARGHESE O K,et al.Titanium oxide nanotubearrays prepared by anodic oxidation[J].Journal of Materials Research,2001,16(12):3331-3334.
[10]QUAN X,YANG S G,RUAN X L,et al.Preparation of titania nanotubes and theri environmental applications as electrode[J].Environmental Science Technology,2005,39(10):3770-3775.
[11]HIROMASA T,MASAHIRO M.N-doped TiO2nanotube with visible light activity[J].Chemistry Letters,2004,33(9):1108-1109.
[12]CHEN Y S,JHON C,STEPHEN H,et al.Preparation of a novel TiO2-based p-n junction nanotube photocatalyst[J].Environmental Science and Technology,2005,39(5):1201-1208.
[13]ANDREI G,MACAK J M,HIROAKI T,et al.Ion Implantation and annealing for an efficient N-doping of TiO2nanotubes[J].Nano Letters,2006,6(5):1080-1082.
[14]PARK J H,KIM S W,BARD A J.Novel carbondoped TiO2nanotube arrays with high aspect ratios for efficient solar water splitting[J].Nano Letters,2006,6(1):24-28.
[15]MOR G K,SHANKAR K,PAULOSE M,et al.Use of highly-ordered TiO2nanotube arrays in dye-sensitized solar cells [J].Nano Letters,2006,6(2):215-218.
[16]PAULOSE M,VARGHESE O K,MOR G K,et al.Unprecedented ultra-high hydrogen gas sensitivity in undoped titania nanotubes[J].Nanotechnology,2006,17(2):398-402.
[17]VARGHESE O K,YANG X,KENDIG J,et al.A transcutaneous hydrogen sensor:from design to application[J].Sensor Letters,2006,4(2):120-128.
[18]UCHIDA S,CHIBA R,TOMIHA M,et al.Application of titania nanotubes to a dye-sensitized solar cell[J].Electrochemistry(Tokyo,Japan),2002,70(6):418-420.
[19]WANG Y G,ZHANG X G.Preparation and electrochemical capacitance of RuO2/TiO2nanotubes composites [J]. Electrochimica Acta,2004,49 (12):1957-1962.
[20]WANG N,LI X Y,WANG Y X,et al.Evaluation of bias potential enhanced photocatalytic degradation of 4-chlorophenol with TiO2nanotube fabricated by anodic oxidation method [J].Chemical Engineering Journal,2009,146:30-35.
[21]赖跃坤,孙岚,左娟,等.氧化钛纳米管阵列制备及形成机理[J].物理化学学报,2004,20(9):1063-1066.
Complete catalytic oxidation of formaldehyde over Pt-supported TiO2nanotubes
HE Yun-bing,JI Hong-bing
(Department of Chemical Engineering,School of Chemistry and Chemical Engineering,Sun Yat-sen University,Guangzhou 510275,China)
Highly-ordered and uniform TiO2nanotube arrays are fabricated by anodization and after supporting Pt they are applied directly in the catalytic oxidation of 60 mg/m3formaldehyde under dynamic conditions.Experiment results indicate that the as-prepared nanotube catalyst exhibits excellent activity towards formaldehyde oxidation,with 98%conversion of HCHO and 100%conversion to CO2and H2O under 60000 h-1GHSV and 100℃.SEM,XRD and TPR are used for the characterization of TiO2nanotubes and the corresponding catalyst.The diameter of the resulting TiO2nanotubes is about 130nm and it changes from amorphous to anatase after 2h's calcination at 450℃.Supporting 1%Pt does not change the crystal structure of nanotubes,but the peaks corresponding to platinum oxide appear in XRD patterns.This finding indicates Pt is not highly dispersed on TiO2nanotubes,which further indicates the catalytic acitivity may be promoted by enhancing Pt dispersion on nanotubes.From TPR result,supported Pt not only brings out more surface oxygen species,but also weakens Ti—O bond and enhances the mobility of crystal oxygen,which furter promote the activity of surface oxygen over nanotubes.Therefore,we come to the conclusion that 1%Pt/TiO2-NT exhibits excellent activity in the oxidation of formaldehyde under ambient conditions and that the complete catalytic oxidation of indoor formaldehyde under even more ambient conditions may be achieved through further investigation.
platinum;titanium dioxide nanotube;formaldehyde;catalytic oxidation
TQ 032.41
A
1673-9981(2010)04-0397-05
2010-10-20
广东省科技计划项目;广东省高等学校高层次人才资助项目
何运兵(1981—),男,江西乐平人,博士.

