锌同位素测量方法及其在环境地球化学、营养学研究中的应用
逯 海,王 军,任同祥,周 涛,李金英
(1.中国计量科学研究院,北京 100013;2.中国原子能科学研究院,北京 102413)
锌在自然界中分布广泛,是生物体必需的营养元素之一,与生命活动息息相关。锌同位素组成受热力学和动力学分馏的控制,通过研究锌同位素组成可以揭示自然界中生物作用和地质过程,因此深受地球化学、环境、海洋学、营养学等领域科学家的关注。
最早的锌同位素研究报道见于1972年[1],Rosman等采用热电离同位素质谱仪(thermal ionization mass spectrometry,TIMS)分析了矿石中锌的同位素组成。但由于测量精度较低,他们没有发现自然界中锌同位素组成的变化,故忽视了其地质应用价值。随着多接收-电感耦合等离子体质谱仪(multi-collector inductively coupled plasma mass spectrometry,MC-ICP-MS)的出现,测量精度获得极大提高。1999年,Maréchal等[2]首次采用等离子体质谱测定了锌同位素组成,并研究了沉积物和生物样品化学处理方法。他们发现,自然界中锌同位素组成的微小变化可以作为示踪剂指示海洋中的生物化学过程[3]。此后,锌同位素测量技术,包括分离技术[4-5]、质谱测量[6]及应用[7-10]、成盐成矿机理研究[6]等逐渐成为研究热点。国内外相关的论文数量[11-12]呈逐年递增之势。
下面介绍锌同位素测量相关的基本情况,包括自然界锌同位素组成、样品处理方法、测量方法包括质谱仪质量歧视校正方法、分馏机理、应用领域等。
1 锌同位素概况
1.1 锌同位素基本情况
锌共有 30个同位素,分别为54Zn、55Zn、56Zn、57Zn、58Zn、59Zn、60Zn、61Zn、62Zn、63Zn、64Zn、65Zn、66Zn、67Zn、68Zn、69Zn、70Zn、71Zn、72Zn、73Zn、74Zn、75Zn、76Zn、77Zn、78Zn、79Zn、80Zn、81Zn、82Zn、83Zn。其中 ,64Zn、66Zn、67Zn、68Zn、70Zn等是自然存在的稳定同位素,其他均为放射性同位素。
锌稳定同位素的基本情况列于表1。
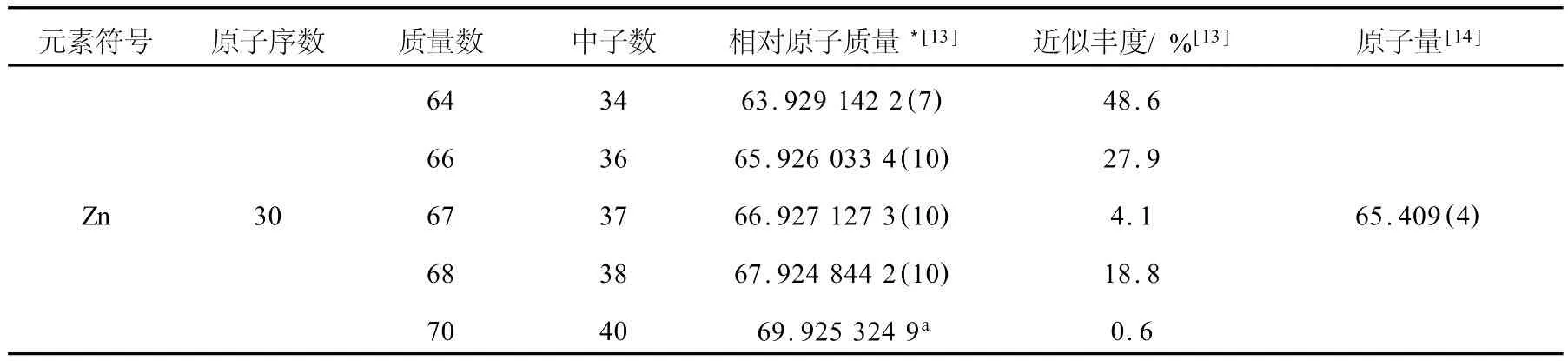
表1 锌稳定同位素及其基本参数Table 1 The naturally stable isotopes of zinc and their basic parameters
1.2 自然界中锌同位素的组成特征
文献[1]报道,不同来源的锌具有差异明显的同位素组成。自然界中部分样品的锌同位素组成分布示于图1。
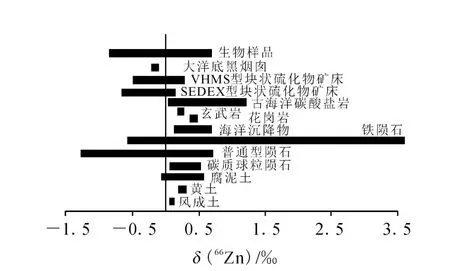
图1 锌同位素在自然界中的变化图[15]
组成差异表明,锌可以作为合适的示踪剂,指示地质、生物过程等,揭示变化的本质,推论未来的气候或环境变迁。
2 实验方法
2.1 样品前处理
锌广泛存在于岩石、沉积物、大豆等食品,血清等生物样品和水体中,不同基体的消解方式不同。一般采用 HNO3[2,16]、HNO3+HF[17]或HNO3+HCl[17]消解,消解液蒸发至干,然后用高浓度的 HCl把其中的锌完全转化为 Zn(Ⅱ)的氯络合物ZnCl42-,待树脂分离。
2.2 树脂分离
目前多采用阴离子树脂法将锌与其他离子(如 Cu、Fe、Pb、Na、K、Ca、阴离子等)分开 ,达到纯化样品的目的。其基本原理是:适当浓度的盐酸体系中,Zn2+与Cl-发生可逆络合反应(1)形成络合阴离子;在树脂柱中取代Cl-(阴离子树脂已预先用盐酸处理为氯型),如反应(2);通过适当浓度的盐酸淋洗,梯度去除 Cu、Fe、Pb、Na、K、Ca、阴离子等;回收锌时,只要降低 Cl-浓度,反应(1)即反向进行,络合阴离子被破坏,Zn从树脂中解离。
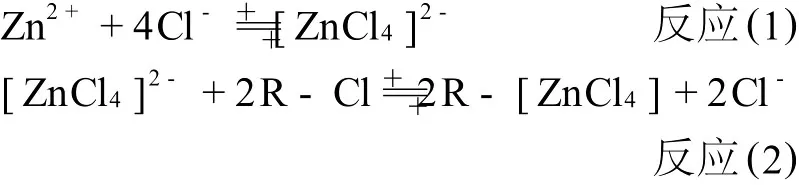
典型的分离流程列于表2。
对于锌含量很低的海水样品,Bermin等[19]研究了络合和共沉淀两种预富集方法。处理流程列于表3。预沉淀后的样品,用AG MP-1阴离子树脂分离。
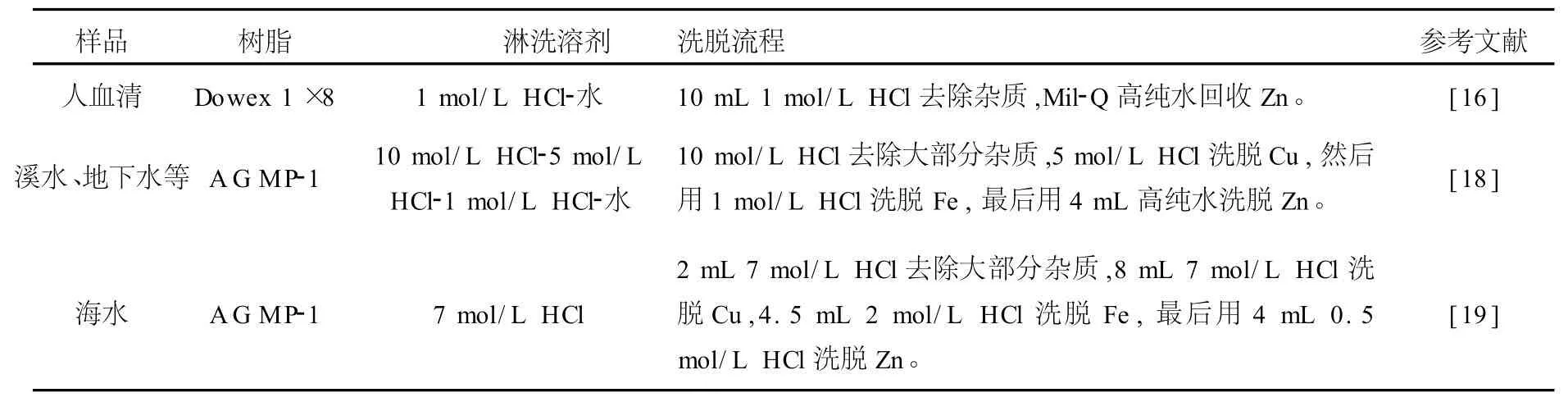
表2 阴离子树脂法分离ZnTable 2 Separation of Zn by anion resin

表3 低含量样品络合/共沉淀富集方法Table 3 Complex/coprecipitation method for lowcontent samples
2.3 质谱测定
20世纪 70年代,Rosma等[1]首先利用TIMS测量了锌同位素组成。近年来,MC-ICPMS的应用报道日渐增多。目前,文献报道的锌同位素分析方法主要有2种:传统的热电离同位素质谱法和多接收电感耦合等离子体质谱法。
TIMS具有离子束动能扩散很小(约0.5 eV),同量异位素干扰少等优点。邓中国,王军等分别利用多接收-TIMS方法测量了金属锌[20]、人血清[16]、人体排泄物[21]中的锌丰度 ,测量均采用铼带单带形式,以硅胶-磷酸为发射剂提高电离效率。其中,硅胶影响离子流强度,磷酸对离子流的稳定性影响较大。邓中国等[20]采用如下涂样流程:首先将5μL硅胶悬浊液涂在铼带上,1 A电流加热3 min,出现白色硅胶薄层后,滴加5μL待测锌溶液,1 A电流加热3 min,滴加5 mL 0.25 mol/L磷酸溶液,1.5 A电流加热3 min;然后,10 min内加热电流增至2 A,断开2 min后,再缓慢提高加热电流至带上出现暗红色涂层时,迅速断开,这一过程被称为“红化”过程。64Zn/67Zn、66Zn/67Zn、68Zn/67Zn、70Zn/67Zn的测量精度分别为 0.03%、0.03%、0.05%、0.11%。王军等[21]则首先将样品与磷酸混合,然后涂样,在已处理好的样品中加入15μL 0.17 mol/L H3PO4。首先在铼带上涂5μL硅胶悬浮液,恒定加热电流2.0 A,当硅胶近干时,滴涂样品;待溶液全干,缓慢升高加热电流至3.5 A,使铼带瞬间红化,然后断开电流。人血清、人体排泄物中64Zn/66Zn、67Zn/66Zn、68Zn/66Zn 的测量精度分别为0.10%、0.067%、0.063%。测量精度可以满足同位素稀释质谱法的需要。
但是,TIMS法最大的缺点是质量分馏随时间变化较大,这个缺陷严重影响了测量结果的准确性。TIMS法的质量分馏主要发生在样品蒸发阶段,轻重同位素蒸发速率不同,造成质量分馏。以64Zn/66Zn为例,蒸发伊始,轻质量的64Zn优先蒸发,随后其他较重的同位素蒸发几率增大,故64Zn/66Zn比值呈现由大到小,最终平衡的状态。由于升温、调节聚焦等阶段64Zn已有损失,所以这种方法获得的64Zn/66Zn比值不会是真实值。
MC-ICP-MS法一般以氩气为工作气体,火焰温度可达8 000~10 000℃,远远超过元素周期表中大多数元素的第一电离能。周期表中80%的元素可以被电离,电离效率高于75%,是目前国际上用于锌同位素测量的首选仪器。但是,与 TIMS法相比,MC-ICP-MS法具有两方面明显缺陷:1)进样过程(包括自提升进样和激光烧蚀)、离子传输过程会引起质量分馏。因此,需要具有特定量值的锌同位素标准物质校正仪器的系统偏差;2)同量异位素干扰。Ar、H、O、N、Cl、C等元素往往相互间或与某些金属元素组成离子团,干扰待测离子。目前,有效去除同量异位素干扰的手段有高分辨和碰撞反应方法。锌同位素分析过程中可能产生的同量异位素离子团,用高分辩方法分开各相应核素所需的分辨率列于表4。
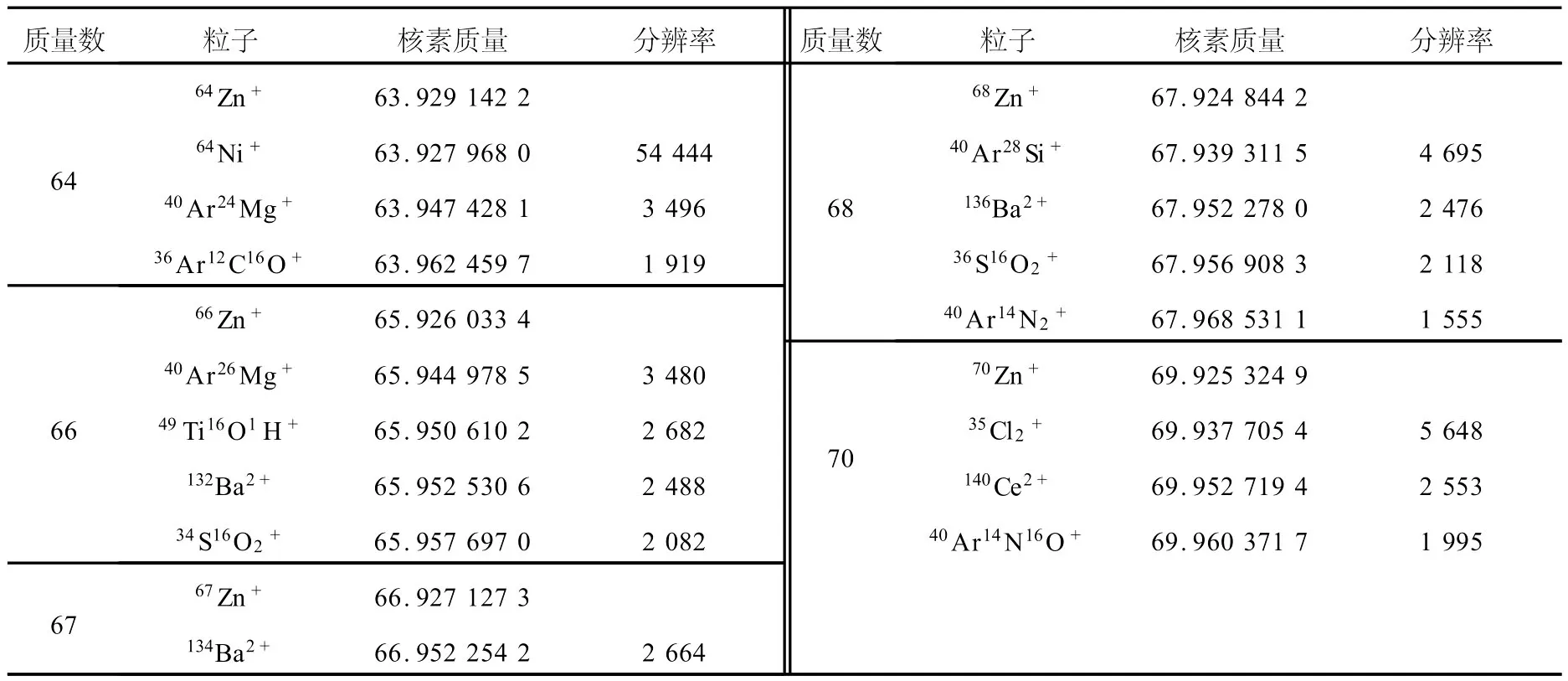
表4 锌同位素的同量异位素干扰及分开相应核素所需的分辨率Table 4 Isobars on Zn isotopes and needed resolution
表4表明,对于大多数同量异位素干扰,3 000的分辨可以满足要求。而前期工作表明[22],采取Ar气碰撞反应的方法可以有效去除相应的同量异位素(除64Ni+外)。
需要特别指出的是,在锌同位素测量中,最严重的干扰来自64Ni+对64Zn+的干扰。因为大多数ICP-MS法采用镍锥,仪器背景相对较高,而无论采用高分辨方式还是碰撞反应手段,均不能有效消除Ni的干扰。所以,当前最有效的方式是扣除空白和通过检测62Ni+扣除64Ni+对64Zn+的干扰。
2.4 质量歧视校正方法
如前文所分析,分析过程中 TIMS法和MC-ICP-MS法均产生质量歧视,故均不能获得“真值”。目前,采用相对值测量法和绝对质谱法校正质量歧视。
相对值测量法通用于国际地质领域。该方法是测量结果与共同认可的某“标准”相比较,获得Zn同位素的相对值(δ值)。表示如下:
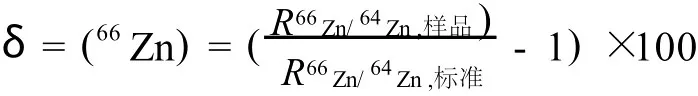
其中,R66Zn/64Zn,标准一般采用Johnson&Mattey公司提供的JMC3-0749L或Aldrich公司提供的Zn溶液[23]。这两种锌“标准”不是严格意义上的同位素丰度标准物质,故其同位素丰度值必须由各实验室自己定值。做法是:将NIST 976 Cu同位素标准物质按特定比例加入JMC3-0749L或Aldrich-Zn中,通过仪器的系统校正系数 K(65Cu/63Cu),按照指数公式计算出锌各个丰度比的系统校正系数 K(iZn/jZn,i,j=64,66,67,68,70)。K(iZn/jZn)校正过的JMC3-0749L或Aldrich-Zn测量值即认为是该标准的标准值,样品的测量方法同标准。其测量精度可达0.04‰[2]。
绝对质谱法在原子量测量工作中广泛采用。Chang 等[24]将64Zn(丰度 97.3%)、66Zn(丰度96.1%)、68Zn(丰度98.5%)3种浓缩同位素重量法称重,配制成64Zn/66Zn、66Zn/68Zn两种混合溶液,通过公式 (1)计算 K(64Zn/66Zn)和K(66Zn/68Zn)。
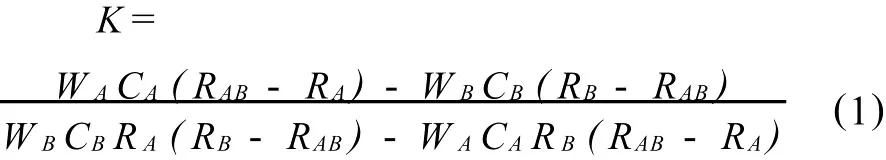
式中:CA、CB为浓缩同位素溶液中两种主同位素的含量;WA、WB分别为浓缩同位素溶液A和溶液B的称重质量;RAB、RA和RB分别为混合溶液、浓缩同位素 A、B溶液同位素丰度比的测定值。
两种混合溶液获得的 K(64Zn/66Zn)和K(66Zn/68Zn)经迭代后分别为 0.986 91和0.986 75。取其平均值0.986 83作为仪器的校正系数 K(64Zn/66Zn),按照 K(70Zn/66Zn)=K-2(64Zn/66Zn),K(68Zn/66Zn)= K-1(64Zn/66Zn),K(67Zn/66Zn)=K1/2(68Zn/66Zn)计算其他校正系数 K。
对于相对测量法,Cu和Zn的物理化学性质存在差别,因此,单位质量歧视因子 fCu≠fZn。而且对于MC-ICP-MS,指数公式不能适用。故此,这种方法获得的结果是错误的。
对于绝对质谱法,非常适用于 TIMS测量,但是对于 MC-ICP-MS,单位质量歧视因子f64Zn/66Zn≠f66Zn/68Zn,即单位质量歧视因子不相等,而是呈线性。而且,指数公式不能适用。
绝对质谱法需要配制相同比值对、比值接近的“基准物质”,这使该方法复杂化。
3 锌同位素在自然界中的分馏原因[25]
3.1 生物过程引起的锌同位素分馏
锌参与体内多种酶的组成、代谢,在这些生理过程中,可能存在锌的同位素分馏。
Weiss等[26]研究了水稻、莴苣、西红柿的吸收、转运锌的过程。结果发现,3种植物均造成了明显的同位素分馏,且分馏的情况基本一致,即根部富集锌的重同位素,而顶部轻同位素的丰度相对增加。其中,根部的66Zn相对于培养液富集了0.04‰~0.09‰,而相对于植株顶部富集了0.13‰~0.26‰。由此推测,锌从根部至顶部的迁移应该由细胞膜完成。锌在细胞膜间的出入过程中,轻同位素更容易穿过,结果是穿过大量的细胞膜后,到达终点的轻同位素数量相对较多,造成轻同位素富集。
Gélabert等[27]研究了海洋浮游生物和淡水微生物对锌的吸附及其同位素分馏情况,发现重同位素明显富集,相对于生长环境,δ66Zn富集了0.08‰~0.25‰。
David等[28]研究了美国和欧洲多种水流中溶解锌的丰度变化,发现当样品循环流动一昼夜(24 h)后,只有一个样品的δ66Zn变化了大约0.3‰,大部分样品的δ66Zn没有明显变化。他们认为这是微生物在新陈代谢过程中优先吸收轻质量同位素的结果。
3.2 成盐成矿过程引起的锌同位素分馏
Marechal等[29]研究了 ZnCl2在30 ℃和50℃时,分别与方解石反应生成菱锌矿(ZnCO3)的过程,发现 a均为 1.000 04;而Zn(NO3)2在 30℃和50℃时,分别与方解石反应生成菱锌矿的过程中,a几乎都为1.000 11。这验证了化学反应成矿过程中锌同位素分馏现象的存在,而且说明,温度对锌同位素分馏不会产生明显的影响。
Laurie等[30]研究了无定形 Fe(OH)3吸附过程中锌的同位素分馏情况。发现吸附过程造成分馏因子为0.999 48±0.000 04。这表明,因为短的Zn-O键,重同位素优先被氢氧化物表面吸附。他们还研究了 Cu、Fe、Zn在无定形Fe(OH)3表面的吸附行为,发现引起同位素分馏的强弱为Cu>Fe>Zn。
化学反应条件的变化可引起元素化合价、配位数的变化,从而导致晶格中原子之间键能的改变。
3.3 样品分离富集过程引起的锌同位素分馏
无论是 TIMS还是MC-ICP-MS测量,均存在基体效应影响,因此,需要将基体元素(如 K、Na、Ca、Mg等)去除。目前,一般采用离子交换树脂纯化样品。Marechal等[31]发现,样品在经过离子交换树脂分离纯化的过程中,Zn发生了明显的同位素分馏。他们研究了12 mol/L HCl条件下,A GMP-1型阴离子交换树脂对锌同位素的保留情况。发现1.6 mL树脂造成了66Zn/68Zn 0.02‰的分馏,这说明树脂优先吸附锌的轻同位素。因此,在用树脂分离锌时,应该获得100%的回收率,否则将引入分离过程的同位素分馏。
4 锌同位素的应用
4.1 在环境地球化学中的应用
锌同位素在自然界中的分馏主要受源区成份和地质过程热力学或动力学分馏的控制。随着现代分析技术的提高,自然界中锌同位素组成的变异规律逐步明晰,展露了其在环境地球化学、岩石学、古海洋学等研究领域中的重要应用前景。
海洋生物生产力影响着海洋与大气间的CO2交换,反过来气候变化又影响着生物生产力。因此,研究参与海洋生物过程的元素(如Zn、Fe等)的生物地球化学循环是理解气候变化的基础。由于被浮游生物吸收,Zn在海洋表层海水中呈贫化状态,而在深层海水中,死亡的浮游生物体在细菌作用下发生氧化、分解,Zn和CO2又重新释放。研究 Zn的生物行为也是理解CO2吞吐过程的钥匙。
Pichat等[32]研究了赤道太平洋地区175 ka以来,深海碳酸盐中锌同位素的分馏情况。δ66Zn值在35.2 ka和21.2 ka时,显示明显的周期性。他们认为,这说明海洋中锌同位素的变化与年代有关。
Mason等[17]借助锌同位素分析探究了俄罗斯乌拉尔地区的V HMS型块状硫化物矿床的成因,发现δ66Zn变化明显。他们认为锌同位素可以用于指示成盐成矿物质的来源、成矿过程和机理。
锌同位素分馏也可以用于指示环境污染的来源。Chen等[33]研究了法国塞纳河污染的来源,发现66Zn/64Zn有明显的变化(0.07‰~0.58‰),与河两岸居民区金属屋顶中的 Zn、工厂排出物中的Zn等锌污染源中同位素组成相比对,可以准确探究污染的来源。
4.2 在营养学研究中的应用
锌是人体内200多种酶和蛋白质等生命大分子的重要组成成分。缺锌导致骨骼生长缓慢、发育迟缓,导致皮脂腺失调、产生褐斑。锌还能增强大脑细胞的活力,提高智力。
锌同位素示踪研究可用于示踪锌代谢途径和研究锌代谢同膳食以及机体的生理、病理相互影响的机制,有助于研究病理成因,制订补锌计划。而且,可以为家畜、家禽等饲养、繁殖提供科学的依据。
Turnlund等[34]进行了为期63天的α-纤维素和肌醇六磷酸对年青人锌摄入影响的跟踪研究。按摄入的食物,实验分为3组:基本食物,基本食物+0.5 gα-纤维素/kg体重,基本食物+2.34 g肌醇六磷酸。每组食物中加入67Zn,通过TIMS测量排泄物中67Zn监控锌的摄入情况。实验发现:以上3组人员的平均锌摄入量分别为(34.0±6.2)%、(33.8±2.9)%、(17.5±2.5)%。结果显示,肌醇六磷酸抑制了锌的吸收,如果食物中肌醇六磷酸的含量高,将导致人体缺锌。
Egli等[35]研究了谷类辅助食品中植酸对锌、铜的吸收影响。9个成年人分为两组,分别进食天然谷类辅食和去除植酸的同类谷类辅食,两种食品中均添加70Zn和65Cu。用 TIMS测量排泄物中的锌、铜,计算锌、铜的吸收率。实验结果表明:去除植酸后锌的吸收率(34.6±8.0)%比未去除植酸的吸收率(22.8±8.8)%高;而去除植酸后铜的吸收率(19.7±5.1)%与未去除植酸的吸收率(23.7±8.1)%相比,没有明显的改善。
5 展望
当前,MC-ICP-MS和MC-TIMS的测量精度都已达到10-6,完全可以区分不同样品中Zn同位素组成的微小差异。因此,Zn同位素的研究在诸多领域显示出广阔的应用前景及潜在的应用价值。但有4个方面的问题值得特别关注:1)Zn同位素研究起步较晚,分馏机理的研究及一些参考数据还需进一步完善和考证。Zn同位素研究自20世纪末开始,相比于 C、N、O、H、Pb、Sr、Nd 等同位素 ,研究积累较少 ,研究水平不深。2)当前的测量属于“相对测量”,从数据的可比性、长效性角度考虑,绝对数据应该是追求的目标。如前文所述,目前各实验室的测量结果均以δ表示,与测量结果相比较的所谓“标准”不具有准确的绝对量值。短期内各测量结果可以相互比较,但随着数据的累积和研究时间的延长,势必造成数据的混乱。如果以具有绝对量值的标准物质校正测量结果,各数据在任何时候都可以溯源到同一个标准摩尔,其可比性将得到保障。3)样品处理技术还需要进一步提高。特别对于含量较低的样品,提高分离、富集效率和防止污染是重要问题。4)由于MC-ICP-MS分析速度快,且在一个测量周期内质量歧视稳定,因此,该方法是当前最重要的锌同位素分析方法。但是,作者实验室的前期研究发现:MC-ICP-MS的单位质量歧视因子随同位素组成变化明显,这意味着单纯的指数校正不能适用于该方法。所以应当从同位素电离能、电离与传输过程中离子淌度、密度、相互间的作用力,以及仪器构造(如锥间体积)等方面入手,建立新的 MC-ICP-MS质量歧视校正模型。
[1]ROSMAN KJ R.A surver of the isotopic and elemental abundances of zinc[J].Geochimica et Cosmochimica Acta,1972,36(7):801-818.
[2]MARÉCHAL C N,TÉLOU K P,ALBARÉDE F.Precise analysis of copper and zinc isotope composition by plasma source mass spectrometry[J].Chemical Geology,1999,156(1/2/3/4):251-273.
[3]MARÉCHAL C,ALBARÈDE F.Ion-exchange fractionation ofcopper and zinc isotopes[J].Geochim Cosmochim Acta,2002,66(9),1 499-1 509.
[4]MALINOVSKY D.Fractionation of Fe and Zn I-sotopes:methods and some applications in aqueous geochemistry[D].Sweden:Lulea University,2004.
[5]PEEL K,WEISS D,CHAPMAN J,et al.A simple combined sample standard bracketing and interelement correction procedure for accurate mass bias correction and precise Zn and Cu isotope ratio measurements[J].J Anal At Spectrom,2008,23(1):103-110.
[6]GELABERT A,POKROVSKY O S,VIERSJ,et al.Interaction between zinc and freshwater and marine diatom species:Surface complexation and Zn isotope fractionation[J].Geochim Cosmochim Acta,2006,70(4):839-857.
[7]LUCKJ M,OTHMAN D B,ALBAREDE F.Zn and Cu isotopic variations in chondrites and iron meteorites:Early solar nebula reservoirs and parent-body processes[J].Geochem Cosmochim Acta,2005,69(22):5 351-5 363.
[8]PICHAT S,DOUCHET C,ALBAREDE F.Zinc isotope variations in deep-sea carbonates from the eastern equatorial Pacific over the last 175 ka[J].Earth Planet Sci Lett,2003,210(1/2):167-178.
[9]SONKE J E,SIVRY Y,VIERSJ,et al.Historical variations in the isotopic composition of atmospheric zinc deposition from a zinc smelter[J].Chem Geol,2008,252(3/4):145-157.
[10]STENBERG A,ANDRÉN H,MALINOVSKY D,et al.Isotopic variations of Zn in biological materials[J].Anal Chem,2004,76(14):3 971-3 978.
[11]WALDER A J,FREEDMAN P A.Communication:Isotopic ratio measurement using a double focusing magnetic sector mass analyzer with an inductively coupled plasma as an ion source[J].J Anal At Spectrom,1992,7:571-575.
[12]蒋少涌.过渡族金属元素同位素分析方法及其地质应用[J].地学前缘,2003,10(2):269-278.
[13]赵墨田,曹永明,陈 刚,等.无机质谱概论[M].北京:化学工业出版社,2006.
[14]DELAETER J R,BÖHL KE J K,DE BIÈVRE P,et al.Atomic weights of the elements:Re-ciew 2000[J].Pure Appl Chem,2003,6(75):683-800.
[15]任邦方,凌文黎,张军波,等.Zn同位素分析方法及其地质应用[J].地质科技情报,2007,26(6):30-35.
[16]王 军,赵墨田.同位素稀释热电离质谱法测定人血清中痕量铜和锌[J].分析化学,2006,34(3):355-358.
[17]MASON T F D,WEISS D J,CHAPMAN J B,et al.Zn and Cu isotopic variability in the Alexandrinka volcanic-hosted massive sulphide(VHMS)ore deposit,Urals,Russia[J].Chemical Geology,2005,221(3/4):170-187.
[18]BORRO K D M,WANTY R B,RIDL EY W I,et al.Separation of copper,iron and zinc from complex aqueous solutions for isotopic measurement[J].Chemical Geology,2007,242(3/4):400-414.
[19]BERMIN J,VANCE D,ARCHER C,et al.The determination of the isotopic composition of Cu and Zn in seawater[J].Chemical Geology,2006,226(3/4):280-297.
[20]邓中国,高鼎顺.锌同位素比值和含量的双稀释质谱测量法[J].核化学与放射化学,1994,16(3):142-150.
[21]王 军,赵墨田.热表面电离质谱精确测定人体排泄物中锌同位素丰度比[J].质谱学报,2000,21(3/4):187-188.
[22]周 涛,王 军,逮 海,等.同位素稀释多接收电感耦合等离子体质谱法测量红酒中的痕量铁[J].原子能科学技术,2009,43(11):992-996.
[23]ARCHER C,VANCE D.Mass discrimination correction in multiple-collectorplasma source mass spectrometry:An example using Cu and Zn isotopes[J].JAnal AtSpectrom,2004,19:656-665.
[24]CHANG T L,ZHAO M T,LI W J,et al.Absolute isotopic composition and atomic weight of zinc[J].International Journal of Mass Spectrometry,2001,208(1/2/3):113-118.
[25]ZHU X K,GUO Y,WILLIAMS R J P,et a1.Mass fractionation processes of transition metal isotopes[J].Earth and Planetary Scfence Letters,2002,200(1/2):47-62.
[26]WEISS D J,MASON T F D,KIRK GJ D,et al.Isotopic discrimination of zinc in higher plants[J].New Phytologist,2005,165(3):703-710.
[27]GÉLABERT A,POKROVSKY O S,VIERS J,et al.Interaction between zinc and freshwater and marine diatom species:Surface complexation and Zn isotope fractionation[J].Geochimica et Cosmochimica Acta,2006,70(4):839-857.
[28]BORRO K D M,NIMICK D A,WANTY R B,et al.Isotopic variation of dissolved copper and zinc in stream waters affected by historical mining[J].Geochimica et Cosmochimica Acta,2008,72(2):329-344.
[29]MARÉCHAL C N,SHEPPARD S M F.Isotope fractionation of Cu and Zn between chloride and nitrate solutions and malachite or smithsonite at 30℃and 50℃[J].Geochimica et Cosmochimica Acta,2002,66:S484.
[30]BALISTRIERI L S,BORROKD M,WANTY R B,et al.Fractionation of Cu and Zn isotopes during adsorption onto amorphous Fe(III)oxyhydroxide:Experimentalmixing ofacid rock drainage and ambient river water[J].Geochimica et Cosmochimica Acta,2008,72(2):311-328.
[31]MARÉCHAL C,ALBARÈDE F.Ion-exchange fractionation of copper and zinc isotopes[J].Geochimica et Cosmochimica Acta,2002,66(9):1 499-1 509.
[32]PICHA T S,DOUCH ET C,ALBARÈDE F.Zinc isotope variations in deep-sea carbonates from the eastern equatorial Pacific over the last 175 ka[J].Earth and Planetary Science Letters,2003,210(1/2):167-178.
[33]CHEN J,GAILLARDET J,LOUVAT P.Zinc isotopes in the Seine river waters,France:A probe of anthropogenic contamination[J].Environ Sci Technol,2008,42(17):6 494-6 501.
[34]TURNIUND J R,KINGJ C,KEYES W R,et al.A stable isotope study of zinc absorption in young men:effects of phytate and a-cellulose[J].The American Journal of Clinical Nutrition,1984,40(5):1 071-1 077.
[35]EGLI I,DAVIDSSON L,ZEDER C,et al.Dephytinization of a complementary food based on wheat and soy increases zinc,but not copper,apparent absorption in adults[J].J Nutria,2004,134(5):1 077-1 080.

