对苯二甲酸与1,4 -环己烷二甲醇直接酯化反应的研究
蔡智怡,黄关葆
(北京服装学院材料学院,北京100029)
对苯二甲酸与1,4 -环己烷二甲醇直接酯化反应的研究
蔡智怡,黄关葆*
(北京服装学院材料学院,北京100029)
研究了对苯二甲酸(TPA)与1,4环己烷二甲醇(CHDM)的直接酯化反应,讨论了酸/醇配比、催化剂用量对酯化反应的程度、反应时间的影响,对实验过程及动力学处理方法进行了分析探讨,并对实验结果进行了相应的整理,得到了该反应的动力学参数,确定了较佳的工艺条件。此外,在相同酸/醇配比和催化剂用量时还进行了TPA与乙二醇(EG)的直接酯化实验并进行了酯化动力学分析。结果表明,较佳的工艺条件为酸/醇比1∶1.6,催化剂用量0.035%(占TPA质量比,下同);TPA与CHDM的直接酯化反应比TPA与EG的反应对温度的敏感程度低,反应时间短、活化能小。
对苯二甲酸;1,4环己烷二甲醇;酯化反应;动力学;工艺条件
0 前言
1 实验部分
1.1 主要原料
TPA,纤维级,中国石化天津分公司;
CHDM,化学纯,江苏康恒化工有限公司;
EG,纤维级,中国石化天津分公司;
钛酸正四丁酯,分析纯,北京嘉仕腾贸易有限责任公司。
1.2 样品制备
采用钛系催化剂常压酯化法,反应原料投入三口烧瓶中,纯间歇(无底料),电热套加热控温;投料阶段:由于常温下CHDM为固态,因此预先将CHDM加热至70~80℃,待固体完全融化后再投进三口烧瓶,随后,将粉末颗粒状的TPA投入到已融化的CHDM熔体中,反应过程中生成的水和蒸馏出的CHDM经过刺形冷凝管冷凝、分离,再通过冷凝管收集副产物水,当第一滴水滴下时反应开始计时,每隔5min记录一次反应时间、反应内温、塔顶温度及出水量;随着酯化反应的进行,反应内温逐渐上升,顶温始终保持在100℃左右,当内温达到270~278℃、酯化率为95%左右时,反应液呈现清晰态,此处记为“清晰点”;反应继续进行,待塔顶温度开始下降,即没有水生成时,反应达终点,瓶内产物为对苯二甲酸1,4环己烷二甲醇酯(BHCT);
酸/醇配比(TPA/CHDM)的影响:本文的酯化实验中,固定催化剂用量为0.03%,研究酸/醇配比的变化范围为1∶1.4~1∶1.9;
催化剂用量的影响:固定酯化实验的酸/醇配比为1∶1.6,改变催化剂用量分别为0.03%、0.035%、0.04%。
1.3 动力学模型的建立
1.3.1 动力学模型的基本假设
TPA与CHDM的直接酯化反应在液相中进行,初期TPA以固态粉末状悬浮在CHDM中,随着搅拌和温度升高,只有少量TPA溶解在CHDM中直至达到饱和状态。随着反应的进行,溶液中已溶解的TPA不断参与反应,固相中TPA又不断地溶解补充到液相中参与反应,直至固态TPA全部溶解,体系物料颜色呈清晰态,反应到达“清晰点”。因此,在“清晰点”前,整个体系处于一种TPA溶解的动态平衡过程中,反应体系宏观上是非均相的。反应器内悬浮态TPA的量逐渐减少到全部溶解时,反应体系由非均相变为均相,即“清晰点”,本体系中,此时的酯化率约为95%。遵循前人对聚对苯二甲酸乙二醇酯(PET)的动力学研究成果[7-8],本文对“清晰点”前,TPA 与 CHDM 的酯化过程作如下基本假设:
(1)固相TPA的溶解速率比TPA的反应速率快,“清晰点”前只有少部分TPA溶解在液相混合物中,整个体系为溶解与反应的动态平衡过程,反应溶液始终处于饱和状态且液相体积不变;
(2)反应只在液相中进行,只有溶解的TPA参与反应,未溶解的固态TPA对反应不产生影响;
(3)由于“清晰点”前,体系始终是TPA的饱和溶液,且假设反应符合官能团等活性原则,因此反应的表观速度与反应物浓度无关,只是温度的函数;
(4)忽略逆反应和其他反应对主反应的影响。
1.3.2 动力学模型的建立
根据上述基本假设,对于“清晰点”前的反应动力学按零级方程处理,TPA直接酯化的反应速率方程式为:

式中 Np——TPA的量,mol
V——液相体积,dm3
t——反应时间,min
Cp——TPA在液相中的浓度,mol/dm3
Cc——CHDM 在液相中的浓度,mol/dm3
k1——酯化反应的速率常数
依据官能团等活性理论和TPA在液相中始终处于饱和状态,即TPA在液相中的浓度为一常数,因此Cp为常数,令k1Cp=k2,则式(1)为:
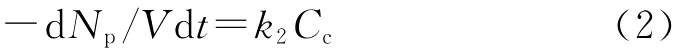
再令,

式中 Np0——TPA的初始量,mol
X——反应酯化率,X=实际出水量/理论出水量
又有每次反应对TPA的投料为1mol,因此式(2)变为:

因此,零级反应模型为:
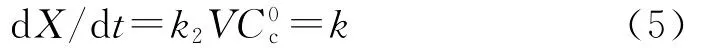

对式(6)求一阶导数,即可得:

根据上文的基本假设,以零级处理得到的dX/dt=k,带入不同t值可求得各个时刻对应的k。
根据Arrhenius方程k=k0exp(-Ea/RT),经过处理得lnk=lnk0-Ea/RT,再将lnk对1/T作图,由斜率即可求出此酯化反应的表观活化能(Ea)。活化能结果对于加深对反应机理的理解、合理设定或调整反应工艺条件有重要的指导意义。
2 结果与讨论
2.1 酸/醇配比对酯化反应的影响
如表1所示,投料的酸/醇比为1∶1.5和1∶1.4时,酯化反应的酯化率为0.96和0.97,TPA没有完全酯化,反应进行得不彻底。且多次重复实验,实验室条件下酯化率均不能达到1。从图1可以看出,完成化学反应(酯化率为1)时,酸/醇比为1∶1.6所需反应时间最短,且反应完全。因此,本文确定选用1∶1.6的酸/醇配比进行后续的实验研究。

表1 酸/醇比对酯化反应的影响Tab.1 Effects of the molar ratio of TPA and CHDM on esterification
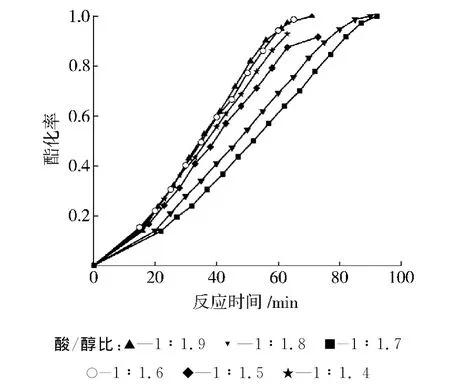
图1 不同酸/醇比时酯化率与时间的关系Fig.1 Relationship between esterification rate and reaction time at different molar ratio of TPA and CHDM
2.2 催化剂用量对酯化反应的影响
如表2所示,酸/醇配比为1∶1.6,改变催化剂用量对反应时间有一定的影响,即随着催化剂用量的增加,酯化反应时间减少,催化剂用量为0.035%时,酯化反应所需的时间最短。继续增加催化剂含量对于缩短反应时间的作用并不十分明显。同时,催化剂对同一温度下酯化率的高低也有影响,如图2所示,反应随着催化剂用量的增加,生成第一滴水的温度降低。同一温度下,催化剂含量高时酯化率也高。重复实验多次,均得到上述结果。

表2 催化剂用量对酯化反应的影响Tab.2 Effects of contents of catalyst on the esterification

图2 不同催化剂用量时酯化率与温度(T)的关系Fig.2 Relationship between esterification rate and reaction temperature at different contents of catalyst
2.3 TPA直接酯化的动力学分析
本文利用1.3.2中的动力学模型的建立,分别对不同催化剂用量的酯化反应进行动力学处理,如图3、4和表3所示,选取催化剂用量为0.035%的反应无论是在反应时间上还是在活化能上都占有一定的优势。酸/醇比为1∶1.6、催化剂用量为0.035%的条件下,反应所需时间短,反应活化能小,酯化效率也高。此动力学计算结果也验证了3.2中的分析。此外,本文还将无催化剂的TPA与EG进行酯化反应,并做动力学处理,所得活化能为35.03kJ/mol。

图3 不同催化剂用量时酯化率与时间的关系Fig.3 Relationship between esterification rate and reaction time at different contents of catalyst

表3 不同催化剂用量时的动力学方程Tab.3 Kinetic equation of the esterification at different contents of catalyst

图4 不同催化剂用量时的lnk1/T 曲线Fig.4 Plots of lnkversus 1/Tat different contents of catalyst
2.4 PET与PCT的直接酯化阶段的活化能比较
本文对TPA和EG进行酯化实验(9#),选择酸/醇比1∶1.6、催化剂(钛酸正四丁酯)含量为0.03%,生成对苯二甲酸乙二醇酯(BHET)。同样按零级反应进行动力学处理,所得PET酯化阶段的表观活化能为101.027kJ/mol,与4#样品的比较如表4所示。经比较得出,TPA与CHDM的直接酯化反应比TPA与EG的反应对温度的敏感程度低,反应时间短,活化能小。

表4 PCT与PET的酯化反应的活化能比较Tab.4 Comparison of activation energies between PCT and PET
3 结论
(1)PCT的直接酯化合成中,在反应到达“清晰点”前,按零级反应建立动力学模型,符合实际反应;
(2)TPA与CHDM直接酯化的较佳工艺条件为:酸/醇比1∶1.6,催化剂用量0.035%;
(3)在上述较佳工艺条件下,TPA与CHDM的酯化反应活化能为15~20kJ/mol,酯化时间小于100min;而同样工艺合成PET时,TPA与EG的酯化反应活化能约为100kJ/mol,酯化反应时间大于400min。
[1] 陈 洵.PCT制造加工和应用进展[J].企业技术开发,2000,(1):4.
[2] 刘春秀,于德之,周 良.PCT及其共聚酯的开发概括及应用[J].聚酯工业,2005,18(4):8-10.
[3] 喻爱芳,蒋 瑜,李文刚,等.新型耐高温聚酯PCT[J].合成技术及应用,2004,19(3):31-35.
[4] 王 源.PET-PCT共聚酯及其离聚物的制备及结构与性能[D].上海:东华大学材料科学与工程学院,2007.
[5] 喻爱芳,蒋 瑜,李文刚,等.新型耐高温聚酯PCT的等温结晶性能研究[J].功能材料,2004,35:3379-3382.
[6] Howell,Earl,Edmondson J R.Process for Manufacture of Polyesters Based on 1,4-cyclohexanedimethanol and Isophthalic Acid:US,WO02057334[P].2002-07-25.
[7] 张旭霞,汪少朋,杨立英.TPA直接酯化过程动力学的研究[J].合成纤维工业,2003,26(6):15-17.
[8] 王新兰,王利生.高温聚酯化反应动力学的研究[J].高分子材料与工程,2002,18(4):34-41.
Study on Direct Esterification of Terephthalic Acid and 1,4-Cyclohexanedimethanol
CAI Zhiyi,HUANG Guanbao*
(School of Materials Science &Engineering,Beijing Institute of Fashion Technology,Beijing 100029,China)
In this research,the effects of the molar ratio of TPA/CHDM and the mass ratio of catalyst on the esterification extent and reaction time were studied.Based on the systematic experiments,the esterification kinetics equation and activation energy were obtained.For comparison,the esterification of TPA and EG was also studied at the same conditions.It showed that the best recipes were TPA/CHDM=1∶1.6,and the content of catalyst was 0.035%.It also found that the activation energy,reaction time of the reaction between TPA and CHDM was lower than those of TPA and EG,and the effect of temperature on the reaction between TPA and CHDM was also moderate.
terephthalic acid;1,4-cyclohexanedimethanol;esterification;kinetics;processing
TQ316.37
B
1001-9278(2011)08-0034-04
2011-04-28
*联系人,guanbaohuang@sina.com

