HPLC-ELSD法测定散结镇痛片中贝母素甲、贝母素乙
唐 云, 刘汉清
(南京中医药大学,江苏南京210046)
散结镇痛片是由同方 (三七、浙贝母、龙血竭、薏苡仁)全粉末胶囊剂改制而成的半膏片,用于子宫内膜异位症所致的继发性痛经、月经不调、盆腔包块和不孕等病症,疗效确切。主药三七的质控研究已另文发表[1],本实验对散结镇痛片的贝母素甲、贝母素乙的定量测定进行研究,为进一步完善其质控指标提供实验依据。
1 仪器、对照品与试剂
1.1 仪器 Waters 2695液相色谱仪,Waters2420 ELS Detector(Waters科技有限公司);BP211D电子天平 (十万分之一);SYZ-A石英亚沸高纯水蒸馏器 (江苏信达仪器厂);HH-4数显电子恒温水浴锅 (江苏金坛市晶玻实验仪器厂)。
1.2 对照品 贝母素甲 (批号1022-050123)、贝母素乙 (批号110751-200504),均购自中国药品生物制品检定所,供定量测定用。
1.3 试剂 乙腈、甲醇 (色谱纯,购自美国 Honeywell公司),乙醇、盐酸、三氯甲烷等 (分析纯,购自上海化学试剂有限公司)。
2 散结镇痛片及其阴性样品制备
2.1 饮片 浙贝母、三七、薏苡仁、龙血竭 (购自安徽亳州),经南京中医药大学王春根教授鉴定,均符合《中国药典》相关标准[2-3]。
2.2 散结镇痛片制备 取处方量龙血竭 (124 g)粉碎,过100目筛,备用;另取浙贝母 (200 g)、三七 (124 g)、薏苡仁 (352 g)粉碎成粗粉,用90%乙醇回流提取两次,每次10倍量提取2 h,合并滤液,减压回收乙醇,并浓缩至相对密度为1.00~1.10(50℃)的稠膏;所得稠膏与龙血竭细粉混匀,减压干燥,粉碎成细粉,加适量淀粉混匀,制粒,干燥,加0.5%硬脂酸镁,混匀,压制成1 000片 (0.3 g/片)(制备工艺研究另文发表)。3批 供 试 品 批 号 分 别 为 20100801、20100802、20100803。
2.3 缺浙贝母散结镇痛片制备 取处方比例量龙血竭 (124 g)粉碎,过100目筛,备用;另取处方比例量三七 (124 g)、薏苡仁 (352 g)粉碎成粗粉,用90%乙醇回流提取两次,以下制法同散结镇痛片制备方法。
3 方法与结果
3.1 供试液的制备
3.1.1 混合对照品贮备液的制备 精密称取贝母素甲、贝母素乙对照品适量,置50 mL量瓶中,加甲醇至刻度,制得质量浓度为每1 mL含贝母素甲0.340 4 mg、贝母素乙0.246 4 mg的混合对照品贮备液。
3.1.2 供试品溶液的制备 取散结镇痛片研细(过80目),取2.0 g,精密称定,置锥形瓶中,精密加入含1%HCl的30%乙醇溶液100 mL,精密称定,超声1 h,放冷,再称定质量,用含1%HCl的30%乙醇溶液补足减失的质量,摇匀,离心,精密量取上清液75 mL置250 mL分液漏斗中,加氨水15 mL,用三氯甲烷250 mL萃取5次,每次50 mL,合并三氯甲烷液,水浴蒸干,残渣加甲醇溶解并转移至5 mL量瓶中,加甲醇至刻度,摇匀,即得。
3.1.3 缺浙贝母阴性溶液的制备 取缺浙贝母散结镇痛片研细 (过80目),取2.0 g,照供试品溶液制备方法制备,即得。
3.1.4 浙贝母溶液的制备 取浙贝母粉末约2 g,精密称定,置烧瓶中,加浓氨试液4 mL浸润1 h,精密加入三氯甲烷-甲醇 (4∶1)的混合溶液40 mL,称定质量,混匀,置80℃水浴中加热回流2 h,放冷,再称定质量,加上述混合溶液补足减失的质量,滤过。精密量取续滤液10 mL,置蒸发皿中蒸干,残渣加甲醇溶液溶解并转移至2 mL量瓶中,加甲醇至刻度,摇匀,即得。
3.2 方法学考察
3.2.1 系统适应性[4-13]Thermo Hypersil Gold C18ODS色谱柱 (5 μm,4.6 mm×250 mm);流动相为乙腈-0.06%二乙胺溶液 (70∶30);蒸发光散射检测器;体积流量1.0 mL/min;柱温30℃;载气体积流量2.2 L/min;漂移管温度85.0℃;进样量10 μL。理论板数按贝母素甲峰计算,应不低于5 000。
3.2.2 专属性考察 取混合对照品溶液、供试品溶液、阴性样品溶液、药材溶液,按3.2.1项下方法测定,结果表明,贝母素甲、贝母素乙峰与其他色谱峰分离度均大于1.5,达到基线分离,阴性无干扰,结果见图1。
3.2.3 线性关系考察 分别精密量取混合对照品贮备液0.5、1、2、4、6、8、10 mL置10 mL量瓶中,加甲醇稀释至刻度,即得各质量浓度混合对照品溶液,按3.2.1项下方法测定,分别将峰面积及相应的进样量取以10为底的对数,经EXCEL线性回归,以峰面积的对数 (Y)为纵坐标,进样量的对数 (X)为横坐标,得贝母素甲回归方程为:Y=1.532 5X+1.117 8,相关系数r=0.999 7;得贝母素乙回归方程为:Y=1.525 3X+1.065 6,相关系数r=0.999 4。贝母素甲、贝母素乙分别在170.2~3 404 ng、123.2~2 464 ng范围内具有良好的线性关系。
3.2.4 精密度实验 取散结镇痛片 (批号20100801)适量,研细 (过80目),精密称定,按3.1.2项下方法制得供试品溶液,照3.2.1项下方法,重复进样5次,结果贝母素甲峰面积分别为823 695、 814 818、 807 731、 818 070、 807 928;贝母素乙峰面积分别为305 308、307 020、294 844、298 209、298 231,以峰面积计算进样精密度,RSD分别为0.84%、1.73%,表明仪器的精密度良好。
3.2.5 稳定性实验 取散结镇痛片 (批号20100801)适量,研细 (过80目),精密称定,按3.1.2项下方法制得供试品溶液,照3.2.1项下方法分别在0、1、2、4、6、8、12 h进样,结果贝母素甲峰面积分别为813 695、807 731、807 928、815 293、802 256;贝母素乙峰面积分别为300 308、294 844、298 231、301 566、295 032,以峰面积计算,结果贝母素甲、贝母素乙的RSD分别为0.65%、1.02%,表明供试品溶液在12 h内稳定。

图1 样品 (A)、阴性样品 (B)、浙贝母药材 (C)和混合对照品溶液 (D)HPLC-ELSD色谱图Fig.1 HPLC chromatograms of sample(A),negative sample(B),Fritillariae thunbergii Bulbus(C)and reference substance(D)
3.2.6 重复性试验 取散结镇痛片适量,研细(过80目),平行取6份,分别精密称定,按3.1.2项下方法制得供试品溶液,照3.2.1项下方法测定,采用外标两点法计算质量分数,结果贝母素甲的质量分数分别为 0.397、0.396、0.396、0.396、0.393、0.388 mg/g,贝母素乙的质量分数分 别 为 0.240、0.238、0.235、0.239、0.242、0.239 mg/g,两者的平均质量分数分别为0.394 mg/g、0.239 mg/g,RSD分别为0.90%、1.05%,表明本方法重复性良好。
3.2.7 加样回收实验 取散结镇痛片适量,研细(过80目),平行取9份,每份1.0 g,精密称定。每3份为1组,按重复性中贝母素甲、贝母素乙含有量的0.8倍、1.0倍、1.2倍,分别准确加入贝母素甲对照品、贝母素乙混合对照品溶液 (贝母素甲、贝母素乙质量浓度分别为0.40 mg/mL、0.24 mg/mL),精密加入含1%HCl的30%乙醇溶液至100 mL,精密称定,按3.1.2项下方法制得供试溶液,照3.2.1项下方法测定,采用外标两点法计算含有量,结果见表1~2。
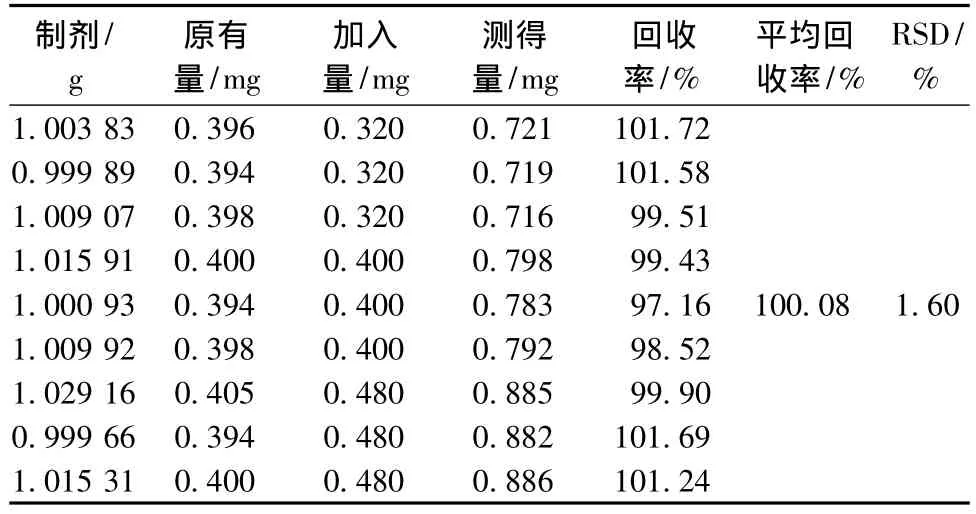
表1 贝母素甲回收率测定结果Tab.1 Recovery test results of verticine

表2 贝母素乙回收率测定结果Tab.2 Recovery test results of verticinone
3.3 供试品测定 取3批供试品,每批平行3份,按3.1.2项下方法制得供试品溶液,照3.2.1项下方法测定,采用外标两点法计算含量,结果见表3。
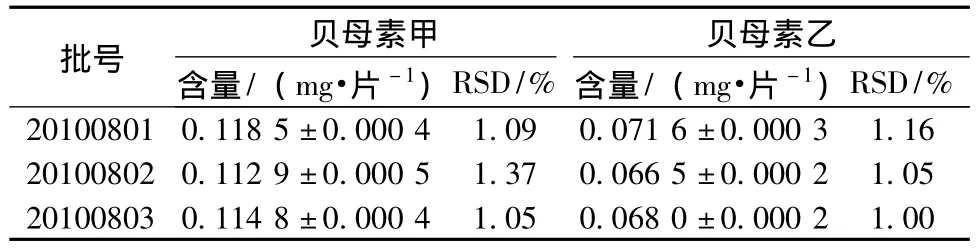
表3 样品中贝母素甲、贝母素乙测定结果(n=3)Tab.3 Contents of verticine and verticinone in tablets(n=3)
4 讨论
4.1 文献关于浙贝母成分贝母素甲、贝母素乙含有量测定样品制备的报道[4-19],多采用浓氨试液浸润,再加入三氯甲烷-甲醇 (4∶1)混合溶液提取的方法。实验亦曾按此法进行,但因龙血竭、薏苡仁等成分干扰,提取液中有黏液状团块出现,抽滤、离心较困难,所得样品测定结果平行性不佳。本实验采用低浓度酸醇提取,氨水碱化后三氯甲烷萃取的方法能制得理想供试品溶液,测定结果稳定。且经对比试验发现,文献处理方法与本实验所采用的提取方法,无论贝母药材或本制剂,2种方法贝母素甲和贝母素乙的含量测定结果一致。本方法不仅可用于本制剂,也可作为浙贝母药材生物碱提取处理的新方法。
4.2 实验中采用乙腈-0.06%二乙胺溶液 (70∶30)为流动相,在研究过程中发现,二乙胺在作为改性剂应用时蒸馏后使用为佳,直接使用或用量较大时基线容易出现较大的波动。
[1]唐 云,倪玮烨,束志凌.HPLC法测定散结镇痛胶囊中三七皂苷R1、人参皂苷Rg1及人参皂苷Rb1的含量[J].药学进展,2009,33(7):328-329.
[2]国家药典委员会.中华人民共和国药典:2010年版一部[S].北京:中国医药科技出版社,2010:274-275,11-12,353-354.
[3]WS3-082(Z-016)-99(Z)[S]//新药转正标准:第22册.北京:人民卫生出版社,1999:651-652.
[4]姜 艳,李 萍.HPLC-ELSD测定浙贝母中贝母素甲、贝母素乙含量[J].中国药学杂志,2005,40(16):1257-1259.
[5]刘红宁,颜冬梅.HPLC-ELSD测定彭泽贝母中浙贝甲素和浙贝乙素[J].中草药,2006,37(4):600.
[6]韩 静,丁永辉,宋平顺.HPLC-ELSD法同时测定平贝母中贝母素甲、贝母素乙的含量[J].中国药师,2009,12(5):595-597.
[7]张东杰,张爱武,王丽杰.HPLC-ELSD法测定平贝母中贝母素甲、贝母素乙含量[J].中草药,2009,9(2):194-199.
[8]薛 燕,顾好粮.HPLC-ELSD法测定浙贝母中主要生物碱的含量[J].药学学报,2005,40(6):550-552.
[9]刘汉珍,戴云志.HPLC法同时测定皖贝母2种生物碱成分含量[J].中国林副特产,2006(6):18-20.
[10]王 曙,徐小平,李 涛.川贝母与其他贝母类药材总生物碱和总皂苷的含量测定与比较[J].中国中药杂志,2002,27(5):342-344.
[11]高光伟,张建业,冯向东.HPLC-ELSD法测定复方川贝母片中贝母素甲的含量[J].中国药师,2010,13(6):833-835.
[12]张 洁,李成网.HPLC-ELSD法测定皖贝止咳胶囊中贝母素甲和贝母素乙的含量[J].中国实验方剂学杂志,2009,15(5):3-5.
[13]王 玥,张庆林,陈信义,等.HPLC法测定市售贝母中贝母乙素含量[J].中草药,2001,32(1):24-25.
[14]薛 燕,王 峰.不同产地浙贝母药材中3种活性成分的分析研究[J].中国中药杂志,2007,32(16):1628.
[15]俞 滢,朱亚尔.HPLC-MS测定癃闭康泰片中贝母素甲、贝母素乙的含量[J].中国药学杂志,2006,41(13):1026-1028.
[16]程显隆,肖新月,张南平,等.HPLC-MS法测定中药材浙贝母中贝母素甲、贝母素乙的含量[J].中国药师,2008,11(7):770-772.
[17]王冲之,孙 健,李 萍.贝母类药材生物碱及生物碱苷含量测定方法学研究[J].中国药学杂志,2003,38(6):415-418.
[18]于海英,程秀民,王晓坤,等.三相静态萃取HPLC鉴别五种贝母的研究[J].中药材,2008,31(2):210-213.
[19]李 萍,曾令杰,李松林.无紫外吸收的贝母总生物碱定量分析方法研究[J].中国药学杂志,2002,37(8):614-617.

