长春新碱固体脂质纳米粒的制备工艺优化*
夏爱晓,孙 渊,马红丹
(浙江省台州医院药剂科,浙江 台州 317000)
长春新碱(vincristin,VCR)用于治疗急性淋巴细胞性白血病,疗效较好[1],但神经毒性大,且对光不稳定,临床使用不便。靶向制剂可降低长春新碱的神经毒性,并提高其体外稳定性,从而提高疗效,这将是今后新剂型的研究趋势。固体脂质纳米粒(solid lipid nanoparticles,SLN)能将药物包裹于类脂核中而使药物稳定性增加,并可改变被包封药物的体内分布,使药物主要在骨髓、脾、肺和肝等组织器官中积蓄,从而提高药物的治疗指数,具有缓控释、靶向、低毒等优点[2-3]。笔者在单因素考察的基础上,采用L9(34)正交表设计试验,优化处方组成和制备工艺,为开发长春新碱新型制剂提供试验基础。
1 仪器与试药
Waters高效液相色谱仪,TU-1901型双光束紫外可见光分光光度计(北京普析通用仪器有限责任公司);N4 PLUS型纳米粒度分析仪(美国贝克曼库尔特有限公司);日立H-7500型透射电子显微镜(日本Hitachi公司);AF100 Scotsman型制冷机(美国斯科茨曼公司);AL104型电子天平(梅特勒-托利多仪器有限公司);SB25-120超声波清洗器(宁波新芝生物科技股份有限公司);88-1型定时恒温磁力搅拌器(上海司乐仪器厂);Soniprep 150型超声细胞粉碎仪(英国SANYO公司);pHS-3C pH酸度计(上海雷磁公司)。硫酸长春新碱(海南长春花药业有限公司,含量为97.7%);单硬脂酸甘油酯(上海华精生物高科技有限公司);硬脂酸(德国Cognis公司);大豆卵磷脂(杭州宏博生物工程有限公司);泊洛沙姆188(德国BASF公司);甲醇为色谱纯,其他试剂均为分析纯。
2 方法与结果
2.1 长春新碱含量测定(高效液相色谱法)
2.1.1 色谱条件[4]
色谱柱:Hypersil ODS2 C18柱(200 mm ×4.6 mm,5 μm);流动相:甲醇 -水 -三乙胺(140∶60∶1,磷酸调 pH至=7.0);流速:1.0 mL/min;检测波长:297 nm;柱温:室温;进样量:20 μL。
2.1.2 方法学考察
标准曲线绘制:称取长春新碱对照品1.00 mg,精密称定,置10 mL容量瓶中,用蒸馏水溶解并定容至刻度,作为对照品贮备液。精密量取5.0 mL置50 mL容量瓶中,用75%甲醇定容至刻度,得质量浓度为 0.5,1.0,1.5,2.0,2.5,3.0,5.0 μg/mL 的对照品溶液。按2.1.1项下色谱条件进样,记录峰面积,以长春新碱质量浓度为横坐标、峰面积为纵坐标进行线性回归,得回归方程A=12274 C -2682.3,r=0.9999(n=7)。结果表明,长春新碱质量浓度在0.5~5.0 μg/mL范围内与峰面积线性关系良好。
回收率试验:精密量取空白固体脂质纳米粒2.0 mL共3份,置10 mL容量瓶中,加入对照品溶液适量,用75%甲醇定容,超声处理后,得质量浓度为 0.5,1.5,5.0 μg/mL 的溶液,滤过,取续滤液进样测定,计算回收率。结果表明,低、中、高3种质量浓度溶液的回收率均在98% ~102%之间,平均 RSD为1.6%,说明方法准确度良好,符合方法学要求。
精密度试验:取质量浓度为 1.0,2.0,5.0 μg/mL 的对照品溶液,分别于1 d内重复进样5次和5 d内每天进样1次。结果日内精密度的 RSD=1.18%,日间精密度的 RSD=1.38%。
2.2 包封率和载药量测定[5]
精密吸取长春新碱固体脂质纳米粒(VCR-SLN)1.0 mL,置处理过的透析袋中,两端扎紧,置50.0 mL的重蒸水中,磁力搅拌2.5 h后,精密量取透析袋外液,测定其中游离药物的含量 C1;另外精密吸取等量的VCR-SLN混悬液,75%甲醇定容至刻度,超声时纳米粒充分破碎,测定长春新碱含量 C2。包封率(EE,%)=(1-C1/C2)×100% ,载药量(DL,%)=(EE% ×Wp)/W总×100%。其中,Wp为制剂中长春新碱的含量,W总为制剂中脂质材料和药物的总质量。
2.3 单因素考察
2.3.1 载体材料筛选
精密称取基质(单硬脂酸甘油酯或硬脂酸)200.0 mg,加热溶于无水乙醇,得有机相;精密称取大豆卵磷脂100.0 mg,制成水溶液,作为内水相,第1次超声(600 W,6 min)乳化,形成W/O初乳;加外水相(含表面活性剂1%泊洛沙姆188),第2次超声(600 W,3 min)乳化,形成W/O/W复乳,通氮气下超声挥发有机溶剂。用超声细胞破碎仪于冰浴条件、7 AM振幅下破碎10 min,再加入到稀释水相(蒸馏水0~2℃)中,即得。冰箱保存,放置1周,留样观察其稳定性。结果以单硬脂酸甘油酯为载体材料时无沉淀现象,略带蓝色乳光;以硬脂酸为载体材料时出现沉淀现象,较混浊。故选择单硬脂酸甘油酯作为载体。
2.3.2 乳化剂筛选
称取单硬脂酸甘油酯200.0 mg,共3份,加热溶于无水乙醇,得有机相,以处方量的大豆卵磷脂水溶液为内水相,第1次超声(600 W,6 min)乳化,形成W/O初乳;加外水相(含不同种类乳化剂),第2次超声(600 W,3 min)乳化,形成W/O/W复乳,通氮气下超声挥发有机溶剂。用超声细胞破碎仪于冰浴条件、7 AM振幅下破碎10 min,再加入到稀释水相(蒸馏水0~2℃)中即得。冰箱保存,放置1周,留样观察其稳定性。结果以卵磷脂-泊洛沙姆188(1∶2)为乳化剂时溶液较透明,略带蓝色乳光;以卵磷脂-泊洛沙姆188-Tween-80(1∶2∶1)为乳化剂时溶液略呈黄色,放冷后较混浊;以卵磷脂 -泊洛沙姆188-Tween-80(1∶1∶1)为乳化剂时溶液略呈黄色,出现少许沉淀,较混浊。因此,选卵磷脂-泊洛沙姆188(1∶2)为乳化剂。
2.3.3 制备方法筛选[5-8]
热熔超声法:精密称取处方量泊洛沙姆188和Tween-80,置20.0 mL水中,超声分散均匀,得水相;称取处方量大豆卵磷脂、单硬脂酸甘油酯溶于5.0 mL无水乙醇,得有机相,75℃水浴;将水相加热到与有机相相同温度时注入有机相中,恒温搅拌,制得初乳;趁热将初乳超声,冰水浴冷却、固化2 h,过膜,即得。高温乳化-低温固化法:精密称取处方量泊洛沙姆188和Tween-80,置20.0 mL水中,超声分散均匀,得水相;称取处方量大豆卵磷脂、单硬脂酸甘油酯溶于5.0 mL无水乙醇,得有机相;有机相和水相分别水浴加热至 (75±5)℃,在有机相完全溶解为澄明液体后,搅拌(1000 r/min)下将其倾入水相中,恒温搅拌2 h,使体积挥发至原来的1/3,得初乳;将初乳倾入20.0 mL的1%泊洛沙姆188中,继续搅拌1 h,过膜,即得。
溶剂乳化-超声法:精密称取处方量泊洛沙姆188和Tween-80,置20.0 mL水中,超声分散均匀,得水相;称取处方量大豆卵磷脂、单硬脂酸甘油酯,溶于5.0 mL无水乙醇,得有机相;在超声状态下,将有机相趁热逐滴滴入水相中,通氮气超声挥尽有机溶剂制得初乳,超声细胞粉碎机分散,过膜,即得。
复乳-溶剂扩散法:精密称取处方量的单硬脂酸甘油酯、大豆卵磷脂,溶于无水乙醇为有机相,水为内水相,第一次超声乳化,形成 W/O初乳;加外水相(含表面活性剂1% 泊洛沙姆188),第二次超声乳化,形成W/O/W复乳,然后复乳加入稀释水相(0~2℃)中,分散机分散15 min(10000 r/min),通氮气下超声挥发有机溶剂后,用超声细胞破碎仪在7 AM振幅下破碎10 min,然后复乳加入稀释水相(0~2℃)冷却固化2 h,过膜,即得。
采用浊度法初步评价各种方法制备的VCR-SLN粒径的大小,其原理为脂质材料和乳化剂等在500~800 nm范围内几乎没有吸收,不影响透光率,因此用650 nm处的吸光度值作为体系浊度来间接反映粒子大小。在相同条件下,浊度小者其粒径较小。结果见表1。故采用复乳-溶剂扩散法制备VCR-SLN。
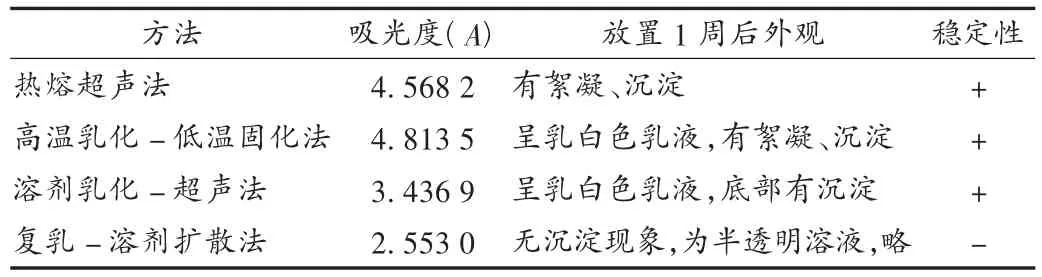
表1 不同制备方法结果比较
2.3.4 破碎振幅和时间考察
复乳-溶剂扩散法制备的空白固体脂质纳米粒分成10份,其中 5份分别在 3,5,8,10,15 AM 超声破碎 6 min,另 5份在 10 AM 下超声破碎时间分别为 1,3,6,8,10 min,用浊度法初步评价SLN粒子大小。确定超声破碎时间为6 min,振幅为8 AM。
2.4 VCR-SLN处方优化
在预试验及单因素考察的基础上,选择长春新碱的用量(因素A)、大豆卵磷脂的用量(因素B)、泊洛沙姆188的用量(因素C)及单硬酸酯甘油酯的用量(因素D)4个因素的3个水平,以SLN包封率、载药量和粒径为指标,优化处方[9]。因素水平见表2。根据以上各因素水平,以VCR-SLN正交L9(34)表进行9次试验,测得平均包封率为36.15%,平均载药量为1.82%,见表3。对试验结果进行直观分析可知,以包封率为衡量指标得出的最佳处方为A3B3C2D2;以粒径为衡量指标得出的最优处方为A3B3C2D1,粒径越小越好。以包封率为主要评价指标,参考粒径,综合分析,最终确定A3B3C2D2为最优处方,即单硬脂酸甘油酯80 mg,长春新碱10 mg,大豆卵磷脂100 mg,泊洛沙姆188150 mg。

表2 正交试验的因素水平表
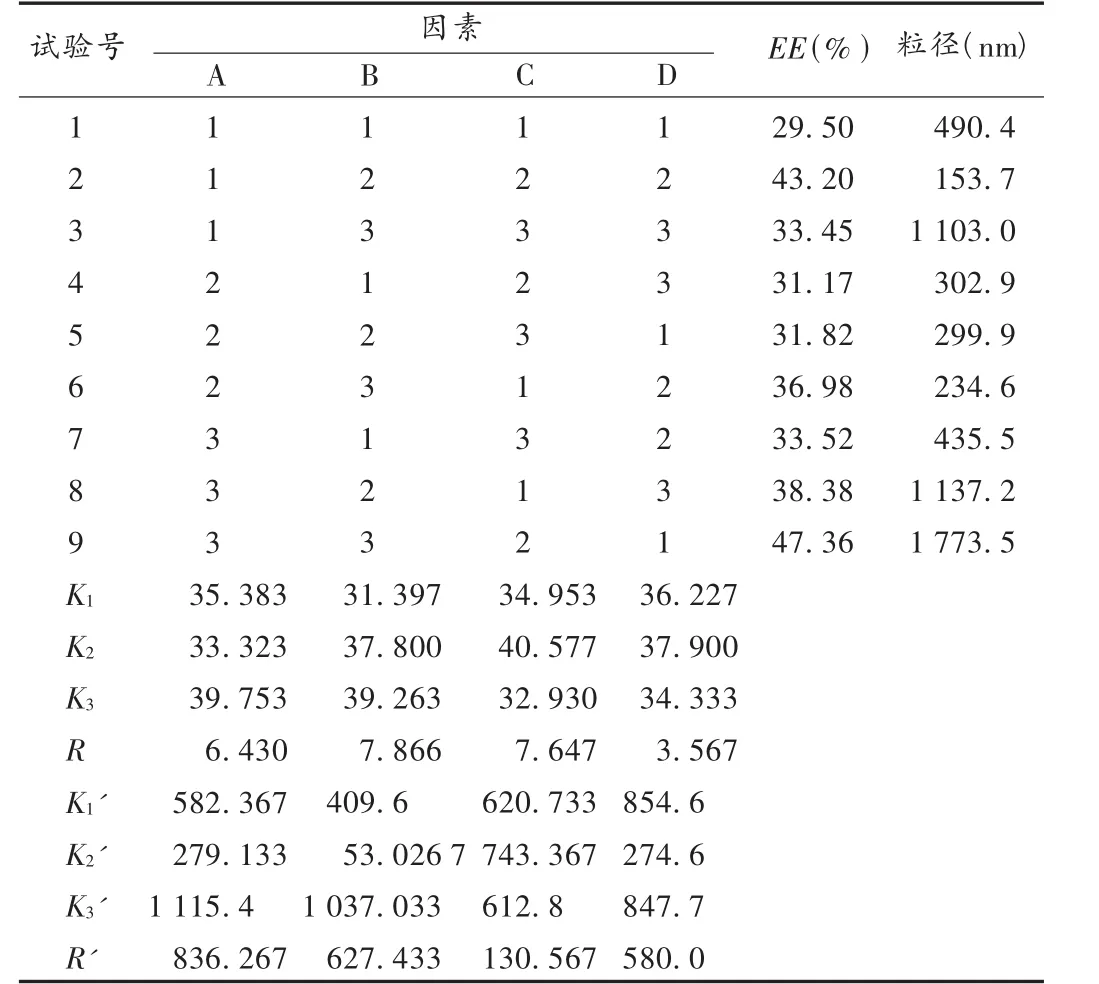
表3 L9(34)正交试验设计及结果
2.5 性质考察
验证性试验:采用复乳-溶剂扩散法,按照优化后的处方制备3批 VCR-SLN,测定粒径、包封率和载药量,平均粒径为(153.7±3.68)nm,包封率为 (55.12 ±1.73)% ,载药量为(3.09 ±0.61)% 。该方法重现性较好。pH 为 5.69 ~6.22,符合静脉注射要求。
外观形态:取VCRSLN适量,加重蒸水稀释,滴于铜网上,用2.0% 磷钨酸进行染色,自然晾干后,透射电镜下观察纳米粒的形态和大小。透射电镜照片见图1,所得制剂为球形或类球形,外观形态较圆整。
粒度及分布:取VCRSLN混悬液,用高纯水稀释调至仪器显示电信号值,折光度为90°,采用N4 PLUS纳米粒度分析仪测定纳米粒粒径(d)。测得粒径为(153.7 ±3.68)nm(n=3),粒度多分散性指数(PI)为0.791。

图1 VCR-SLN透射电镜照片(×100000)
3 讨论
本试验曾尝试用热熔超声法、高温乳化-低温固化法、复乳 -溶剂扩散法,溶剂乳化-超声法等不同方法制备VCRSLN,由于长春新碱为水溶性,见热和光易分解,不易采用热熔和高温等条件,最终确定复乳-溶剂扩散法,且该方法适合水溶性强药物,包封率高。若采用高压匀质机制备水溶性的SLN将更有优势。
骨架脂质的种类是SLN能否形成的关键因素。单硬脂酸甘油酯既可作为一种脂质材料,又是一种弱的W/O型乳化剂,在制备SLN初乳时,能稳定初乳。硬脂酸SLN稳定性明显低于单硬脂酸甘油SLN,可能是由于硬脂酸是直链分子结构,黏度较大,晶格的有序性较高,在贮存过程中易发生晶型转化,产生凝胶化现象[10]。
常用的乳化剂有大豆磷脂、泊洛沙姆、聚山梨酸酯等,都可用来稳定SLN,在制备复乳时,采用泊洛山姆188作为乳化剂。泊洛沙姆188有空间位阻作用,一方面可阻止纳米粒的聚集从而增加其稳定性,另一方面又有避免体内网状内皮系统吞噬的趋势[11]。细胞破碎仪破碎振幅对固体脂质纳米粒有显著影响,在单因素考察中,破碎振幅6 AM,破碎时间8 min,效果最理想,能得到蓝色乳光SLN,且形成的SLN较稳定。由正交试验结果可知,乳化剂卵磷脂的用量对SLN粒径大小影响较大。卵磷脂不仅影响SLN的粒径,对载药SLN的包封率也有较大影响[12]。
SLN包封率测定方法有葡聚糖凝胶柱法、冷冻超速离心法、微型柱法、透析法及超滤法等,其原理均为采用一定的方法使包封的药物和游离药物分离,测定包封或游离药物的浓度,计算包封率。离心法虽然简便但不可靠,不能准确评价包封率的大小。本研究也曾尝试葡聚糖凝胶柱法分离VCR-SLN中的游离药物,试验中采用蒸馏水作为洗脱剂时,由于长春新碱为水溶性,在洗脱过程中SLN在葡聚糖凝胶中容易洗脱,导致包封率过高,且操作烦琐。采用透析法测定VCR-SLN包封率,考察在透析2 h左右游离药物基本达到透析平衡,且在4 h内不发生严重渗漏。为保证透析完全而SLN不渗漏,故选择2.5 h为其透析时间。
由于长春新碱为水溶性,与脂质的结合能力较差,使得VCR-SLN的包封率低于脂溶性好的药物。对于水溶性药物,应根据所载药物的性质选择与其结合力好的脂质和乳化剂进行优化,提高药物的脂溶性,减缓药物的释放[13]。总体来说,本方法制备SLN较适合水溶性药物,适用性广泛。新型给药系统是改善长春新碱不良反应大、生物利用度低的最好方法。目前,长春新碱脂质体虽已进入了临床研究,但其临床耐受性及药物累积毒性仍需密切关注。如何使长春新碱达到更加精确的靶向治疗,进一步降低其不良反应,延长其作用时间,将是长春新碱新型给药系统不断的追求。本研究中成功制备了VCR-SLN,制备工艺简单,考察制剂质量较理想,为进一步开发疗效好、毒性低的长春新碱制剂奠定了基础。
[1]Sikorska A,Slomkowski M,Marlanka K,et al.The use of vinca alkaloids in adult patients with refractory chronic idiopathic thrombocytopenia[J].Clin Lab Haematol,2004,26(6):407-411.
[2]Uner M.Preparation,characterization and physico-chemical properties of solid lipid nanoparticles(SLN)and nanostructured lipid carriers(NLC):their benefis as colloidal drug carrier systems[J].Pharmazie,2006,61(5):375-386.
[3]Sawant KK,Dodiya SS.Recent advances and patents on solid lipid nanoparticles[J].Recent Pat Drug Deliv Formul,2008,2(2):120-135.
[4]赵 妍,邓意辉,孟胜男,等.硫酸长春新碱脂质体的释放度和药效学研究[J].广东药学院学报,2007,23(1):25 -27.
[5]李燕真.吡拉西坦固体脂质纳米粒的制备和脑靶向性研究[D].开封:河南大学,2010.
[6]刘少彬,胡海洋,赵秀丽,等.长春西汀固体脂质纳米粒的制备及其性质考察[J].沈阳药科大学学报,2010,27(5):335-338.
[7]张先洲,陈晓清,潘细贵,等.青藤碱固体脂质纳米粒的制备[J].中国医院药学杂志,2008,28(24):2081-2084.
[8]贾慧卿.地高辛固体脂质纳米粒的制备及其药物动力学研究[D].保定:河北大学,2008.
[9]杜 洋,黄 华,胡 荣.醋酸地塞米松固体脂质纳米粒的制备与处方优化[J].中国医院药学杂志,2009,29(11):888-890.
[10]王 影,宦定才,陆 兵.固体脂质纳米粒的特点及存在问题[J].解放军药学学报,2006,22(1):512 -541.
[11]Cavalli R,Gasco MR,Chetoni P,et al.Solid lipid nanoparticles(SLN)as ocular delibery systemfor tobramycin[J].Int J Pharm,2002,238(1-2):241-245.
[12]SchubertM A,Müller-Goymann CC.Characterisation of surface-modified solid lipid nanoparticles(SLN):Influence of lecithin and nonionic emulsifier[J].Eur J Pharm Biopharm,2005,61(1-2):77-86.
[13]You J,Wan F,Cuisinart F,et al.Preparation and characteristic of vinorelbine bitartrate-loaded solid lipid nan oparticles[J].Int J Pharm,2007,343(1-2):270-276.

