替考拉宁目标治疗革兰阳性菌感染的回顾性研究
黄莉萍,张庆,黄国华,苏瑾,程远雄#(1.南方医科大学南方医院妇产科,广州510515;.南方医科大学南方医院药材科,广州 510515;.南方医科大学南方医院呼吸内科,广州 510515)
近年来,革兰阳性菌在医院感染中的分离率逐渐升高[1],其对抗菌药物的耐药率也明显增加。替考拉宁作为一种新型的糖肽类抗菌药[2],通过阻碍细胞壁肽所必需的双糖十肽转运,特异性地抑制细胞壁的生物合成,而导致细菌死亡[3],其对大多数革兰阳性菌敏感,已经成为治疗革兰阳性菌感染的最重要武器[4]。笔者对南方医科大学南方医院2010年6-12月革兰阳性菌感染住院患者中给予替考拉宁治疗的病例进行分析,旨在观察替考拉宁目标治疗革兰阳性菌感染的疗效和安全性。
1 资料与方法
1.1 病例选择
采用回顾性队列研究,收集南方医科大学南方医院2010年6-12月的住院患者中给予替考拉宁治疗的确诊或拟诊为革兰阳性菌感染住院患者的病历资料。以下情况予以筛除:(1)无革兰阳性菌感染依据;(2)用药<72 h;(3)住院时间>2个月;(4)死亡病例;(5)替考拉宁的剂量和用法不一致;(6)病例资料不全,不能提供替考拉宁治疗前、后实验室检查结果及影像学依据。
1.2 分组与治疗
入选105例分成2组。目标治疗组63例,在培养出革兰阳性菌后立即应用替考拉宁治疗;经验治疗组42例,根据体征、症状等拟诊为革兰阳性菌感染后立即应用替考拉宁治疗。替考拉宁每天静脉给药0.4 g,连续用药3 d以上。
1.3 观察项目及指标
(1)根据病程记录观察患者疗程中的症状、体征变化及出现不良反应的情况;(2)患者用药前、疗程中及用药后血常规、C反应蛋白、肝肾功能变化等情况;(3)患者用药前、疗程中及用药后影像学变化。
1.4 疗效评价[5]
将临床疗效分为痊愈、显效、进步、无效,按痊愈和显效病例计算有效率。将细菌学疗效分为清除、部分清除、未清除、无法评价,按清除和部分清除病例计算细菌清除率。
1.5 不良反应评价
汇总病程中有关不良反应的记录以及用药前、后实验室指标的异常,评定与药物的关联性:肯定、很可能、可能、可能无关、待评价、无法评价,前三者计为不良反应[6]。
1.6 统计分析
应用SPSS 13.0进行统计处理,定量资料用t检验,定性资料用χ2检验,以P<0.05为差异有统计学意义
2 结果
2.1 一般资料
105例患者中,男性74例,女性31例,年龄4~89岁,平均年龄46.30岁。诊断为下呼吸道感染71例(67.6%),败血症8例(7.6%),导管相关感染5例(4.8%),中性粒细胞减少伴发热14例(13.3%),其他感染(包括腹腔、创面、胸腔等感染)7例(6.7%)。有80例伴1~3种基础疾病,有恶性肿瘤63例,脑血管疾病10例,慢性阻塞性肺疾病5例,结缔组织病1例,糖尿病9例。2组患者的性别(P=0.26)、年龄(P=0.47)、疗程(P=0.28)、感染疾病构成比(P=0.32)差异无统计学意义,详见表1、表2。
表1 2组一般资料比较(±s )Tab 1 Comparison of general information between 2 groups(±s )

表1 2组一般资料比较(±s )Tab 1 Comparison of general information between 2 groups(±s )
项目性别(男∶女)年龄/岁疗程/d经验治疗组(n=42)27∶15 47.5±20.81 11.9±7.25目标治疗组(n=63)47∶16 44.5±20.25 10.4±7.40
2.2 合并用药情况
目标治疗组患者在使用替考拉宁治疗过程中有61.9%合并使用其他抗菌药物,经验治疗组为66.7%,2组合并用药情况经χ2检验,差异无统计学意义(P=0.62)。
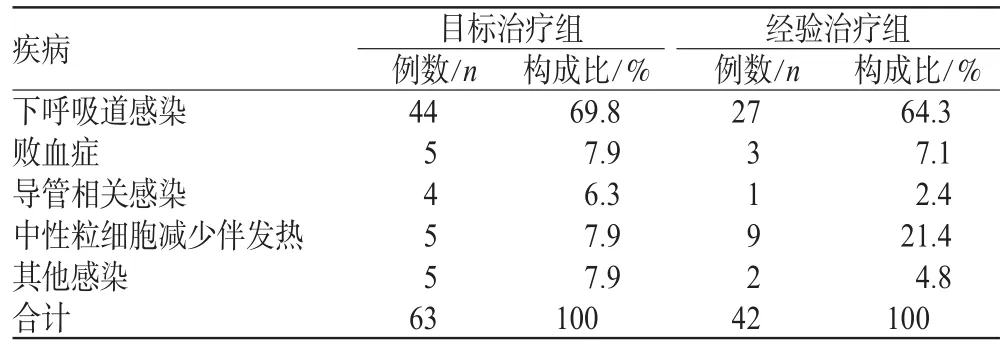
表2 2组感染疾病构成比统计Tab 2 Constituent ratio of infectious disease types in 2 groups
2.3 临床疗效
目标治疗组与经验治疗组的痊愈率分别为33.3%、7.1%,经χ2检验,差异有统计学意义(P=0.001);有效率分别为77.8%、54.8%,经χ2检验,差异有统计学意义(P=0.005),结果见表3。

表3 2组痊愈率及有效率比较Tab 3 Comparison of cure rate and effective rate between 2 groups
2.4 细菌学疗效
从105例患者体内共分离出革兰阳性菌123株,包括金黄色葡萄球菌21株(17.1%)、凝固酶阴性表皮葡萄球菌17株(13.8%)、溶血葡萄球菌17株(13.8%)、肠球菌属43株(35.0%)、链球菌属21株(17.1%),其他革兰阳性菌4株(3.3%)。2组细菌分布无差异(P=0.227),2组细菌清除率也无差异(P=0.224),细菌总清除率为81.3%,详见表4。
2.5 不良反应
目标治疗组在使用替考拉宁期间出现1例皮肤瘙痒,1例肾功能损害,2例低钾血症,不良反应发生率为6.4%;经验治疗组出现3例肝功能损害,不良反应发生率为7.1%。2组比较差异无统计学意义(P=0.87)。
3 讨论
近年来由于抗菌药物的广泛应用,出现了多种耐药的革兰阳性菌,如耐甲氧西林金黄色葡萄球菌(MRSA)、耐甲氧西林表皮葡萄球菌(MRSE)等[7,8]。替考拉宁作为一种新型的糖肽类抗菌药物,通过抑制细胞壁的形成而达到杀菌目的,且其脂溶性强,易于深入组织和细胞,对大部分革兰阳性菌敏感,被认为是耐药革兰阳性菌的最后一道防线[6]。
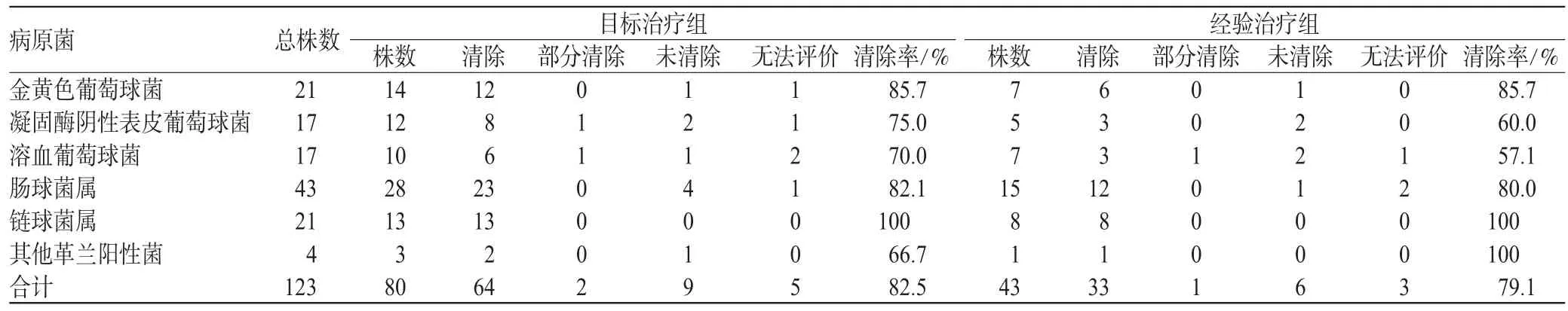
表4 2组细菌清除率比较Tab 4 Comparison of clearance rate of bacteria between 2 groups
本研究中,替考拉宁目标治疗能有效控制革兰阳性菌感染,有较高的有效率和安全性。病情危重的感染患者,如不及时经验用药,可能导致死亡率增加,故应及时经验用药以提高生存率。但一般患者应采用目标治疗,待细菌培养确诊为革兰阳性菌或MRSA感染后,根据疾病种类、患者情况和药理学理论选择最佳的药物,制订或者调整给药方案,使治疗更加有效、安全、有针对性,最终达到改善预后、减低医疗费用的目的。
替考拉宁的不良反应主要为转氨酶升高、皮疹、瘙痒、粒细胞减少和胃肠道反应[9]。本研究中总共出现了7例不良反应,目标治疗组与经验治疗组的不良反应发生率分别为6.4%、7.1%,差异无统计学意义。但由于患者常常存在多重感染,需联合用药才能有效控制,而联合用药会增加其不良反应,尤其是肾功能损害,所以在使用替考拉宁的时候应注意联合用药的问题。
[1]陈恒屹,崔社怀.替考拉宁在革兰阳性菌重症感染中的疗效观察[J].中华医院感染学杂志,2010,20(3):391.
[2]Livermore DM.Antibiotic resistance in staphylococci[J].Int J Antimicrob Agents,2000,16(Suppl 1):3.
[3]Reynolds PE.Structure,biochemistry and mechanism of action of glycopeptide antibiotics[J].Eur J Clin MicrobiolInfect Dis,1989,8(11):943.
[4]Kanellakopoulou K,Papadopoulos A,Varvaroussis D,et al.Efficacy of teicoplanin for the prevention of surgical site infections after total hip or knee arthroplasty:a prospective,open-label study[J].Int J Antimicrob Agents,2009,33(5):437.
[5]卫生部抗生素临床药理基地.抗菌药物临床研究指导原则[J].中国临床药理学杂志,1987,3(2):126.
[6]中华人民共和国卫生部.药品不良反应报告和监测管理办法[S].卫生部令第81号,2011-05-04.
[7]Manfredi R,Sabbatani S.Novel pharmaceutical molecules against emerging resistant gram-positive cocci[J].Braz J Infect Dis,2010,14(1):96.
[8]刘策时,艾效曼,刘 蕾,等.我院2007-2010年糖肽类抗菌药的使用与革兰阳性球菌的耐药性分析[J].中国药房,2011,22(30):2 833.
[9]彭 红,瞿云中,陈 平.替考拉宁治疗下呼吸道感染革兰阳性球菌的疗效和安全性评价[J].中华医院感染学杂志,2009,19(16):2 172.

