兴奋剂检测方法的研究进展
李卫东
(天津商业大学体育卫生部,天津 300134)
兴奋剂检测方法的研究进展
李卫东
(天津商业大学体育卫生部,天津 300134)
目前常用的兴奋剂检测方法有气相色谱、高效液相色谱、气相色谱-质谱联用、液相色谱-质谱联用、化学发光免疫分析法和电化学法等。色谱-质谱联用技术仍是兴奋剂检测的主要方法,气相色谱-质谱法和液相色谱-质谱法以及不断衍生的各类质谱联用技术可被用于检测大部分兴奋剂。免疫分析法主要被应用于类固醇类兴奋剂和激素类兴奋剂的检测。电化学法只能针对具有特定电活性的物质进行检测。基因兴奋剂的检测仍处在初级阶段。
兴奋剂检测;色谱/质谱联用;免疫分析;基因兴奋剂
1964年,国际运动医学会的国际兴奋剂会议将兴奋剂的概念定义为:参加竞赛的运动员使用任何异体物质,或以不正常的量和不正常的进入机体的途径使用生理物质,试图人为地以不正当方式提高其竞赛成绩的行为[1]。众所周知,使用兴奋剂对运动员的身体和心理都有严重的伤害。在体育竞技比赛中使用兴奋剂也是一种不道德行为,不仅不符合诚实和公平竞争的体育道德,也是对运动员誓言的背叛,和对奥林匹克宪章的亵渎。因此对兴奋剂的检测研究始终是反兴奋剂工作的重点之一。
检测仪器的发展,特别是色谱-质谱联用技术的长足进步,使得复杂生物基质中的微量成分可以被精确测定,并极大促进了兴奋剂检测手段的进步。目前,兴奋剂检测的主要方法有气相色谱[2]、高效液相色谱[3]、气相色谱-质谱联用[4]、液相色谱-质谱联用[5]、免疫分析法[6]、流动注射电化学发光[7]、高效毛细管电泳[8]、毛细管电泳-离子阱质谱[9]等方法。本文对目前主流的兴奋剂检测方法进行了综述。
1 色谱-质谱法
色谱仪具有高效的分离能力,质谱仪可以通过直接测定物质的质量数与电荷的比值准确快速地对物质进行定性分析。色谱-质谱联用技术将色谱仪的高效分离作用与质谱仪对未知样品的准确鉴别能力相结合,是色谱技术、质谱技术与计算机技术三种现代化技术紧密结合的产物。色谱-质谱联用技术主要分为气相色谱-质谱法和液相色谱-质谱法,可被用于检测大部分兴奋剂,包括蛋白同化制剂、肽类激素、b22激动剂、有抗雌激素作用的制剂、利尿剂和其他掩蔽剂、刺激剂、麻醉剂、大麻(酚)类、糖皮质类固醇等[10]。
1.1 气相色谱-质谱法
由于从气相色谱柱分离后的样品呈气态,流动相也是气体,与质谱仪的进样要求相匹配,因此气相色谱仪和质谱仪最容易实现联用。气相色谱-质谱(gas chromatography-mass spectrometry,GC-MS)法综合了气相色谱和质谱的优点,弥补了各自的缺陷,具有灵敏度高、分析速度快和鉴别能力强的特点,可同时完成待测组分的分离和鉴定,特别适用于多组分混合物中未知组分的定性和定量分析,判断化合物的分子结构,准确测定化合物的分子量。
1972年慕尼黑奥运会兴奋剂检测实验室首次使用GC-MS联用仪对兴奋剂进行检测[11]。之后,GC-MS联用技术有了长足进步,特别是毛细管气相色谱柱的使用,使GC-MS技术的分离效果和进样量有了极大改善。1984年洛杉矶奥运会的1 510份尿样全部使用GC-MS联用仪进行类固醇类兴奋剂的筛选和确证[11]。
20世纪90年代,高分辨质谱(high resolution mass spectrometry,HRMS)技术通过测量离子的精确质量,从而避开其它具有相同整数质量离子的干扰,显著降低了化学噪声,提高了测量的信噪比。采用HRMS技术检测残留激素类物质成为欧洲共同体认可的方法[12]。Schänzer等[13]通过检测6 700份运动员尿样中的蛋白同化雄性激素类固醇(anabolic androgenic steroids,AAS)含量,对比研究了GC-HRMS法和GC-MS法的检测能力。采用GC-MS法仅检出41份阳性尿样,而GC-HRMS法检出了116份阳性尿样。这是由于其中75份阳性尿样属低浓度样品,用GCMS法无法检出,采用GC-HRMS才可检出。因此,1993年在德国Stuttgart举行的世界田径锦标赛,首次将GC-HRMS法用于兴奋剂检测[14]。1996年亚特兰大奥运会也首次采用GC-HRMS法对兴奋剂进行检测,并首次报告检出1种新的免疫刺激剂布罗曼坦(bromantan)[11]。
2000年悉尼奥运会首次引进了气相色谱-燃烧-同位素比质谱(gas chromatography-combustion-isotope ratio mass spectrometer,GC-C-IRMS)法,主要用于检测内源性类固醇制剂。这种质谱技术广泛用于地质、石油等行业,用于测量目标化合物中C13和C12的比值,其原理见图1[11]。
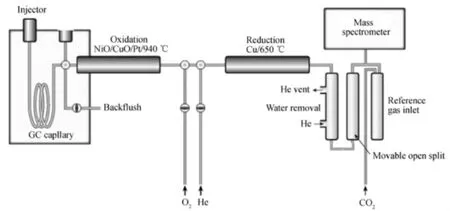
图1 气相色谱-燃烧-同位素比质谱原理示意图
目标化合物经由气相色谱分离后进入氧化炉,所有碳氢化合物催化氧化成CO2和H2O,通过冷阱或膜除去水,CO2进入质谱仪,由法拉第杯检测质量数44、45和46的信号,然后计算得出该化合物C13和C12的比值。由于人体自身合成与分泌的内源性类固醇激素C13和C12的比值与制药工业制备的类固醇制剂的同位素比不同,所以通过该法可以检测运动员是否使用了类固醇制剂。但是该方法也存在操作繁琐、费时、灵敏度低等缺点,因此,目前该方法不用于初筛,只用于可疑阳性样本的确定。
1.2 液相色谱-质谱法
液相色谱-质谱(liquid chromatography-mass spectrometry,LC-MS)联用技术始于20世纪70年代,1992年巴塞罗那奥运会上使用LC/MS联用仪很方便地检出刺激剂美沙卡伯(mesocarb)的代谢物,显示了LC-MS联用的优越性,但当时的接口和离子化技术限制了LC-MS联用技术在常规检测中的广泛应用[11]。
随着20世纪80年代中后期大气压电离技术(atmosphere pressure ionization,API)的成熟,LC-MS联用技术得以迅速发展[15]。LC-MS的API技术是一种软电离方式,通过调节离子源电压,可以控制离子的断裂,获取结构信息,大大拓宽了LC-MS的分析范围,可被用来分析蛋白质和脱氧核糖核酸等生物大分子。在兴奋剂检测领域,LC-MS法不仅可以检测刺激剂等小分子兴奋剂,也可以对肽类激素和蛋白质等大分子兴奋剂进行检测[16-19]。
针对刺激剂利他林及其主要代谢物利他林酸,陆江海等[20]利用固相萃取-液相色谱-串联质谱法建立了检测它们在人尿中含量的方法。他们将尿样中的药物经反相C18固相萃取柱净化、氮气吹至干,以甲睾为内标,用流动相溶解后进行液相色谱-串联质谱法测定。研究表明,该方法的最低检出限为5 μg· L–1,利他林和利他林酸的回收率分别为80.6%和68.4%,批内和批间的相对标准偏差小于6.0%,满足国际反兴奋剂机构对其最低检测能力500 μg·L–1的要求。
在体内主要以代谢产物形式存在的禁用药物,如合成类固醇、刺激剂、麻醉剂和B2阻断剂等,LC-MS可以通过测定葡萄糖醛酸甙或硫酸酯结合物来确定药物的代谢情况,从而实现对这些药物的定量测定[21,22]。另外,一些采用GC-MS法检测结果不理想的甾体化合物、糖皮质激素等也可采用LC-MS检测,并且检出限可以达到世界反兴奋剂委员会的最低检出限水平[23]。2004年雅典奥运会就采用了液相色谱-离子阱质谱技术分析检测糖皮质激素[11]。
对于肽类激素和蛋白质检测通常采用的是免疫检测方法,但随着LC-MS技术的成熟,样品前处理技术以及仪器的选择性和特异性的不断提高,不少基于LC-MS-MS的检测方法也被用于检测肽类激素和蛋白质[18,24-26]。蛋白质通过酶解后产生多个肽段,经液相色谱分离后用串联质谱获得肽的质量谱,从而对肽段进行鉴别和测定。通过蛋白质序列数据检索,得出蛋白质序列信息,从而实现对蛋白质的快速高灵敏度的鉴别和测定[18]。
目前,由于LC-MS技术的不同电离源对不同类型物质的电离条件各不相同,受液相色谱条件影响大,裂解信息少,往往需要测定多级裂解的谱图才能达到鉴别的目的。因此谱图解析技术的不成熟和较高的仪器成本,导致LC-MS技术的普及性还不及GC-MS技术。
2 免疫分析法
免疫分析法是利用抗原与抗体的特异性免疫反应来实现对禁用药物的检测,具有快速、高灵敏度和高特异性的特点。该方法主要包括酶联免疫分析(enzyme-linked immunosorbent assay,ELISA)、化学发光免疫分析(chemiluminescence immunoassay,CIA)和放射免疫分析(radioimmunoassay,RIA),主要被应用于类固醇类兴奋剂和激素类兴奋剂的检测。
睾酮是常见的内源性类固醇类兴奋剂,其代谢产物主要有脱氢睾酮和甲基脱氢睾酮等。对运动员血清睾酮的检测大多采用放射免疫法,但该方法自动化程度低,不适用于快速检测,又有放射污染。因此目前更多的研究集中于采用酶联免疫吸附法对睾酮及其代谢产物进行分析[27]。Kramer等[28]将脱氢勃地酮半抗原和甲基脱氢勃地酮半抗原与匙孔帽贝血蓝蛋白(keyhole limpet hemocyanine,KLH)和牛血清白蛋白偶联,然后通过腹部注射入免疫小鼠和兔子,产生相应的单克隆和多克隆抗体。利用酶联免疫分析法测定17β-脱氢勃地酮和甲基脱氢勃地酮,检出限分别达到0.13 μg/L和0.54 μg/L,满足国际反兴奋剂机构的测定要求。Salvador等[29]制备了四氢孕三烯酮(tetrahydrogestrinone,THG)的多克隆抗体,与牛血清白蛋白偶联后建立了对THG的竞争性酶联免疫分析方法,在缓冲溶液中检出限可以达到(0.045±0.015) μg/L,对经过简单预处理的实际尿样检出限可达到(0.25±0.14)μg/L,盲样分析表明,该方法具有较好的精确度。
促红细胞生成素(erythropoietin,EPO)属于单链酸性糖蛋白,能促进骨髓红细胞的生成,提高机体血红蛋白的浓度,改善机体的携氧能力和耐力,对肌体的有氧工作能力有明显的促进作用,可减少肌体的运动性疲劳,故而有人在比赛中滥用,以提高运动成绩[30]。1990年,国际奥委会就将重组人促红细胞生成素(recombinant human EPO,rhEPO)及其衍生产品列为兴奋剂,但因rhEPO与内源性EPO的蛋白部分完全一致,药物代谢动力学的半衰期仅3至10h,尿中排泄浓度极低,而且体内EPO含量的个体差异很大,个体本身EPO值也会因缺氧、贫血、pH值、运动状态、昼夜节律的变化而变化,因此一直缺乏行之有效的检测方法[31-33]。直至2000年悉尼奥运会才对运动员实施血检、尿检结合的方法对其进行检测[34]。
世界反兴奋剂组织采用的方法是由 Lasne等[35,36]于2002年提出的等电聚焦(isoelectric focusing,IEF)结合免疫双印迹化学发光法。该方法基于rhEPO与内源性EPO等电点的不同从而判断被检测者是否滥用该类药物。样品经过有效富集后进行等电聚焦,之后将凝胶上的条带转移到聚偏二氟乙烯膜上进行二次印迹,二次印迹可以有效地阻止第二抗体的非特异性结合,从而避免假阳性结果的出现,最后在发光氨和过氧化氢的作用下进行化学发光检测。该方法的误检率仅为0.006% ~0.03%。最近,针对此方法研制了特定的图像分析软件GASepo,可进行阈值计算、条带分割和算法分类,从而达到对EPO定量的目的[37]。
3 电化学方法
电化学方法不需要复杂的样品预处理和衍生过程,在兴奋剂检测领域已针对一些特定的具有电活性的物质发展出相应的电化学分析方法。Goyal等[38,39]利用循环伏安法、示差脉冲伏安法和方波伏安法构建了对诺龙的电化学分析方法。他们采用示差脉冲伏安法在pH为7.2的条件下,使用金纳米颗粒修饰的铟锡氧化物电极,在诺龙癸酸盐浓度为50 nmol/L~1.5 μmol/L的范围内研究得到了良好的线性曲线,检出限为1.36×10–7mol/L[38]。他们还研究了不同电极对诺龙电化学行为的影响,结果表明与裸玻碳电极相比,富勒烯修饰电极对诺龙表现出更好的催化活性。利用方波伏安法得到的诺龙的线性浓度范围为0.1 nmol/L~50 μmol/L,检出限为0.42 nmol/L[39]。电化学法对人血清和尿液中诺龙的测定结果与GCMS测定结果有很好的一致性。
4 基因兴奋剂的检测
基因治疗技术的出现,导致部分运动员通过使用基因兴奋剂来达到提高成绩目的,因此从2003年开始,国际奥委会将基因兴奋剂列入违禁药物的黑名单。2008年禁用清单中规定“禁止非治疗性使用细胞、基因、遗传构件,或调控基因表达的方法来提高运动能力”。德国科隆体育学院在2009年3月21日表示,已开发出新的利用质谱检测基因兴奋剂的方法,通过该方法可以检测出可被用于提高耐力的禁药GW1516,该方法将从 2012年伦敦奥运会开始使用[40]。
用于基因转移的DNA来自人类本身,因此与其他兴奋剂相比,基因兴奋剂的隐蔽性更强,检测方法也更难。现在的检测手段虽然能检测一些已知基因兴奋剂,但是对于绝大多数基因兴奋剂还没有相应的检测办法,目前主要是从基因和蛋白质的表达进行研究。因为cDNA中没有内含子,所以有可能把编码转基因蛋白的mRNA反转录得到的 cDNA从自身的DNA序列中区分出来,可以通过PCR、Southern印迹、分子探针以及基因测序等技术检测外源基因,从而实现对基因兴奋剂的检测[41]。基因兴奋剂的使用也会改变目的基因及上下游基因的表达水平,可利用cDNA微阵列技术和基因表达系列分析技术等技术对相关基因表达水平进行检测,进而判断是否使用了基因兴奋剂[42]。蛋白质组学可以定量分析个体蛋白,也可以定性分析、鉴别个体蛋白的亚型,因此也可以通过检测目的蛋白质和上下游相关蛋白质表达水平的改变,或利用免疫学技术检测外源蛋白质所引起的免疫效应来实现基因兴奋剂的检测[43]。总之,目前基因兴奋剂的检测还面临着转入部位的确定、取材和载体进入体内的代谢时间不确定等很多问题,有待进一步深入研究。
5 结论
随着检测仪器的发展和跨学科研究的深入,越来越多的技术被应用于兴奋剂检测,检测技术也越来越准确、便捷、快速。在众多检测方法中,色谱-质谱联用技术仍是兴奋剂检测的主要方法,气相色谱-质谱法和液相色谱-质谱法以及不断衍生的各类质谱联用技术可被用于检测大部分兴奋剂。免疫分析法主要被用于检测类固醇类兴奋剂和激素类兴奋剂。电化学法只能针对具有特定电活性的物质进行检测。基因兴奋剂的检测仍处在初级阶段,应加强跨学科合作,探索出准确快捷的基因兴奋剂检测方法。
[1]史立峰,盛俊林.近10年反兴奋剂研究评述与思考[J].成都体育学院学报,2010,36(5):35-38
[2]孟品佳,姚丽娟,王景翰,等.生物检材中杜冷丁、美沙酮的萃取与检测[J].中国人民公安大学学报(自然科学版),2004(4):7-9
[3]刘玉华,李太平.高效液相色谱法测定构椽酸他莫昔芬片的含量[J].色谱,1995,13(6):484-484
[4]Reza Ahmadkhaniha,Abbas Shafiee,Noushin Rastkari,Mohammad Reza Khoshayand,Farzad Kobarfardd.Quantification of endogenous steroids in human urine by gas chromatography mass spectrometry using a surrogate analyte approach[J].Journal of Chromatography B,2010,878(11-12):845-852
[5]Jianghai Lu,San Wang,Ying Dong,Xiaobing Wang,Shuming Yang,Jianli Zhang,Jing Deng,Yang Qin,Youxuan Xu,Moutian Wu,Gangfeng Ouyang.Simultaneous analysis of fourteen tertiary amine stimulants in human urine for doping control purposes by liquid chromatography-tandem mass spectrometry and gas chromatography-mass spectrometry[J].Analytica Chimica Acta,2010,657(1):45-52
[6]Franäoise Lasne,Jacques de Ceaurriz.Recombinant erythropoietin in urine[J].Nature,2000,(405):635
[7]柴晓莉,赵常志,陶晟辰,等.流动注射电化学发光法测定盐酸麻黄碱[J].分析试验室,2008,27(6):108-111
[8]肖惠,童萍,冯强,等.毛细管区带电泳用于多种类兴奋剂的同时快速分离检测[J].色谱,2008,26(4):444-448
[9]Anita B Wey,Jitka Caslavska,Wolfgang Thormann.Analysis of codeine,dihydrocodeine and their glucuronides in human urine by electrokinetic capillary immunoassays and capillary e-lectrophoresis-ion trap mass spectrometry[J].Journal of Chromatography A,2000,895(1-2):133-146
[10]Richard I.G.Holt,Ioulietta Erotokritou-Mulligan,Peter H.S?nksen.The history of doping and growth hormone abuse in sport[J].Growth Hormone&IGF Research,2009,19(4):320-326
[11]张亦农,徐友宣,吴侔天.质谱技术和奥运会兴奋剂检测[J].质谱学报,2009,30(5):257-262
[12]Laying down the methods to be used for detecting residues of substances having a hormonal action and of substances having a thyrostatic action.Official Journal of the European Communities,1987,OJL223:18-36
[13]Wilhelm Schänzer,Philippe Delahaut,Hans Geyer,Mark Machnik,Stevan Horning.Long-term detection and identification of metandienone and stanozolol abuse in athletes by gas chromatography-high-resolution mass spectrometry[J].Journal of Chromatography B:Biomedical Sciences and Applications,1996,687(l):93-108
[14]徐友宣.气相色谱(GC)-高分辨质谱(HRMS)联用在兴奋剂检测中的应用[J].质谱学报,1998,19(4):43-47
[15]徐友宣,彭师奇.蛋白质及多肽的液相色谱-电喷雾离子化质谱研究进展[J].药学学报,1997,32(10):76-80
[16]秦旸,徐友宣,杨树民,等.液相色谱-质谱联用在兴奋剂检测中的应用及进展[J].色谱,2008,26(4):431-436
[17]Catrin Goebel,Graham J.Trout,Rymantas Kazlauskas.Rapid screening method for diuretics in doping control using automated solid phase extraction and liquid chromatographyelectrospray tandem mass spectrometry[J].Analytica Chimica Acta,2004,502(1):65-74
[18]M.Thevis,J.Maurer,M.Kohler,H.Geyer,W.Sch?nzer.Proteases in Doping Control Analysis[J].International Journal of Sports Medicine,2007,28(7):545-549
[19]Phaedra Dora Simitsek,Panagiota Giannikopoulou,Haralabos Katsoulas,Efstathios Sianos,George Tsoupras,Maria-Helen Spyridaki,Costas Georgakopoulos.Electrophoretic,size-exclusion high-performance liquid chromatography and liquid chromatography–electrospray ionization ion trap mass spectrometric detection of hemoglobin-based oxygen carriers[J].Analytica Chimica Acta,2007,583(2):223-230
[20]陆江海,王杉,秦旸,等.液相色谱-串联质谱法确证人尿中的利他林及其主要代谢物[J].质谱学报,2009,30 (5):267-270,274
[21]Tiia Kuuranne,Tapio Kotiaho,Stig Pedersen-Bjergaard,Knut Einar Rasmussen,Antti Leinonen,Steven Westwood,Risto Kostiainen.Feasibility of a liquid-phase microextraction sample clean-up and liquid chromatographic/mass spectrometric screening method for selected anabolic steroid glucuronides in biological samples[J].Journal of Mass Spectrometry,2003,38(1):16-26
[22]Emmanuel Strahm,Christophe Saudan,Pierre-Edouard Sottas,Patrice Mangin,Martial Saugy.Direct detection and quantification of 19-norandrosterone sulfate in human urine by liquid chromatography-linear ion trap mass spectrometry[J].Journal of Chromatography B,2007,852(1-2):491-496
[23]Don H.Catlin,Michael H.Sekera,Brian D.Ahrens,Borislav Starcevic,Yu-Chen Chang,Caroline K.Hatton.Tetrahydrogestrinone:discovery,synthesis,and detection in urine[J].Rapid Communications in Mass Spectrometry,2004,18(12):1245-1249
[24]Mario Thevis,Wilhelm Sch?nzer.Mass spectrometric identification of peptidehormones in doping-control analysis[J].Analyst,2007,132(4):287-291
[25]Fuyu Guan,Cornelius E.Uboh,Lawrence R.Soma,Eric Birks,Jinwen Chen,Janis Mitchell,Youwen You,Jeffrey Rudy,Fran Xu,Xiaoqing Li,Gustave Mbuy.LC-MS/MS Method for Confirmation of Recombinant Human Erythropoietin and Darbepoetin α in Equine Plasma[J].Analytical Chemistry,2007,79(12):4627-4635
[26]Gerald Stübiger,Martina Marchetti,Marietta Nagano,Christian Reichel,Günter Gmeiner,Günter Allmaier.Characterisation of intact recombinant human erythropoietins applied in doping by means of planar gel electrophoretic techniques and matrix-assisted laser desorption/ionisation linear time-offlight mass spectrometry[J].Rapid Communications in Mass Spectrometry,2005,19(5):728-742
[27]Huihui Lu,Grainne Conneely,Mark A.Crowe,Margaret Aherne,Miloslav Pravda,George G.Guilbault.Screening for testosterone,methyltestosterone,19-nortestosterone residues and their metabolites in bovine urine with enzymelinked immunosorbent assay(ELISA)[J].Analytica Chimica Acta,2006,570(1):116-123
[28]K.Kramer,A.Hubauer,R.Lausterer,J.-P.Salvador,M.-P.Marco.Production of Antibodies for the Quantitative Detection of the Anabolically Active Androgens 17β-Boldenone and Methylboldenone[J].Analytical Letters,2007,40 (7):1461-1472
[29]J.-Pablo Salvador,Francisco Sanchez-Baeza,M.-Pilar Marco.Preparation of antibodies for the designer steroid tetrahydrogestrinone and development of an enzyme-linked immunosorbent assay for human urine analysis[J].Analytical Chemistry,2007,79(10):3734-3740
[30]邢延一,张力思,徐友宣,等.人体尿液中新型促红细胞生成素受体激动剂的检测[J].药学学报,2009,44(7):820-823
[31]J L Spivak,B B Hogans.The in vivo metabolism of recombinant human erythropoietin in the rat[J].Blood 1989,73 (1):90-99
[32]S.Chapel,P.Veng-Pedersen,R.J.Hohl,R.L.Schmidt,E.M.McGuire,J.A.Widness.Changes inerythropoietin pharmacokinetics following busulfan-induced bone marrow ablation in sheep:Evidence for bone marrow as a major erythropoietin elimination pathway[J].Journal of Pharmacology and Experimental Therapeutics,2001,298 (2):820-824
[33]P.Mary Cotes,M.J.Pippard,C.D.L.Reid,C.G.Winearls,D.O.Oliver,J.P.Royston.Characterization of the anaemia of chronic renal failure and the mode of its correction by a preparation of human erythropoietin(r-HuEPO).An investigation of the pharmacokinetics of intravenous erythropoietin and its effects on erythrokinetics[J].QJM: An International Journal of Medicine,1989,70(2):113-137
[34]M.Tsivou,N.Kioukia-Fougia,E.Lyris,Y.Aggelis,A.Fragkaki,X.Kiousi,Ph.Simitsek,H.Dimopoulou,I.-P.Leontiou,M.Stamou,M.-H.Spyridaki,C.Georgakopoulos.An overview of the doping control analysis during the Olympic Games of 2004 in Athens,Greece[J].Analytica Chimica Acta,2006,555(1):1-13
[35]Françoise Lasne,Laurent Martin,Nathalie Crepin,Jacques de Ceaurriz.Detection of isoelectric profiles of erythropoietin in urine:differentiation of natural and administered recombinant hormones[J].Analytical Biochemistry,2002,311 (2):119-126
[36]Françoise Lasne.Double-blotting:a solution to the problem of non-specific binding of secondary antibodies in immunoblotting procedures[J].Journal of Immunological Methods,2001,253(1-2):125-131
[37]I.Bajla,I.Holländer,M.Minichmayr,G.Gmeiner,Ch.Reichel.GASepo—a software solution for quantitative analysis of digital images in Epo doping control[J].Computer Methods and Programs in Biomedicine,2005,80(3):246-270
[38]Rajendra N.Goyal,Munetaka Oyama,Anuradha Tyagi,Sudhanshu P.Singh.Voltammetric determination of anabolic steroid nandrolone at gold nanoparticles modified ITO electrode in biological fluids[J].Talanta,2007,72(1):140-144
[39]Rajendra N.Goyal,Vinod K.Gupta,Neeta Bachheti.Fullerene-C60-modified electrode as a sensitive voltammetric sensor for detection of nandrolone—An anabolic steroid used in doping[J].Analytica Chimica Acta,2007,597 (1):82-89
[40]王磊,康琰琰.基因兴奋剂的检测现状与展望[J].体育科技,2010,31(1):48-49,58
[41]Anna Baoutina,Ian E.Alexander,John E.J.Rasko,Kerry R.Emslie.Developing strategies for detection of gene doping[J].The Journal of Gene Medicine,2008,10(1):3-20
[42]C.Lundby,P.Robach,R.Boushel,J.J.Thomsen,P.Rasmussen,M.Koskolou,J.A.L.Calbet.Does recombinant human Epo increase exercise capacity by means other than augmenting oxygen transport?[J].Journal of Applied Physiology,2008,105(2):581-587
[43]Fran?oise Lasne,Laurent Martin,Jacques de Ceaurriz,Thibaut Larcher,Philippe Moullier,Pierre Chenuaud.“Genetic Doping”with erythropoietin cDNA in primate muscle is detectable[J].Molecular Therapy,2004,10(3):409-410
Advance in Doping Detection Methods
LI WEI-dong
(Department of Physical Education and ministry of public health,Tianjin 300134,China)
The commonly used doping control methods are gas chromatography,high performance liquid chromatography,gas chromatography-mass spectrometry,liquid chromatography-mass spectrometry,chemiluminescence immunoassay and electrochemical method.Chromatography-mass spectrometry is still the main method of doping control.Gas chromatographymass spectrometry,liquid chromatography-mass spectrometry and the various types of mass spectrometry which are derivatived continuously can be used to detect most of the stimulants.Immunosorbent assay is primarily used to detect the steroid stimulants and hormone doping.Electrochemical method only can detect the material with specific electrical activity.Detection of gene doping is still in early stages.
doping detection;chromatography/mass spectrometry;immunosorbent assay;gene doping
G804.7
A
1007-323X(2012)03-0038-06
2011-10-09
李卫东(1973-),男,天津市人,副教授
研究方向:运动人体科学

