二氧化钛颗粒表面的光催化反应过程
韦冰心,王亭杰,赵 琳,陈 林,金 涌
(清华大学 化工系,北京 100084)
进展与述评
二氧化钛颗粒表面的光催化反应过程
韦冰心,王亭杰,赵 琳,陈 林,金 涌
(清华大学 化工系,北京 100084)
综述了TiO2颗粒表面光催化反应过程的研究进展。以电子空穴机理为主线,结合最新研究结果,分析了电子空穴机理的具体反应历程。并按照光生电子空穴分离、自由基产生和自由基氧化3个过程分析了TiO2颗粒表面光催化反应历程,重点分析了自由基产生过程,明确了Ti3+和O2-等基团的形成过程和在光催化反应过程中的作用。基于TiO2光催化反应历程,提出了TiO2光催化活性的调控措施。通过提高电子和空穴复合几率,可抑制TiO2的光催化活性;通过减小禁带宽度,或抑制电子和空穴复合,可提高TiO2的光催化活性。
二氧化钛;光催化;光生电子;光生空穴;自由基
TiO2有“白色颜料之王”的美誉,广泛用于涂料、塑料、化纤、造纸、光敏材料等行业;同时,TiO2在光照尤其是紫外光照射条件下具有很强的催化活性,利用TiO2的光催化性能降解有机污染物成为目前的研究热点;TiO2也以其无毒、稳定等优点而受到广泛关注[1-2]。但是,在涂料、塑料、化纤等应用过程中,TiO2较强的光催化活性会使得有机基体被氧化降解,降低材料的耐候性和使用寿命[3-4]。揭示TiO2颗粒表面的光催化反应机理是有效调控TiO2催化活性的基础。屏蔽和抑制TiO2的催化活性,可提高钛白粉作为颜料的耐候性;强化和提高TiO2的催化活性,可发挥TiO2的光敏特性和作为光催化剂的降解作用。
有关TiO2的光催化活性有较多研究报道,但大多是根据对催化机理的已有认识来分析具体问题[1-2],如引用已有的催化机理解释或分析表面包覆或掺杂改性等对TiO2催化性能的影响,或是研究催化过程中的某一问题[5],而对催化反应过程未见完整系统的报道。目前采用电子空穴机理解释TiO2光催化特性的报道较多。近年来的研究发现,TiO2在光催化过程中存在Ti3+和O2-的影响,因此对TiO2的光催化机理有了更深入的认识。
本文综述了TiO2颗粒表面光催化反应的最新研究进展,结合本课题组在TiO2颗粒表面包覆屏蔽光催化活性方面的长期研究,系统地阐述了TiO2颗粒表面的光催化反应过程。
1 电子空穴机理
电子空穴机理是以晶体结构的能带理论为基础[6-7]。以锐钛型TiO2为例,其禁带宽度为3.2 eV,当受到波长小于387.5 nm的紫外光照射时,价带中的电子会吸收光子能量而跃迁至导带,形成在导带中带负电的电子和价带中带正电的空穴,电子和空穴可自由移动,这种带电粒子的移动便产生了电流,即它们可作为载流子,使TiO2成为良好的半导体。当电子/空穴迁移到TiO2颗粒表面时,与环境中的空气、水等接触和反应,生成羟基和过羟基自由基,这些自由基有很强的活性,可以氧化与TiO2颗粒接触的很多有机介质。如TiO2颗粒和有机物制成的涂料,当其中的有机物被氧化降解时,涂料中的TiO2颗粒暴露出来,造成涂层粉化。
除电子空穴机理外,也有一种原子氧机理曾被用来解释TiO2的催化过程[8]。原子氧机理认为,TiO2表面存在晶格缺陷,成为光活化点,在紫外光照射下,晶格上的氧离子会失去两个电子变为氧原子,释放出来的电子被Ti4+捕获,还原成Ti3+。其光化学反应如下:

反应过程中释放出来的氧是原子氧,具有很强的氧化性,使涂膜中的有机物氧化。Ti2O3稳定性差,在空气中又被氧化为TiO2,但有机物的氧化降解是不可逆的,最终导致涂层粉化。在原子氧机理解释中,TiO2颗粒表面的光催化过程不需要氧和水的存在,不如电子空穴机理被广泛认可。
2 TiO2光催化反应过程解析
TiO2光催化过程包括光生电子空穴分离、自由基生成、自由基氧化3个过程,其中自由基生成是光催化过程的关键环节。
2.1 光生电子空穴分离
当TiO2受到小于387.5 nm波长的紫外光照射时,价带中的电子吸收光子能量跃迁至导带,而在价带中留下带正电的空穴,该过程可表示如下[9]:

光生电子和空穴的生成速率很快,且数量巨大。电子/空穴在晶格中可自由移动,在移动过程中,大部分电子和空穴发生复合反应[10],且这种复合反应的时间在微微秒量级[11]。小部分电子和空穴分别被Ti4+位点和OH-位点捕获,这些被捕获的电子/空穴还有可能发生复合反应。迁移到TiO2颗粒表面的电子/空穴与氧气/水进行后续的自由基生成反应[10]。电子和空穴的产生和迁移过程如图1所示。
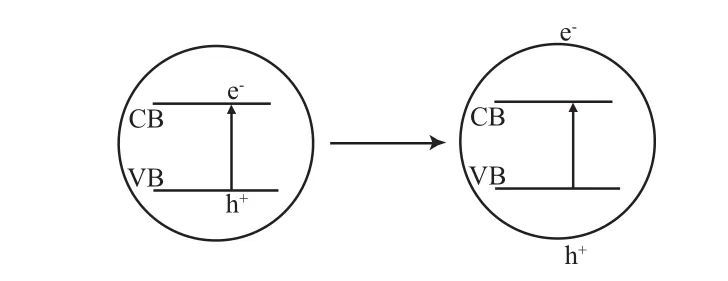
图 1 TiO2中的电子吸收光子能量跃迁及跃迁后电子和空穴的迁移Fig.1 Electron excitation from the photon absorption,and then the
2.2 自由基生成
迁移到TiO2颗粒表面的电子/空穴与氧气/水反应,生成羟基和过羟基自由基,其中空穴与水反应生成自由基的过程较为简单,而电子与氧气和水的反应则比较复杂。
2.2.1 空穴的反应
迁移到TiO2颗粒表面的空穴与表面吸附的水反应,水以水分子和带负电的氢氧根两种形式(H2O/OH-)参与反应,生成羟基自由基。反应方程式如下[12]:
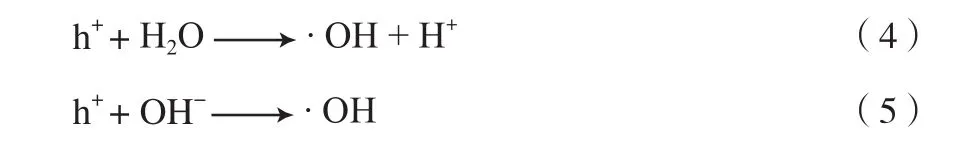
也有研究认为,是氧离子捕获空穴,产生光催化反应的活性位。Micic等[13]通过电子顺磁共振检测发现,TiO2颗粒表面存在氧离子捕获空穴生成的Ti4+—O-自由基,捕获空穴按式(6)的方式进行。


2.2.2 电子的反应
电子的反应历程相对复杂,本文将电子的反应历程分为Ti3+生成、生成和自由基生成3个阶段。
2.2.2.1 Ti3+的生成
与通常认为电子直接与氧气和水反应生成自由基不同,最新研究认为[15-17],电子与空穴分离后,可被Ti4+捕获生成Ti3+,这种捕获在颗粒内部和表面均可发生,可用式(8)表示:

针对 TiO2光催化过程,该反应历程已被提出[16-17],且在TiO2颗粒内部和表面生成Ti3+缺陷的过程也被普遍认同[18-20]。
存在于TiO2颗粒表面和内部的Ti3+对光催化过程有不同的作用。在颗粒表面,Ti4+捕获电子生成Ti3+,降低了空穴的复合几率;同时,Ti3+吸附O2生成,使催化活性提高[14,21-22]。Suriye等[5]研究发现,TiO2的光催化活性随表面Ti3+数量的增加而增强。在颗粒内部,Ti3+可被视为电子和空穴的复合中心,消耗电子和空穴,抑制光催化作用的发生。Murakami等[23]研究发现,电子和空穴的复合速率与颗粒中的Ti3+浓度呈正相关,即电子和空穴复合速率与电子被捕获速率比值的对数正比于Ti3+浓度。
Ti3+与其接触的氧分子反应,电子从Ti3+转移到氧分子上形成,该过程的进行至少有两种方式[14,24],主要取决于Ti3+的两种形式。一种是五配位的Ti3+,因其比四配位的Ti3+稳定从而成为主要的存在形式[5],它与O2的反应过程较简单,即Ti3+上的一个电子直接转移到吸附的O2上,生成Ti4+和,这种在可见光照射下几乎无活性。另一种是含有氧缺位的Ti3+结构,氧分子首先攻击氧缺位上两个相邻的Ti3+,生成的与两个Ti4+分别成键[25-26];当受到足够能量的光子照射时,一个电子从转移到其中一个Ti4+上,O—Ti键断裂,生成和Ti3+,检测结果中与Ti3+的比例为1∶1也证实了该反应过程[19]。两种反应过程如图2所示。

图 2 两种Ti3+位点上生成的途径Fig.2 Two kinds of Ti3+ sites for generation.
由于反应在TiO2颗粒表面发生,氧缺位的Ti3+位点显著多于五配位的Ti3+位点[25];且氧缺位的Ti3+位点上产生的自由基在与有机物接触时表现出更强的催化活性[27]。
2.2.2.3 自由基的生成

也有研究认为[30],羟基自由基是由过羟基自由基经反应得到,其反应过程为:

但无论哪种反应方式,在反应过程中均可生成· OH和 · O2H两种自由基。
至此,电子和空穴完成了自由基生成的反应,以上一系列反应的示意图见图3。
2.3 自由基的氧化作用
自由基的活性很强,可催化降解几乎所有的有机物,并且氧化有机物至生成CO2为止[9]。以 · OH为例,氧化反应如下:
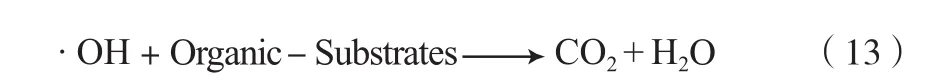
TiO2在紫外光照射下,发生光催化反应,从光生电子空穴分离、自由基生成到自由基氧化的过程中,自由基与有机物的氧化反应是整个光催化过程的决速步骤[13]。

图 3 TiO2颗粒表面生成自由基的过程Fig.3 Formation of the active free radicals on the particle surface of titania.
3 TiO2光催化活性调控
TiO2颗粒的典型特征在于其优异的光学性能和较强的光催化活性,针对TiO2不同的应用目标,可通过对TiO2颗粒进行改性处理来抑制或强化其光催化活性。
TiO2用作白色颜料时,需要发挥其优异的光学性能,抑制其光催化活性,表面包覆是屏蔽TiO2光催化活性、提高TiO2涂层耐候性的有效手段。该过程最初只是被理解为形成物理阻隔膜层,从空间上隔绝催化主体TiO2与有机介质的接触;根据原子氧机理,这种阻隔进一步被解释为对原子氧的阻隔。随着电子空穴机理的提出,膜层的作用被解释为对电子和空穴的复合和捕获,膜层对催化活性的抑制,取决于膜层对电子和空穴提供的复合位点和捕获性能。通过设计能够对电子和空穴提供丰富复合位点和有较强捕获作用的包覆膜层结构,可以最大限度地抑制TiO2的催化活性。
TiO2用于光电转换电池和用做催化剂处理有机污染物时,通常选用纳米TiO2,它具有比表面积大、化学稳定性高、无毒和成本低等优点;而在催化效率方面,它具有光谱响应范围窄、电子和空穴复合率高、光量子效率低的问题。为提高纳米TiO2的光催化活性,通常在其中掺杂一些离子,如金属掺杂、稀土金属掺杂和非金属掺杂等[31]。将金属离子引入到TiO2晶格中,可在其禁带中引入杂质能级,减小禁带宽度,使价带中的电子能接受长波长光的激发,电子可先跃迁到杂质能级,再吸收能量由杂质能级跃迁至导带,这样就降低了激发能量,从而增大 TiO2的光谱响应范围。同时,在TiO2中引入特定的掺杂离子,可形成电子或空穴的捕获位点,从而抑制电子和空穴的复合,显著提高其催化活性。其中,过渡金属离子的掺杂效果尤其显著,既可扩大光谱响应范围,又可提高光生自由基的氧化还原电位,从而大幅度提高TiO2的光催化活性[17]。稀土金属由于可提供空轨道,很可能成为电子“中转站”,因此成为提高TiO2光催化活性的研究新方向[32]。此外,两种或两种以上元素的共掺杂,因协同效应可能提供更多的晶格缺陷,阻止电子和空穴复合,因而成为提高TiO2光催化活性的重要方法[33]。
4 结语
TiO2的光催化活性是影响TiO2光学性能发挥的重要因素。TiO2光催化反应的具体历程包括光生电子空穴分离、自由基产生和自由基氧化3个过程,其中自由基产生包括Ti3+和O2-的生成等过程。根据TiO2的光催化反应历程,通过设计能够对电子和空穴提供丰富复合位点和有较强捕获作用的包覆膜层结构,可抑制TiO2的催化活性。通过减小禁带宽度,以及通过掺杂特定离子,形成电子或空穴的捕获位点,抑制电子和空穴复合,可提高TiO2的光催化活性。进一步揭示TiO2光催化反应机理,有助于从理论上指导TiO2光催化活性的调控,从而提高TiO2的应用性能。
[1]石建稳,郑经堂. 纳米TiO2光催化剂可见光化的研究进展[J]. 化工进展, 2005, 24(8): 841 - 844.
[2]余锡宾,王桂华,罗衍庆,等. TiO2微粒的掺杂改性与催化活性[J]. 上海师范大学学报,2000,29(1):75 - 82.
[3]Taylor M L,Morris G E,Smart R S. In fl uence of Aluminum Doping on Titania Pigment Structural and Dispersion Properties[J].J Colloid Interface Sci,2003,262(1):81 - 88.
[4]Sidky P S,Hocking M G. Review of Inorganic Coatings and Coating Processes for Reducing Wear and Corrosion[J].Br Corros J,1999,34(3):171 - 183.
[5]Suriye K,Praserthdam P,Jongsomjit B. Control of Ti3+Surface Defect on TiO2Nanocrystal Using Various Calcination Atmospheres as the First Step for Surface Defect Creation and Its Application in Photocatalysis[J].Appl Surf Sci,2007,253(8):3849 - 3855.
[6]文尚胜, 彭俊彪. 固体物理简明教程[M]. 广州:华南理工大学出版社, 2007:219 - 221.
[7]陈治明. 半导体概论[M]. 北京:电子工业出版社, 2008:12 - 14.
[8]唐振宁. 钛白粉的生产与环境治理[M]. 北京:化学工业出版社, 2000:14 - 16.
[9]Scotti R,Bellobono I R,Canevali C,et al. Sol-Gel Pure and Mixed-Phase Titanium Dioxide for Photocatalytic Purposes:Relations Between Phase Composition,Catalytic Activity, and Charge-Trapped Sites[J].Chem Mater,2008,20(12): 4051-4061.
[10]Ke Shyue-Chu,Wang Ting-Chung,Wong Ming-Show,et al. Low Temperature Kinetics and Energetics of the Electron and Hole Traps in Irradiated TiO2Nanoparticles as Revealed by EPR Spectroscopy[J].J Phys Chem B,2006,110(24):11628 - 11634.
[11]Leytner S,Hupp J T. Evaluation of the Energetics of Electron Trap States at the Nanocrystalline Titanium Dioxide/Aqueous Solution Interface via Time-Resolved Photoacoustic Spectroscopy[J].Chem Phys Lett,2000,330(3/4):231 - 236.
[12]Li Youji,Sun Shuguo,Ma Mingyuan,et al. Kinetic Study and Model of the Photocatalytic Degradation of Rhodamine B(RhB) by a TiO2-Coated Activated Carbon Catalyst:Effects of Initial RhB Content, Light Intensity and TiO2Content in the Catalyst[J].Chem Eng J, 2008, 142(2): 147 - 155.
[13]Micic O I,Zhang Yuenian,Cromack K R,et al. Trapped Holes on TiO2Colloids Studied by Electron- Paramagnetic-Resonance[J].J Phys Chem,1993,97(28):7277 - 7283.
[14]Nakaoka Y,Nosaka Y. ESR Inverstigation into the Effects of Heat Treatment and Crystal Structure on Radicals Produced over Irradiated TiO2Powder[J].J Photochem Photobiol,A,1997,110(3):299 - 305.
[15]Green J,Carter E,Murphy D M. Interaction of Molecular Oxygen Vacancies on Reduced TiO2:Site Specific Blocking by Probe Molecules[J].Chem Phys Lett,2009,477(4/6):340 - 344.
[16]Berger T,Diwald O,Knozinger E,et al. Hydrogen Activation at TiO2Anatase Nanocrystals[J].Chem Phys,2007,339(1/3): 138 - 145.
[17]Coronado J M,Maira A J,Martinez-Arias A,et al. EPR Study of the Radicals Formed upon UV Irradaiton of Ceria-Based Photocatalysts[J].J Photochem Photobiol,A,2002, 150(1/3): 213 - 221.
[18]Sirisuk A,Klansorn E,Praserthdam P. Effects of Reaction Medium and Crystallite Size on Ti3+Surface Defects in Titamium Dioxide Nanoparticles Prepared by Solvothermal Method[J].Catal Commun,2008,9(9):1810 - 1814.
[19]Komaguchi K,Maruoka T,Nakano H,et al. ESR Study on the Reversible Electron from O22-to Ti4+on TiO2Nanoparticles Induced by Visible-Light Illumination[J].J Phys Chem C,2009, 113(4): 1160 - 1163.
[20]Komaguchi K,Nakano H,Araki A,et al. Photoinduced Electron Transfer from Anatase to Rutile in Partially Reduced TiO2(P-25) Nanoparticles: An ESR Study[J].Chem Phys Lett, 2006,428(4/6): 338 - 342.
[21]Howe R F,Gratzel M. Electron-Paramagnetic-Res Observation of Trapped Electrons in Colloidal TiO2[J].J Phys Chem,1985,89(21):4495 - 4499.
[22]Park D R,Zhang Jinlong,Ikeue K,et al. Photocatalytic Oxidation of Ethylene to CO2and H2O on Ultra fi ne Powdered TiO2Photocatalysts in the Presence of O2and H2O[J].J Catal,1999, 185(1): 114 - 119.
[23]Murakami S Y,Kominami H,Kera Y,et al. Evaluation of Electron-Hole Recombination Properties of Titanium(Ⅳ)Oxide Particles with High Photocatalytic Activity[J].Res Chem Intermed, 2007,33(3/5):285 - 296.
[24]Carter E,Carley A F,Murphy D M. Evidence for O2-Radical Stabilization at Surface Oxygen Vacancies on Polycrystalline TiO2[J].J Phys Chem,2007,111(28):10630 - 10638.
[25]Oviedo J,Gillan M J. First-Principles Study of the Interaction of Oxygen with the SnO2(110)Surface[J].Surf Sci,2001,490(3):221 - 236.
[26]de Lara-Castells M P,Krause J L. Theoretical Study of the Interaction of Molecular Oxygen with a Reduced TiO2Surface[J].Chem Phys Lett,2002,354(5/6):483-490.
[27]Carter E,Carley A,Murphy D M. Free-Radical Pathways in the Decomposition of Ketones over Polycrystalline TiO2:The Role of Organoperoxy Radicals[J].Chem Phys Chem,2007,8(1):113 - 123.
[28]Chen Shifu,Zhang Sujuan,Zhao Wei,et al. Study on the Photocatalytic Activity of TiN/TiO2Nanoparticle Formed by Ball Milling[J].J Nanopart Res,2009,11(4):931 - 938.
[29]Zhao Jincai,Wu Taixing,Wu Kaiqun,et al. Photoassisted Degradation of Dye Pollutants:3. Degradation of the Cationic Dye Rhodamine B in Aqueous Anionic Surfactant/TiO2Dispersions Under Visible Light Irradiation:Evidence for the Need of Substrate Adsorption on TiO2Particles[J].Environ Sci Technol,1998,32(16):2394 - 2400.
[30]Wu Taixing,Liu Guangming,Zhao Jincai,et al. Photoassisted Degradation of Dye Pollutants:Ⅴ. Self-Photosensitized Oxidative Transformation of Rhodamine B Under Visible Light Irradiation in Aqueous TiO2Dispersions[J].J Phys Chem B,1998,102(30):5845 - 5851.
[31]石建稳,陈少华,王淑梅,等. 纳米二氧化钛光催化剂共掺杂的协同效应[J]. 化工进展,2009,8(2):251 - 258.
[32]肖俊霞,吴贤格. TiO2光催化氧化技术的研究与发展[J]. 石油化工,2011, 40(2):225 - 231.
[33]张庆祝,罗远建,李越湘,等. Zr和S共掺杂TiO2光催化剂的制备及性能[J]. 石油化工,2009, 38(1):15 - 19.
Photocatalytic Reaction Process on Titania Particle Surface
Wei Bingxin,Wang Tingjie,Zhao Lin,Chen Lin,Jin Yong
(Department of Chemical Engineering,Tsinghua University,Beijing 100084,China)
The photocatalytic reaction process on titania particle surface and its research progress were analyzed. According to the electron-hole mechanism the detailed reaction process was summarized combining the newest research achievements,including the separation of the photoelectron and photohole, formation of the free radicals and oxidation of the free radicals. The formation of Ti3+andand their roles in the photocatalytic process were clarified. Based on the photocatalytic reaction mechanism, the control of TiO2photocatalytic activity was elucidated systematically. The photocatalytic activity can be restricted by providing plenty recombination sites and increasing capture capability for photoelectrons and photoholes with a specially coated fi lm. The activity can be increased by reducing the band gap or doping specific ions to form capture sites for restriction of the recombination of photoelectron and photohole.
titania; photocatalysis;photoelectron;photohole;free radical
1000 - 8144(2012)02 - 0219 - 05
TQ 426
A
2011 - 07 - 09;[修改稿日期]2011 - 2 - 07。
韦冰心(1988—),女,广西省都安县人,硕士生。联系人:王亭杰,电话 010-62788993,电邮 wangtj@tsinghua.edu.cn。
国家自然科学基金项目(20906055, 21176134)。
(编辑 安 静)

