不结球白菜BcMPK4基因的诱导表达分析
马景蕃,黄素华,刘喜明,黎 英,周酵琼
(1.龙岩学院生命科学学院,福建 龙岩 364012;2.龙岩学院资源工程学院,福建 龙岩 364012)
蛋白激酶催化的蛋白磷酸化和蛋白磷酸酶催化的去磷酸化作用在植物细胞感受各种环境信号及其信号转导与放大过程中起重要作用[1],其中促分裂原活化蛋白激酶(Mitogen-activated protein kinases,MAPKs)的作用受到广泛关注。近年来,研究发现大多数MAPK参与激素应答、环境胁迫反应以及植物抗病反应[2]。在植物抗病反应调控方面,发现MAPK可以参与抗病基因介导的抗病反应、过敏性反应中细胞死亡以及植物的先天性免疫反应等[3]。例如在拟南芥(Arabidopsis thaliana)中,使用MPK4特异性抗体进行生物化学分析发现,各种各样的生物和非生物胁迫都能够诱导MPK4激活[4]。
植物防御与病原菌侵染是一个互动过程,在此过程中植物针对病原菌不同的侵染方式会做出相应特异的防卫反应[5]。研究表明水杨酸(Salicylic acid,SA)、茉莉酸(Jasmonic acid,JA)和脱落酸(Abscisic acid,ABA)等植物激素也参与植物抗病、抗逆过程[6],其中SA和JA是植物防卫信号转导途径中关键的信号分子。由水杨酸和茉莉酸介导的防卫反应是植物抵御病原菌的最重要方式。很多研究表明这两种防卫反应方式存在明显交叉和拮抗,一些植物主要通过茉莉酸介导的防卫反应方式抵抗对非专性寄生性病原菌的侵染[7]。拟南芥MPK4是水杨酸和茉莉酸介导的防卫反应调节基因,其功能缺失突变体表现出对坏死型病原菌高度敏感,表明该基因在抗坏死型病原菌中起作用[8],但至今为止,还没有关于这些病害防御信号分子与不结球白菜MPK4基因表达之间关系的报道。
不结球白菜(Brassica campestrisssp.chinensisMakino)原产于中国,其营养丰富,是长江中下游地区主要蔬菜品种之一,但不结球白菜病害相当严重,其中菌核病[Sclerotinia sclerotiorumde(Bary)]是最主要病害之一,常给菜农造成极大经济损失[9]。不结球白菜菌核病属非专性寄生[10],能产生坏死斑,而草酸是菌核病主要的致病因子。
本研究将采用实时荧光定量PCR法研究不结球白菜BcMPK4在核盘菌接种、核盘菌致病因子草酸处理、病害防卫反应信号分子SA、JA类似物MeJA和植物激素ABA处理后的表达变化差异,期望了解菌核病及其致病因子草酸、防卫反应信号分子、植物激素ABA与BcMPK4表达的关系,为不结球白菜抗菌核病的研究奠定基础。
1 材料与方法
1.1 材料
供试材料为不结球白菜抗菌核病品种003-R-6和高感品种003-S-7,由龙岩学院生物技术课题组提供。将两个品种的种子用0.1%HgCl2浸泡5 min,然后用蒸馏水冲洗干净,置于铺有湿润滤纸的培养皿内,于25℃催芽24 h。然后将催芽后的种子播种于灭菌基质中,于人工培养箱在白天25℃、夜晚15℃、12 h/12 h光周期条件下培养,待幼苗培育至四叶一心时用于试验。
1.2 方法
1.2.1 菌核病的接种
核盘菌(Sclerotinia sclerotiorum)菌核采自龙岩学院生命科学学院试验田内的不结球白菜茎秆。选好菌核后,用75%乙醇浸泡30 s,0.1%HgCl2消毒10 min,再用无菌水冲洗4次,把灭菌菌核切去两端,中间部分切成绿豆大小,切面朝下,接种于PDA(Potato dextrose agar)培养基。在25℃下暗培养4 d,待菌丝长满培养皿后,用打孔器将菌丝截成直径为0.4 cm大小的菌丝琼脂块,用于接种。待幼苗长至四叶一心时对第三叶进行菌核病菌接种处理,接种前5 d将植株22℃恒温培养,选用核盘菌的菌丝块进行活体接种,对照接种无菌培养基块。每个处理设3次重复。
1.2.2 化学诱导处理
草酸(Oxalic acid,OA),分析纯,购自同济大学生物技术开发公司;水杨酸、甲基茉莉酸(Methyl jasmonate,MeJA)和脱落酸购自Sigma公司。
当不结球白菜幼苗长至四叶一心时进行诱导处理,处理前5 d将植株进行22℃恒温培养。分别用5 mmol·L-1草酸(OA)、0.1 mmol·L-1水杨酸(SA)[11]、0.1 mmol·L-1甲基茉莉酸(MeJA)、0.1 mmol·L-1脱落酸(ABA)[12]喷雾四叶期植株的第三片真叶,灭菌双蒸水喷雾处理相同苗龄的相应叶片为对照。喷雾至叶片上均匀布满液滴为止。每种处理20株,3次重复。将各种不同处理的植株分别放入不同的密封间,22℃恒温保湿培养。
1.2.3 取样
上述核盘菌及不同化学试剂处理不结球白菜抗感品种后,分别在0、4、8、16、24、48、72 h剪下处理叶片(包括对照叶片),用锡箔纸包裹,迅速置于液氮中,8 min后转入-80℃冰箱保存。
1.2.4 总RNA提取及cDNA第1链的合成
不结球白菜叶片总RNA提取参考Ma等方法进行[13],所用玻璃和塑料制品均经0.1%DEPC浸泡过夜,高温高压灭菌处理。利用TaKaRa公司宝生物反转录试剂盒(Primescript 1st strand cDNA synthesis kit)合成第一链cDNA。
1.2.5 实时定量PCR检测
实时定量PCR方法参照SYBR Green Realtime PCR Master Mix试剂盒(TaKaRa),以不结球白菜3-磷酸甘油醛脱氢酶基因(BcGAPDH,DDBJ登录号AB331373)作为内标基因,引物为:5'CTGTCT CGCTCCATTCG 3'和5'AGTTTCCCTTTGAGGTTAG 3',BcMPK4基因引物序列为:5'GACACTGATC TCCACCAG 3'和 5'ATCCTATAAGCTCAGTGAT 3'。引物由金思特生物技术有限公司合成。反应在Rotor Gene 3000(Corberr Research公司)荧光梯度PCR仪上进行扩增,总体系为25 μL,热启动程序为95℃预变性2 min;95℃变性20 s,52℃退火20 s,72℃延伸20 s,共45个循环;熔解曲线测定为从60℃到95℃,3次重复。数据由Opticon Monitor TM 1.02(MJ公司)软件和Excel软件进行分析。
2 结果与分析
2.1 核盘菌侵染后BcMPK4分别在抗、感病品种中表达的变化
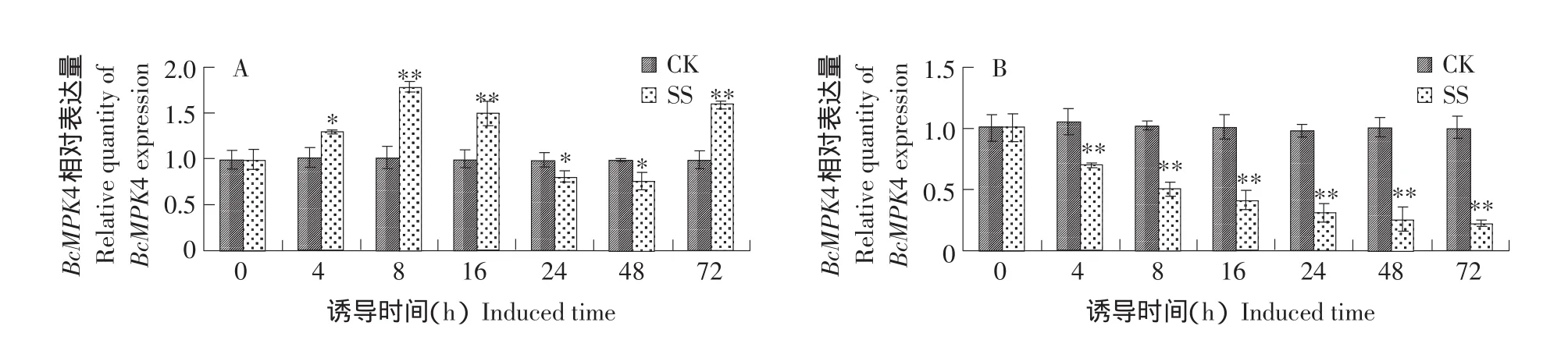
图1 实时定量PCR检测不结球白菜经核盘菌诱导后BcMPK4基因的表达Fig.1 qPCR analysis of relative expression levels of BcMPK4 induced by Sclerotinia sclerotiorum
拟南芥MPK4功能缺失突变体对非专化寄生性病原菌Alternaria brassicicola表现出增加感病性表型,并且伴随防卫素基因的表达降低[8]。为检测不结球白菜BcMPK4基因是否在防卫非专化寄生性病原菌Sclerotinia sclerotiorum的侵染中行使功能,采用实时荧光定量PCR检测BcMPK4在不结球白菜抗感品种中被核盘菌侵染后的表达变化。结果显示,在抗性品种003-R-6中,当核盘菌侵染4 h时,BcMPK4表达量迅速上升,与对照相比差异显著(P<0.05)。当侵染8 h时,BcMPK4表达量上升至最高,约是对照的1.8倍,与对照相比差异达极显著水平(P<0.01)。之后BcMPK4表达量开始下降,当侵染24和48 h时,BcMPK4表达量显著低于对照,当侵染72 h时,BcMPK4表达量再次升高,与对照相比差异极显著(P<0.01)。而感病品种003-S-7接种核盘菌后,BcMPK4表达量与抗病品种迥然不同,感病品种均表现为下调表达,而且随着侵染时间的延长,BcMPK4表达量逐渐下降,当侵染72 h时,BcMPK4表达量达最低,约为对照的0.22倍(见图1)。
2.2 草酸诱导BcMPK4在抗、感病品种中表达的动态变化
草酸是一种包括核盘菌在内的许多病原真菌分泌的植物毒素。为研究草酸与BcMPK4之间的关系,选用5 mmol·L-1草酸来处理不结球白菜抗感品种叶片,观察这个基因在不同抗感品种中不同处理时间点的表达变化。结果显示,在品种003-R-6中,经草酸诱导4 h时,BcMPK4表达量迅速上升,与对照相比差异显著(P<0.05)。当诱导8 h时,BcMPK4表达量上升至最高,约是对照的1.7倍,与对照相比差异达极显著水平(P<0.01)。当诱导24、48和72 h时表达量均下调,大约分别是对照的82%、67%和43%,与各自对照相比差异均达显著水平(P<0.05)。而感病品种003-S-7经草酸诱导后,BcMPK4表达量均表现为下调表达,而且随着诱导时间的延长,其表达量逐渐下降,当侵染72 h时,BcMPK4表达量达到最低,约为对照的16%(见图2)。

图2 实时定量PCR检测不结球白菜经草酸诱导后BcMPK4基因的表达Fig.2 qPCR analysis of relative expression levels of BcMPK4 induced by oxalic acid
2.3 水杨酸诱导BcMPK4在抗、感病品种中表达的动态变化
经水杨酸诱导后,在品种003-R-6中,BcMPK4表达总体呈现先升后降趋势(见图3)。诱导4 h时,BcMPK4表达量迅速上升,与对照相比差异显著(P<0.05)。当诱导8 h时,BcMPK4表达量上升至最高,约是对照的1.8倍,与对照相比差异达极显著水平(P<0.01)。诱导16 h时,表达量开始下降,诱导24 h时,表达量下降到对照的76%,到72 h下降至21%。表明在不结球白菜抗性品种中水杨酸可快速诱导MPK4上调表达。感病品种003-S-7经水杨酸诱导后,BcMPK4表达量均表现为下调表达,随着诱导时间的延长,其表达量逐渐下降,当侵染72 h时,BcMPK4表达量达到最低,约为对照的27%(见图3)。
2.4 甲基茉莉酸诱导BcMPK4在抗、感病品种中表达的动态变化

图3 实时定量PCR检测不结球白菜经水杨酸诱导后BcMPK4基因的表达Fig.3 qPCR analysis of relative expression levels of BcMPK4 induced by salicylic acid
茉莉酸是植物防御反应信号转导途径中重要的信号分子,而甲基茉莉酸(MeJA)是其功能类似物。采用信号分子茉莉酸的类似功能处理不结球白菜叶片,通过研究在不同处理时间点BcMPK4在不结球白菜体内表达差异来探讨该基因与茉莉酸的关系。如图4所示,不结球白菜抗感两个品种经MeJA处理后,BcMPK4表达都被抑制,抗性品种于处理后4 hBcMPK4相对表达量约为对照的50%,但处理后8 h,其表达量逐渐上升,于处理后72 h表达量达最大,约为对照的84%。可见处理8 h后,MeJA对不结球白菜BcMPK4表达抑制率逐渐下降。感病品种经MeJA处理后4 h,BcMPK4相对表达量约为对照的27%,与抗性品种相比,抑制幅度更大。处理后8 h,其表达量逐渐上升,但与抗性品种相比,上升幅度更小(见图4)。
2.5 ABA诱导BcMPK4在抗、感病品种中表达的动态变化
ABA等植物激素也参与植物抗病、抗逆过程[14]。经ABA处理后,BcMPK4表达水平变化在抗感品种中各不相同,在抗性品种中,ABA处理对BcMPK4表达影响不大,在整个研究时间范围内,处理与对照的差异均未达显著水平(P<0.05)。而在感性品种中,于处理后4 h,表达量开始逐渐下降,经处理后72 h,BcMPK4表达量达最低,约为对照的47%,表达差异达极显著水平(P<0.01)(见图5)。

图4 实时定量PCR检测不结球白菜经甲基茉莉酸诱导后BcMPK4基因的表达Fig.4 qPCR analysis of relative expression levels of BcMPK4 induced by methyl jasmonate

图5 实时定量PCR检测不结球白菜经脱落酸诱导后BcMPK4基因的表达Fig.5 qPCR analysis of relative expression levels of BcMPK4 induced by abscisic acid
3 讨论
SIPK和WIPK是在烟草中发现的MAP激酶,其生物学功能说明MAPK链参与抗性基因介导的信号传递,即含有抗TMV的抗性基因—N基因的烟草植株,在与无毒菌株互作时,通过Ser/Thr和Tyr氨基酸位点的磷酸化可激活WIPK蛋白发挥作用。虽然很多抗性基因介导的防卫反应大多依赖SA存在,但WIPK的激活却不依赖SA[15],说明这个蛋白在“基因对基因”(gene-for-gene)介导的抗病反应中起作用。此外,Romeis等用来自病原菌无毒基因Avr9处理含有抗性基因Cf29的烟草悬浮细胞,发现Cf29/Avr9的互作激活SIPK和WIPK两种蛋白,推测MAP激酶可能位于抗性基因介导的信号传递链下游[3]。目前已知SA以及非特异激发子等都能激活SIPK和WIPK蛋白,说明它们诱导的多个抗性基因信号途径是通过SIPK或WIPK等MAPK链发挥作用。
本试验研究结果显示,核盘菌侵染初期,不结球白菜抗性品种BcMPK4表达量迅速上升,而感性品种该基因表达量逐渐下降(见图1),表明BcMPK4参与不结球白菜对核盘菌抗性反应。草酸能够诱导BcMPK4在不结球白菜抗性品种中表达,表现在经草酸诱导初期BcMPK4在抗性品种中表达迅速上升(见图2),由图1和2可以看出,草酸与核盘菌诱导BcMPK4基因的表达在0~48 h内是一致的,这个结果支持核盘菌在侵染植物时释放草酸毒素是其重要致病机理。同时也说明植物通过增加BcMPK4表达抵御侵染胁迫。但是与草酸不同,核盘菌是活性生物,可以持续对植物细胞进行侵染破坏,所以经核盘菌处理后,在抗性品种中BcMPK4表达出现两次高峰(见图1),这种表达动态可能暗示植物与核盘菌之间存在动态相互作用。经草酸和SA诱导后,BcMPK4表达在抗感品种中的变化趋势是高度一致的。另外,在0~48 h,草酸、SA、核盘菌诱导BcMPK4表达反应趋势也一致。这说明不结球白菜对SA、草酸以及核盘菌反应机制的分子网络中包含BcMPK4。
MeJA和SA诱导BcMPK4在抗性品种中的表达趋势截然不同,特别是在诱导4 h的初期反应中,SA和MeJA分别诱导BcMPK4上调和下调表达(见图3、4)。因此BcMPK4在不结球白菜中可能调节SA介导的防卫反应。这与拟南芥中AtMPK4的研究结果是一致的[4]。经ABA处理后BcMPK4表达水平在抗性品种中几乎无变化(见图5),说明ABA不能介导BcMPK4在不结球白菜中的防卫反应。
4 结论
本研究采用实时荧光定量PCR法研究不结球白菜BcMPK4在菌核病防卫反应中的作用。结果表明,核盘菌、OA和SA能快速诱导BcMPK4在抗性品种中表达,而MeJA抑制其表达,ABA对BcMPK4表达响应不明显,由此推测BcMPK4在核盘菌诱抗信号转导和SA信号通路中起关键作用。
[1]Tena G,Asai T,Chiu W L,et al.Plant mitogen-activated protein kinase signaling cascades[J].Curr Opin Plant Biol,2001(4):392-400.
[2]丁俊杰,文景芝,束永俊,等.两个大豆灰斑病抗性相关SCAR标记的发现与鉴定[J].东北农业大学学报,2010,14(12):1-5.
[3]Romeis T,Piedras P,Zhang S,et al.RapidAvr-9 andCf-9-dependent activation of MAP kinases in tobacco cell cultures and leaves:Convergence of resistance gene,elicitor,wound and salicylate responses[J].Plant Cell,1999(11):273-287.
[4]Ren D,Yang H,Zhang S.Cell death mediated by MAPK is associated with hydrogen peroxide production inArabidopsis[J].J Biol Chem,2002,277:559-565.
[5]Jonathan D G J,Jeffery L D.The plant immune system[J].Nature,2006,444:323-329.
[6]Wan J R,Zhang S Q,Stacey G.Activation of a mitogen-activated protein kinase pathway inArabidopsisby chitin[J].Mol Plant Pathol,2004(5):125-135.
[7]Brodersen P,Petersen M,Bjern N H,et al.ArabidopsisMAP kinase 4 regulates salicylic acid-and jasmonic acid/ethylenedeacid/ethylene-dependent responses via EDS1 and PAD4[J].Plant J,2006,47:532-546.
[8]Thomma B P,Penninckx A,Broekaert W F,et al.The complexity of disease signaling inArabidopsis[J].Curr Opin Immunol,2001,13:63-68.
[9]马景蕃,侯喜林,肖栋,等.不结球白菜抗芜菁花叶病毒蛋白BcTuRsO的生物信息学分析[J].江苏农业学报,2010,26(2):280-285.
[10]Kostina L.The influence of space flight factors on viability and mutability of plants[J].Adv Space Research,1984(4):65-70.
[11]Park C J,Kim K J,Shin R,et al.Pathogenesis-related protein 10 isolated from hot pepper functions as a ribonuclease in an antiviral pathway[J].The Plant Journal,2004,37:186-198.
[12]Salazar M,Gonzalea E,Casaretto J A,et al.The promoter of the TLC1.1 retrotransposon fromSolanum chilenseis activated by multiple stress-related signaling molecules[J].Plant Cell Rep,2007(2):1861-1868.
[13]Ma J F,Hou X L,Xiao D,et al.Cloning and characterization of theBcTuR3 gene related to resistance toTurnip Mosaic Virus(TuMV)from non-heading Chinese cabbage[J].Plant Mol Biol Rep,2010,28:588-596.
[14]刘胜毅,Fitt B D L.油菜防御素和草酸氧化酶基因的克隆与诱导表达水平研究[J].中国油料作物学报,2004,26(3):43-49.
[15]Mishra N S,Tuteja R,Tuteja N.Signaling through MAP kinase networks in plants[J].Arch Biochem Biophys,2006,452:55-68.

