大孔树脂对倍花单宁酸的吸附特性及其动力学模型
欧阳玉祝,张辞海,魏 燕
(吉首大学食品科学研究所,湖南 吉首 416000)
单宁酸是一类广泛存在于植物组织中的多酚化合物,这种多酚结构赋予它独特的生理活性和优良的抗氧化活性与自由基清除能力[1-3],广泛用于食品、酿酒、日化、医药和皮革等领域[4-6]。目前,单宁酸的生产主要以五倍子为原料,用水浸出,再用沉淀法、透析法、溶剂法、凝胶柱色谱法等方法分离纯化[7-8]。倍花也是一种单宁酸生产原料,单宁酸含量为20%~30%。由于倍花中单宁酸含量低,杂质含量高,分离技术难度大,至今未引起重视。而倍花原料丰富,价格低廉,具有很高的开发应用价值[9]。大孔树脂以其分离的高效性和高选择性被广泛用于天然产物中活性成分的分离纯化[10-14]。大孔树脂的吸附量不仅与树脂的孔径和比表面积有关,而且与吸附的外部条件有关,其吸附能力直接影响目标产物的分离效率。本实验以倍花为原料,研究D-101大孔树脂对倍花单宁酸的吸附动力学特性和热力学参数,研究成果能为倍花单宁酸的分离纯化和开发利用提供理论依据。
1 材料与方法
1.1 材料、试剂与仪器
铬皮粉 中国林业科学研究院林产化学研究所;倍花 湖南吉首市场;单宁酸标准品(含量≥99%) 中国林业科学院林产化工研究所;盐酸、氢氧化钠均为国产分析纯;D-101大孔吸附树脂 天津市光复精细化工研究所。
UV-2450型紫外-可见分光光度计 日本岛津公司;DF-101S集热式恒温磁力搅拌器 郑州长城科工贸有限公司。
1.2 方法
1.2.1 树脂的预处理
大孔树脂按参考文献[15]进行预处理,贮存在锥形瓶中备用。
1.2.2 倍花单宁酸的制备
倍花水提物中加入一定量的石灰乳进行沉淀,抽滤,滤饼经酸解后,抽滤,滤液真空蒸发、干燥后得浅黄色粉末。产品按LY/T 1642—2005《单宁酸分析实验方法》测得单宁酸含量为81%,贮存于冰箱中备用。
1.2.3 静态吸附实验
用制备的倍花单宁酸产品(单宁酸含量为81%)配制1.0871mg/mL溶液。称取经预处理的湿树脂5.000g(相当于干树脂4g)于200mL具塞锥形瓶中,加入75mL倍花单宁酸溶液,置于恒温磁力搅拌器上180r/min搅拌,30℃静态吸附,每间隔10min取样,用紫外-可见分光光度计测276nm波长处的吸光度,直到吸附平衡。结合标准曲线的回归方程计算单宁酸质量浓度,按式(1)、(2)计算吸附量(qt)和吸附率(A)。

式中:V为溶液体积/mL;ρ0为倍花单宁酸溶液的起始质量浓度/(mg/mL);ρt为t时刻倍花单宁酸溶液质量浓度/(mg/mL);ρe为吸附平衡时倍花单宁酸溶液质量浓度/(mg/mL);m为湿树脂质量/g。
1.2.4 吸附等温线
称取经预处理的湿树脂5.000g于200mL具塞锥形瓶中,分别加入75mL质量浓度为1.3、2.5、5.0、7.5、9.9mg/mL的倍花单宁酸溶液,于35、40、45、50℃温度条件下恒温搅拌吸附直到吸附平衡,用紫外-可见分光光度计测吸附平衡时的溶液质量浓度,建立吸附等温线。
1.3 分析方法
倍花单宁酸根据LY/T 1642—2005法用紫外-可见光分光光度计结合标样作定性和定量分析。
准确配制1.000mg/mL单宁酸标准溶液,将该溶液稀释成各种梯度的标准溶液,用紫外-可见分光光度计测 276nm波长处的吸光度,绘制标准曲线,实验数据经线性回归得回归方程为:ρ=0.0204A(R2=0.9996)式中:ρ为倍花单宁酸质量浓度/(mg/mL);A为标准溶液的吸光度。
2 结果与分析
2.1 吸附动力学特性
2.1.1 吸附动力学曲线
为了考察倍花单宁酸的吸附量随吸附时间的变化,以确定平衡吸附量,按方法1.2.3节进行吸附,每隔10min取样分析,测定吸附10、20、30、40、50、60、70、80、90、100、110、120min时的吸附量,并以吸附量为纵坐标,吸附时间为横坐标绘图,结果见图1。

图 1 30℃时大孔树脂对单宁酸吸附的动力学曲线Fig.1 Adsorption kinetic curve of tannic acid on macroporous resin at 30 ℃
由图1可知,在50min内单宁酸在树脂上的吸附量快速增加,随后吸附量增加变得缓慢,说明该吸附在90min时基本达到吸附平衡。
2.1.2 吸附动力学特性
为了考察倍花单宁酸在大孔树脂上的吸附动力学特性,探讨大孔树脂对倍花单宁酸的吸附机理,用一级动力学模型、二级动力学模型和颗粒扩散动力学模型来描述吸附过程。动力学模型按式(3)~(5)表示[16]:

式中:qt为t时刻的吸附量/(mg/g);qe为平衡吸附量/(mg/g);k1为准一级动力学速率常数/min-1;k2为准二级动力学速率常数/(g/(mg·min));kd为颗粒扩散动力学速率常数/(mg/(g·min1/2));C为常数。
分别以时间t或t1/2为横坐标,ln(qe-qt)、t/qt或qt为纵坐标绘制准一级动力学曲线、准二级动力学曲线和颗粒扩散动力学曲线,得到3条直线,经线性回归得3种动力学参数如表1所示。

表1 大孔树脂对倍花单宁酸的吸附动力学参数Table 1 Kinetic parameters of tannic acid adsorption on D-101 resin
由表1 可知,二级吸附动力学的相关系数达到0.9995,颗粒扩散动力学方程的相关系数最小,仅为0.8730,说明该吸附过程符合准二级动力学模型。虽然颗粒扩散动力学模型不能描述整个吸附过程,但是可以描述一些特殊阶段的吸附机理。颗粒扩散动力学曲线见图2所示。

图 2 颗粒扩散动力学曲线Fig.2 Kinetic curves for particle diffusion
根据Lorenc-Grabowska等[17]的研究结果,如果这条线经过原点,且为直线,说明该过程是单一的颗粒扩散速控步骤。由图2可知,颗粒扩散图形不经过原点,也不是直线,证明该过程不是唯一的颗粒扩散速控步骤,边界层扩散也在一定程度上影响吸附过程。边界层扩散以外(0~10min)的吸附过程包括2个阶段,第一阶段(10~50min)属于逐渐吸附阶段,颗粒扩散速率很小;第二阶段(50~120min)被认为是最终的平衡吸附阶段。因此,颗粒扩散与边界层扩散交互影响单宁酸在D-101树脂上的吸附。
2.2 吸附等温线
为了更好的研究D-101树脂的吸附特性,按1.2.4节方法进行吸附实验,绘制树脂在35、40、45、50℃ 4个不同温度条件下倍花单宁酸的平衡吸附等温线,结果如图3所示。

图 3 不同温度条件下D-101树脂对单宁酸的吸附等温线Fig.3 Adsorption isotherms for D-101 resin at different temperatures
由图3可知,图中的B点4条线汇聚,认为固体表面发生的是多分子层可逆吸附,B点是树脂上第一单分子层的平衡吸附量[18],与经典的BET吸附等温线相吻合。
目前,描述吸附平衡最经典的模型是Langmuir和Freundlich模型。这两个模型的方程式如式(6)、(7)[11]所示:
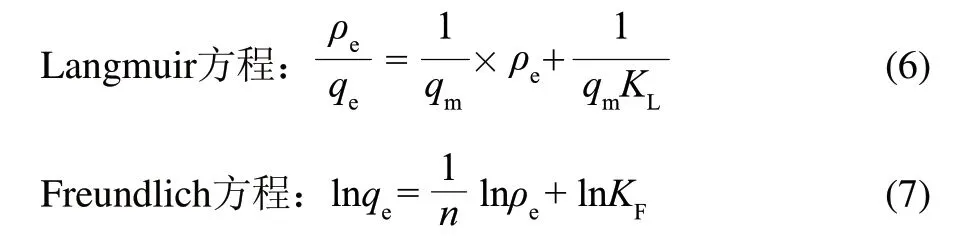

用线性拟合来描述不同温度条件下不同质量浓度吸附质和吸附剂的吸附平衡关系。以ρe为横坐标,ρe/qe为纵坐标对Langmuir方程进行线性拟合。同时,以lnρe为横坐标,lnqe为纵坐标对Freundlich方程进行线性拟合。不同模型拟合的相关系数列于表2。

表2 大孔树脂对倍花单宁酸的吸附等温线参数Table 2 Adsorption isotherm parameters of tannic acid adsorption on D-101 resin
由表2可知,各种温度条件下的相关系数都较高。同比之下,相同温度Langmuir方程的相关系数比Freundlich方程的相关系数都要高,说明Langmuir吸附等温线更能准确反映该吸附过程。
2.3 吸附热力学
吸附自由能变ΔG与平衡常数K有关,而K与Langmuir常数(KL)有关[19],方程式如式(8):

式中:M为单宁酸的摩尔质量(1701g/mol)。
自由能变ΔG可由Gibbs方程求解,方程式见式(9):

式中:R是气体常数(8.314J/(mol·K));T为绝对温度(273K)。
焓变ΔH和熵变ΔS可由Van’t Hoff方程(10)计算:

以1/T为横坐标,lnK为纵坐标对Van’t Hoff方程进行线性拟合,焓变ΔH和熵变ΔS可由直线的斜率和截距分别算出。吸附焓变及拟合直线的相关系数(R2)、吸附自由能变、吸附熵变的结果列于表3。

表3 大孔树脂对倍花单宁酸吸附时热力学参数Table 3 Adsorption thermodynamics parameters of tannic acid adsorption on D-101 resin
由表3可知,4个温度的吸附自由能变都是负值,熵变为正值表明吸附过程是自发的,而且这4个吸附自由能变的数值很接近,说明在所做实验的温度范围内温度不是影响吸附过程的主要因素,与参考文献[20]报道一致。吸附焓变值也为负值,表明吸附过程是一个放热过程,理论上升高温度会不利于吸附。但实验表明当温度在35~50℃之间增加时,树脂的吸附量也在增加。究其原因,是因为温度升高,吸附质的传质效率增加,扩散速率加快,促使吸附量增加,此为动力学控制过程;而温度升高不利于吸附导致吸附量减小,是热力学控制过程;由于前者影响大于后者导致吸附量稍有增加。而且吸附焓变绝对值为5.509kJ/mol,小于43kJ/mol,表明该吸附过程属于物理吸附[21]。
3 结 论
通过研究D-101树脂吸附倍花单宁的动力学和热力学特性,发现大孔树脂对倍花单宁酸的吸附符合准二级动力学方程模型,颗粒扩散与边界层扩散交互影响单宁酸在D-101大孔树脂上的吸附。D-101树脂对倍花单宁酸的吸附符合Langmuir吸附等温线,是一种物理吸附过程,体系放热约为5.5kJ/mol。
[1] 曹鹏飞. 石榴皮和绿茶中单宁的抗氧化作用研究[J]. 安徽农业科学, 2011, 39(20): 12136-12137.
[2] FUKUDA T, ITO H, YOSHIDA T. Antioxidative polyphenols from walnut (Juglans regia L. )[J]. Phytochemistry, 2003, 63(7): 795-801.
[3] 张亮亮, 李敏, 林鹏, 等. 李子果肉单宁结构及其抗氧化能力的研究[J]. 林产化学与工业, 2008, 28(4): 1-6.
[4] CHUNG K T, WEIB C I, JOHNSONC M G. Are tannins a double edged sword in biology and health[J]. Trends in Food Science& Technology, 1998, 9(4): 168-175.
[5] SALEEM A, HUSHEEM M, HÄRKÄNEN P. Inhibition of cancer cell growth by crude extract and phenolics of Terminalia chebula Retz[J]. Fruit Journal of Ethnopharmacology, 2002, 81(3): 327-336.
[6] 柳世萍, 李毅. 五倍子提取单宁酸的工艺研究[J]. 河北化工, 2007, 30(10): 10-11.
[7] 申明乐. 五倍子加压提取单宁的工艺研究[J]. 山东化工, 2007, 36(12): 11-13.
[8] 王妙飞, 程庚金生, 张道英, 等. 水解法制取五倍子鞣花酸的研究[J]. 食品工业科技, 2010, 31(2): 233-234.
[9] 周丽珠. 化学法倍花制取工业单宁酸的试验研究[J]. 林产化工通讯, 2002, 36(1): 19-21.
[10] ZHANG Yinglao, YIN Caiping, KONG Lichun, et al. Extraction optimisation, purification and major antioxidant component of red pigments extracted from Camellia japonica[J]. Food Chemistry, 2011, 129(2): 660-664.
[11] LIU Pengwei, DU Yingfeng, ZHANG Xiaowei, et al. Rapid analysis of 27 components of Isodon serra by LC-ESI-MS-MS[J]. Chromatographia, 2010, 72(3/4): 265-273.
[12] LI Hua, LIU Juan, LI Dan, et al. Study on separation and purification of genistein in the soybean residue using macroporous resin adsorption[J]. Industrial & Engineering Chemistry Research, 2012, 51(1): 44-49.
[13] LIN Lianzhu, ZHAO Haifeng, DONG Yi, et al. Macroporous resin purification behavior of phenolics and rosmarinic acid from Rabdosia serra (MAXIM.) HARA leaf[J]. Food Chemistry, 2012, 130(2): 417-424.
[14] 欧阳玉祝, 李佑稷, 石爱华, 等. 大孔树脂对单宁酸的吸附与解吸行为研究[J]. 食品工业科技, 2009, 30(2): 152-154.
[15] 欧阳玉祝, 吕程丽, 郑胜丰, 等. 大孔树脂吸附法分离过路黄中的总多酚[J]. 食品科学, 2009, 30(22): 213-215.
[16] HO Y, NG J, MCKAY G. Kinetics of pollutant sorption by biosorbents: review[J]. Separation and Purification Methods, 2000, 29(2): 189.
[17] LORENC-GRABOWSKA E, GRYGLEWICZ G. Adsorption of lignitederived humic acids on coal-based mesoporous activated carbons[J]. Journal of Colloid and Interface Science, 2005, 284(2): 416-423.
[18] LIU Y F, LIU J X, CHEN X F, et al. Preparative separation and purification of lycopene from tomato skins extracts by macroporous adsorption resins[J]. Food Chemistry, 2010, 123(5): 1027-1034.
[19] BULUT Y, AYDM H. A kinetics and thermodynamics study of methylene blue adsorption on wheat shells[J]. Desalination, 2006, 194(1): 259-267.
[20] YANG Bin, GAO Yanxing, LIU Xuan, et al. Adsorption characteristics of crocin in the extract of gardenia fruits (Gardenia jasminoides Ellis) on macroporous resins[J]. Journal of Food Process Engineering, 2009, 32(1): 35-52.
[21] GÖKMEN V, SERPEN A. Equilibrium and kinetic studies on the adsorption of dark colored compounds from apple juice using adsorbent resin[J]. Journal of Food Engineering, 2002, 53(3): 221-227.

