促红细胞生成素对小鼠心肌缺血损伤的心脏保护作用及机制
王媛媛 曹 建 陈 勤 欧阳先国
1.南昌市第三医院心内科,江西南昌 330009;2.南昌大学第二附属医院,江西南昌 330006
促红细胞生成素对小鼠心肌缺血损伤的心脏保护作用及机制
王媛媛1曹 建2陈 勤1欧阳先国1
1.南昌市第三医院心内科,江西南昌 330009;2.南昌大学第二附属医院,江西南昌 330006
目的 探讨类似促红细胞生成素(EPO)对小鼠心肌缺血损伤的保护作用。 方法 采用结扎冠状动脉前降支的方法建立大鼠心肌梗死模型。治疗组大鼠(n=40)采用腹腔注射方法给予EPO(1 μg/kg),对照组大鼠(n=40)在相同的时间点给予等量的生理盐水。处理后24 h通过TCC染色测量心肌梗死面积,处理后3、24 h,通过Western-blot法检测STAT3蛋白表达。处理8周后,通过超声心动图测量左心室舒张期末容积、左心室收缩期末容积、左心室射血分数。 结果治疗组小鼠心肌梗死面积为24.6%,对照组小鼠心肌梗死面积为48.6%(P<0.05);EPO干预后,与对照组比较,治疗组STAT3蛋白表达增高(P<0.05);治疗组左心室舒张期末容积、左心室收缩期末容积、左心室射血分数分别为 592 μl、371 μl、36%,对照组上述指标分别为 740 μl、526 μl、27%,两组差异有统计学意义(P<0.05)。 结论EPO在小鼠心肌缺血损伤中具有心脏保护作用。
促红细胞生成素;心肌梗死;信号转导子与转录激活子3
近年来研究表明促红细胞生成素(erythropoietin,EPO)具有多种非促造血方面的细胞保护作用,特别是在抑制心脏重构方面的作用日益受到关注,但其作用机制目前尚不十分明确,可能与抑制心肌细胞肥大和凋亡、抗炎、抗氧化、抑制成纤维细胞增殖等有关[1-2]。也有报道显示其细胞保护作用与抑制胶原合成及影响基质金属蛋白酶活性等方面有关[3-4]。本实验拟在探讨EPO在心肌缺血损伤中的保护机制,为临床应用EPO防治缺血再灌注引起的心脏功能损伤提供依据。
1 材料与方法
1.1 动物及材料
取雄性Sprague-Dawley小鼠120只,8周龄,由南昌大学动物实验中心制备成急性心肌梗死(AMI)模型,全部小鼠分3组,分别为对照组(40只),重组人促红细胞生成素(rhEPO)组(40 只),假手术组(40 只)。 对照组小鼠诱导心肌梗死模型后给予生理盐水,rhEPO组小鼠诱导心肌梗死模型后输注rhEPO,假手术组在前降支留置一松结,不结扎。重组人红细胞生成素注射液(益比奥,批号:20120207V,沈阳三生制药有限公司),兔抗STAT3、辣根过氧化物酶标记的羊抗兔IgG均购自美国Santa生物公司。
1.2 方法
1.2.1 大鼠AMI模型的制作 参照Olivetti等[5]的手术方式结扎冠状动脉左前降支制作AMI模型。假手术组仅在前降支留置一松结,不结扎。所有动物均分笼饲养,标准饮食。1.2.2 EPO的心肌保护作用检测 在结扎后5 min接受腹腔注射 rhEPO(1 μg/kg)(n=10)[6],存活小鼠在 24 h 后处死,通过TCC染色测量心肌梗死面积。取新鲜大鼠心脏,用PBS缓冲液冲洗,滤纸吸干,-20℃冰冻30 min后将其横断面切成 1~2 mm 切片,1%TTC37℃染色25 min,切片放4%甲醛中过夜以增强颜色对比,非心肌梗死区染色为红色,梗死区不染色。扫描仪扫描心脏切片,使用image proplus6.0软件测量相关区域面积,梗死面积(%)=左心室组织切片梗死区面积/左心室组织切片总面积×100%。
1.2.3 STAT3蛋白表达 选取2组小鼠诱导心肌梗死模型后(n=20),分别用 rhEPO(1 μg/kg)、生理盐水进行处理(方法同1.2.2),手术处理后的存活小鼠在心肌梗死后3、24 h处死。通过组织颜色改变鉴别心肌缺血组织和正常组织,进行组织切片后放入液氮冷冻,采用Western blot方法测定转录激活因子3(STAT3)。取大鼠左心室梗死边缘区心肌组织标本液氮研碎,加入裂解液,匀浆离心后,取上清液用BCA法测定蛋白浓度,变性后-80℃冰箱保存。取各组样品50 μg,进行12%SDS-PAGE电泳将总蛋白电转移至PVDF膜上,用5%脱脂奶粉室温摇床封闭1.5 h后,加入一抗稀释液稀释的 STAT3(1∶500)单克隆抗体,4℃冰箱中孵育过夜,用 TBST洗涤15 min×3次,加入二抗(HRP标记二抗,1∶5000稀释),室温下摇床孵育 1.5 h,用 TBST洗涤15 min×3次。ECL发光液显色,胶片扫描后用Image J软件进行图像分析,以β-actin(1∶1000稀释)作为内参照对比,比值结果表示其蛋白的相对含量。
1.2.4 大鼠心功能测定 冠状动脉结扎后5 min内腹腔注射rhEPO1 μg/kg(n=10),生理盐水 1 ml/kg(n=10),超声心动图基础参考值由假手术组测得,所有小鼠在外科处理后8周后进行超声心动图检查。将小鼠用异氟烷(2%in oxygen)行轻度全身麻醉后,用12 MHz探头进行超声心动图检查。二维的心室图可以从四个腔室和胸骨旁长轴和短轴定位获得。左心室舒张期末容积(LVEDV)和收缩期末容积(LVESV)可以通过Modified Simpson Rule测量,左心室射血分数(LVEF)=(LVEDV-LVESV)/LVEDV×100%。 所有测量均由同一观察者行双盲法测量,所有测量结果均连续测3~5次后取平均值。
1.3 统计学方法
采用SPSS 13.0统计学软件,各组间不同时间阶段超声心动图数据比较采用方差分析,同一时间组间比较采用单因素方差分析,以P<0.05为差异有统计学意义。
2 结果
2.1 不同处理组心肌梗死范围的比较
冠状动脉结扎注射5 min后注射药物,24 h后处死存活小鼠,rhEPO处理组心肌梗死范围为24.6%,对照组心肌梗死范围为48.6%,心肌梗死面积减少近50%,两组差异有统计学意义(P<0.05);提示EPO对大鼠心肌梗死具有保护作用。
2.2 EPO对STAT3蛋白表达的影响
Western-blot分析STAT3蛋白,冠状动脉结扎3、24 h后心肌梗死区域STAT3蛋白表达在冠状动脉结扎后3 h就开始增高,在24 h恢复为正常,rhEPO组STAT3蛋白表达明显高于对照组(P < 0.05)(表 1)。
表1 rhEPO对小鼠心梗后STAT3蛋白表达的影响(±s,n=10)
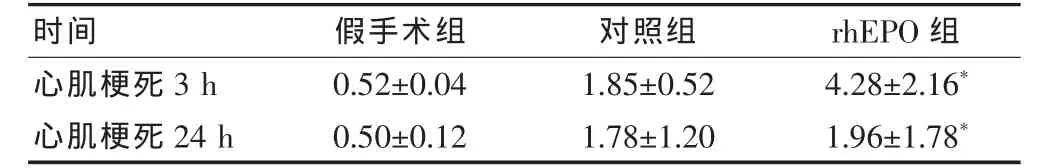
表1 rhEPO对小鼠心梗后STAT3蛋白表达的影响(±s,n=10)
与对照组比较,*P<0.05
?
2.3 rhEPO对小鼠左室容积及射血分数的影响
对照组、药物处理组、假手术组小鼠冠状动脉结扎5 min内注射药物,8周后通过超声心动图测量LVEDV、LVESV、LVEF。对照组LVEDV、LVESV、LVEF与假手术组差异有统计学意义(P<0.05),rhEPO组与假手术组差异有统计学意义(P<0.05)(表 2)。
表2 rhEPO对小鼠左室容积及射血分数影响(±s,n=10)

表2 rhEPO对小鼠左室容积及射血分数影响(±s,n=10)
与假手术组比较,*P<0.01,**P<0.05
组别 LVEDV(μl) LVESV(μl) LVEF(%)假手术组对照组rhEPO组420±4.2 740±5.6*592±2.7**182±3.6 526±2.4*371±3.6**56±1.4 27±3.7*36±1.3**
3 讨论
EPO是由成人肾脏分泌的分子量为34 kD的调节红细胞生成的生长因子,它通过抗细胞凋亡的机制来促进红系祖细胞的增殖、分化和成熟,是一种重要的细胞保护因子,对缺血缺氧性损伤的大脑、肾脏、心脏等多种器官组织起保护作用。本研究证实了EPO具有心脏保护作用,本实验中EPO处理组小鼠心肌梗死面积较对照组减少,提示EPO对大鼠心肌梗死具有保护作用。超声心动图检测结果显示,EPO组LVEDV、LVESV、LVEF与对照组差异有统计学意义。在冠状动脉永久结扎后的小鼠实验模型注射EPO后LVEDV、LVESV均较对照组下降,LVEF较对照组提高,提示EPO可以延缓心室重构,改善心功能。
EPO对心脏保护作用的机制是非常复杂的,EPO可以促进血管再生和祖细胞增殖,对于减少细胞凋亡和炎症反应具有重要作用。rhEPO减少小鼠心肌梗死面积可能归功于它的促血管生成作用,有研究表明[7],在心内膜内皮细胞培养液中加入rhEPO可以明显加快新生血管的形成,其效果甚至可以和血管内皮生长因子(VEGF)相媲美,同时有研究证实rhEPO能够刺激神经和内皮祖细胞的分化[8],因此rhEPO动员未分化细胞进入缺血心肌组织并刺激其分化,可能也是其缩小心肌梗死范围的一个机制。
EPO可以激活心脏保护级联信号通路,特别是P13K/Akt通路[9-10]。对EPO神经保护机制的研究发现[11-12],EPO通过与EPO-R结合,激活JAK2-PI3K-Akt通路,以及丝裂素激活蛋白激酶(MAPK)/细胞外信号调节激酶(ERK)等路径,增加保护性基因转录或保护性蛋白表达上调,产生抗凋亡作用
STAT3属于STAT蛋白家族,具有抗凋亡作用,包括7个成员,均在心肌细胞中表达。STAT3作为细胞内的转录调节因子,参与多种基因表达调控,并参与多种心脏生理、病理活动,如心肌细胞存活、线粒体能量代谢、AngⅡ信号转导、心肌细胞与血管再生、细胞外基质变化及炎症反应[13-14]。EPO在冠状动脉结扎3、24 h后,Western blot结果分析显示出EPO激活了抗凋亡途径,STAT3蛋白表达增加。而EPO最大的抗凋亡途径在3 h后激活,效应在24 h内消退。这与EPO血浆半衰期有关,EPO血浆半衰期只有2 min[13],可以在很短时间内激活抗凋亡途径。本研究发现,应用rhEPO后小鼠心肌梗死面积减少,心肌功能明显改善,而且心肌STAT3表达比对照组明显增加。推测rhEPO可能通过增加核转录调节因子STAT3蛋白的表达,阻断其引起的应激相关凋亡途径的信号传导,而发挥心肌保护作用。可以考虑进一步积极开展药物处理后的基础及临床研究,对于防治缺血心肌的再灌注损伤具有重要理论意义和临床应用价值。
[1]Wang W,Kagaya Y,Asaumi Y,et al.Protective effects of recombinant human erythropoietin against pressure overload-induced left ventricular remodeling and premature death in mice[J].Tohoku J Exp Med,2011,225(2):131-143.
[2]Brines M,Cerami A.Erythropoietinmediated tissue protection:reducing collateral damage from the primary injury responses[J].Intern Med,2008,264(4):405-432.
[3]Bogoyevitch MA.An update on the cardiac effects of erythropoietin cardioprotection by erythropoietin and the lessons learnt from studies in neutoprotection[J].Cardiovasc Res,2004,63(2):208-216.
[4]Riksen NP,Hausenloy DJ,Yellon DM,et al.Erythropoietin:ready for prime-time cardioprotection[J].Trends Pharmacol Sci,2008,29(8):258-267.
[5]Olivetti G,Capasso JM,Meggs LG,et al.Cellular basis of chronic ventricular remodeling after myocardial infarction in rats[J].Circ Res,1991, 68(9): 856-859.
[6]Lippi G,Franchini M,Favaloro EJ.Thrombotic complications of erythropoiesis stimulating agents[J].Semin Thromb Hemost,2010,36(5):537-549.
[7]付振虹,董蔚,盖鲁粤,等.促红细胞生成素联合粒细胞集落刺激因子治疗大鼠急性心肌梗死[J].南方医科大学学报,2011,30(1):17-21.
[8]马宝新.促红细胞生成素衍生物研究进展[J].心血管病学进展,2011,32(2):288-391.
[9]Tramontano AF,Muniyappa R,Black AD,et al.Erythropoietin protects cardiacmyocytes from hypoxia-induced apoptosis through an aktdependent pathway[J].Biochem Biophys Res Commun,2003,308 (4):990-994.
[10]Chen Z,Li T,Zhang B,et al.Morphine postconditioning protects against reperfusion injury in the isolated rat hearts[J].J Surg Res,2008,145(2):287-294.
[11]马骥,郑鸣之.促红细胞生成素抑制心梗大鼠心肌核转录因子CHOP表达的研究[J].中国药学杂志,2011,46(1):24-27.
[12]Joshi D,Tsui J,Yu R,et al.Potential of novel EPO derivatives in limb ischemia[J].Cardilol Res Pract,2012,2(22):1155-1785.
[13]Burger D,Xenocostas A,Feng QP.Molecular basis of cardioprotection by erythropoietin[J].Curr Mol Pharmacol,2009,2(7):56-69.
[14]秦晓毅,卢新政.STAT3与心肌重构[J].国际心血管病杂志,2012,39(3):22-24.
The cardioprotective effect of erythropoietin on heart ischemic myocardial damage in rat
WANG Yuan-yuan1CAO jian2CHEN qin1OUYANG Xian-guo1
1.Department of Cardiology,the Third Hospital of Nanchang City in Jiangxi Province,Nanchang 330006,China;2.The Second Affiliated Hospital of Nanchang University,Nanchang 330006,China
ObjectiveTo investigate the protective effects of erythropoietin(EPO)on heart ischemic myocardial damage in the rat.MethodsRat models of acute myocardial infarction(AMI)which were built by ligating the left anterior descending coronary artery were divided into two groups,treatment group(n=40)
1 μg/kg EPO through introperitoneal injection,and control group(n=40)received the same volume of saline through the same procedures.After 24 hours of treatment,the myocardial infarction area was evaluated by TCC dyeing,after 3,24 hours of treatment,the expression of STAT3 was analyzed by Westen blot,we assessed the LV end-diastolic volume (LVEDV),LV end-systolic volume(LVESV),LV ejection fraction(LVEF)of the rat by echocardiography after 8 weeks.ResultsThe myocardial infarct size of the erythroietin group was 24.6%,that of the control group was 48.6%(P<0.05).After treated with erythroietin,compared with the control group,the expression of STAT3 was increased(P<0.05),the LVEDV,LVESV,LVEF of the erythroietin group was 592 μl,371μl,36%,these of the control group were 740 μl,526 μl,27%.There was significant difference between control group and erythroietin group(P<0.05).ConclusionEPO has a cadioprotective effect on heart ischemic damage.
Erythropoietin;Myocardial infarction;Signal transducer and activator of transcription(STAT3)
R-332
A
1674-4721(2013)08(c)-0020-03
2013-01-31 本文编辑:魏玉坡)

