鼠胚胎干细胞定向诱导为角膜上皮细胞的实验研究
杨成明 滕 利 黄谙飞
1.广东省深圳市南山区西丽人民医院眼科,广东深圳 518055;2.广东省深圳市南山区西丽人民医院病理科,广东深圳 518055
角膜上皮位于眼角膜表面,是维持眼表正常生理功能的重要条件。健全的角膜上皮细胞是角膜抵御外界各种有害因素损伤的重要条件。人的角膜自我更新由位于角膜缘外围区域的角膜缘干细胞来维持,结构与功能健全的角膜缘干细胞是角膜上皮再生的主要来源,当角膜受到化学及热烧伤,以及患有Stevens-Johnson syndrome等疾病时,角膜缘上皮细胞将会缺失,导致增加角膜感染、穿孔、新生血管化的危险[1]。因此,重建完整的角膜上皮就显得异常重要。
胚胎干细胞(embryonic stem cells,ES细胞)是从早期胚胎内细胞团分离获得的,具有体外增殖和全能性两大特点。近年来随着ES细胞研究的不断深入,其逐渐应用于细胞、组织的修复和移植[2]。绿色荧光蛋白(green fluorescent protein,GFP)基因是一种新型的报告基因,用GFP作为标志物来标记ES细胞,可用来追踪ES细胞在体内的分化[3]。本研究利用质粒pEGFP-N1脂质体复合体转染鼠ES细胞,并在体外诱导鼠ES细胞向角膜上皮细胞分化,为治疗角膜损伤及重建角膜上皮提供细胞组织来源。
1 材料与方法
1.1 实验材料
鼠ES细胞由北京大学深圳研究生院分子生物学实验室提供。DMEM、胎牛血清、胰蛋白酶、B-巯基乙醇、非必需氨基酸,购自Sigma公司;丝裂霉素C,购自Kogyo公司;脂质体Lipofectamine 2000、G418,均购自Invitrogen公司;白血病抑制因子 (1eukemia inhibitory factor,LIF)、L-谷氨酰胺,购自Sigma公司;质粒pEGFP-N1,购自Clontech公司;明胶、TaqDNA聚合酶,购自博大泰克公司;CK14、CK12、CD44引物,委托宝生物工程公司合成;免疫组化二抗试剂盒、DAB显色试剂盒,购自武汉博士德公司;其余为国产分析纯试剂。
1.2 实验方法
1.2.1 ES细胞的培养 ES 细胞复苏后,经丝裂霉素C灭活的小鼠胚胎成纤维细胞(MEF)做饲养层培养,加入预先铺有明胶(Ⅳ型胶原)的培养皿中,37℃,50 mL/L CO2培养箱中培养,每日更换ES细胞培养液为高糖DMEM (内含0.1 mol/L β-巯基乙醇、2 mmol/L 谷氨酰胺、150 mL/L 胎牛血清、1 000 U/mL LIF、15 g/L非必需氨基酸)。2~3 d传代1次。
1.2.2 转染及诱导ES细胞 将真核细胞表达载体pEGFPN1转染ES细胞作为实验组,空载质粒转染ES细胞作为对照组。在转染前2 h改为无血清的DMEM培养液;含载体pEGFP-N1质粒的无血清DMEM培养液与含脂质体Lipofectamine 2000的无血清DMEM培养液混合,加入ES细胞培养皿中,置37℃的CO2培养箱中培养,换液,培养基为不含LIF的ES细胞培养基。G418筛选GFP阳性细胞克隆,接种在丝裂霉素C处理的MEF饲养层上,继续扩增培养,获得稳定的转染细胞系。ES细胞诱导前去除饲养层细胞,接种于涂抹明胶(Ⅳ型胶原)的培养皿中,加入无LIF的ES细胞培养液,隔日换液,传3~4代,诱导ES细胞分化成角膜上皮细胞。
1.2.3 形态学和免疫组织化学鉴定 显微镜下观察ES细胞形态,诱导培养7 d后,细胞基本融合,将培养分化的ES细胞用PBS洗涤3次后,冷4%多聚甲醛固定30 min,正常山羊血清封闭30 min,滴加K14、K12及CD44单抗,4℃过夜,0.02%Triton-PBS洗涤,加人生物素标记的二抗,室温下孵育40 min,PBS洗涤数次后,加入链亲和素一过氧化物酶溶液,放置于室温下10 min,0.02%Triton-PBS洗涤,最后DAB显色,显微镜下观察。
1.2.4 RT-PCR检测 Trizol R试剂盒提取ES细胞总RNA,具体过程参照Trizol Reagent说明书。引物序列分别为:CD44正义链5'-atcaacctgcctatgcaacc-3',反义链5'-cttggacgggaactgacact-3'(248 bp);K12 正义链 5'-cgagagtggtatgaaaca-3', 反义链 5'-tgggctctcatttcattg-3'(218 bp); K14 正义链 5'-ggtcgatttgatggatttgg-3',反义链 5'-gttcagtgttggcctcttcc-3'(192 bp);内参照 β-actin正义链 5'-gatgacgatatcgctgcgctg-3', 反义链 5'-gtccgaccagaggcatacagg-3'(512 bp)。每个周期参数如下:94℃ 30 s, 60℃ 35 s, 72℃ 60 s,共30个循环周期。采用小鼠角膜上皮细胞做阳性对照,每组PCR反应均设一个阴性对照。取RT-PCR产物20 μL行琼脂糖凝胶电泳,紫外分析仪观察结果,凝胶成像系统拍照。
2 结果
2.1 ES细胞的形态
在饲养层上培养的ES细胞生长旺盛,边界光滑,呈现巢状生长,集落大多呈多角形或椭圆形,集落内细胞排列紧密,边界不清;细胞边界清,胞浆较丰富,细胞核大,核仁大。GFP阳性ES细胞在荧光显微镜下可观察到细胞内有微弱的绿色荧光(图1~2)。
2.2 诱导分化的角膜上皮细胞形态
GFP阳性ES细胞经Ⅳ型胶原诱导培养1周,可见在细胞集落中爬出上皮样细胞,贴壁生长,增殖迅速,逐渐呈集落式生长,生长胞体多为扁平,呈多角型或不规则形态生长,表现出典型的上皮细胞形态,在荧光显微镜下可观察到细胞内有很强的绿色荧光(图3~4)。
2.3 K12、K14及CD44表达情况

图1 光镜下的ES细胞(×100)

图2 荧光显微镜下GFP未转染的ES 细胞(×100)

图3 诱导后的角膜上皮样细胞(×100)
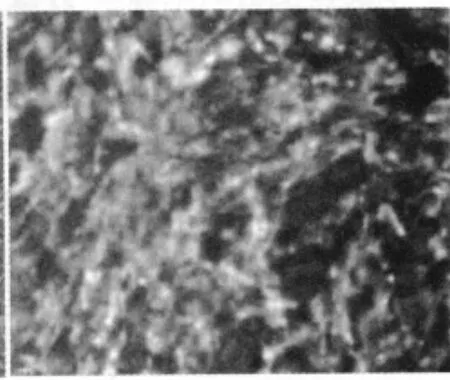
图4 GFP转染后诱导的角膜上皮样细胞(×100)
RT-PCR检测发现:诱导分化的ES细胞中有K12及CD44表达,而K14则无表达,证实转染后ES细胞向角膜上皮细胞方向分化(图5);免疫组化结果显示:角膜上皮样细胞K14的表达很少,而K12及CD44的免疫细胞化学染色阳性(图6)。

图5 K12、K14及CD44 RT-PCR表达情况

图6 K12、K14及CD44免疫组化结果
3 讨论
严重的角膜损伤一直是眼科治疗的难题。一些严重的化学或热烧伤,以及Stevens-Johnson syndrome等疾病,常导致角膜上皮的大量缺失。传统的移植方法虽有一定疗效,但由于供体缺乏、移植免疫及伦理等问题,在临床上的应用发展受到很大限制[4]。重建角膜的关键是获得足够的角膜上皮材料。本研究探索采用诱导有多向分化潜能的ES细胞向角膜上皮细胞分化,为角膜上皮移植提供无限的供体来源。
ES细胞是一种具有全能性、可无限增殖和多向分化潜能的未分化细胞,具有两个重要特性:①自我更新潜能。干细胞在未分化状态下可不断增殖,从而可自我更新。②多向分化潜能。在体内外ES细胞均有分化成许多特定细胞类型的能力。它能迁移到不同部位分化成相应的细胞类型,恢复受损细胞的功能,成为一种新型细胞替代治疗和基因治疗的途径。经丝裂霉素C处理的含LIF的MEF作为饲养层,能够抑制ES细胞的分化和促进其增殖,并使其保持未分化状态以及多向分化潜能[5]。本研究将Ⅳ型胶原作为诱导剂,加入不含LIF的培养板中,诱导体外培养的ES细胞向角膜上皮细胞分化。
GFP是一种由238个氨基酸组成的蛋白,作为荧光标记分子,在研究细胞的分化、细胞移植中具有重要作用[6]。本研究用脂质体方法将含有GFP的质粒转染至小鼠ES细胞中,选择G418筛选并纯化后的GFP阳性ES细胞。将这些能够持续表达GFP的ES细胞在诱导条件下分化成角膜上皮样细胞,并稳定表达GFP,证明GFP基因已完全整合到ES细胞基因组中,这对ES细胞在体内的分化、迁移及整合具有重要意义。
本研究对诱导分化后的ES细胞进行了形态学观察,发现分化后的细胞符合具有典型上皮细胞的形态学特征。细胞呈集落式生长,排列紧密,边界不清;细胞边界清,胞浆较丰富,细胞核大,核仁大。对于眼表上皮而言,区分角膜上皮细胞与结膜上皮细胞是非常重要的,因为它们在功能上有很大区别,影响角膜上皮组织的移植。细胞角蛋白(cytokeratin)是细胞骨架成分中间丝的重要组成部分,是一类在上皮细胞中表达丰富的蛋白质,也是某些上皮细胞重要的标志物,其中,K14主要在结膜上皮表达而不在角膜上皮表达,K12则是在角膜上皮细胞表达的角蛋白,是特异性角膜上皮细胞标志物。而CD44也存在于角膜上皮细胞中,功能与组织修复有关,它可以促进角膜上皮的愈合。本实验诱导分化的上皮细胞CD44和K12表达阳性,而表达K14阴性,说明诱导分化的细胞是角膜上皮细胞,而非结膜上皮细胞。提示ES细胞能在体外定向诱导分化为角膜上皮样细胞。本研究应用RT-PCR技术检测ES细胞及分化的角膜上皮样细胞中均有K12及CD44的表达,而结膜上皮标志物K14则无表达,证实转染GFP后的ES细胞向角膜上皮细胞方向分化。
总之,通过以上实验本研究成功建立了转染GFP基因的ES细胞系,并利用Ⅳ型胶原体外诱导ES细胞定向分化为角膜上皮样细胞,为临床治疗角膜损伤提供新的材料来源。
[1]Kinoshita S,Adachi W,Sotozono C,et al.Characteristics of the human ocular surface epithelium[J].Prog Retin Eye Res,2001,20(5):639-673.
[2]Martin GR.Isolation of a pluripotent cell line from early mouse embryos cultured in medium conditioned by teratocarcinoma stem cells[J].Proc Natl Acad Sci USA,1981,78(12):7634-7638.
[3]唐仕波,邱观婷,黄冰,等.胚胎干细胞向神经细胞诱导分化的实验研究[J].中华医学杂志,2000,80(12):936-938.
[4]Boheler KR,Czyz J,Tweedie D,et al.Differentiation of pluripotent embryonic stem cells into cardiomyocytes[J].Circ Res,2002,91(3):189-201.
[5]Michelini M,Franceschini V,Sihui CS,et al.Primate embryonic stem cells create their own niche while differentiating in three-dimensional culture systems[J].Cell Prolif,2006,39(3):217-229.
[6]Chen BP,Fu S,Qin L,et al.Effects of basic fihroblast growth factor(bFGF)on early stages of tendon healing:a rat patellar tendon model[J].Acta Orthop Scand,2000,71(5):513-518.

