新加达原饮体外抗HBV的实验研究
王礼凤,李长秦,冯海杲,郑旭锐,曹宁
(1.陕西中医学院,陕西 咸阳 712046;2.汾阳市中医学会,山西 汾阳 032200)
乙型肝炎是由HBV引起的,以肝脏炎性病变为主的一种传染性疾病。目前公认的抗病毒治疗药物主要是干扰素及核苷类等,但其疗效均不理想。新加达原饮(Influence of XinjiaDaYuanYin,IXJDY)是在我国明代著名医家吴又可创立的达原饮的基础上,经过长期临床实践加减变化组成的、对慢性乙型肝炎具有较好治疗效果的经验方,本实验以转染HBV DNA全基因HepG2.2.15细胞株为对象,研究新加达原饮体外抗HBV的效果。
1 材料
HepG 2.2.15细胞株购自上海佛雷堡生物发展公司;新加达原饮药液由陕西中医学院药学院制取。
HBsAg和HBeAg酶联免疫检测试剂盒(西安永屹生物发展有限公司,批号CK-E10545H);1640培养基(Gibico公司,批号3856);胎牛血清(Hyclone公司,批号20060404);G418(美国Sigma公司,批号108321-42);0.25%胰酶(Trypsin,Gibco公司,批号 0527);拉米夫定(lamivudine,3TC,葛兰素史克制药有限公司,批号09030037);四甲基偶氮唑蓝(美国Sigma公司),二甲基亚砜(美国Sigma公司)。
2 方法
2.1 IXJDY含药培养液的配制 将新加达原饮药物加入1 000ml水煎煮40min,第2次加入500ml水煎煮0.5h,合并煎液,滤过后得水煎液500ml;将煎好的药液冷却浓缩至每毫升含生药1g,然后醇沉使其体积分数达到80%,即用900ml乙醇静置24h后取上混悬液离心,然后将乙醇回收并定容至350ml备用,然后在超净工作台先用0.45μm的微孔滤膜过滤,再用0.22μm的微孔滤膜过滤除菌,分装于无菌的玻璃瓶中保存于4℃冰箱中备用。实验时用完全培养液将IXJDY稀释成所需终浓度的应用液。
2.2 IXJDY的细胞毒性实验
根据Mosmann建立的四甲基噻唑蓝(MTT法)比色法检测药物对细胞的毒性作用。将2×104个/mL的细胞悬液加入96孔培养板中,每孔100μL,置CO2孵箱(37℃,5%CO2)中培养24h后,细胞贴壁且生长良好,吸除全部培养液,加入用完全培养液将IXJDY系列5 倍稀释成200,40,8,1.6,0.32mg/mL 的应用液100μL,每个质量浓度设6个复孔。连续培养72h,培养结束前4h,每孔加入MTT 10μL,于CO2孵箱中继续培养。4h后小心吸弃上清液后,每孔加DMSO 100μL,微量振荡器振荡5min,使结晶紫完全溶解。自动酶标仪(检测波长570nm,参考波长630nm)读取各孔OD值,记录结果。按Reed-Muench法计算半数细胞毒浓度(TC50)和最大无毒浓度(TC0)。TC50=Antilog[B+(50-B)/(A -B)×C],A=log>50%药物浓度,B=log<50%药物浓度,C=log释稀倍数。
2.3 IXJDY 对 HepG2.2.15 细胞分泌 HBV DNA 的影响
将2×104个/mL的细胞悬液加入24孔细胞培养板,每孔1mL,置 CO2孵箱(37℃,5%CO2)中培养24h后,细胞贴壁且生长良好,吸除全部培养液,根据细胞毒性试验结果,分别加入最大无毒浓度以下系列2倍稀释成5个终质量浓度的应用液:8(A组)、4(B组)、2(C 组)、1(D 组)、0.5(E 组)mg/mL,每个质量浓度设3个复孔。以等量的完全培养液为空白对照,以证实有效的拉米夫定(3TC,0.1mg/mL)为阳性对照药。连续培养72h后,分别吸出上清液于1.5mL灭菌Eppendorf管中,-20℃保存,统一待检。再次加入上述含不同浓度药物的培养液继续培养72h后,分别吸出上清液于1.5mL灭菌Eppendorf管中,-20℃保存,统一待检。
将装有上清液的冷藏管进行逐一排序标号,用离心机分离,然后移入生物安全柜,从每个离心好的冷藏管中取40ul上清液加入离心管中,然后在每个离心管中加入40μl的DNA提取液,置于漩涡混合器振荡混匀5s,取出样品放置于100℃恒温加热金属仪,煮10min,冷确后移入离心机12 000r/min离心5min后将离心管取出,送到生物安全柜,从每个管中吸取上清液2μl加入DNA反应管,将反应管盖好置于离心机离心20s,使上清液在 PCR管中穿过蜡层与反应管中的HBV-PCR反应液Taq酶系充分结合,上机检测结果并记录数据。
2.4 统计学处理 数据采用SPSS 17.0统计软件进行处理,结果以(±s)表示,两组间比较采用成组t检验。P<0.05为差异有统计学意义。
3 结果
3.1 IXJDY 对 HepG2.2.15 细胞毒性
按照Reed-Muench法计算得出:TC0=8.13mg/mL,TC50=14.22mg/mL,即当药物浓度≤TC0时,HepG2.2.15细胞无论在形态上还是数量上与空白对照组比较没有发生明显变化。结果提示,IXJDY对HepG2.2.15 细胞毒性较低,见表 1。
表1 新加达原饮对HepG2.2.15细胞毒性的毒性作用(±s,n=6)
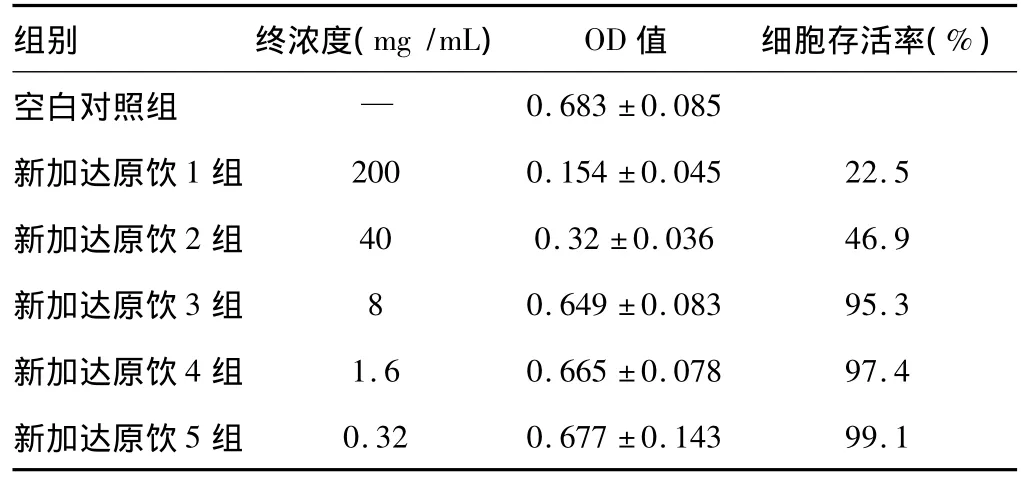
表1 新加达原饮对HepG2.2.15细胞毒性的毒性作用(±s,n=6)
组别 终浓度(mg/mL) OD值 细胞存活率(%)空白对照组 —0.683 ±0.085新加达原饮1 组 200 0.154 ±0.045 22.5新加达原饮2 组 40 0.32 ±0.036 46.9新加达原饮3 组 8 0.649 ±0.083 95.3新加达原饮4 组 1.6 0.665 ±0.078 97.4新加达原饮5组0.32 0.677 ±0.143 99.1
表2 新加达原饮对HepG2.2.15分泌 HBV DNA的抑制作用(±s,n=3)
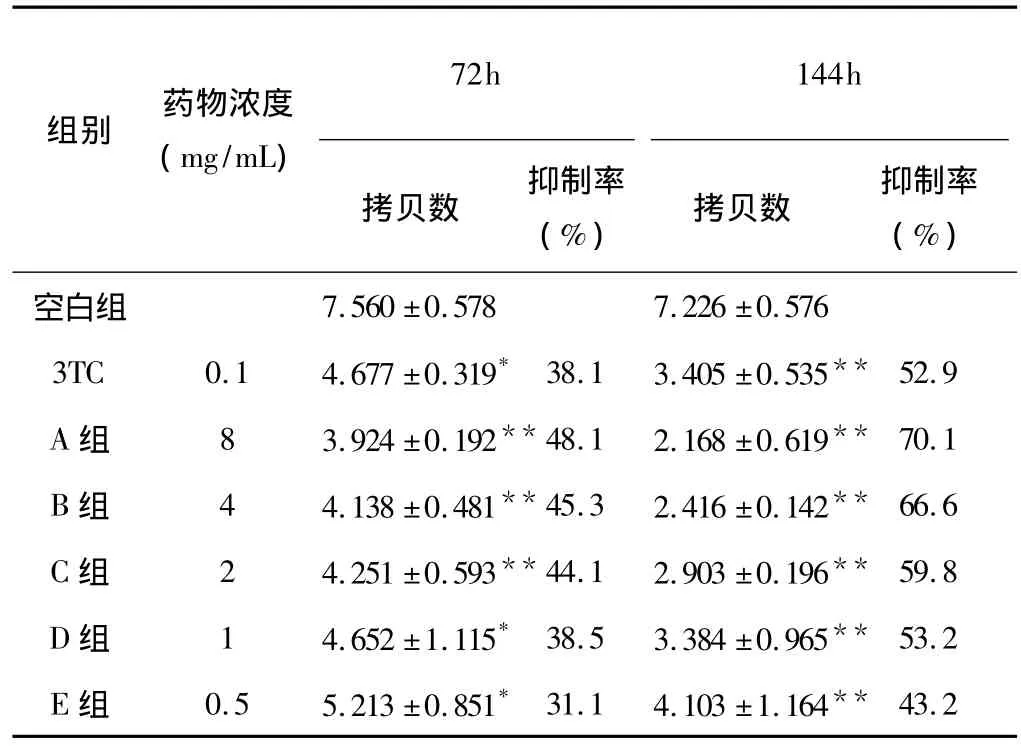
表2 新加达原饮对HepG2.2.15分泌 HBV DNA的抑制作用(±s,n=3)
注:与空白组比较,*P<0.05,**P<0.01。
72h 144h(%) 拷贝数 抑制率(%)空白组组别 药物浓度(mg/mL)拷贝数 抑制率7.560 ±0.578 7.226 ±0.576 3TC 0.1 4.677 ±0.319* 38.1 3.405 ±0.535** 52.9 A 组 8 3.924 ±0.192**48.1 2.168 ±0.619** 70.1 B 组 4 4.138 ±0.481**45.3 2.416 ±0.142** 66.6 C 组 2 4.251 ±0.593**44.1 2.903 ±0.196** 59.8 D 组 1 4.652 ±1.115* 38.5 3.384 ±0.965** 53.2 E 组 0.5 5.213 ±0.851* 31.1 4.103 ±1.164**43.2
3.2 IXJDY 对 HepG2.2.15 细胞上清液中 HBV DNA的抑制作用
阳性对照药物3TC和IXJDY在最大无毒浓度下作用 72h,144h后,对 HepG 2.2.15 细胞分泌 HBV DNA均有一定抑制作用,与空白组比较,有显著性差异(P<0.05,P<0.01),且随着药物浓度和作用时间的增加,其抑制作用逐渐增强,呈现较明显的量效和时效反应关系,见表2。
4 讨论
乙型肝炎是由HBV感染所引起的慢性肝脏炎症性病变,发病率高,目前抗病毒药物很难彻底清除病毒,长期迁延不愈,部分患者将转化为肝硬化、肝癌,或者病情恶化发生肝衰竭,最终引起死亡,严重影响人类健康。中医学认为,乙肝病毒属外感邪气,从其致病特征分析将其归纳为湿热疫毒之邪,本病的产生与肝胆脾胃脏腑关系密切,因脾为湿土之脏,易受湿热所犯,湿热困脾,不能运化水谷,日久湿邪停滞、精微不化,气虚湿盛;湿热中阻,熏蒸肝胆,肝失疏泄,横逆犯脾,脾气益伤;湿热疫毒胶着难解,以致肝胆脾胃互相影响,是导致乙型肝炎慢性化,临床治疗难以速效的根本原因。本实验所用新加达原饮,是以《温疫论》中达原饮为基本方,在多年临床实践的基础上不断筛选优化而成,也曾以消毒丹、消毒饮为名进行过临床观察。《温疫论》达原饮由草果、苍术、槟榔、黄芩、白芍组成,具有开达膜原,辟秽化浊之功效,是治疗湿热疫毒之邪留滞膜原的证候。新加达原饮在达原饮中加入叶下珠、厚朴、柴胡、丹参、姜黄、僵蚕、灵芝、甘草、蝉蜕,全方重用叶下珠、苍术为君,其中叶下珠清热解毒,苍术燥湿健脾,两药相伍清热祛湿各擅其长。以黄芩、厚朴、槟榔为臣,黄芩清热燥湿泻火解毒,厚朴行气燥湿,槟榔行气利水,三味药相互协同加强祛湿清热之功。柴胡与白芍配伍柴胡疏肝理气,白芍柔肝敛阴,既能养肝体,又能助肝用,姜黄、僵蚕、蝉蜕活血化瘀,理气通络,灵芝既可扶正祛邪,又可防止邪气内传。方中僵蚕能升阳中之阳气,姜黄、槟榔降阴中之浊阴,一升一降,内通外和,而杂气之流毒顿消;用柴胡配伍姜黄,一升一降加强气机舒畅的功能;诸药配合可使气机通畅,湿热清除,气血调和。故本方意在清热利湿解毒,疏肝理气活血。圆机活法,方证对应,临床用于治疗慢性乙型肝炎取得较好疗效[1-2]。
实验所用 HepG2.2.15 细胞模型是 Sells等人[3]在1987年将克隆的个头尾相连的HBV DNA全基因及抗G418质粒直接导入受体细胞—人肝癌细胞株HepG2细胞构建而成。该细胞不仅支持HBV DNA的复制,且支持Dane样颗粒的包装与分泌[4],是目前国内外学者公认且广泛用于抗HBV药物筛选和评价等研究的模型。应用HepG2.2.15细胞证实中药在体外的抗乙肝病毒作用的研究屡见不鲜,从1982年Thyagarajan 等[5]首次利用 HepG2.2.15 模型证实了苦味叶下珠的体外抗病毒作用,单味中药、中药单体化合物及有效成分抗HBV活性的研究越来越受到重视。中药复方制剂虽然临床疗效显著,但因其成分复杂,普通的制取工艺难以清除杂质等,通过细胞学研究其抗HBV还比较少。本实验观察到,新加达原饮具有较好地体外抗HBV的效果,为临床应用提供了依据,同时也证实本方组方的思路符合慢性乙型肝炎的发病机制。
为了排除药物非特异性细胞毒性作用造成细胞死亡而影响实验数据,本实验通过醇水双提工艺制取药液,尽量减少中药复方杂质对细胞活性的影响,并采用MTT法观察了IXJDY对HepG2.2.15细胞的毒性作用,结果表明,TC50=14.22mg/mL,TC0=8.1mg/mL,提示IXJDY在8.0mg/mL以下浓度对HepG2.2.15细胞是无毒的,可以以此浓度作为实验的起始药物浓度。实验表明,新加达原饮在体外具有较好的抗HBV作用,与临床应用所反映出的疗效一致,但其确切的作用机制,还有待进一步研究证实。
[1]李长秦,刘国强,杜卫星,等.柴胡甘露饮治疗慢性乙型肝炎193例[J].吉林中医药,2003,23(8):12 -13.
[2]李长秦,郝明霞,刘国强,等.加味消毒丹治疗慢性肝炎停药后远期临床疗效随防[J].陕西中医学院学报,2007,30(1):17 -18.
[3]Sells MA,Chen ML,Acs G.Production ofhepatitisB virus particles in HepG2 cells transfected with cloned hepatitisB virusDNA[J].Proc-NatlAcad SciUSA,1987,84(4):1005 -1009.
[4]Sells MA,Zelent AZ,Shvartsman M,et al.Replicative intermediates of hepatitisB virus inHepG2 cells thatproduce infectiousvirions[J].JVirol,1988,62(8):2836 -2844.
[5]Thyagarajan SP,Thiruneelakantan K,Subramanian S,et al.Invitroinactivation of HbsAg by Ecliptaalba Hasskand Phyllan-thusniruri Linn[J].Indian J Med Res,1982,76(Suppl):124-130.

