新型含嘧啶环的六芳基取代苯的合成*
梁东健, 杨 蕾, 张灯青, 李贤英,1b, 金武松
(1. 东华大学 a. 化学化工与生物工程学院; b. 环境科学与工程学院,上海 201620)
带芳香环的炔类化合物和多取代苯类化合物是两类非常重要的化合物,在生物医药、纳米科学、材料科学以及信息存储等领域具有广阔的应用前景,如,2,3,6,7,10,11-六取代苯并菲是液晶邻域中的典型化合物,具有导电与光导特性[1]; 苯丙素类化合物是非常重要的药物中间体[2];烯二炔类抗生素以其独特的化学结构和高效抗肿瘤活性成为新型抗肿瘤药物[3]等。因此,对其合成方法的研究具有重要的理论与现实意义。
含嘧啶环的六芳基取代苯是一类重要的多取代苯类化合物,从分子结构上看,其刚性芳环内核与外围多官能团赋予了其独特的化学性质。但是,带有多官能团和区域选择性的六取代苯类化合物的合成十分困难,国内外文献鲜见其完整的合成报道。而关于烷基取代的二嘧啶炔的合成至今未见文献报道。
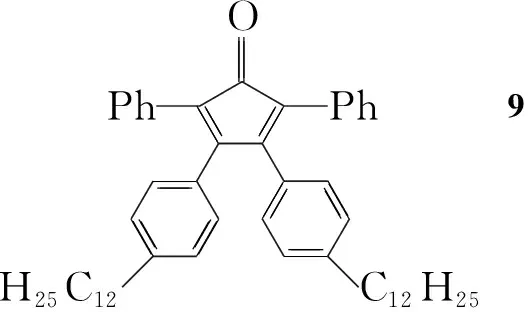
本文以1-十二烯为起始原料,经过Suzuki偶联反应制得5-溴-2-十二烷基嘧啶(2); 2在Pd/Cu催化下与TMSA(三甲基硅乙炔)发生偶联反应制得5-三甲基硅乙炔基-2-十二烷基嘧啶(3);3在TBAF(氟化四丁基铵)作用下制得5-乙炔基-2-十二烷基嘧啶(4);4在Pd/Cu催化下与2发生Sonogashira反应制得未见文献报道的2,2′-二(十二烷基嘧啶)乙炔(5);5与四芳基环戊二烯酮(9)经Diels-Alder环加成反应合成了新型含嘧啶环的六芳基取代苯(1, Scheme 1),总收率7.7%,其结构经1H NMR和13C NMR表征。
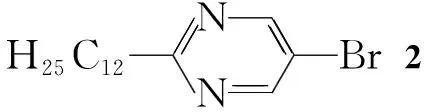
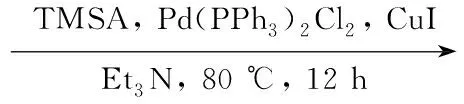

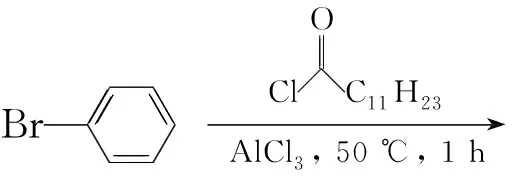
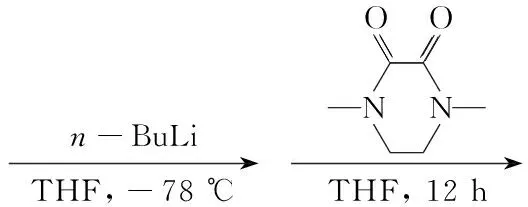
Scheme1
1 实验部分
1.1 仪器与试剂
Brucker Model Advance DMX 400型核磁共振仪(CDCl3为溶剂,TMS为内标)。
2[4,5], 4-溴-1-十二酰基苯(6), 4-溴-1-十二烷基苯(7)和4,4′-十二烷基联苯甲酰(8)[3,6],四芳基环戊二烯酮(9)[7]按文献方法合成;其余所用试剂均为分析纯;二氯甲烷和THF在使用前用金属钠片在氮气保护下回流24 h;三乙胺和1,4-二氧六环加入氢化钙回流3 h后减压蒸出。
1.2 合成
(1)3的合成
氩气保护,在两口瓶中加入2500 mg(1.53 mmol)和三乙胺50 mL,搅拌10 min;加入Pd(PPh3)2Cl225 mg(0.035 mmol)和CuI 12.5 mg(0.018 mmol),回流(80 ℃)下加入TMSA 346.5 mg(3.525 mmol)(反应体系立即变黑),反应24 h。减压蒸除三乙胺,残余物用乙醚溶解,过滤,滤液浓缩后经硅胶柱层析[洗脱剂:V(石油醚) ∶V(乙酸乙酯)=20 ∶1]分离得淡黄色油状液体3420 mg,产率79.5%;1H NMRδ: 8.71(s, 2H), 2.94(t,J=8.0 Hz, 2H), 1.78(m, 2H), 1.32~1.22(m, 18H), 0.87(t,J=8.0 Hz, 3H), 0.28(s, 9H)。
(2)5的合成
在单口瓶中加入3420 mg(1.22 mmol)的THF(3 mL)溶液,搅拌下缓慢滴加TBAF 0.77 g
(2.42 mmol)的THF溶液(体系颜色立即变黑),反应25 min。加蒸馏水30 mL,用二氯甲烷(3×50 mL)萃取,合并有机相,用无水MgSO4干燥,浓缩后经硅胶柱层析(洗脱剂:石油醚)分离得黄色蜡状晶体4 298 mg,产率90%(直接用于下一步反应)。
氩气保护,在两口瓶中依次加入2360 mg(1.11 mmol), Pd(PPh3)2Cl225 mg(0.035 mmol), CuI 12.5 mg(0.018 mmol)和三乙胺20 mL,搅拌下回流(80 ℃)反应30 min;加入4298 mg(1.10 mmol)(反应体系立即变黑),反应24 h。减压蒸除三乙胺,残余物用乙醚溶解,过滤,滤饼用CH2Cl2溶解后经硅胶柱层析[洗脱剂:A=V(石油醚) ∶V(二氯甲烷)=1 ∶5]分离得白色固体5270 mg,产率47%;1H NMRδ: 8.82(s, 4H), 2.98(t,J=8.0 Hz, 4H), 1.82(m, 4H), 1.34~1.25(m, 36H), 0.87(t,J=8.0 Hz, 6H)。
(3)1的合成
氩气保护,在Schlenk管(50 mL)中依次加入9105 mg(0.193 mmol),5100 mg(0.193 mmol)和二苯醚2 mL,搅拌下于300 ℃反应9 h。冷却至室温,直接经硅胶柱层析(洗脱剂:A=1 ∶1)分离得淡黄色固体1183 mg,产率91.5%;1H NMRδ: 8.19(s, 4H), 6.93(d,J=7.0 Hz, 6H), 6.80(d,J=7.0 Hz, 4H), 6.67(s, 8H), 2.82(t,J=7.6 Hz, 4H), 2.34(t,J=7.5 Hz, 5H), 1.64(m, 7H), 1.34(m, 71H), 0.88(t,J=8.0 Hz, 13H);13C NMRδ: 159.95, 159.66, 158.00, 166.28, 142.59, 141.64, 139.03, 138.16, 136.64, 133.24, 131.16, 130.78, 127.35, 126.86, 126.15, 77.32, 77.00, 76.68, 38.79, 35.27, 31.92, 31.06, 29.66, 29.56, 29.47, 29.37, 29.04, 28.77, 28.34, 22.68, 14.11。
2 结果与讨论
由于4在空气中不稳定且易升华,不能长时间放置。因此3在TBAF作用下进行脱去三甲基硅保护基团的反应,得到黄色蜡状固体4后,要立即进行下一步反应。
在1的制备中,由于反应温度很高,氮杂环有可能高温分解,因此严格控制反应时间非常关键。而且,一定要保证在氩气保护下进行,因为是高温反应,所以即使混入少量空气,也会因氧化等副反应导致反应失败。
本文以1-十二烯为主要原料,首次通过Suzuki偶联反应、Sonogashira反应、Diels-Alder环加成反应等合成了未见文献报道的5和1,为六芳基取代苯及其衍生物的合成与应用研究拓展了新的思路。
[1] Ishi-i T, Yaguma K, Kuwahara R,etal. Self-assembling ofn-type semiconductor tri(phenanthrolino)hexaazatriphenylenes with a large aromatic core[J].Org Lett,2006,8(4):585-588.
[2] Stepp B R, Gibbs-Davis J M, Koh D L F,etal. Cooperative melting in caged dimers of rigid small molecule-DNA hybrids[J].J Am Chem Soc,2008,130(30):9628-9629.
[3] 刘文. 烯二炔类抗肿瘤抗生素的生物合成研究进展[J].世界科技研究与发展,2006,27(3):24-31.
[4] 张扬,吴洋,张灯青,等. 新型 5-溴嘧啶衍生物的选择性合成[J].合成化学,2011,19(5):662-664.
[5] Stabel Herwig, Müllen Rabe. Diodelike current-voltage curves for a single molecule-tunneling spectroscopy with submolecular resolution of an alkylated,peri-condensed hexabenzocoronene[J].Angew Chem Int Ed,1995,34(15):1609-1611.
[6] Wehmeier M, Wagner M, Müllen K. Novel perylene chromophores obtained by a facile oxidative cyclodehydrogenation route[J].Chem Eur J,2001,7(10):2197-2205.
[7] Draper S M, Gregg D J, Madathil R. Heterosuperbenzenes:A new family of nitrogen-functionalized, graphitic molecules[J].J Am Chem Soc,2002,27(14):3486-3487.

