白云石煅烧/加压碳酸化循环捕获CO2实验研究
陈惠超 赵长遂
(东南大学能源与环境学院,南京 210096)
(东南大学能源热转换及其过程测控教育部重点实验室,南京 210096)
目前,世界各国在大规模减排、分离CO2技术方面正进行着广泛的研究.然而,经济性是决定CO2分离技术大规模应用的重要因素之一.石灰石、白云石等吸收剂以其分布广泛、价格低廉,其主要成分碳酸钙的分解与合成具有可逆性,能实现循环利用捕获CO2等优势,引起学者们的广泛关注.运用钙基吸收剂在双流化床进行循环煅烧/碳酸化反应是捕集CO2的重要工艺,具体过程是:石灰石送入流化床煅烧炉内煅烧,形成的CaO送入增压流化床碳酸化炉中捕捉CO2,从而使烟气中CO2的排放量降低.碳酸化反应生成的CaCO3通过气固分离器分离至煅烧炉中再生,同时适当补充新鲜的石灰石以保证吸收剂的活性.煅烧炉采用纯氧燃烧方式,便于形成高浓度的CO2(>95%).该工艺可以实现电站在煤燃烧或煤气化以及煤、生物质气化制氢过程中CO2的大规模、高效、经济分离[1-3].分离出的CO2纯度大于95%,可用于石油开采提高石油开采率,或进一步纯化用于食品加工等.
然而,在循环煅烧/碳酸化过程中,石灰石的碳酸化能力随着反应次数的增加下降迅速[4].Abanades等[5]进行了大量实验工作,并对实验数据分析整理后提出了CaO碳酸化转化率与循环次数的函数关系,该式适用实验条件宽(碳酸化温度600~866℃、碳酸化气氛中CO2分压0.01~0.13MPa,煅烧温度750~1060℃,煅烧气氛中CO2分压0~0.4MPa),具有重要参考价值.然而,根据该函数关系式,循环反应20次后,CaO的碳酸化转化率降至0.174.
为此,研究者从对吸收剂进行改性[6-11]、制备高效吸收剂[12]等方面开展了一系列研究工作,以提高钙基吸收剂循环捕获CO2性能.虽然这些研究结果显示,CaO循环捕获CO2能力均有不同程度的提高,但它们离大规模应用还有一定距离,仍需作进一步的检验,并降低改性、制备成本.
研究表明,CaO的碳酸化速率与碳酸化气氛中CO2分压力成比例[13];Oakeson等[14]在碳酸化温度为850~1044℃,CO2分压力为0.245~2.487MPa的条件下获得的研究结果表明碳酸化反应速率是碳酸化温度和CO2分压力的函数,CO2分压力的影响与Langmuir等温吸附形式有很好的关联性.Sun等[15]认为CaO碳酸化本征反应速率与CO2分压力存在变化的反应级数,当CO2分压力大于10kPa时,反应级数由一级转变为零级.虽然学者们对于CaO与CO2分压力之间反应速率关系的意见不完全一致,但普遍认为在一定的CO2分压力范围内,CaO的碳酸化反应与CO2分压力成比例,即提高CO2分压力可望能促进碳酸化反应的进行.因此,采用增加碳酸化压力的方法提高钙基吸收剂的CO2捕获效率,不仅能提高吸收剂循环利用率,减少煅烧耗热量及失活吸收剂处理量,降低煅烧炉耗氧量,而且还能缩小碳酸化炉和煅烧炉的体积,大大降低CO2的捕获成本.采用加压碳酸化/煅烧循环捕获CO2的方法高效捕集CO2将具有更广泛的应用前景.
本文从提高吸收剂循环碳酸化性能出发,考察白云石在不同碳酸化反应压力、温度、碳酸化气氛和煅烧气氛中CO2浓度以及颗粒粒径等条件下的循环碳酸化特性,并与石灰石的循环特性作比较,为推广利用钙基吸收剂循环高效捕集CO2提供理论指导.
1 实验装置及方法
图1为常压煅烧/加压碳酸化反应系统简图.该系统包括常压煅烧炉和加压碳酸化炉,智能温控系统能够准确控制炉内的工作温度,温度偏差为±1℃.实验过程中,将反应样品平铺在磁舟内形成薄层,放置煅烧炉内煅烧充分后,送入加压碳酸化炉内,炉内迅速升压至所需反应压力,待炉内温度稳定后,将气氛切换到碳酸化反应气氛.反应结束后,将炉内压力卸去,取出样品,在高精度电子天平上称重,天平精度为±0.5mg,如此反复,进行循环碳酸化反应.调整给气流量,使进入炉内的气速大于0.1m/s以消除反应过程中外扩散的影响.对样品做预备性实验以确定充分煅烧时间和碳酸化反应时间,分别为10和25min.表1和表2分别示出了本实验的主要反应条件和反应样品的主要成分.循环碳酸化转化率XN按下式计算:
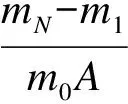
(1)
式中,XN为循环N次后的碳酸化转化率;mN为第N次循环反应后样品质量,g;m1为第1次煅烧后的样品质量,g;m0为反应前样品质量,g;A为样品中CaO含量;WCaCO3和WCaO分别为CaCO3和CaO的摩尔质量,g/mol.

图1 常压煅烧/加压碳酸化反应系统简图

表1 反应条件

表2 白云石的成分分析 %
2 实验结果与分析
2.1 实验结果误差分析
图2给出了碳酸化反应压力(Pcarb)为0.5MPa,碳酸化反应温度(Tcarb)为650和750℃时,白云石的XN随N的变化情况.由图可知,相同碳酸化反应温度条件下,2组实验的碳酸化转化率随循环次数的变化趋势一致,Tcarb为650℃和750℃时,2组实验结果的相对误差分别为2.8%和0.5%.其他工况条件下的实验结果在相似的实验过程下获得,因此本实验结果相对误差可认为均小于5.0%.
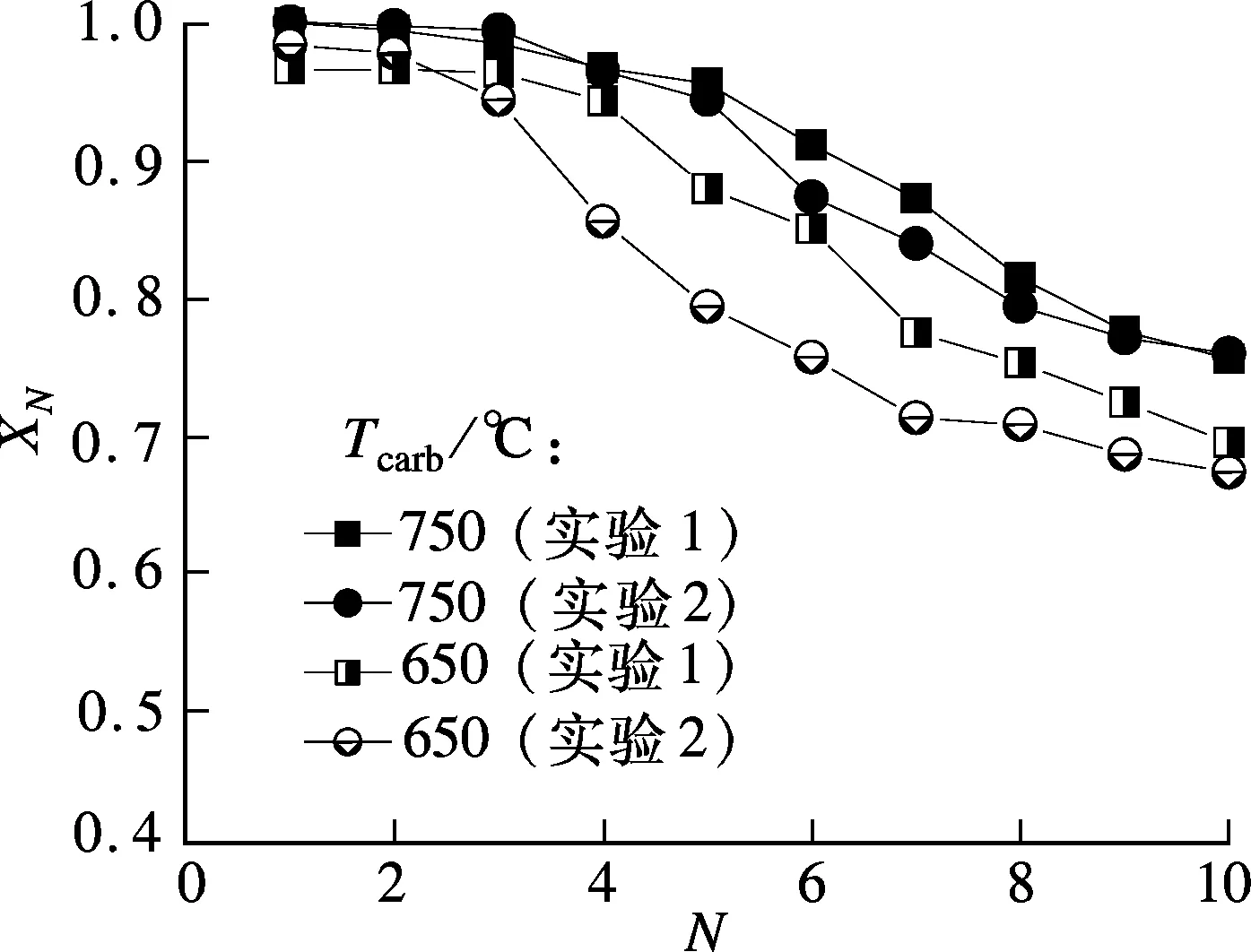
图2 白云石XN随N的变化情况
2.2 Pcarb和Tcarb对白云石加压碳酸化的影响
图3展示了Pcarb和Tcarb对白云石XN的影响.当Tcarb=650℃时,随着N的增加,XN呈下降趋势,如图3(a)所示.随着Pcarb的增加,XN呈现先增加后减小的趋势,白云石在0.5MPa左右呈现出最佳的XN.当Tcarb=700℃时,各压力下的XN均比Tcarb=650℃时大,如图3(b)所示.由化学反应动力学原理可知,反应温度增加,反应速率增大,有利于碳酸化反应的进行.同时,由吉布斯自由能最小原理可得,CaO与CO2反应过程中CO2分压力与平衡温度存在如下关系[16]:
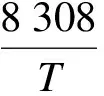
(2)
式中,Peq为CO2平衡分压力,MPa;T为热力学平衡温度,K.
由式(2)可知,Tcarb=700℃对应的CO2平衡分压力为3.5kPa,随着Pcarb从0.1MPa增加至0.7MPa,CO2分压力从15kPa增加至90kPa,碳酸化反应驱动力(CO2分压力与反应温度下CO2平衡分压力之差)增加,有利于碳酸化反应的进行.然而,当CO2分压力增加到一定程度时,XN并不相应增加.其原因可能是,Tcarb=700℃时,CaO与CO2本身的反应速率较快,随着CO2分压力的增加,碳酸化反应速率加快,然而,对于具有一定微观孔隙结构的吸收剂,过快的反应速率将使得CO2来不及通过孔道进入颗粒内部进行反应,便与表面CaO反应生成CaCO3产物层.由于CaCO3产物层的摩尔体积(36.9mol/cm3)较大,为CaO(16.9 mol/cm3)的2倍多,CaO颗粒的孔隙容易被堵塞而阻碍碳酸化反应的继续进行,导致XN并不与Pcarb成比例.Tcarb=700℃时,存在着最佳的Pcarb使得白云石获得最高的XN.
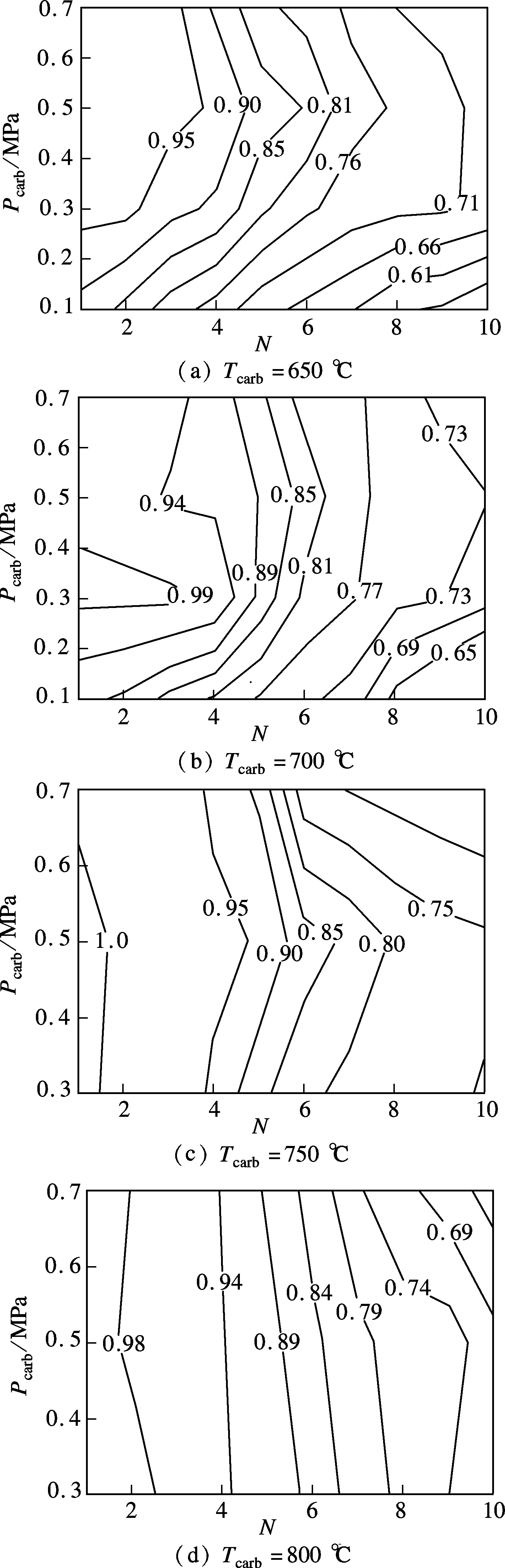
图3 Tcarb和Pcarb对白云石XN的影响(dp<125μm)
当Tcarb=750℃时,XN随Pcarb和N的变化趋势如图3(c)所示,可发现该趋势与图3(a)和(b)类似,且XN与Tcarb=700℃时非常接近.这表明,白云石在Tcarb=700~750℃,Pcarb=0.5MPa时具有相近的循环碳酸化反应特性.当Tcarb=800℃时,XN随N增加下降相对较快,如图3(d)所示.其原因主要是,Tcarb增加,对应的CO2平衡分压力增加,在一定Pcarb下吸收剂的碳酸化反应驱动力减小,不利于碳酸化反应进行,随着N的增加,煅烧过程和碳酸化过程的烧结作用造成了吸收剂在高、低Tcarb下的孔隙结构改变,并逐渐产生差异,使得有利于CO2扩散和反应的中孔和微孔在高Tcarb下大量减少,不利于碳酸化反应进行,XN随N的增加下降较快.
2.3 dp对白云石加压碳酸化的影响
钙基吸收剂的颗粒粒径对其碳酸化反应有一定的影响.一般而言,固体颗粒粒径dp越小,其在气固化学反应控制条件下的反应程度越大,转化率越高;dp越大,孔扩散在反应中占主导地位,气固反应阻力增大,对气固反应不利[17].图4展示了dp对白云石XN的影响.由图可知,在Tcarb=700℃,Pcarb为0.5和0.7MPa下,3种dp下白云石前4次循环反应的XN均非常接近1.0.第5次循环反应开始,0.7MPa压力下各dp的XN随N的增加下降较快,但XN差别不大,循环10次后XN为0.68左右.这表明,高Pcarb对dp具有较好的适应性.而在0.5MPa下,存在最佳的dp,为150~300μm,经历10次循环反应后,XN=0.77.由烧结动力学可知,固体粉末dp越大,其比表面积越小,本征表面能驱动力越小;dp越小,比表面越大,本征表面能驱动力越大[18].dp较大的白云石抗烧结能力比dp较小的白云石强,而白云石的dp较大时,其在碳酸化过程中又容易限制CO2的扩散,因此,在孔扩散控制和烧结机理共同作用下,白云石在dp=150~300μm时获得了最高的XN.
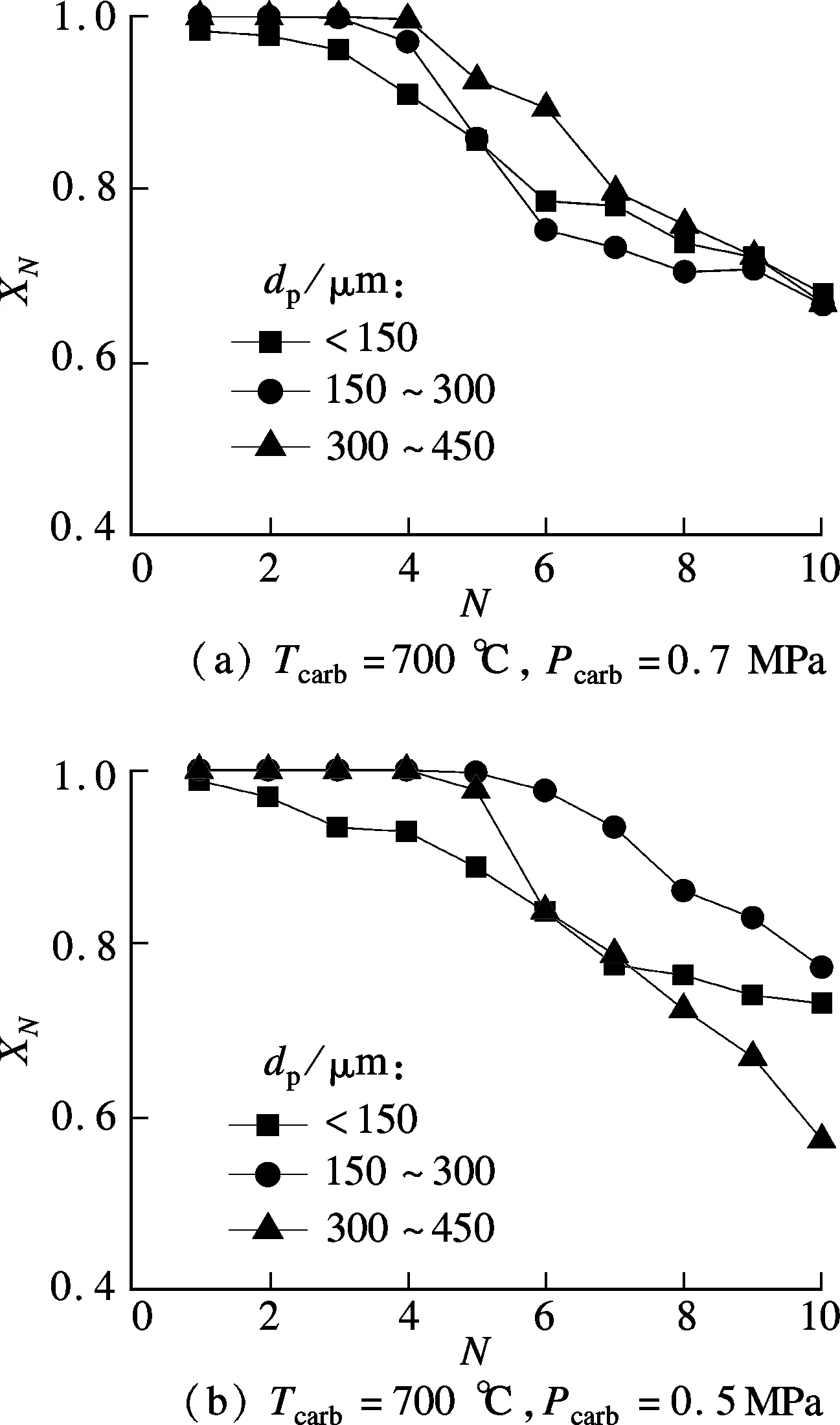
图4 dp对白云石XN的影响
2.4 碳酸化气氛中CO2浓度对白云石加压碳酸化的影响
Mess等[4]认为,CaO的碳酸化反应过程中,CO2通过孔隙扩散的有效扩散系数Deff为

(3)
式中,D为孔扩散系数,cm/s2;Cs为反应气相本体中CO2浓度,mol/cm3(假设CaO表面CO2浓度为零);MCaO为CaO的摩尔质量,g/mol;ρCaO为CaO的真实密度,g/cm3.由此可见,反应气氛中CO2浓度越大,CO2的有效扩散系数也越大,碳酸化反应越快,对碳酸化反应越有利.
然而,在加压碳酸化反应过程中,XN并不随碳酸化气氛中CO2浓度的增加而增加.图5示出了Pcarb=0.5MPa,Tcarb=700℃,dp<125μm时碳酸化气氛中CO2浓度对白云石XN的影响.由图可知,碳酸化气氛中CO2浓度从15%增加到100%时,XN随N的增加均呈下降趋势,各CO2浓度下转化率差别非常小.这主要是因为白云石本身拥有优良的孔隙结构,Pcarb=0.5MPa,Tcarb=700℃下的碳酸化反应较快,碳酸化气氛中CO2浓度的增加对进一步增加碳酸化反应速率的贡献有限,XN没有明显地提高.白云石本身具有一定的抗烧结能力,其在不同的CO2浓度下,随着N的增加,能保持比较高的碳酸化转化率.因此,对于孔隙结构优越的吸收剂,在加压碳酸化条件下,其对碳酸化气氛中CO2浓度具有很好的适应性.对于本实验,在Tcarb=700℃和Pcarb=0.5MPa条件下,烟气CO2浓度为15%时便可获得较高的XN,表明0.5MPa和700℃下对捕捉烟气中的CO2非常适合,可高效捕获具有不同CO2浓度气体中CO2,净化烟气或合成气.

图5 碳酸化气氛中CO2浓度对白云石XN的影响
2.5 煅烧气氛中CO2浓度对白云石加压碳酸化的影响
CO2已被普遍认为是一种烧结媒介,会强烈影响石灰石煅烧产物的微观结构,其分压力的增加对石灰石分解的动力学特性存在影响[19].然而,煅烧气氛中CO2浓度对钙基吸收剂加压碳酸化的影响程度是一个值得关注的问题.
图6给出了dp<125μm的白云石在Tcarb=700℃时,煅烧气氛中CO2浓度对XN的影响.由图可知,Pcarb=0.1MPa时,XN受煅烧气氛中CO2浓度的影响相对较大,煅烧气氛中无CO2时X1为0.88~0.92,循环反应10次后,XN下降为0.55,而CO2浓度为80%时XN则下降为0.46,多衰减了9%.常压碳酸化反应下,煅烧气氛中CO2浓度的增加加速了XN的衰减.Pcarb=0.5MPa时,随着煅烧气氛中CO2浓度从0增加到100%,各CO2浓度下的XN差异较小,循环反应10次后,XN均大于0.73,其中无 CO2时的XN比 CO2浓度为100%时高2%,CO2浓度为80%与CO2浓度为100%时的XN几乎没有差别.表明煅烧气氛中CO2浓度对加压碳酸化反应XN的影响较小,加压碳酸化反应对煅烧气氛具有较好的适应性,0.5MPa和700℃的碳酸化反应条件在某种程度上可以弥补煅烧气氛中CO2浓度的增加导致吸收剂微观结构改变的影响.

图6 煅烧气氛中CO2浓度对白云石XN的影响
2.6 白云石与石灰石的加压碳酸化特性比较
图7给出了在Tcarb=700℃,Pcarb=0.5MPa,dp<125μm,CO2浓度为15%和100%的碳酸化气氛下,白云石与石灰石的循环碳酸化特性及其循环反应10次后的孔容积特性.由图7(a)可知,白云石在2种碳酸化气氛中的XN均比石灰石高.经历10次循环后,15%CO2浓度下白云石的XN为0.73,而石灰石的为0.62.白云石在较宽的CO2浓度下均获得比较高的XN.而石灰石的XN随着碳酸化中CO2浓度的增加下降较快.白云石对CO2浓度的适应性更强,在循环碳酸化过程能保持较高的XN.图7(b)说明了在CO2浓度为15%的碳酸化气氛下白云石的XN较石灰石高的主要原因.白云石的加压碳酸化/循环煅烧反应对颗粒粒径、煅烧气氛及碳酸化气氛中CO2浓度等具有相对宽松的适应范围,易实现高效捕获烟气中CO2及净化合成气的规模化应用.
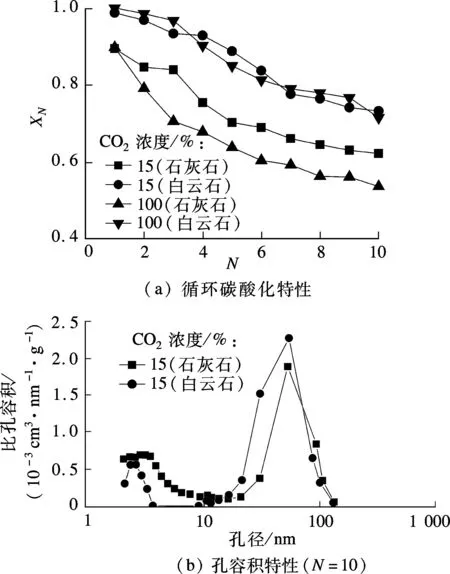
图7 白云石与石灰石的循环碳酸化特性及孔容积特性比较
3 结论
1)Pcarb一定时,XN随Tcarb增加先增加后减小,在Tcarb=700℃左右,XN随N的增加下降缓慢;在15% CO2浓度下,Tcarb一定时,在一定范围内提高Pcarb有利于碳酸化反应.随着Pcarb的进一步增加,由于CaCO3产物层的快速形成抑制了碳酸化反应的继续进行,XN并不随Pcarb的增加成比例增加.
2)Tcarb和Pcarb对CaO的碳酸化反应具有相互补偿的作用,存在最佳的Tcarb和Pcarb使得CaO获得最佳的XN,在本实验范围内,0.5MPa和700~750℃的碳酸化反应条件下获得最佳的XN.
3) 白云石的加压碳酸化对煅烧气氛中CO2浓度具有较好的适应性,并具有较宽的粒径(dp=0~450μm)适应范围.相同反应条件下其XN较石灰石的大.
4) 增加碳酸化气氛中CO2浓度并不一定能提高钙基吸收剂加压条件下的XN,在0.5MPa和700℃下提高CO2浓度,XN没有显著提高.
5) 白云石具有较石灰石优越的孔隙结构是其获得较高XN的主要原因.
)
[1]Abanades J C,Rubin E S,Anthony E J.Sorbent cost and performance in CO2capture systems [J].IndustrialandEngineeringChemistryResearch,2004,43(13): 3462-3466.
[2]Koppatz S,Pfeifer C,Rauch R,et al.H2rich product gas by steam gasification of biomass with in situ CO2absorption in a dual fluidized bed system of 8 MW fuel input [J].FuelProcessingTechnology,2009,90(7/8): 914-921.
[3]Weimer T,Berger R,Hawthorne C,et al.Lime enhanced gasification of solid fuels: examination of a process for simultaneous hydrogen production and CO2capture [J].Fuel,2008,87(8/9): 1678-1686.
[4]Mess D,Sarofim A F,Longwell J P.Product layer diffusion during the reaction of calcium oxide with carbon dioxide [J].EnergyandFuels,1999,13(5): 999-1005.
[5]Abanades J C,Alvarez D.Conversion limits in the reaction of CO2with lime [J].EnergyandFuels,2003,17(2): 308-315.
[6]Roesch A,Reddy E P,Smirniotis P G.Parametric study of Cs/CaO sorbents with respect to simulated flue gas at high temperature [J].IndustrialandEngineeringChemistryResearch,2005,44(16): 6458-6490.
[7]Li Y J,Zhao C S,Chen H C,et al.Cyclic CO2capture behavior of KMnO4-doped CaO-based sorbent [J].Fuel,2010,89(3):642-649.
[8]Hughes R W,Lu D,Anthony E J,et al.Improved long-term conversion of limestone-derived sorbents for in situ capture of CO2in a fluidized bed combustor [J].IndustrialandEngineeringChemistryResearch,2004,43(18): 5529-5539.
[9]Manovic V,Anthony E J.Steam reactivation of spent CaO-based sorbent for multiple CO2capture cycles [J].EnvironmentalScienceandTechnology,2007,41(5): 1420-1425.
[10]Sun P,Grace J R,Lim C J,et al.Investigation of attempt to improve cyclic CO2capture by sorbents hydration and modification [J].IndustrialandEngneeringChemistryResearch,2008,47(6): 2024-2032.
[11]Chen H C,Zhao C S,Duan L B,et al.Enhancement of reactivity in surfactant-modified sorbent for CO2capture in pressurized carbonation [J].FuelProcessingTechnology,2011,92(3): 493-499.
[12]Lu H,Smirniotis P G.Calcium oxide doped sorbents for CO2uptake in the presence of SO2at high temperatures [J].IndustrialEngineeringChemicalResearch,2009,48(11): 5454-5459.
[13]Grasa G S,Abanades J C,Alonso M,et al.Reactivity of highly cycled particles of CaO in a carbonation/calcination loop [J].ChemicalEngineeringJournal,2008,137(3): 561-567.
[14]Oakeson W G,Cutler I B.Effect of CO2pressure on the reaction with CaO [J].JournaloftheAmericanCeramicSociety,1979,62(11/12): 556-558.
[15]Sun P,Grace J R,Lim C J,et al.Determination of intrinsic rate constants of the CaO-CO2reaction [J].ChemicalEngineeringScience,2008,63(1): 47-56.
[16]Baker E H.The calcium oxide-carbon dioxide system in the pressure range 1-300 atmospheres [J].JournalofChemicalSociety,1962,70: 464-470.
[17]塞克利.气-固反应 [M].北京: 中国建筑工业出版社,1986.
[18]崔国文.缺陷、扩散与烧结 [M].北京: 清华大学出版社,1990.
[19]Adanez J,Diego L F,Garcia-Labiano F.Calcination of calcium acetate and calcium magnesium acetate: effect of the reacting atmosphere [J].Fuel,1999,78(5): 583-592.

