樟子松树皮多酚螯合亚铁制备工艺
刘 荣,王 蕾,栾淑莹,姜元松,王振宇
(1.东北林业大学林学院,黑龙江哈尔滨150040;2.哈尔滨工业大学食品科学与工程学院,黑龙江哈尔滨150090)
传统的矿物质产品,往往由于其分子量较大而不能通过肠壁,因而不能为人体所吸收利用;而如硫酸亚铁等传统的小分子化合物由于其在胃酸消化过程中,亚铁离子与载体分离变为自由基后容易被氧化,从而也会降低其生物效价。多酚螯合亚铁同氨基酸螯合亚铁类似具有极高的生物效价,由于其分子量相对较小,因而能够轻松通过肠壁被人体所吸收。并且多酚螯合亚铁不随着外界环境pH的变化而改变,即使在胃部消化较低pH条件下依然能稳定存在不分解,因此,能够随着血浆顺利地进入人体各个组织,最终在不同组织酶的作用下最终分解释放原子耦合剂到更稳定的运铁蛋白中,被人体所利用。笔者通过水体系合成法研究建立了樟子松树皮多酚与亚铁离子螯合的工艺,并通过响应面法优化了螯合工艺方法,得到了螯合率较高的环状螯合物,并对其结构进行了分析,旨在提升松多酚以及亚铁离子的生物效价。
1 材料与方法
1.1 材料
1.1.1 药品及试剂。无水碳酸钠、福林酚试剂,均为分析纯,天津市光复精细化工研究所;浓盐酸,标品级,Sigma公司;氢氧化钠、无水乙醇、抗坏血酸、氯化亚铁、还原铁粉,均为分析纯,天津市东丽区天大化学试剂厂;溴化钾,光谱纯,天津市东丽区天大化学试剂厂。
1.1.2 仪器与设备。DK-8D三孔电热恒温水槽,上海一恒科技有限公司;JA2003电子天平,上海良平仪器仪表有限公司;PB-10 pH计,SARTORIUS AG Made by Sartorious;DHG-9240电热恒温鼓风干燥箱,上海一恒科技有限公司;T6紫外可见分光光度计,北京普析通用仪器有限责任公司;722可见分光光度计,上海光谱仪器有限公司;TGL-16G低速台式离心机,上海安亭科学仪器厂;Nicolet Avatar360红外光谱仪,美国Nicolet公司。
1.2 方法
1.2.1 原料的制备。称取一定质量的樟子松树皮粉末,以体积分数50%的乙醇为作为溶剂,按料液比1∶25 g/ml进行水浴浸提,水浴温度为50℃,浸提时间4 h,将浸提液在4 000 r/min的转速下高速离心20 min后减压浓缩蒸去乙醇,得到多酚粗提物;将上述粗提物在上样体积30 ml,上样浓度3 mg/ml,洗脱剂乙醇浓度为53%条件下进行一次纯化,控制进样速度以及洗脱速度分别为5.0 BV/h以及4.5 BV/h;收集纯化物,减压浓缩蒸去乙醇,得到樟子松树皮多酚一级纯化产物。将上述得到一级纯化物在上样浓度为4.3 mg/ml,上样体积为60.7 ml,径高比为1∶30.6的条件下进行二次纯化,控制洗脱流速为2.0 BV/h;收集纯化物,减压浓缩蒸去乙醇,得到樟子松树皮多酚二级纯化产物,备用。
1.2.2 Folin-Ciocalteu法测定多酚含量。
1.2.2.1 标准曲线的绘制。精确称取0.100 g干燥的没食子酸用蒸馏水溶解并定容于100 ml容量瓶中,配置成1 000 μg/ml的没食子酸标准储备液;同时分别移取等体积的1.0~7.0 ml的没食子酸标准溶液于100 ml容量瓶中并定容,配置成浓度分别为 10、20、30、40、50、60、70 μg/ml的工作液。在10 ml棕色容量瓶中分别移取不同浓度的工作液1 ml,各加入体积分数10%福林酚试剂5 ml后充分振荡摇匀,反应5 min加入质量分数为7.5%的碳酸钠溶液4 ml并通过蒸馏水定容;置于25℃恒温水浴条件下反应1 h,以蒸馏水为空白对照于765 nm波长下测定混合体系吸光值[1]。
将横坐标定为没食子酸质量浓度,纵坐标定为765 nm波长下混合体系吸光值,最终绘制标准曲线。
1.2.2.2 样品含量的测定。在10 ml棕色容量瓶中加入样液1 ml,加入体积分数10%福林酚试剂5 ml后充分振荡摇匀,反应5 min加入质量分数为7.5%的碳酸钠溶液4 ml并通过蒸馏水定容;置于25℃恒温水浴条件下反应1 h,以蒸馏水为空白对照于765 nm波长下测定混合体系吸光值。根据标准曲线计算样品含量。纯度公式:
P(%)=[(C×V)/W]×100%
式中,C为复溶后多酚的浓度(mg/ml);V为复溶时定容的体积(ml);W为烘干后的干物质重(mg)。
1.2.3 松多酚螯合亚铁制备工艺的研究。
1.2.3.1 松多酚螯合亚铁制备工艺流程。量取一定体积的浓度为1 mg/ml的樟子松树皮多酚二级纯化物溶液于具塞试管,用1 mol/L氢氧化钠溶液以及1 mol/L盐酸溶液调节所需pH,按照一定质量比加入一定体积的1 mg/ml的氯化亚铁溶液,并向体系中按照氯化亚铁质量的1/10加入复合抗氧化剂(还原铁粉以及抗坏血酸)[2],封口后放入水浴条件下按照一定温度反应1 h,将所得溶液取出在10 000 r/min条件下离心分离除去沉淀,收集上清液并按照公式计算亚铁离子螯合率。

1.2.3.2 pH对多酚螯合亚铁螯合效果的影响。量取7份浓度为1 mg/ml的樟子松树皮多酚二级纯化物溶液,每份各10 ml置于具塞试管中,用1 mol/L氢氧化钠溶液以及1 mol/L盐酸溶液将多酚溶液 pH 分别调节为 3、4、5、6、7、8、9,并按照质量比为2∶1加入浓度为1 mg/ml的氯化亚铁溶液,并向体系中按照加入氯化亚铁质量的1/10加入复合抗氧化剂(还原铁粉以及抗坏血酸),封口后放入50℃水浴条件下反应1 h,将所得溶液取出在10 000 r/min条件下离心分离除去沉淀,收集上清液测定游离多酚含量,并按照公式计算亚铁离子螯合率。确定pH对多酚螯合亚铁螯合效果的影响,并确定最适宜螯合pH。
1.2.3.3 松多酚与亚铁离子质量比对多酚螯合亚铁螯合效果的影响。量取7份浓度为1 mg/ml的樟子松树皮多酚二级纯化物溶液,每份各10 ml置于具塞试管中,用1 mol/L氢氧化钠溶液以及1 mol/L盐酸溶液调节多酚溶液pH为7,并分别按照质量比为 1.0∶1、1.5∶1、2.0∶1、2.5∶1、3.0∶1、3.5∶1、4.0∶1加入浓度为1 mg/ml的氯化亚铁溶液,并向体系中按照加入氯化亚铁质量的1/10加入复合抗氧化剂(还原铁粉以及抗坏血酸),封口后放入50℃水浴条件下反应1 h,将所得溶液取出在10 000 r/min条件下离心分离除去沉淀,收集上清液测定游离多酚含量,并按照公式计算亚铁离子螯合率。确定质量比对多酚螯合亚铁螯合效果的影响,并确定最适宜螯合质量比。
1.2.3.4 反应温度对多酚螯合亚铁螯合效果的影响。量取7份浓度为1 mg/ml的樟子松树皮多酚二级纯化物溶液,每份各10 ml置于具塞试管中,用1 mol/L氢氧化钠溶液以及1 mol/L盐酸溶液调节多酚溶液pH为7,按照质量比为3∶1加入浓度为1 mg/ml的氯化亚铁溶液,并向体系中按照加入氯化亚铁质量的1/10加入复合抗氧化剂(还原铁粉以及抗坏血酸),封口后分别放入 30、35、40、45、50、55、60 ℃水浴条件下反应1 h,将所得溶液取出在10 000 r/min条件下离心分离除去沉淀,收集上清液测定游离多酚含量,并按照公式计算亚铁离子螯合率。确定反应温度对多酚螯合亚铁螯合效果的影响,并确定最适宜螯合反应温度。
1.2.4 响应面法优化松多酚螯合亚铁制备工艺。根据樟子松多酚与亚铁离子螯合单因素试验结果,选取对螯合效果影响较大的3个因素,根据Box-Behnken设计原理,以螯合率为响应值,做3因素3水平共17组响应面分析试验,以研究所选的3个因素对樟子松多酚与金属亚铁离子螯合的综合影响。
1.2.5 松多酚亚铁离子螯合物紫外光谱法结构分析。
1.2.5.1 松多酚亚铁离子螯合物的制备。量取浓度为1 mg/ml的多酚二级纯化物溶液60 ml于100 ml三角瓶中,用1 mol/L氢氧化钠及1 mol/L盐酸调节所需pH为7,按照质量比3∶1加入20 ml的1 mg/ml的氯化亚铁溶液,并向体系中按照加入氯化亚铁质量的1/10加入复合抗氧化剂(还原铁粉以及抗坏血酸),封口后放入水浴内于45℃条件下反应1 h,将所得溶液取出在10 000 r/min条件下离心分离洗涤收集沉淀,烘干待用。
1.2.5.2 紫外光谱分析。分别配制质量分数为5%的松多酚螯合亚铁以及松多酚甲醇溶液,采用紫外-可见分光光度计进行200~700 nm全波长扫描,以甲醇为参比溶液测定松多酚及其亚铁离子螯合物的光谱并绘制全波长扫描曲线。
1.3 数据分析 该研究所有进行试验均平行3次,数据表示为:结果±标准差;图像及图表分析均采用Excel(2007)、Design-expert(7.0)软件进行处理。
2 结果与分析
2.1 标准曲线的绘制 根据“1.2.2.1”方法测得没食子酸标准曲线方程为:y=0.010 56x+0.009 9,其中横坐标x表示没食子酸质量浓度,纵坐标y表示765 nm波长下的吸光值。在0~70 μg/ml的没食子酸质量浓度范围内,其吸光值大小与浓度线性关系良好,相关系数R2=0.999 7。根据标准工作曲线方程按照“1.2.2.2”方法中纯度计算公式计算,得樟子松树皮多酚二级纯化物纯度为(62.06±1.67)%。
2.2 pH对多酚螯合亚铁螯合率的影响 pH条件带来的环境体系变化是影响金属离子与多酚进行螯合反应的一个重要因素。在pH较低的强酸体系环境中,氢离子将与微量元素金属离子共同争夺供电基团,严重影响鳌合物的形成;而在pH较高的强碱环境体系中,羟基会存在与供电基团共同争夺微量元素离子生成沉淀的可能性[3]。此外,植物多酚配体的化学结构以及金属配体的构型,甚至是加料顺序以及有机抗衡离子特性,甚至是微小的反应条件的改变,都会影响螯合物的螯合效果[4]。
由图1可知,pH在3~7范围内,随着pH的升高,亚铁离子螯合率升高,当pH=7时亚铁离子螯合率达到最大,为(28.11±1.83)%,随后开始逐渐降低,这是因为pH升高意味着体系环境中羟基增加,游离的亚铁离子与羟基结合形成氢氧化亚铁的机会增加,不利于松多酚螯合亚铁的生成和稳定,且生成的副产物氧化亚铁极易氧化,生成沉淀。同时,pH增大带来的碱性环境会增加亚铁离子氧化的机会,不利于亚铁离子的稳定存在。因此,考虑pH=7为螯合反应最适宜pH。
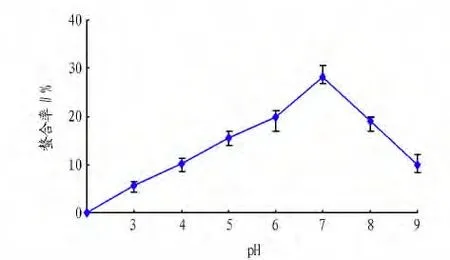
图1 pH对螯合率的影响
2.3 反应质量比对多酚螯合亚铁螯合率的影响 不同微量元素金属离子其配位数量也自然不同,鳌合物中微量元素金属离子与植物多酚的摩尔比可以是 1∶1、1∶2、1∶3。事实证明,当反应体系为较低浓度时,微量元素与植物多酚易形成配位数为1∶1的鳌合物;当浓度升高时可形成配位数为2∶1的鳌合物[5]。而通常情况下考虑植物多酚与金属离子以1∶1的配位数形成螯合物时是具有一定电荷的,因此易被胶体吸附固定;而以2∶1的配位数形成的的内络盐电荷趋于中性,螯合环最为稳定。
当多酚与金属离子形成螯合物时,一个中心金属离子可以和多个多酚类化合物形成螯合环,形成环数越多其化学结构越稳定。反应质量比是影响金属离子与多酚螯合反应的因素之一。由图2可知,随着反应物质量比的增大,多酚与亚铁离子螯合率先逐渐增大,当反应质量比为3∶1时,螯合率达到最大,为(37.74±2.66)%,这是因为反应质量比较小时,部分亚铁离子未与多酚形成环状螯合物,或形成的环状螯合物结构不稳定,经过离心操作,亚铁离子可能再次游离出来;随着反应质量比继续增大,亚铁离子螯合率出现逐渐降低,这可能是由于超过一定反应质量比,多酚与亚铁离子形成的环状螯合物结构不稳定。此外,加入过量多酚显然在经济上造成一定的浪费。因此,考虑反应物质量比为3∶1时为最适宜。
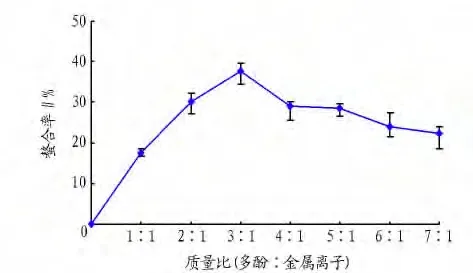
图2 反应质量比对螯合率的影响
2.4 反应温度对亚铁离子螯合率的影响 鳌合温度及鳌合时间对鳌合效果的影响不如配位比作用明显,大多数不同来源的植物多酚与微量元素金属离子常温下就能螯合成环,30 min螯合过程即可完成[6]。但是考虑实际生产中不同来源植物多酚种类较多,不同的植物多酚物质再同金属离子鳌合对反应条件要求也略有差别,所以对不同反应选择最适宜鳌合温度与时间也较为关键。更重要的是,螯合温度的升高有利于植物酚类物质的充分浸出[7],因此要调节温度至适于反应的进行。
由图3可知,在反应温度为30~45℃范围内,随着温度的升高,亚铁离子螯合率先逐渐增大;当温度达到45℃时,亚铁离子螯合率达到最大,为(38.71±1.84)%。这是由于多酚与亚铁离子螯合反应为吸热反应,因此会随着反应温度的升高而鳌合反应进行越迅速;但是,当反应温度超过45℃并且继续增大时,多酚与亚铁离子螯合率逐渐降低,这是因为事实上螯合反应温度过高反而会使螯合反应进行不完全,而且会对原料多酚结构造成不可逆破坏,造成原料的损失;且在高温下反应又会对螯合物结构造成不可逆破坏。因此,考虑螯合温度45℃为最适宜反应温度。

图3 反应温度对螯合率的影响
2.5 响应面法优化樟子松树皮多酚与亚铁离子螯合试验 根据樟子松树皮多酚与亚铁离子螯合单因素试验结果,选取螯合pH,螯合质量比以及螯合温度作为3个影响因素,根据Box-Behnken设计原理,以螯合率为响应值,做3因素3水平共17组响应面分析试验,以研究所选的3个因素对樟子松树皮多酚亚铁离子螯合的综合影响,3因素3水平编码见表1。利用Design-Expert 7.0设计响应面试验方案,试验测定结果见表2。
通过Design-expert7.0软件进行二次响应面回归分析,对所测得的结果拟合后得到的回归方程为:R=38.52-3.27X1+0.57X2-0.69X3+0.41X1X2+0.65X1X3+0.53X2X3-6.77X12-3.12X22-1.45X32,相关系数R2=0.996 5。回归模型方差分析见如下:

表1 多酚与亚铁离子螯合工艺响应面试验因素水平
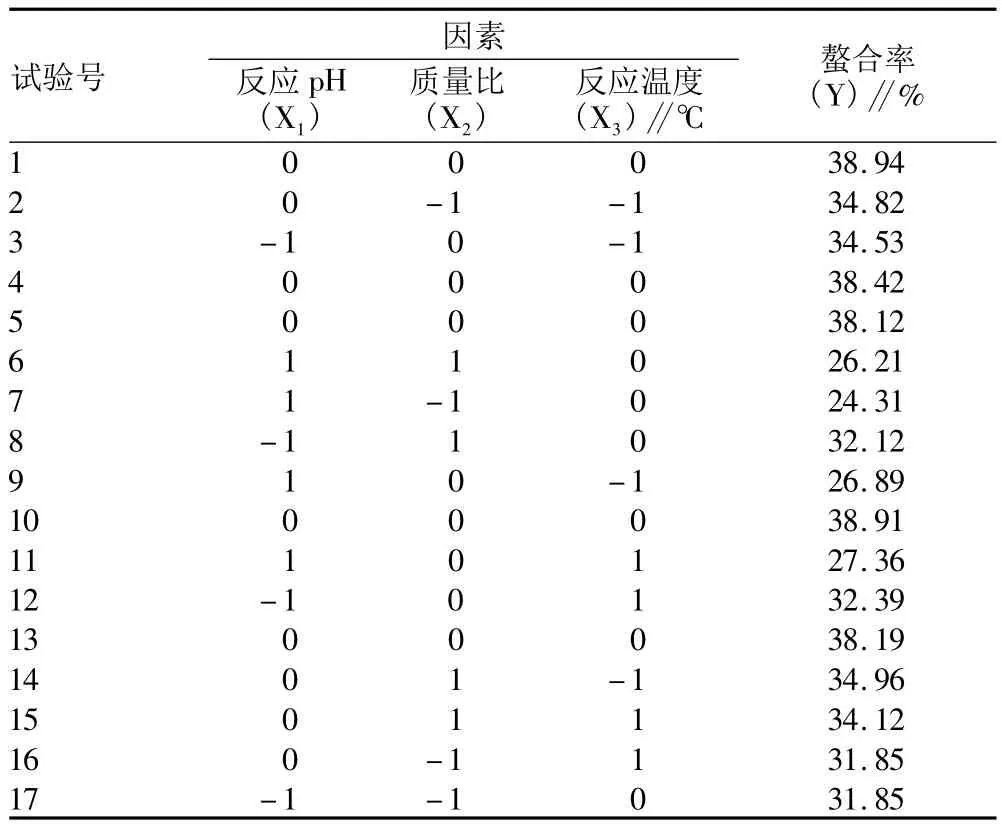
表2 多酚与亚铁离子螯合工艺响应面数据分析
由此看出,模型的回归显著性水平P<0.000 1,小于0.05,表明亚铁离子螯合率与各因素(螯合pH、质量比、反应温度)之间有显著关系,而误差项不显著,说明该方程与实际情况拟合很好,说明此模型能充分解释响应中的变异。从分析结果可以看出,反应pH(X1)、质量比(X2)以及反应温度(X3)(P<0.01)均极显著,说明3个因素对亚铁离子螯合率的影响均极为突出;除了反应pH(X1)与质量比(X2)间的交互影响(P>0.05)不显著外,其他因素间的交互影响(P<0.05)均显著。为进一步验证最佳点的数值,应用SAS8.0响应面分析方法对回归模型进行分析,寻找最优响应结果为:樟子松树皮多酚与亚铁离子螯合的最优工艺条件的编码值对应的试验值为X1=6.75,X2=3.05,X3=43.58℃,此时方程的最大预测值为39.04%。
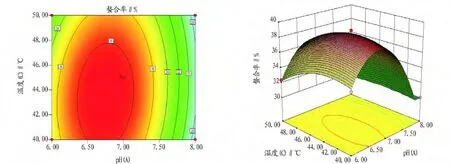
图4 螯合pH与反应温度交互作用对多酚螯合亚铁螯合率的综合影响

图5 螯合质量比与反应温度交互作用对多酚螯合亚铁螯合率的综合影响
其中螯合pH与反应温度、质量比与反应温度间存在着交互作用,具体交互作用如图4、5所示。在响应面优化的条件下进行验证,获得最大螯合率的螯合条件是螯合pH=6.8,反应质量比为3.1∶1,反应温度为43.6℃,平行试验测得制备出的亚铁离子螯合物螯合率(39.16±0.89)%,回归模型的预测值与实测值非常接近。
2.6 紫外光谱分析 从松多酚与松多酚亚铁离子螯合物的紫外全波长扫描图谱可以看出:当松多酚与亚铁离子螯合成环后,其吸收峰会产生一定程度的偏移,说明松多酚与亚铁离子发生了螯合反应而改变了松多酚原有结构,由松多酚以及其亚铁螯合物紫外图谱(图6)可知,松多酚的最大吸收峰出现在波长为317 nm处,且最大吸光值为2.642;而松多酚螯合亚铁的最大吸收峰出现在波长为299 nm处,且最大吸收峰高度明显下降,最大吸光值仅为1.451,说明松多酚与亚铁离子因发生螯合反应而导致结构发生改变。

图6 樟子松树皮多酚二级纯化产物及其螯合亚铁紫外图谱
3 结论
通过响应面法优化水体系合成法制备樟子松树皮多酚螯合亚铁制备工艺,得到最佳条件为螯合pH为6.8,质量比为3.1∶1,螯合温度为43.6℃,此工艺条件下樟子松树皮多酚与亚铁离子发生螯合反应螯合率可达到(39.16±0.89)%。通过紫外光谱分析研究表明,樟子松树皮多酚与亚铁离子发生螯合反应,导致其原有结构发生改变,反应产品呈螯合物特征结构。
[1]赵玉红,翟亚楠,王振宇.樟子松树皮中松多酚的提取工艺研究及提取方法比较[J].食品工业科技,2013(4):304-309.
[2]张晓鸣.甘氨酸螯合铁合成及其理化性质的研究[D].无锡:江南大学,2004.
[3]张小燕,杜建强,李亚萍,等.复合氨基酸鳌合铜的制备工艺研究[J].西北大学学报,2002,32(1):36-38.
[4]WANG R H,HONG M C,ZHAO Y J,et al.Synthesis and crystal structure of a novel two-dimensional corrugated coordination polymer[J].Inorg Chem Commun,2002,5(7):487-489.
[5]褚鹏云,张同超.氨基酸鳌合铁的研究及应用现状[J].高师理科学刊,2008,28(2):65-68.
[6]林萍,宋常英,张晓鸣.甘氨酸鳌合铁的合成工艺[J].无锡轻工业大学学报,2004,23(2):53-57.
[7]穆杰,徐阳春,沈其荣.废弃鸡毛化学降解工艺研究[J].农村生态坏境,2005,21(2):77-80.

