三磷酸胞苷二钠注射液中精氨酸含量的测定
苏 雨,张 娜
(济南利民制药有限责任公司,山东济南250200)
三磷酸胞苷二钠注射液中精氨酸含量的测定
苏 雨,张 娜
(济南利民制药有限责任公司,山东济南250200)
目的建立一种三磷酸胞苷二钠注射液中精氨酸的含量测定方法。方法茚三酮分光光度法,检测波长567 nm。结果精氨酸在2~12μg·m L-1范围内呈良好的线性关系,R2=0.998 2,标准曲线回归方程为:A=0.078 8C+0.032 9。平均回收率98.96%(n=9),RSD为1.24%。结论此法结果准确,简便快速,可用于三磷酸胞苷二钠注射液中精氨酸的测定。
三磷酸胞苷二钠注射液;精氨酸;茚三酮
三磷酸胞苷二钠为核苷酸衍生物,是一种应用广泛的辅酶类药,具有调节物质代谢、营养神经和抗血管硬化的药理作用。由于三磷酸胞苷二钠分子内含高能磷酸键,导致其对热和水解都不稳定。目前,市售产品主要有冻干粉针和注射剂两个剂型,且都加入精氨酸或碳酸胍作为稳定剂[1]。根据《关于发布化学药品注射剂和多组分生化药注射剂基本技术要求的通知》(国食药监注【2008】7号)附件1的要求,注射剂应采用符合注射用要求的辅料,但目前为止,没有药用级碳酸胍。精氨酸是《中国药典》2010年版(二部)收载的常用氨基酸类药,有注射级和口服级,因此精氨酸将成为三磷酸胞苷二钠注射用制剂稳定剂的唯一选择。注射用剂型辅料用量直接影响药品的安全性和有效性,根据国食药监注【2008】7号附件1对注射剂辅料的要求和已经开展的仿制药一致性评价的要求(注射剂的一致性评价虽然尚未开始但已安排在固体口服制剂之后进行),需要对辅料用量进行控制。精氨酸具有药理活性,作为辅料使用更需要严格控制。因此建立三磷酸胞苷二钠注射液中精氨酸含量的测定方法有实践意义。已报导及收载入《中国药典》的精氨酸的测定方法包括HPLC法[2]、电位滴定法[3]和分光光度法[4,5]。HPLC法分为衍生化和非衍生化两种,衍生化方法操作过程相对繁琐,易引入操作误差;非衍生化方法[2]检测波长较低(206 nm),易受色谱系统干扰。分光光度法是基于坂口反应显色,但显色物质不稳定易褪色,所以可将显色物质萃取转移至有机相中形成稳定体系再测,虽然能解决稳定性的问题但增加了操作步骤。辅料含量的测定方法应针对具体品种针对性研究。本文采用基于茚三酮反应的分光光度法测三磷酸胞苷二钠注射液中精氨酸的含量[6]。一方面,茚三酮反应法是测定氨基酸的经典方法,简便快捷、准确度高;另一方面,三磷酸胞苷二钠注射液中原料及其他辅料(pH调节剂)不干扰测定。
1 仪器与试药
T6新世纪型紫外-可见分光光度计(北京普析通用分析仪器有限公司);精氨酸(湖北省潜江市四维氨基酸有限公司,批号:20090801);三磷酸胞苷二钠(杭州美亚药业有限公司,批号:120103);茚三酮(天津市科密欧化学试剂有限公司,批号:HG/T 3456-2000);其他试剂均为分析纯,纯化水为公司自制。
2 方法与结果
2.1 溶液的配制和检测方法
2.1.1 溶液的配制 2%茚三酮试液(显色剂):称取茚三酮2.0 g置100 mL量瓶中,乙醇溶解并定容,得2%茚三酮试液。
磷酸盐缓冲液(pH 6.5及其他):配制0.05 mol ·L-1的KH2PO4水溶液用0.1 mol·L-1的NaOH水溶液调至pH为6.5以及其他目标pH值。
对照品溶液(0.2 mg·mL-1):准确称取精氨酸20 mg,加纯化水溶解并定量稀释至100 mL,得精氨酸对照品溶液。
供试品溶液:按照注射液处方配制三磷酸胞苷二钠溶液,取适量用纯化水定量稀释制成含精氨酸约0.2 mg·mL-1的供试品溶液。
空白溶液:按照三磷酸胞苷二钠注射液处方配制不含精氨酸的三磷酸胞苷二钠溶液,并按照供试品溶液配制的稀释步骤稀释,得空白溶液。
2.1.2 检测方法 分别精密量取精氨酸对照品溶液0.5、1.0、1.5、2.0、2.5、3.0 mL,各置50 mL量瓶中,各加磷酸盐缓冲液(pH 6.5)6 mL,再加入2%茚三酮试液1.5 mL,摇匀,置沸水浴中20 min,取出迅速冷却至室温,纯化水定容,同步做空白,以空白为参比,于567 nm测吸光度,以对照品溶液浓度值与相应的吸光度值计算线性回归方程。精密量取三磷酸胞苷二钠注射液适量,用纯化水定量稀释制成含精氨酸约0.2 mg·mL-1的供试品溶液。精密量取供试品溶液2 mL,置50 mL量瓶中,同法操作并同步做空白,以空白为参比,于567 nm测吸光度,计算精氨酸含量。
2.2 检测波长的确定 分别按“2.1.2”项下制备对照品显色溶液和空白显色溶液,以水为参比在400~790 nm波长范围内进行扫描[7],确定各溶液的吸收情况。配制过程及扫描结果见表1。

表1 对照品显色溶液、空白显色溶液制备及扫描结果
结果表明,对照品显色溶液的最大吸收波长为567 nm,空白显色溶液无吸收。
2.3 显色时间的确定 精密量取对照品溶液各2 mL,置50 mL量瓶中,共6份,分别加磷酸盐缓冲液(pH 6.5)6 mL,再分别加入2%茚三酮试液1.5 mL,摇匀,沸水浴加热,分别于不同时间取出,迅速冷却至室温,纯化水定容,同法做空白,以纯化水为参比,于567 nm测对照品显色溶液和空白的吸光度,结果见表2。
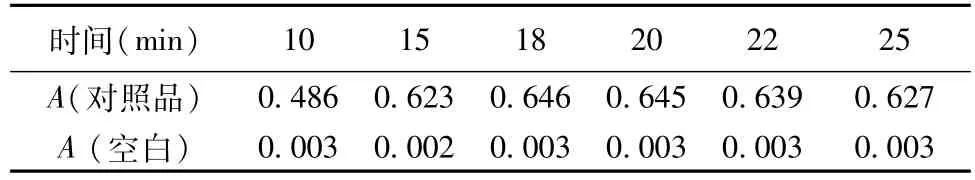
表2 不同显色时间的吸光度
结果表明,沸水浴条件下,在15~22 min之间对照品显色溶液吸光度值稳定且较高,22 min之后吸光度下降,空白的吸光度在实验的时间范围内稳定,因此,可选择沸水浴显色时间20 min。
2.4 显色剂用量的确定 精密量取精氨酸对照品溶液各2 mL,置50 mL量瓶中,共5份,分别加磷酸盐缓冲液(pH 6.5)6 mL,再分别加入不同量2%茚三酮试液,摇匀,沸水浴加热20 min,取出迅速冷却至室温,纯化水定容,同步做空白,以空白为参比,于567 nm测吸光度,结果见表3。

表3 显色剂用量
结果表明,加入1.5 mL显色剂时吸光度A最大,说明显色充分,选择显色剂用量为1.5 mL。
2.5 缓冲盐pH和用量的确定 据理论推测和相关文献[8]报道,茚三酮反应的最佳酸碱度环境为弱酸性环境,强酸和强碱均不利于显色产物的稳定。本研究采用磷酸盐缓冲对研究了不同pH对显色反应的影响。精密量取精氨酸对照品溶液各2 mL,置50 mL量瓶中,共5份,分别加入pH为6.5、6.6、6.7、6.8、7.0的磷酸盐缓冲液6 mL,再分别加入2%茚三酮试液1.5 mL,摇匀,沸水浴加热20 min,取出迅速冷却至室温,纯化水定容,同步做空白,以空白为参比,于567 nm测吸光度,结果见表4。
三磷酸胞苷二钠注射液pH偏碱性,需加入足量的缓冲盐才能保证反应体系维持在预定pH范围,本文研究了pH为6.5的磷酸盐缓冲液用量对显色反应的影响。操作同上,结果见表5。

表4 不同pH对显色反应的影响
结果表明pH为6.5,吸光度A最大,因此选择pH 6.5的缓冲盐进行试验;缓冲盐用量6 mL时显色最充分,所以选择用量为6 mL。
2.6 线性关系试验 分别精密量取精氨酸对照品溶液0.5、1.0、1.5、2.0、2.5、3.0 mL,各置50 mL量瓶中,各加磷酸盐缓冲液(pH 6.5)6 mL,再加入2%茚三酮试液1.5 mL,摇匀,置沸水浴20 min,取出迅速冷却至室温,纯化水定容,同步做空白,以空白为参比,于567 nm测吸光度,结果如表6。

表6 线性关系试验数据
以对照品溶液浓度值与相应的吸光度值计算线性回归方程,得A=0.078 8C+0.032 9,相关系数(R2)为0.998 2。结果表明精氨酸浓度在2.0~12.0μg·mL-1的范围内,浓度与吸光度呈良好的线性关系。
2.7 仪器精密度试验 通过相应试验考察仪器的精密度。精密量取精氨酸对照品溶液2 mL,置50 mL量瓶中,加磷酸盐缓冲液(pH 6.5)6 mL,加2%茚三酮试液1.5 mL,摇匀,沸水浴加热20min,取出迅速冷却至室温,纯化水定容,同步做空白,以空白为参比,于567 nm处测吸光度,连续测定6次吸光度,结果如表7。

表7 仪器精密度试验
对照品显色溶液平均吸光度为0.639,RSD为0.15%,表明仪器精密度良好。
2.8 回收率试验 精密量取对照品溶液1.6 mL 3份,分别置50 mL量瓶中,各加空白溶液2 mL、加磷酸盐缓冲液(pH 6.5)6 mL、2%茚三酮试液1.5 mL,摇匀,沸水浴加热20 min,取出迅速冷却至室温,纯化水定容,作为80%(6.4μg·mL-1)的供试品显色溶液1、2、3,同步以空白溶液做空白,以空白为参比测吸光度;精密量取对照品溶液2.0 mL 3份,分别置50 mL量瓶中,同法操作测定3份100%(8μg·mL-1)的供试品显色溶液的吸光度;精密量取对照品溶液2.4 mL 3份,分别置50 mL量瓶中,同法操作测定3份120%(9.6μg·mL-1)的供试品显色溶液的吸光度。根据上述线性回归方程计算供试品中精氨酸的测得量,计算回收率,数据见表8。

表8 精氨酸含量测定回收率试验数据
平均回收率为98.96%,RSD为1.24%,结果表明该方法测定三磷酸胞苷二钠注射液中精氨酸回收率良好。
2.9 重复性试验 精密量取三磷酸胞苷二钠注射液(中试样品,批号:130903)适量用纯化水定量稀释制成含精氨酸约0.2 mg·mL-1的供试品溶液。取供试品溶液2 mL,置50 mL量瓶中,加磷酸盐缓冲液(pH 6.5)6 mL,加2%茚三酮试液1.5 mL,摇匀,沸水浴加热20 min,取出迅速冷却至室温,纯化水定容。共测定6份样品。同步做空白,以空白为参比,于567 nm测吸光度,结果见表9。
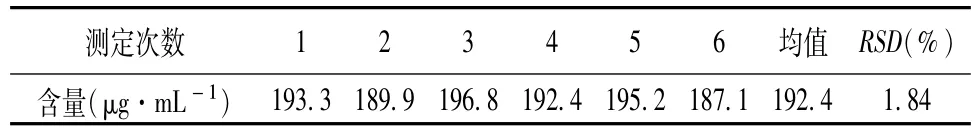
表9 含量测定重复性试验
测定结果RSD为1.84%,表明本方法重复性良好。
3 讨论
本方法基于经典的氨基酸检测方法—茚三酮反应法,此方法研究充分,稳定可行,并且已被定为多种不同行业领域的法定方法。该方法对氨基酸类没有专属性,但本品中原料及其他辅料不含氨基酸结构,所以不影响精氨酸的检测。制剂中辅料的检查方法应根据具体品种而具体研究,因此对于本品中精氨酸的检查不需要用色谱来实现分离后再检测,本方法已能完全满足对辅料控制的要求。
[1]张存国,孙平,胡方锋.三磷酸胞苷二钠注射液生产工艺筛选[J].武汉工程大学学报,2013,35(8):27-32.
[2]国家药典委员会.中华人民共和国药典2010年版(二部)[S].北京:中国医药科技出版社,2010:176.
[3]王刚毅,赵长缨,关一鸣.电位滴定法测定L-精氨酸的含量[J].黑龙江医药,1997,10(2):69.
[4]蒙绮芳,赖碧清,周锡梁.L-精氨酸测定方法的研究[J].氨基酸和生物资源,1998,20(3):1-4.
[5]梁新红,赵功玲,赵瑞香.分光光度法测定发酵液中L-精氨酸含量[J].食品与发酵工业,2007,33(4):122-125.
[6]黄松,吴月娜,刘梅,等.茚三酮比色法测定青天葵中总游离氨基酸的含量[J].中国中医药信息杂志,2010,17(12):50-51.
[7]朱瑾,李新霞,陈坚.茚三酮比色法测定蒜氨酸原料药中总氨基酸的含量[J].西北药学杂志,2008,23(3):136-138.
[8]张鉴棠,汤秀玉,韩红.不同pH对氨基酸与茚三酮呈色反应的影响[J].东南大学学报(医学版),1992,11(2):126-128.
Determ ination of arginine in Cytidine Disdoium Triphosphate Injection
SU Yu,ZHANG Na
(Jinan Limin Pharmaceutical Co.,Ltd.,Jinan 250200,China)
ObjectiveTo develop amethod for the determination of arginine in Cytidine Disdoium Triphosphate Injection.MethodsNinhydrin spectrophotometry based on ninhydrin reaction was studied at 567nm.ResultsThere was a good linear relationship in the range of2~12μg·mL-1for arginine(R2=0.998 2).The standard curve equation was A=0.078 8C+0.032 9.The average recovery was 98.96%with RSD of1.24%(n=9).ConclusionThemethod was accurate,simple and rapid,and it can be used for the determination of arginine in Cytidine Disdoium Triphosphate Injection.
Cytidine Disdoium Triphosphate Injection;Arginine;Ninhydrin
R927.2
A
2095-5375(2014)09-0522-004
苏雨,男,研究方向:制药工艺及设备管理,E-mail:sulucky11017@163.com
张娜,女,研究方向:药物研发,Tel:1861554855,E-mail:zhangwenna1130@126.com

