2-碘苯甲酰胺类化合物的合成
刘 晓,陈万里,莫卫民,
(1.浙江工业大学化工学院,浙江 杭州 310014;2.浙江工业大学分析测试中心,浙江 杭州 310014)
酰胺类化合物是一类重要的具有杀菌活性的化合物[1-2]。1966 年自第一个酰胺类杀菌剂萎锈灵成功开发以来,酰胺类化合物作为杀菌剂一直是新农药领域研究的热点,近年来成功开发出新型的酰胺类杀菌剂,例如啶酰菌胺(Bosealid)、氟啶酰菌胺(Fluopicolid)、吡噻菌胺(Penthiopyra)、噻唑菌胺(Ethaboxam)和苯酰菌胺(Zoxamid)等[3],解决了最初的作用点单一、杀菌谱不广[4]等问题,并因其活性高、作用机理独特、环境友好等优点,在杀菌剂市场中占据着相当重要的地位。除了杀菌活性,很多酰胺类化合物还呈现出独特的杀虫机制[5]和良好的除草性能,因此对于酰胺类化合物的合成研究具有十分广阔的发展前景。
笔者设计并合成了7 个新的酰胺类衍生物(3a~3g,式1),其结构通过1H NMR、13C NMR 分析确证。具体合成路线如下。
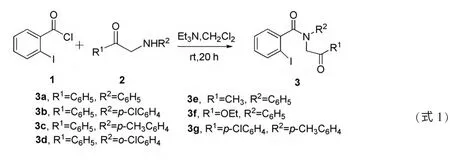
1 实验部分
1.1 仪器和试剂
仪器:Bruker 500 MHz 型核磁共振仪(CDCl3为溶剂,TMS 为内标);WRS—l 型数字熔点仪(温度未校正)。
试剂:均为市售AR 或CP,使用前经常规处理。
1.2 中间体的合成
中间体1 的合成:在100 mL 反应瓶中加入7.4 g 邻碘苯甲酸,然后加入过量的氯化亚砜,在100 ℃下回流2 h,减压蒸馏得到邻碘苯甲酰氯7.1 g。
中间体2 的合成(以溴代苯乙酮与苯胺的反应为例)[6]:在干燥的250 mL 单口烧瓶中,加入苯 胺(6.5 mL,70 mmol)、溴代苯乙 酮(6.7 g,35 mmol)、乙腈(70 mL),常温下反应24 h。产生的胺盐过滤掉,把滤液蒸干,残留物溶于乙酸乙酯(100 mL),加入水(50 mL)、5%柠檬酸(50 mL)、饱和食盐水(25 mL)萃取。有机层用无水MgSO4干燥,蒸干,用乙醇重结晶,得到黄色固体6.8 g(产率93%)。
1.3 目标产物3 的合成(以合成化合物3a 为例)[7]
在干燥的50 mL 两口烧瓶中,加入1-苯基-2-苯胺基乙酮(2.1g,10mmol)、无水二氯甲烷(30 mL)、三乙胺1.7 mL(1.2 equiv),反应瓶置于冰浴中,慢慢滴加溶于无水二氯甲烷(10 mL)中的邻碘苯甲酰氯3.2 g(1.2 equiv),滴加完后常温下反应20 h。反应液蒸干,加水,乙酸乙酯萃取,无水MgSO4干燥,蒸干,用乙醇重结晶,得到淡黄色固体3a 3.1 g。
2 结果与讨论
结合1.2 与1.3 所述方法得到产物3a,计算其收率为71%,m.p.123 ℃~125 ℃。1H NMR(500 MHz,CDCl3):δ 8.03(d,J=7.3 Hz,2H),7.71(d,J=7.9 Hz,1H),7.61(t,J=7.4 Hz,1H),7.50(t,J=7.7 Hz,2H),7.35 (d,J=7.6 Hz,2H),7.26 (dd,J1=7.7 Hz,J2=1.5 Hz,1H),7.20~7.10(m,4H),6.89(td,J1=7.7 Hz,J2=1.5 Hz,1H),5.37 (s,2H);13C NMR(125 MHz,CDCl3):δ 193.3,170.3,142.6,141.8,139.2,135.2,133.7,129.9,129.2,129.0,128.8,128.1,127.7,127.5,127.3,93.6,56.3。
采用类似方法合成3b~3g。
3b:橙色固体,收率66%;m.p.63 ℃~65 ℃。1H NMR(500 MHz,CDCl3):δ 8.02(d,J=7.4 Hz,2H),7.72(d,J=7.9 Hz,1H),7.62(t,J=7.4 Hz,1H),7.51(t,J=7.8 Hz,2H),7.31(d,J=8.7 Hz,2H),7.26 (dd,J1=7.7 Hz,J2=1.6 Hz,1H),7.21~7.17 (m,1H),7.16(d,J=8.7 Hz,2H),6.93 (td,J1=7.8 Hz,J2=1.6 Hz,1H),5.33 (s,2H);13C NMR (125 MHz,CDCl3):δ 193.2,170.2,141.5,141.1,139.3,135.0,133.8,133.3,130.2,129.2,129.1,128.8,128.1,127.5,93.4,56.2。
3c:淡黄色固体,收率70%;m.p.62 ℃~64 ℃。1H NMR (500 MHz,CDCl3):δ 8.03 (d,J=7.2 Hz,2H),7.71(d,J=7.6 Hz,1H),7.61(t,J=7.4 Hz,1H),7.50(t,J=7.7 Hz,2H),7.26~7.23(m,3H),7.16(td,J1=7.4 Hz,J2=0.7 Hz,1H),6.97 (d,J=8.2 Hz,2H),6.89 (td,J1=7.8 Hz,J2=1.7 Hz,1H),5.33(s,2H),2.22(s,3H);13C NMR(125 MHz,CDCl3):δ 193.4,170.4,141.9,140.0,139.1,137.3,135.2,133.6,129.8,129.6,129.1,128.8,128.1,127.5,127.3,93.5,56.3,20.9。
3d:棕黄色固体,收率63%;m.p.115 ℃~117 ℃。1H NMR (500 MHz,CDCl3):δ 8.03 (d,J=7.9 Hz,2H),7.84(dd,J1=7.5 Hz,J2=1.8 Hz,1H),7.78(d,J=7.9 Hz,1H),7.60(t,J=7.4 Hz,1H),7.50(t,J=7.7 Hz,2H),7.35 (dd,J1=7.8 Hz,J2=1.9 Hz,1H),7.20(dd,J1=7.7 Hz,J2=1.2 Hz,1H),7.14~7.07(m,3H),6.89 (td,J1=7.8 Hz,J2=1.6 Hz,1H),6.04 (d,J=17.5 Hz,1H),4.63 (d,J=17.5 Hz,1H);13C NMR(125 MHz,CDCl3):δ 192.7,170.5,141.0,139.7,139.4,135.2,133.6,132.7,131.6,130.3,130.0,129.5,128.7,128.1,127.7,127.2,127.1,93.9,54.0。
3e:米黄色固体,收率65%;m.p.103 ℃~105 ℃。1H NMR (500 MHz,CDCl3):δ 7.70 (d,J=8.0 Hz,1H),7.27(d,J=7.4 Hz,2H),7.18(t,J=7.7 Hz,2H),7.15~7.09(m,3H),6.87(td,J1=7.8 Hz,J2=2.0 Hz,1H),4.68(s,2H),2.29(s,3H);13C NMR(125 MHz,CDCl3):δ 202.1,170.2,142.5,141.5,139.2,130.0,129.0,127.5,127.3,93.6,59.4,27.4。
3f:米白色固体,收率91%;m.p.88 ℃~90 ℃。1H NMR (500 MHz,CDCl3):δ 7.70 (d,J=7.9 Hz,1H),7.32~7.29 (m,2H),7.20 (t,J=7.6 Hz,2H),7.15~7.09(m,3H),6.90~6.85(m,1H),4.62(s,2H),4.28(d,J=7.1 Hz,2H),1.33(t,J=7.1 Hz,3H);13C NMR (125 MHz,CDCl3):δ 170.3,168.8,142.4,141.5,139.2,130.0,129.0,128.9,127.6,127.2,93.5,61.5,51.4,14.2。
3g:米白色固体,收率73%;m.p.116 ℃~118 ℃。1H NMR (500 MHz,CDCl3):δ 7.97 (d,J=8.5 Hz,2H),7.71(d,J=7.9 Hz,1H),7.47(d,J=8.5 Hz,2H),7.25~7.21(m,3H),7.16(t,J=7.5 Hz,1H),6.97(d,J=8.2 Hz,2H),6.89 (td,J1=7.8 Hz,J2=1.6 Hz,1H),5.29(s,2H),2.22(s,3H);13C NMR(125 MHz,CDCl3):δ 192.3,170.4,141.8,140.1,139.8,139.1,137.5,133.6,129.9,129.7,129.5,129.1,127.5,127.3,93.5,56.2,20.9。
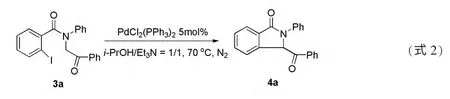
通过对以上7 种产物进行1H NMR 和13C NMR 测试,可以确认其结构为设计的目标产物,且收率均在60%以上。2-碘-N-(2-氧代-2-苯乙基)-N-苯基苯甲酰胺类化合物具有多个官能团,可以发生进一步的转化,丰富该类化合物的应用范围。例如,本实验室以2-碘-N-(2-氧代-2-苯乙基)-N-苯基苯甲酰胺(3a)为底物,在金属Pd催化下发生分子内α-芳基化反应合成异吲哚啉酮类化合物(4a),见式2。
4a:米白色固体,收率88%;m.p.178 ℃~180 ℃。1H NMR(500 MHz,CDCl3):δ 7.99(d,J=7.4 Hz,1H),7.95(d,J=7.5 Hz,2H),7.69(d,J=8.0 Hz,2H),7.64(t,J=7.5 Hz,1H),7.54~7.47(m,4H),7.33(t,J=8.0 Hz,2H),7.29(d,J=7.5 Hz,1H),7.13(d,J=7.4 Hz,1H),6.65 (s,1H);13C NMR (125 MHz,CDCl3):δ 193.3,167.7,138.8,138.1,135.0,134.2,132.3,129.4,129.2,129.1,128.7,125.1,124.8,122.5,121.0,67.0;HRMS-ESI:[M+H]+m/z calcd for C21H16NO2314.1181,found 314.1177。
3 结论
以邻碘苯甲酸为原料,经酰氯化、酰胺化反应合成了各目标产物,路线可行,操作简单,反应条件温和,方法经济、安全。各目标产品经过熔点、核磁共振波谱表征并确认了其结构。本方法为2-碘苯甲酰胺类化合物的合成提供了一条便捷、可靠、经济和通用性强的路线。
[1]刘长令.世界农药大全——杀菌剂卷[M].北京:化学工业出版社,2006.
[2]张一宾.芳酰胺类杀菌剂的沿变——从萎锈灵、灭锈胺、氟酰胺到吡噻菌胺、啶酰菌胺[J].世界农药,2007,29(1):1-7.
[3]杨吉春,张金波,柴宝山,等.酰胺类杀菌剂新品种开发进展[J].农药,2008,47(1):6-9.
[4]Gisi U,Waldner M,Kraus N,et al.Inheritance of resistance to carboxylic acid amide (CAA)fungicides in Plasmopara viticol[J].Plant Pathology,2007,56(2):199-208.
[5]任叶果,罗斐贤,黄明智,等.N-(3,5-二取代基-2-氧-2,3-二氢苯并[d]嗯唑-6-基)苯甲酰胺类化合物的合成及杀菌活性[J].精细化工中间体,2008,38(5):15-18.
[6]Lakner Frederick J,Parker Matthew A,Rogovoy Boris,et al.Synthesis of novel Trisubstituted Imidazolines[J].Synthesis,2009,(12):1987-1990.
[7]Shyamaprosad Goswami,Avijit Kumar Adak,Reshmi Muk herjee,et al.A convenient palladium catalyzed synthesis of symmetric biaryls,biheterocycles and biaryl chiral diamides[J].Tetrahedron,2009,61(17):4289-4295.

