我国O型Mya-98口蹄疫病毒流行情况与毒株分析
何继军,杨亚民,马维民,尚佑军,吕 律,郑海学,靳 野,郭建宏,刘在新,刘湘涛
(中国农业科学院兰州兽医研究所 家畜疫病病原生物学国家重点实验室国家口蹄疫参考实验室,甘肃 兰州 730046)
口蹄疫(Foot and Mouth Disease,FMD)是由口蹄疫病毒(Foot and Mouth Disease Virus,FMDV)引起偶蹄动物急性、热性、高度接触传染性的传染病,以其发病急、传播迅速、发病率高、宿主谱系广、危害大而倍受世界各国重视,国际动物卫生组织(Off i ce International des Epizooties,OIE)将其列为法定报告动物疫病。FMDV属小RNA病毒科(Picornaviridae)口蹄疫病毒属(Aphthovirus),有 O、A、C、Asia1和 SAT1、SAT2、SAT3等7个血清型[1]。血清型间无交叉免疫现象,即使在同一血清型内不同病毒的抗原性也有变化[2-3],这为口蹄疫的防制带来一系列复杂的问题。OIE/FAO世界口蹄疫参考实验室(OIE/FAO World Reference Laboratory for Foot and Mouth Disease,WRLFMD)对全球口蹄疫分子流行病学研究,将O型口蹄疫病毒株分为不同的拓扑型,即中国古典型(CATHAY)、中东-南亚型(Middle East-South Asia,ME-SA)、 东南亚型(South-East Asia,SEA)、印度尼西亚型(Indonesia,ISA)、东非型(East Africa,EA)、西非型(West Africa,WA)、 欧洲-南美型(Europe-South America,EURO-SA)[4-5]。根据国口蹄疫参考实验室流行病学研究资料,我国目前主要流行东南亚 型(SEA)、 中东-南亚型(ME-SA)等2个拓扑型毒株。尤其以SEA拓扑型下Mya-98毒株引起的疫情最为严重。
2010年年初,广东省广州市白云区一猪场发生由Mya-98毒株引起的口蹄疫疫情,随之扑杀了大量的染疫动物和同群畜,经济损失巨大,我国及时向OIE报告了该起疫情。随后,我国大面积暴发由该毒株引起的疫情,发病动物有猪、牛、羊等,疫情形势十分严峻。与此同时,日本、韩国、朝鲜、蒙古、俄罗斯和中国香港、台湾等国家和地区也报告发生由该毒株引起的疫情[6-9]。在此背景下,本研究系统地搜集和整理了我国2010年至2013年年底O型Mya-98毒株,明确了Mya-98毒株在我国的分布与流行情况,同时与世界口蹄疫参考实验室(WRL)、GeneBank等序列数据一起分析了我国Mya-98毒株与周边国家毒株的遗传关系,查明了我国Mya-98毒株的来源和主要易感动物,为今后针对性地防控该毒株提供了科学依据。
1 材料与方法
1.1 材料
1.1.1 病料和毒株
采集或收集自我国2010年至2013年口蹄疫疑似病料共25份,来源于广东省、甘肃省、山西省、江西省、贵州省、宁夏自治区、新疆自治区、西藏自治区、青海省、湖北省、辽宁省、江苏省和四川省等13个省市区。病料通过接种敏感细胞或乳鼠传代分离病毒。病毒培养物均由国家口蹄疫参考实验保存。病料清单详见表1,来源地域分布参见图1。

表1 2010—2013年我国O型Mya-98毒株信息
1.1.2 口蹄疫抗原定型ELISA试剂盒
A、O、Asia1型口蹄疫抗原定型ELISA试剂盒由中国农业科学院兰州兽医研究所提供。
1.1.3 工具酶及试剂盒
总RNA提取试剂盒RNeasy mini Spin-Columns Kit购自德国QIAGEN公司;DNA胶纯化回收试剂盒、DNA Marker、One step RT-PCR kit等购自Takara公司。
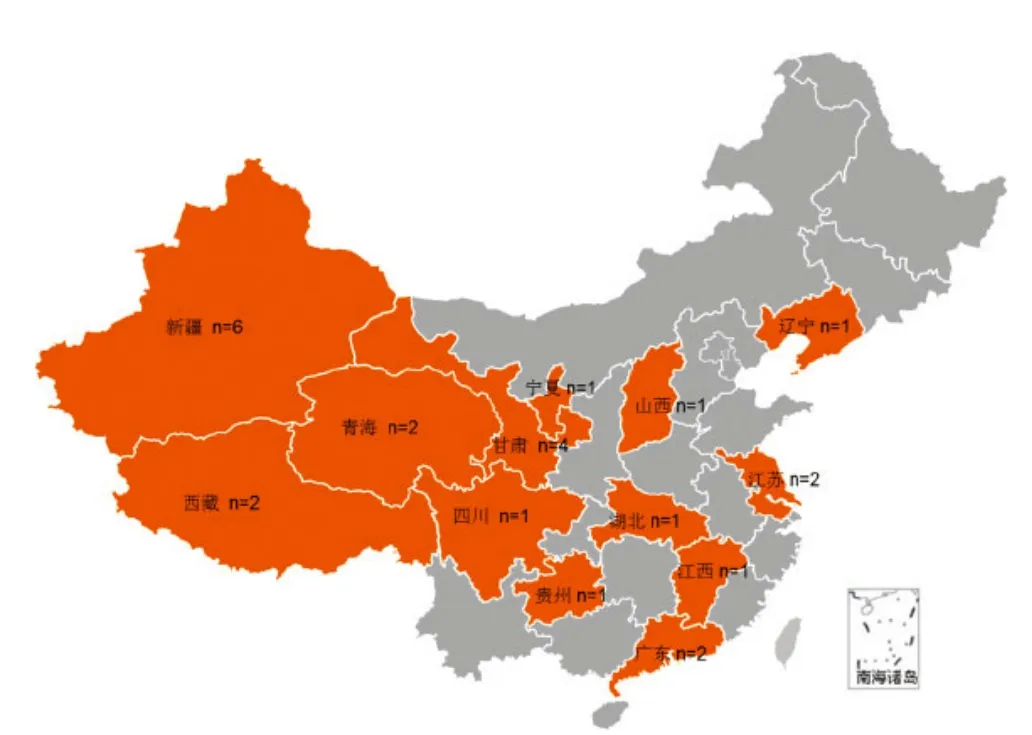
图1 我国2010-2013年Mya-98毒株分布及区域流行图示
1.1.4 标准参考毒株序列
本研究所用中国国内参考毒株序列由国家口蹄疫参考实验室(CNFMDRL)提供,中国香港、中国台湾及世界其它国家毒株序列来自Genbank或CNFMDRL。参考毒株来源背景见表2。
表2 口蹄疫O型病毒株参考毒株

O-LAO-7-2003 老挝 2003EU667448 O-HLJOC12-03 中国 2003DQ119643 O-MOG-2004 蒙古 2004 JQ070324 O-TAI-8-2004 泰国 2004 HQ116233 O-TAI-10-2005 泰国 2005HQ116239 O-TAI-8-2005 泰国 2005 HQ116237 O-VIT-4-2005 越南 2005 HQ116278 O-MYA-2-2006 缅甸 2006HQ116225 O-MYA-1-2006 缅甸 2006JQ070316 O-LAO-4-2007 老挝 2007HQ116178 O-TAI-14-2007 泰国 2007HQ116249 O-TAI-2-2008 泰国 2008 HQ116250 O-MYA-6-2009 缅甸 2009HQ116229 O-TAI-22-2009 泰国 2009HQ116269 O-KOR-1-2010 朝鲜 2010HM143846 O-RUS-Jul-2010 俄罗斯 2010 JQ070329 O-SKR-4-2010 韩国 2010JQ070320 O-SKR-5-2010 韩国 2010JQ070321 O-SKR-12-2010 韩国 2010KC438373 O-MYA-3-2010 缅甸 2010JQ070319 O-JPN-1-2010 日本 2010 KF112885 O-HKN-7-2010 香港 2010JQ070303 O-VITYenBai-06-B 越南 2006 CNFMDRL O-VITHaiphong-06-S 越南 2006 CNFMDRL O-VITLangSon-06-Buff l o 越南 2006 CNFMDRL O-VN-YB08-2010 越南 2010 HQ260718 O-VN-YB09-2010 越南 2010 HQ260719 O-VN-YB10-2010 越南 2010 HQ260720 O-DY-CHA-2010 中国 2010 HQ652078 O-NC-CHA-2010 中国 2010 HQ652080 O-MY-CHA-2010 中国 2010 HQ652079 O-TZ-CHA-2010 中国 2010 HQ652081
1.1.5 引物
FMDV VP1基因扩增用引物为1D2和1D5,VP1基因目的片段大小约810bp。引物由宝生物工程(大连)有限公司合成。
1.2 方法
1.2.1 病料处理
将待检病料(水泡皮、水泡液)用pH 7.40.1mol-L 磷酸缓冲液(PB)洗涤2~3次,用灭菌的滤纸吸去水分,加入石英砂及适量青霉素和链霉素充分研磨1:5悬液,置于4℃过夜浸毒,3000 r-m离心10 min,上清即为待检抗原。取上清液进行病毒分离、血清型鉴定和核酸抽提。
1.2.2 病毒的血清型鉴定
用口蹄疫病毒抗原定型ELISA试剂盒对病料或鼠毒进行血清型鉴定。按照试剂盒说明书操作。
1.2.3 口蹄疫病毒VP1基因RT-PCR扩增
1.2.3.1 口蹄疫病毒RNA的提取
将预处理好的病料(或病毒培养物),5000r-min离心2min,取上清液用于病毒RNA的提取。用QIAGEN公司RNA提取试剂盒进行总RNA的提取。
1.2.3.2 VP1基因的RT-PCR扩增
应用一步法RT-PCR方法进行扩增。以50μL反应体系为例,在250μL的PCR薄壁管中,加入10×One Step RNA PCR Buffer 5μL,dNTP(10mM)5μL,MgCl2(25mM) 10μL,RNase 抑 制 剂1μL(40U-μL),反转录酶(AMV) 1μL(5U-μL),RT-PCR聚合酶 1μL(5U-μL),正向引物1D21μL(50 pmol-μL),反向引物1D51μL(50 pmol-μL),RNA模板 25μL。混匀各反应组份,置于热循环仪中,进行PCR扩增。扩增程序为:42℃ 30 min,95℃ 2 min,95℃ 1 min,55℃ 1 min,72℃ 8 min,30 个循环。
1.2.3.3 PCR产物检测
PCR扩增结束后,取5μL产物在1.5% TAE琼脂糖凝胶中电泳,凝胶中含有0.5μL-mL的溴化乙锭,电泳缓冲液为1×TAE,80V~100V,15min~20min后于紫外凝胶成像系统观察结果。
1.2.4 PCR产物的纯化、回收
用宝生物工程(大连)有限公司Agarose Gel DNA Purif i cation Kit回收DNA。操作按照说明书进行。
1.2.5 PCR纯化产物的测序
纯化后的PCR产物直接进行测序。测序引物与扩增引物一致。
1.2.6 序列分析
用DNAstar(v 6.0)软件对序列进行分析与序列比对,应用Treeview(v 1.6.6)进行基因树作图。
2 结果与分析
2.1 病毒分离和血清型鉴定
本研究收集的25份疑似口蹄疫均分离到口蹄疫病毒,用抗原定型ELISA试剂盒鉴定均为口蹄疫病毒O型。
2.2 口蹄疫病毒VP1基因RT-PCR扩增
以特异性引物1D2、1D5进行RT-PCR扩增,获得约810 bp的含有VP1基因全长目的条带。其大小均与预期的结果相符,见图2。
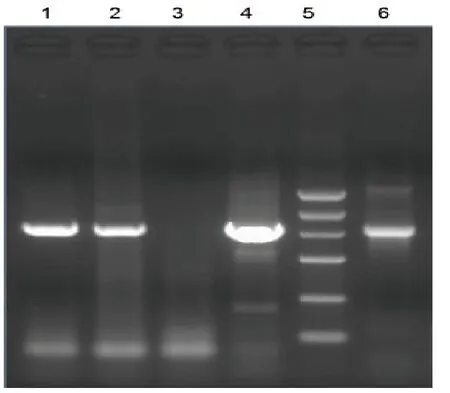
图2 VP1基因RT-PCR产物电泳结果
2.3 VP1基因序列与分析
2.3.1 序列测定与比较
测序结果表明,我国猪口蹄疫O型病毒株的VP1 基因全长均为639bp,编码213个氨基酸,未发现核苷酸的缺失或插入。按WRL建立的分子流行病学分析方法,对25条毒株序列进行基因型分析,结果这些毒株均属于SEA拓扑型(图2)。我国Mya-98流行株VP1基因序列同源性在95%~100%之间。
以我国2010年广东省广州市白云区毒株(O-GDgzh-2010-S-31)为代表,其与中国香港、日本、韩国等(2010年)毒株同源性在99%左右,属高度同源;与越南等东南亚国家(2010年)毒株同源性98.4%以上,而与我国非官方历史Mya-98毒株(O-HLJOC12-03)同源性仅94.1%。
由此可见,我国2010年开始流行的Mya-98毒株,属从东南亚国家传入我国。该结果与WRL分析结果一致。
2.3.2 Mya-98毒株进化分析
结合WRL、国家口蹄疫参考实验室历年Mya-98毒株序列,Mya-98毒可分为3个遗传组别(Group):
组别1(G1),见于越南(1997)、缅甸(1998)、柬埔寨(1998)等国家。发病动物主要为牛。该组别毒株可能为SEA拓扑型毒株的源头,在后来未见相关流行报道。
组别2(G2),包括东南亚国家(如越南、老挝、缅甸、马来西亚等2001~2008年毒株)的毒株。发病动物主要为牛,也可见猪发病,如越南毒株(O-VITHaiphong-06-S)。从WRL分子流行病学报告中发现,该组毒株在俄罗斯、蒙古等2010年也见有引起疫情的报道。疑惑的是,我国大陆未见由该组毒株引发的疫情报告。东南亚特有的毒株如何跨越我国大陆,在蒙古和俄罗斯等国家流行,也是备受关注的话题之一。
组别3(G3),包括我国、东南亚国家及我国周边日本、韩国、俄罗斯、蒙古等Mya-98毒株。根据流行年代不同,又可以分为两个不同的进化分支(G3A和G3B)。G3A主要是2003~2005年流行毒株,如中国O-HLJOC12-03毒株,蒙古O-MOG-2004、越南O-VIT-4-2005等毒株。G3B包括我国2010年以后流行的全部毒株。G3组内毒株同源性94%左右,分支内毒株同源性98%以上。参见图3。该组毒株可引起猪、牛、羊等家畜发病,宿主范围极其广泛。
G1与G2毒株同源性84%左右,G1与G3毒株同源性84%左右,G2与G3毒株同源性89%左右,其间最大可达到15%以上的差异,表明该毒株变异速度之快。这点或许是Mya-98毒株在东南亚长期流行,难以控制的原因之一。
另外,比较不同组别的Mya-98毒株发现,Mya-98(G3B)在VP1基因上,第47位氨基酸P-Q→S,58位S-A→P,138位E→G和198位E→A的替换,142位L→P的零星变异等等,体现了其共同变异特征或趋势。虽然,关乎抗原位点的关键氨基酸并没有改变,但其变异位置已经触及关键位点或区域,或可代表了该毒株进化的方向。
3 讨论
口蹄疫Mya-98毒株在遗传关系上分属于O型SEA拓扑型,因在1998年前后主要在缅甸等东南亚国家流行,因此命名为Mya-98毒株。与之同属一个拓扑型的还有Cam-94毒株(柬埔寨94)。Cam-94毒株主要限制在东南亚国家如柬埔寨(1994,1998)、老挝(1998)、越南(1997,1999)、马来西亚(2001-2003)等国家流行[10-12],近来未见由该毒株引起的疫情,我国历史上也从未监测到Cam-94毒株。
通过本研究表明,Mya-98毒株在东南亚等国家长期流行,于2010年前后传入我国。但遗憾的是,由于缺少详细的流行病学背景资料,该毒株以何路径、以何种方式传入我国不得而知。本文仅根据VP1基因序列分析和比较[4,13-15],推测了我国Mya-98毒株的来源。东南亚越南、老挝、缅甸与我国接壤,边境地区移动、动物及产品贸易频繁,这些国家口蹄疫疫情传入我国的风险极高。而且,在东南亚国家常见由于动物移动或贸易引发的疫情[16],这种跨区域的流行和传播,也催生了东南亚-中国口蹄疫控制行动计划(SEACFMD)的出台。近年来,在全球范围内也常见毒株跨区域传播流行的例子,如2011年中东地区O型PanAsia-2毒株在欧洲国家保加利亚引发疫情[17];2012年SAT2型在北非埃及、利比亚等国家强势流行[18],甚至在亚洲如巴勒斯坦等也监测到SAT2型毒株;2013年9月南亚Ind-2001毒株在北非利比亚等国家引发疫情。因此,如何防堵境外毒株的传入,是我国口蹄疫防控工作面临的一个新课题,或者说如何控制流行毒株的跨区域传播,是今后口蹄疫防控面临的共同难题。在我国,与之相似的情况还有2009年A型Sea-97毒株、2011年新泛亚毒株和2013年A型Sea-97 G2毒株。回顾我国近来的口蹄疫流行历史,几乎造成大流行的毒株均来自于境外,我国防堵境外口蹄疫流行毒株的任务越来越重要。
另外,Mya-98毒株宿主适应和转向值得关注。2010年,我国Mya-98毒株在猪、牛、羊等均可引起发病。之后,我国再未见由该毒株引起牛发病的报道,宿主范围表面上在缩小,但实则引发了更为严重的后续效应,即猪Mya-98疫情的持续和该毒株将来在猪群中的维持和常态化。分析我国口蹄疫流行毒株与易感动物的关系可以看出,某一个毒株如果对牛易感,对猪较为钝感,则易于控制,如2005~2009年Asia1型江苏毒株、2009—2010年A型武汉毒株等。相反,某一个毒株如果对猪易感,则难于在短期内控制,如CATHAY拓扑型毒株和Mya-98毒株。因此,从Mya-98毒株目前流行潜力和对猪的易感性、致病力等方面综合分析,该毒株在我国还将持续流行一段时期。国家口蹄疫参考实验室开展的全国重点省份猪屠宰场口蹄疫监测结果也表明,我国猪群中Mya-98毒株较为常见,如2010年全国19省口蹄疫监测中,在4个省市自治区屠宰场监测到阳性带毒;2012年全国10省猪屠宰场监测中,在3个省监测到猪带毒阳性。
2010年以来,新一轮Mya-98毒株传入我国以来,引起了严重的疫情流行,给我国的养殖业严重的打击,造成了巨大的经济损失。自新毒株确诊以来,国家口蹄疫参考实验室积极地投入对该毒株的研究和疫苗研发工作,并取得突破性进展。针对该毒株的疫苗已经投放市场,并取得了有效控制。2011年,我国发生2起Mya-98疫情,2012年发生3起,2013年仅发生2起,疫情次数(表1)和流行范围(图1)进一步降低或减小。可以肯定,只要扎实做好免疫预防、流调监测和流通环节监管工作,一定可以有效控制该毒株的流行。
[1]Grubman MJ,Baxt B.Foot-and-mouth disease[J].Clinical microbiology reviews,2004,17(2):465-493.
[2]谢庆阁.口蹄疫[M].北京:中国农业出版社,2004:25-27.
[3]谢庆阁,翟中和.畜禽重大疫病免疫防制研究进展[C].北京:中国农业科技出版社,1996:1-31.
[4]Knowles NJ,Samuel AR.Molecular epidemiology of footand-mouth disease virus[J].Virus research,2003,91(1):65-80.
[5]Rweyemamu M,Roeder P,Mackay D,et al.Epidemiological pattern of foot-and-mouth disease Worldwide[J].Transbound Emergence Disease,2008(55):57–72.
[6]Knowles NJ,He J,Shang Y,et al.Southeast Asian foot-andmouth disease viruses in Eastern Asia[J].Emerging infectious diseases,2012,18(3):499-501.
[7]Akashi H.Current situation and future preventive measures of foot-and-mouth disease in Japan[J].Uirusu,2010,60(2):249-255.
[8]Muroga N,Hayama Y,Yamamoto T,et al.The 2010 foot-and-mouth disease epidemic in Japan[J].The Journal of veterinary medical science - the Japanese Society of Veterinary Science, 2012,74(4):399-404.
[9]Park JH,Lee KN,Ko YJ,et al.Control of foot-and-mouth disease during 2010-2011 epidemic, South Korea[J].Emerging infectious diseases, 2013,19(4):655-659.
[10]Abdul-Hamid NF,Firat-Sarac M,Radford AD,et al.Comparative sequence analysis of representative foot-andmouth disease virus genomes from Southeast Asia[J].Virus genes,2011,43(1):41-45.
[11]Madin B.An evaluation of Foot-and-Mouth Disease outbreak reporting in mainland South-East Asia from 2000 to 2010[J].Preventive veterinary medicine,2011,102(3):230-241.
[12]Abdul-Hamid NF,Hussein NM,Wadsworth J,et al.Phylogeography of foot-and-mouth disease virus types O and A in Malaysia and surrounding countries[J].Infection,genetics and evolution:journal of molecular epidemiology and evolutionary genetics in infectious diseases,2011,11(2):320-328.
[13]Stram Y,Molad T,Chai D,et al.Detection and subtyping of foot-and-mouth disease virus in infected cattle by polymerase chain reaction and amplified VP1 sequencing[J].Journal of veterinary diagnostic investigation:official publication of the American Association of Veterinary Laboratory Diagnosticians,Inc,1995,7(1):52-55.
[14]Tsai CP,Pan CH,Liu MY,et al.Molecular epidemiological studies on foot-and-mouth disease type O Taiwan viruses from the 1997 epidemic[J].Veterinary microbiology,2000,74(3):207-216.
[15]Mason PW,Grubman MJ,Baxt B.Molecular basis of pathogenesis of FMDV[J].Virus research,2003,91(1):9-32.[16]Klein J.Understanding the molecular epidemiology of foot-and-mouth-disease virus[J].Infection,Genetics and Evolution,2009,9(2):153-161.
[17]Valdazo-Gonzalez B,Polihronova L,Alexandrov T,et al.Reconstruction of the transmission history of RNA virus outbreaks using full genome sequences:foot-and-mouth disease virus in Bulgaria in 2011[J].PloS one,2012,7(11):e49650.
[18]Ahmed HA,Salem SA,Habashi AR,et al.Emergence of foot-and-mouth disease virus SAT2 in Egypt during 2012 [J].Transboundary and emerging diseases,2012,59(6):476-481.

