化学还原法制备微纳米银粉
鲁志强,甘卫平,黎应芬,周 健,杨 超,戈田田
化学还原法制备微纳米银粉
鲁志强,甘卫平,黎应芬,周 健,杨 超,戈田田
(中南大学材料科学与工程学院,长沙 410083)
采用液相化学还原法,以PVA(聚乙烯醇)作分散剂,硼氢化钠作还原剂,硝酸银为前驱体,制备分散性相对较好的微纳米级银粉。探究银离子浓度、还原剂浓度、分散剂用量和反应温度等因素对银粉品质的影响规律,通过调节上述因素对银粉粒径和分散性进行调控。并运用XRD(X射线衍射仪)、SEM(扫描电子显微镜)和UV-Vis(紫外可见分光广度计)对银颗粒的晶体物相结构、表面形貌和光学特性进行表征。结果表明,当反应温度为40 ℃、银离子浓度为0.2 mol/L、硼氢化钠浓度为0.2 mol/L、硝酸银与PVA质量比为0.6时,可以制备出分散性良好、纯度较高的银粉,银粒子平均粒径在120 nm左右。
硼氢化钠;硝酸银;微纳米银粉;化学还原
银是导电性最高的金属,其化学性质稳定,有优良的导热导电性和加工性能,因此银粉是导电浆料、导电胶、电阻网络、催化和抗菌材料的基本功能材 料[1−2]。银粉在颗粒尺寸低于0.5 μm时按大小可分为微米级超细银粉和纳米银粉(低于0.1 μm)[3]。相对于微米银粉,纳米银粉有很多优势,如在电子浆料中使用纳米银粉代替超细银粉可以在丝网印刷时获得致密度更高的涂层;纳米银粉的熔点低于超细银粉,故其烧结温度低于普通浆料,可降低能耗;制备导电胶时可以减少银用量,降低生产成本[4]。但限于目前的生产工艺条件,工业上电子浆料等领域还是以超细银粉 为主。
如何制备出球形度好、表面光洁、粒度分布窄且分散性好的超细银粉和纳米银粉一直是众多科研工作者研究的课题。就目前而言,制备微纳米级银粉的方法很多,有高能球磨法[5]、等离子体蒸发冷凝法[6]、喷雾热分解法[7]、光诱导法[8]、液相还原法[9]等。其中液相化学还原法因其制备工艺简单、操作方便、粉末粒径大小易控等优点在工业生产中得到广泛应用。液相还原法制备银粉是在分散剂的保护下,用还原剂(如常用的水合肼[10]、葡萄糖[11]、抗坏血酸[12]等)将银粒子还原成单质银颗粒,然后沉淀、过滤、洗涤、干燥,最后得到银粉。用水合肼作还原剂时虽然能制备出纳米银,但由于反应剧烈银粉团聚严重;用葡萄糖和抗坏血酸制备的银粉虽然分散性好,但银粉颗粒大都在微米级。在国内,用硼氢化钠作还原剂,PVP作分散剂,樊新[13]等人制备出不同粒度、分散性较好的纳米球形银粒子。魏春萍[14]用PVP作分散剂,探讨了硼氢化钠还原硝酸银在不同分散介质下的纳米银稳定性问题。但用PVA作分散剂,硼氢化钠作还原剂制备微纳米级银粉的课题还鲜有人研究。
本文作者以PVA作分散剂,硼氢化钠作还原剂,硝酸银作银源,制备平均粒径在60~250 nm的不同粒度的银粒子。通过XRD、SEM和UV-Vis等对制备的银粉进行表征,讨论银离子浓度、还原剂浓度、分散剂用量、反应温度等因素对银粒子粒径、形貌和分散性的影响,并探究出该实验体系下的最优反应条件。
1 实验
1.1 试剂与仪器
所用试剂为:AgNO3(分析纯,99.8%,株冶集团贵金属部),硼氢化钠(分析纯,天津市福晨化学试剂厂),氢氧化钠(分析纯,天津市大茂化学试剂厂),PVA(分析纯,成都金山化学试剂有限公司),无水乙醇(分析纯,99%,天津市富宇精细化工有限公司),去离子水。
采用D-MAX2500型X射线衍射仪对银粉进行物相分析,MIRA 3 LMH/LMU型扫描电镜观察银粉表面形貌,Mastersize2000型激光粒度分析仪测量银粉平均粒径,UV-1801型紫外可见分光光度计表征纳米银溶胶光学特性。
1.2 实验过程
按比例称取一定量的硝酸银、PVA、氢氧化钠、硼氢化钠。将硝酸银和PVA分别溶于去离子水,配制成一定浓度的硝酸银溶液和PVA溶液。然后将PVA溶液加入到硝酸银溶液中混合,搅拌均匀,记为A液。将氢氧化钠溶于去离子水,配制成氢氧化钠溶液,加入称量好的硼氢化钠,搅拌溶解,制成B液。
将A液和B液在水浴锅中一定温度下保温,待温度恒定后,将B液用滴管缓慢滴加到A液中,同时用搅拌器搅拌混合液使溶液混合均匀,可发现溶液先呈棕黄色然后慢慢变黑,待滴加完毕,保温搅拌大约半小时后反应完全,得到黑色的悬浊液。静置一段时间后,进行3 600 r/min离心分离30 min,去掉上层液体,得到黑色的固体粉末颗粒。然后将其用去离子水洗3次、醇洗3次后,在真空干燥箱中60 ℃干燥后得到微纳米级银粉。
2 结果与讨论
硼氢化钠是一种中等强度的还原剂,性能稳定,可以利用其还原性还原金属离子。硼氢化钠还原硝酸银的反应方程式为:
NaBH4+4AgNO3+4NaOH=4Ag↓+NaB(OH)4+
2H2↑+4NaNO3(1)
由方程式(1)可以看出参加反应的摩尔比NaBH4: AgNO3:NaOH=1:4:4。为了确保硝酸银反应完全,设置硼氢化钠和氢氧化钠过量,实际摩尔比为1:2:4。
2.1 PVA用量对银粉品质的影响
当初始反应的硼氢化钠浓度为0.2 mol/L、溶液温度为40 ℃时,不同的分散剂用量下得到银粒子平均粒径如图1所示。
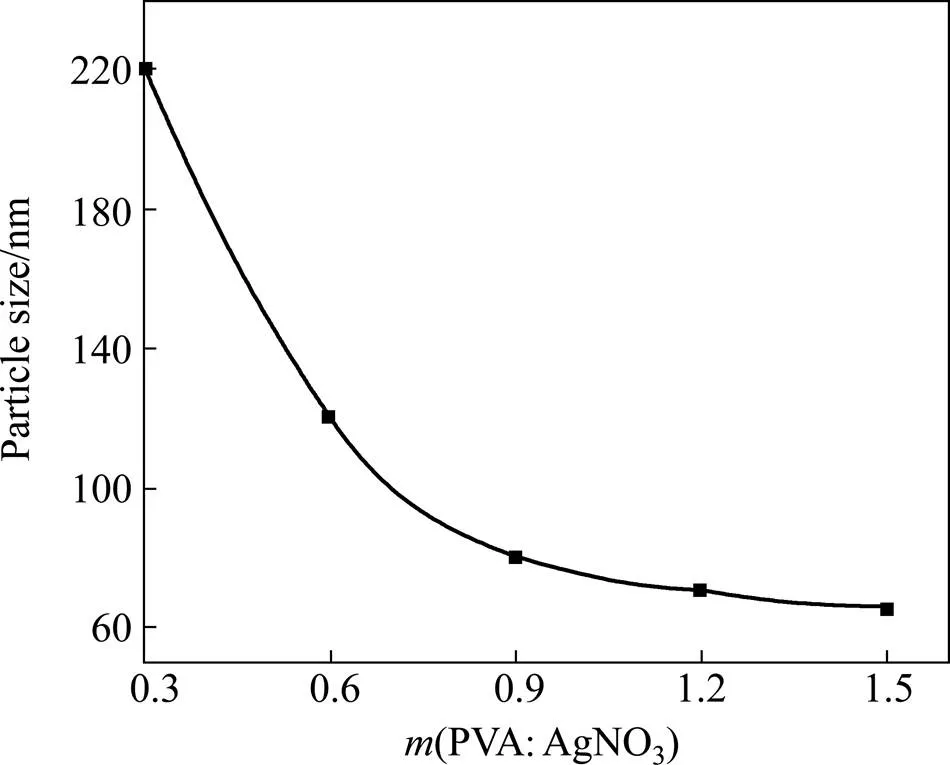
图1 PVA用量对银粒子平均粒径影响
由图1可以看出,随PVA与AgNO3的质量比由0.3增加到1.5时,银粒子平均粒径总体呈减小趋势。当质量比达到0.9时,银粒子粒径达到80 nm左右。此后再增加PVA用量,银粒子粒径减小趋势变缓。图2所示为不同分散剂比例下银粉的SEM照片。
由图2可以看出当分散剂质量比为0.3时分散效果并不理想,银粉颗粒聚集在一起;随着用量增加至0.6时,颗粒粒径减小至120 nm左右且分散效果良好,没有严重团聚的现象。随分散剂用量增加,银粉颗粒虽然进一步减小,只有几十纳米,但团聚非常严重。

图2 不同PVA用量下银粒子电镜照片
PVA分子是含有极性羟基的聚乙烯基骨架。其分散机理如图3所示,利用PVA中O原子的孤对电子与银颗粒表面原子进行配位,形成配位键吸附在银颗粒表面,留下PVA的C—H长链伸向四周在介质中充当位阻部分,使得银颗粒的扩散距离增加,同时减小银颗粒相遇几率(即空间位阻效应),阻止银颗粒的进一步团聚长大[15]。

图3 PVA的空间位阻效应
当分散剂用量较少时,分散剂不能很好地包裹和分隔刚生成的银颗粒,使得银颗粒进一步团聚长大。当分散剂用量增加时,其对银粉包裹程度趋于完全,分散效果变好,颗粒粒径减小。但是当银粉颗粒减小到几十纳米时,由于银纳米颗粒强大的表面张力[16]使得银粉聚集在一起,其聚集趋势远大于分散剂的分散趋势,即使再增加分散剂的用量也体现不出其分散效果,所以出现纳米银粉团聚严重的现象。且当分散剂用量过多时,会给后期洗涤提纯过程带来困难。所以从节省原材料的角度和实际分散效果等方面综合考虑,(PVA:AgNO3)=0.6是最优选择。
2.2 还原剂浓度对银粉品质的影响
保持(PVA:AgNO3)=0.6不变,当(Ag+)=0.2 mol/ L, 反应温度为40 ℃时,调节NaBH4的浓度为0.1、0.2、0.3、0.4和0.5 mol/L,考查还原剂溶液浓度对银粉品质的影响。得到银粒子粒径如图4所示。
由图4可以看出随还原剂浓度增加,银粒子尺寸呈先减小后增加的趋势。在(NaBH4)=0.3 mol/L时达到最小尺寸70 nm左右。出现这种现象的可能原因是,在还原剂浓度较小时,随其浓度增加,反应速度加快,但新生成的晶粒会被分散剂包裹住,阻止晶粒进一步长大,使得形核速率大于银粒子的长大速率,从而使银粒子的粒径不断减小。当还原剂浓度增加到一定程度时,由于反应速度太快,新生成的银晶粒来不及被分散剂完全包裹住,导致银粒子之间不可避免地发生吸附团聚,从而使粒子尺寸变大。图5所示为不同还原剂浓度下银粒子的SEM照片。
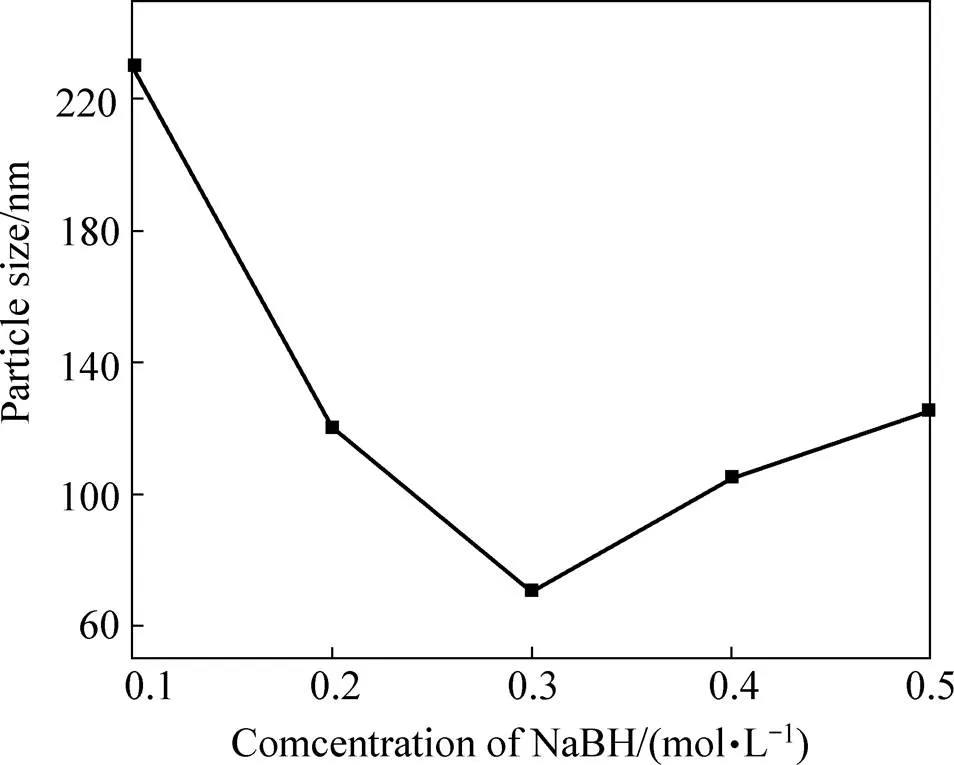
图4 还原剂浓度对银粒子平均粒径的影响
由图5可以看出在(NaBH4)=0.3 mol/L,虽然粒子尺寸最小达到几十纳米,但由于纳米粒子表面效应使得银粒子之间团聚严重,分散性不好。NaBH4浓度为0.2 mol/L和0.4 mol/L时,粒子尺寸相近,100~ 120 nm范围内,由图5(a)和图5(c)可以看出,在NaBH4浓度为0.2 mol/L时粒子之间分散性明显比0.4 mol/L好。所以综合考虑实际粒子分散效果和节省原料两方面,还原剂浓度最佳选择为0.2 mol/L。
2.3 银离子浓度对银粉品质的影响
保持(PVA:AgNO3)=0.6不变,(NaBH4)=0.2 mol/ L、温度为40 ℃时,调节银离子浓度为0.1、0.2、0.3和0.4 mol/L。对应粒径大小如表1所列。
从表1可以看出,随银离子浓度增加,银粒子尺寸增大。这可以从形核动力学角度得到解释。当银离子浓度较低时,银离子在溶液中的分散程度较高,被还原出的银原子扩散到附近晶核所需迁移的距离较大,晶核的长大受到抑制,此时形核速率大于长大速率,所以银粒子尺寸较小。随银离子浓度增加,银晶核分布密度增大,扩散所需迁移距离变小,晶核长大速率增加,宏观上表现为银粒子尺寸增大。

图5 不同还原剂浓度下银粒子电镜照片
2.4 反应温度对银粉品质的影响
保持(PVA:AgNO3)=0.6不变,(NaBH4)=0.2 mol/ L,(AgNO3)=0.2 mol/L时,设置反应水浴温度为30、40、50和60 ℃,在不同温度下分别反应30 min后制备的纳米银溶胶进行UV-Vis分析,得到紫外可见光谱如图6所示。
从图6可以看出,随反应温度升高,纳米银吸收峰位置总体向长波方向移动(红移),说明纳米银的粒径随温度升高而增大。吸收峰强度在30 ℃时最低,可见低温并不利于纳米银粒子获得。当温度升高到 40 ℃,吸收峰强度明显增加,说明生成的纳米银粒子浓度增加显著,此后进一步升高温度,峰强先稍有增加后减小。但当温度超过40 ℃时,吸收峰的半高宽明显宽化,此时纳米银粒子粒度分布变广,不利于获得尺寸均一、粒度分布窄的银粒子。出现这种现象可能是因为随温度升高,反应速率增加,短时间生成的大量银晶核来不及被分散剂完全包裹,导致银粒子之间不断团聚长大,同时也会使银粒子尺寸大小不均、粒度分布广泛[17]。图7所示为反应温度在40 ℃和60 ℃下银粒子的SEM照片。

表1 银离子浓度对银粒子平均粒径的影响
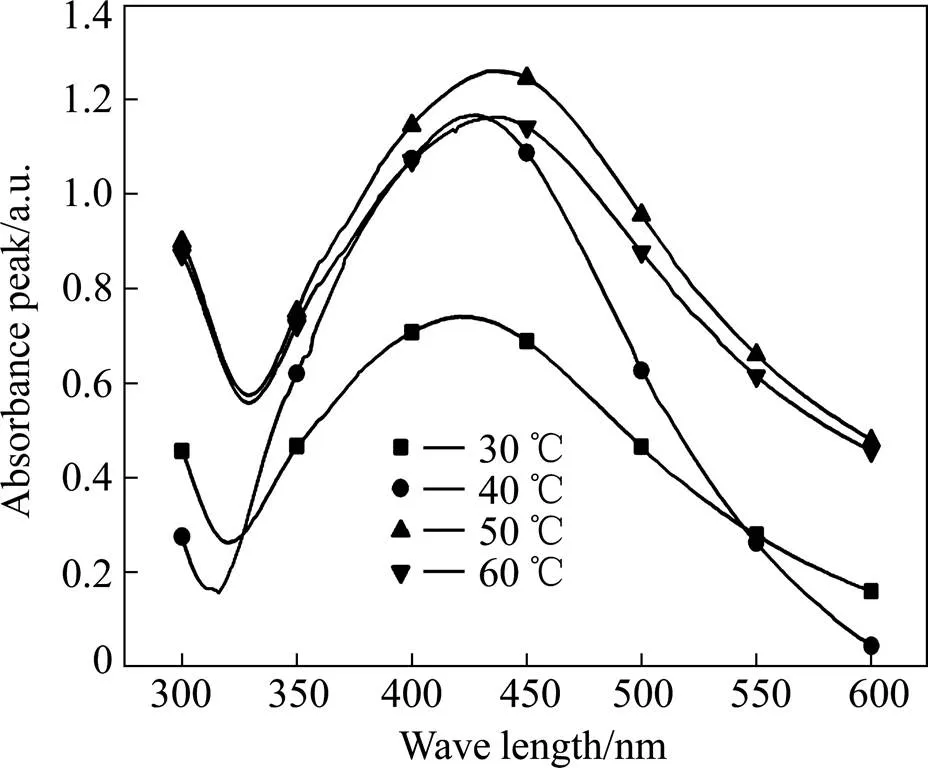
图6 不同反应温度下纳米银溶胶紫外可见光谱
由图7(a)可以看出40 ℃下银粒子分散性良好,粒径大小均匀,在120 nm左右,当温度升高至60 ℃时,从电镜照片图7(b)中可以看出粒子球形度虽然变好,但是银粒子粒径大小不均匀,且分布范围广,这与紫外可见光谱分析一致。综上所述,40 ℃是本实验体系反应温度的最佳选择。
2.5 银粉的分析
由上述分析可知,本实验体系的最佳反应条件为温度40 ℃,(PVA:AgNO3)=0.6,(NaBH4)=0.2 mol/ L,(AgNO3)= 0.2 mol/L。图8为该反应条件下获得的银粒子的SEM照片,可以看出银粒子分散性良好,尺寸均匀在120 nm左右。
将最佳反应条件下制备的银粉进行XRD物相分析,得到XRD图谱,如图9所示。可以看出图中4个衍射峰位置与标准JCPDS卡片上银衍射峰(2为38.096°,44.057°,64.406°和77.452°)吻合。并且图谱中各峰都很尖锐,没有多余杂峰出现,说明制备的银粉纯度很高,结晶度良好。

图7 不同反应温度下银粒子电镜照片

图8 最佳反应条件下银粒子电镜照片

图9 最佳反应条件下制备的银粉XRD谱
3 结论
1) 采用PVA作分散剂,硼氢化钠作还原剂,硝酸银作前驱体,通过液相化学还原法可以制备出平均粒径在60~250 nm的微纳米级银粉。
2) 随分散剂用量增加,银粒子粒径呈减小趋势,当粒径减小到几十纳米时,会出现团聚严重现象;随还原剂浓度增加,银粒子粒径成先减小后增加趋势,在浓度为0.2 mol/L时分散性最好;随银离子浓度增加和反应温度升高,银粒子粒径呈不断增加趋势,当温度超过40 ℃时会出现粒径尺寸不均、粒度分布广的现象。通过调节这些因素可以实现对银粉的粒径、形貌、分散性进行控制。
3) 实验最佳反应条件为反应温度40 ℃,(PVA: AgNO3)=0.6,(NaBH4)=0.2 mol/L,(AgNO3)=0.2 mol/ L。在此反应条件下可制备出分散性良好的平均粒径为120 nm左右的银粉。
REFERENCES
[1] ZHANG Zong-tao, ZHAO Bin, HU Li-ming. PVP protective mechanism of ultrafine silver powder synthesized by chemical reduction processes [J]. Journal of Solid State Chemistry, 1996, 121: 105−110.
[2] NERSISYAN H H, LEE J H, SON H T, et al. A new and effective chemical reduction method for preparation of nanonsized silver powder and colloid dispersion [J]. Materials Research Bulletin, 2003, 38: 949−956.
[3] 宋永辉, 梁工英, 兰新哲. 化学法制备超细银粉的研究进展[J]. 贵金属, 2006, 27(4): 66−71. SONG Yong-hui, LIANG Gong-ying, LAN Xin-zhe. Research and development in preparation of superfine silver powder by chemical methods [J]. Precious Metals, 2006, 27(4): 66−71.
[4] 楚 广, 杨天足, 刘伟峰, 等. 纳米银粉的制备及其应用研究进展[J]. 贵金属, 2006, 27(1): 57−62. CHU Guang, YANG Tian-zu, LIU Wei-feng, et al. Developments on preparation and application of nanometer silver powders [J]. Precious Metals, 2006, 27(1): 57−62.
[5] COSTA F A da, SILVA A G P da, FILHO F A, et al. Synthesis of a nanocrystalline composite W-25wt% Ag powder by high energy milling [J]. Powder Technology, 2008, 188(1): 30−33.
[6] SANG H L, SEUNG M O, DONG W P. Preparation of silver nanopowder by thermalplasma [J]. Materials Science and Engineering, 2007, 27: 1286−1290.
[7] 刘志宏, 刘智勇, 李启厚, 等. 喷雾热分解法制备超细银粉及其形貌控制[J]. 中国有色金属学报, 2007, 17(1): 149−155. LIU Zhi-hong, LIU Zhi-yong, LI Qi-hou, et al. Morphology control of micro-sized spherical silver powder prepared by spray pyrolysis [J]. The Chinese Journal of Nonferrous Metals, 2007, 17(1): 149−155.
[8] 刘亚建, 谭媛媛, 章月红, 等. 辐照法制备纳米银粉的探究[J]. 辐射研究与辐射工艺学报, 2010, 28(1): 24−28. LIU Ya-jian, TAN Yuan-yuan, ZHANG Yue-hong, et al. Study on preparing silver nano-particles with irradiation technique [J]. J Radiat Res Radiat Process, 2010, 28(1): 24−28.
[9] 袁林生, 沈晓东, 崔 升, 等. 液相还原法制备纳米银粉的研究[J]. 电子元件与材料, 2006, 25(6): 40−42. YUAN Lin-sheng, SHEN Xiao-dong, CUI Sheng, et al. Study on nano-silver prepared by method of liquid reduction [J]. Electronic Components and Materials, 2006, 25(6): 40−42.
[10] 宋永辉, 兰新哲, 张秋利. 超声波强化制备超细银粉[J]. 稀有金属, 2005, 29(4): 502−504. SONG Yong-hui, LAN Xin-zhe, ZHANG Qiu-li. Preparation of superfine silver powder by ultrasonic wave intensification [J]. Chinese Journal of Rare Metals, 2005, 29(4): 502−504.
[11] 江建军, 谈定生, 刘久苗, 等. 葡萄糖还原制取超细银粉[J]. 上海有色金属, 2004, 25(1): 5−8. JIANG Jian-jun, TAN Ding-sheng, LIU Jiu-miao, et al. Preparation of ultrafine silver powder by reduction of glucose [J]. Shanghai Nonferrous Metals, 2004, 25(1): 5−8.
[12] WU S P, MENG S Y. Preparation of ultrafine silver powder using ascorbic acid as reducing agent and its application in MLCI [J]. Materials Chemistry and Physics, 2005, 89(2/3): 423−427.
[13] 樊 新, 黄可龙, 刘素琴. 液相还原法制备不同粒度分布的规则球形纳米银粉研究[J]. 纳米科技, 2007, 4(1): 31−33.FAN Xin, HUANG Ke-long, LIU Su-qin.Study of regular spherical nanometer silver powder with different granularity distributions prepared by chemical reduction in the liquid phase [J].Nanoscience & Nanotechnology, 2007, 4(1): 31−33.
[14] 魏春萍. 纳米银粉的制备及表征[J]. 辽宁化工, 2010, 7, 39(7): 697−704. WEI Chun-ping.Preparation and characterization of nano-silver [J].Liaoning Chemical Industry, 2010, 39(7): 697−704.
[15] 李先学, 韩跃新, 印万忠. 纳米银粉制备过程中表面保护剂的作用研究[J]. 矿冶, 2004, 13(3): 51−53. LI Xian-xue, HAN Yue-xin, YIN Wan-zhong. Study on the operation mechanism of surface protecting agent in the preparation of silver nanometric powder [J]. Mining & Metallurgy, 2004, 13(3): 51−53.
[16] 李宇农, 何建军, 龙小兵. 金属纳米粒子研究进展[J]. 稀有金属与硬质合金, 2003, 31(4): 45−47. LI Yu-nong, HE Jian-jun, LONG Xiao-bing. The scientific development of metallic nanometer particles [J]. Rare Metals and Cemented Carbides, 2003, 31(4): 45−47.
[17] 廖 立, 熊 继, 谢克难. 液相还原法制备纳米银粉的研究[J]. 稀有金属材料与工程, 2004, 33(5): 558−560. LIAO Li, XIONG Ji, XIE Ke-nan. Study of preparation of nano-silver powder by reduction process in liquid phase [J]. Rare Metal Materials and Engineering, 2004, 33(5): 558−560.
(编辑 高海燕)
Synthesis of silver powder with micro-nano size by chemical reduction
LU Zhi-qiang, GAN Wei-ping, LI Ying-fen, ZHOU Jian, YANG Chao, GE Tian-tian
(School of Material Science and Engineering, Central South University, Changsha 410083, China)
Micro-nano-size silver powder with good dispersibility was prepared using PVA as dispersing agent, NaBH4as reducing agent and silver nitrate as precursor by liquid phase reducing method. The effects of the concentration of silver ion and reducing agent, the dosage of dispersing agent and the reacting temperature on the quality of silver powder were studied. The size and dispersibility of silver powder can be controlled by changing these factors. X-ray diffraction, SEM and UV-Vis were employed to characterize the crystal structure, surface morphology and optical properties of the silver particles. The results show that, the spherical silver powder with high purity and better dispersibility can be obtained under the condition that the concentration of silver ion is 0.2 mol/L, NaBH4is 0.2 mol/L, the mass ratio of PVA and AgNO3is 0.6 and the reacting temperature is 40 ℃. The average size of silver powder particles is about 120 nm.
sodiumborohydride; silver nitrate; micro-nano-sized silver powder; chemical reduction
TF 123.7+3
A
1673-0224(2015)2-200-07
2014-05-04;
2014-06-24
甘卫平,教授。电话:13707311733;E-mail: gwp@mail.csu.edu.cn

