HPLC-MS/MS法测定犬体内盐酸苯环壬酯的血药浓度及其药动学研究Δ
曾 媛,郑露露,熊 磊,刘 辉#,段 婷(.广州军区武汉总医院药剂科,武汉 430070;.湖北中医药大学药学院,武汉 430065)
盐酸苯环壬酯(PCH)是我国军事医学科学院毒物药物研究所发明的新一代高选择性中枢抗胆碱能抗晕动病Ⅰ类新药[1-2],拥有中国专利2项和英美专利各1项。其制剂盐酸苯环壬酯片用于晕动病的防治,具有疗效可靠、中枢不良反应小的优点[3-5]。由于其给药剂量小(2 mg/d),此剂量下,盐酸苯环壬酯的血药浓度极低[6],因此需要建立简单快速、选择性强且灵敏度高的方法用于血药浓度检测。本研究采用高效液相色谱-质谱联用(HPLC-MS/MS)法建立了盐酸苯环壬酯片在Bealge犬体内的血药浓度测定方法,为盐酸苯环壬酯缓释制剂的开发与临床前研究提供了可靠保证。
1 材料
1.1 仪器
1260 型HPLC 系统,包括二元高压泵系统、自动进样器和切换阀(美国Agilent 公司);API3200 型三重四极杆串联质谱仪,包括电喷雾离子化源(美国AB Sciex公司);Anke TGL-16B型台式离心机(上海安亭科学仪器厂)。
1.2 药品与试剂
盐酸苯环壬酯对照品(批号:100716-200501,纯度:100%)、盐酸戊乙奎醚对照品(批号:100931-201101,纯度:100%)购自中国食品药品检定研究院;盐酸苯环壬酯片(北京华素制药股份有限公司,批号:13082916,规格:每片2 mg);乙腈、甲酸为色谱纯,水为双重蒸馏水,其余试剂均为分析纯。
1.3 动物
2 方法与结果
2.1 色谱条件
色谱柱:Agilent C18(50 mm×3.0 mm,2.7 μm);流动相:乙腈-0.01%甲酸水溶液(60∶40,V/V),流速:0.4 ml/min;柱温:30 ℃;进样量:10µl。
2.2 质谱条件
离子源为电喷雾离子源(ESI 源),正离子方式检测,采用选择性多反应离子监测模式(MRM)同时测定苯环壬酯和内标戊乙奎醚,扫描时间0.2 s。气帘气(CUR):25 psi;雾化器(GS1):40.0 psi;辅助加热器(GS2):55 psi;碰撞气(CAD):5.0 psi;离子喷雾电压(IS):5 500.00 V,离子源温度(TEM):600 。离子去簇电压(DP):61 V(苯环壬酯)、70 V(戊乙奎醚);入口电压(EP):11 V(苯环壬酯)、10 V(戊乙奎醚);碰撞能量(CE):45 eV(苯环壬酯)、55 eV(戊乙奎醚);用于定量分析的离子反应分别为m/z358.3→m/z156.1(苯环壬酯)、m/z316.1→m/z128.1(戊乙奎醚)。
2.3 溶液的制备
2.3.1 盐酸苯环壬酯标准溶液 精密称取盐酸苯环壬酯对照品10 mg,置于100 ml 量瓶中,加乙腈适量,振摇使溶解,加乙腈稀释至刻度,摇匀,即得100µg/ml 的盐酸苯环壬酯贮备液。取该贮备液1 ml,置于100 ml 量瓶中,加乙腈稀释至刻度,得1µg/ml的盐酸苯环壬酯对照品溶液。取上述对照品溶液,以乙腈依次倍比稀释,制备成质量浓度分别为150、100、50、10、5、1 ng/ml 的盐酸苯环壬酯标准溶液,置于4 ℃冰箱保存,备用。
2.3.2 内标溶液 精密称取盐酸戊乙奎醚对照品10 mg,置于100 ml量瓶中,加乙腈适量,振摇使溶解,加乙腈稀释至刻度,摇匀,即得100µg/ml盐酸戊乙奎醚贮备液。取该贮备液适量,加乙腈倍比稀释至250 ng/ml,作为内标溶液,置于4 ℃冰箱保存,备用。
2.4 血浆样品处理
取血浆样品200 μl,加入20µl内标溶液(250 ng/ml),涡漩混匀;再加入400 μl 乙腈,涡旋30 s 后,以离心半径3 cm(下同)、10 000 r/min 离心5 min,取上清液10µl,进行HPLC-MS/MS定量分析。
2.5 方法专属性考察
分别取盐酸苯环壬酯贮备液和盐酸戊乙奎醚贮备液,首先经Q1扫描选择母离子,然后进行二级质谱扫描。根据质谱图分析结果,进行MRM 扫描:苯环壬酯为358.3/156.1(m/z),内标戊乙奎醚为316.1/128.1(m/z)。取空白血浆、空白血浆+盐酸苯环壬酯对照品溶液+内标溶液、犬给药后15 min的血浆样品+内标溶液,按“2.4”项下方法处理后,进行HPLC-MS/MS法分析。结果,空白血浆中内源性杂质和代谢物不干扰盐酸苯环壬酯及内标的测定,盐酸苯环壬酯和内标的保留时间分别为0.692、0.634 min。MRM色谱图见图1。
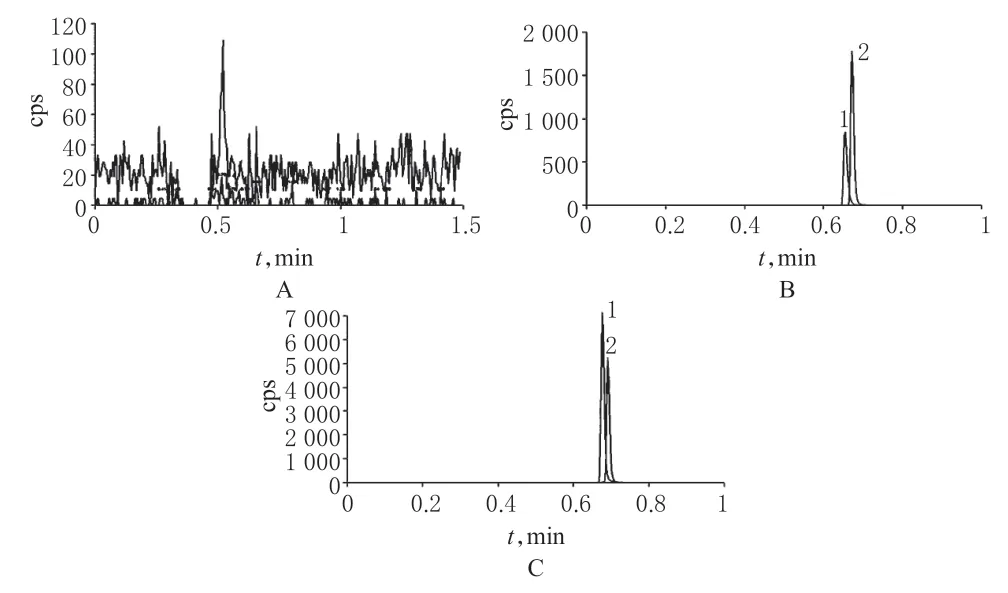
图1 MRM色谱图A.空白血浆;B.空白血浆+盐酸苯环壬酯+内标;C.血浆样品+内标;1.内标;2.盐酸苯环壬酯Fig 1 MRM chromatogramsA.blank plasma;B.blank plasma+PCH+internal standard;C.plasma sample+internal standard;1.internal standard;2.PCH
2.6 标准曲线和定量限考察
取空白血浆180 μl,共12份,加入“2.3.1”项下的盐酸苯环壬酯标准溶液20 μl,制备成盐酸苯环壬酯的质量浓度为15.0、10.0、5.0、1.0、0.5、0.1 ng/ml 的质控样品,按“2.4”项下方法处理,每一浓度进行双样本分析,进样10µl,记录色谱。以盐酸苯环壬酯和内标峰面积比值(y)为纵坐标、盐酸苯环壬酯质量浓度(x)为横坐标,用加权最小二乘法(权重系数:1/c2)进行线性回归,得回归方程为y=0.995 3x+0.066 1(r=0.999 6)。结果,盐酸苯环壬酯检测质量浓度的线性范围为0.1~15.0 ng/ml,定量限为0.1 ng/ml(信噪比为10)。
2.7 回收率与精密度试验
取空白血浆180 μl,按“2.6”项下方法制备盐酸苯环壬酯质量浓度分别为12、7、0.3 ng/ml 的质控样品,各5 份,按“2.4”项下方法处理,进样获得相应色谱峰面积。以其与已知浓度比较计算方法回收率,以其与标准溶液比较计算提取回收率;同一批时间内完成血浆样品处理测定5次考察批内精密度,连续测定3批考察批间精密度。回收率与精密度试验结果见表1。

表1 回收率与精密度试验Tab 1 Results of extraction and precision tests
2.8 血浆样品稳定性考察
取-80 ℃保存0、7、14、21、28 d的血浆样品,按“2.4”项下方法处理后,测定其浓度;同法测定反复冷冻-解冻循环3次的血浆样品和处理后再室温放置0、2、4、8、12、24 h 的血浆样品。结果,盐酸苯环壬酯血浆样品在-80 ℃条件下能稳定保存28 d(RSD=7.2%,n=5);反复冻融3 次并不影响血药浓度测定(RSD=8.9%,n=3);处理后的血浆样品在室温条件下能稳定保存24 h(RSD=5.6%,n=6)。
2.9 基质效应考察
取空白血浆180µl,共6 份,加入400 μl 乙腈沉淀蛋白后,分别加入盐酸苯环壬酯标准溶液和内标溶液,制备成盐酸苯环壬酯质量浓度为12、7、0.3 ng/ml,内标质量浓度为23 ng/ml的对照血浆,按“2.4”项下方法处理后,进行HPLC-MS/MS 法分析获得峰面积。以其与相应质量浓度的盐酸苯环壬酯标准溶液和内标溶液的混合溶液直接进样获得的峰面积之比评价基质效应,比值均在90%~110%之间,表明本试验建立的盐酸苯环壬酯测定方法不受基质效应的影响。
2.10 药动学研究
取犬6 只,实验前1 d 晚8 点开始禁食,实验当天早上8 点分别ig 盐酸苯环壬酯片2 mg 和4 mg。给药后2 h 内禁水,给药4 h 后正常进食进水。给药和实验期间尽量避免犬剧烈运动,食物为低脂肪标准餐。于给药前5 min 和给药后0.17、0.25、0.5、0.75、1.0、1.25、1.5、2、3、4、6、8、10、12、14、16、18、24、36 h时用肝素化真空采血管取前肢静脉血2 ml,4 000 r/min离心10 min,按“2.4”项下方法处理后,采用HPLC-MS/MS 法测定盐酸苯环壬酯的血药浓度。2 周后交叉给药同法测定血药浓度。利用DAS2.0 软件按一级吸收二室模型计算药动学参数。犬血浆中盐酸苯环壬酯的药-时曲线见图2;药动学参数见表2(表中“*”表示高于定量上限浓度的样品采用相应的空白血浆稀释后重新测定的浓度)。
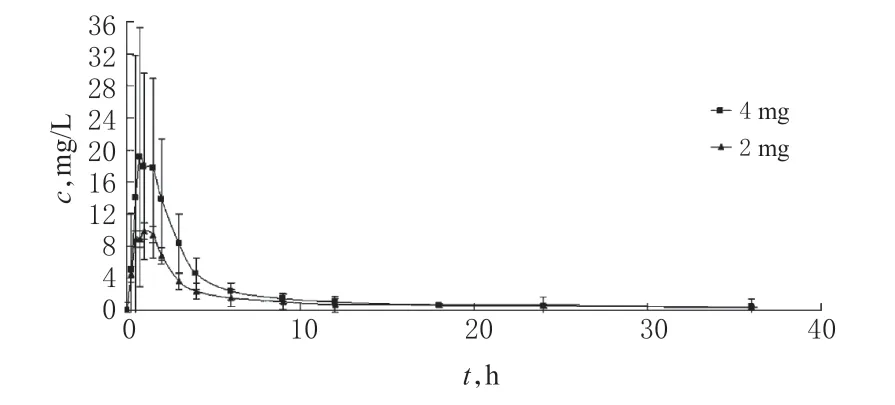
图2 犬血浆中盐酸苯环壬酯的药-时曲线(n=6)Fig 2 Mean plasma concentration-time curves of PCH in the plasma of dogs(n=6)
表2 盐酸苯环壬酯片在犬体内的药动学参数(,n=6)Tab 2 The pharmacokinetic parameters of PCH tablets in dogs(,n=6)
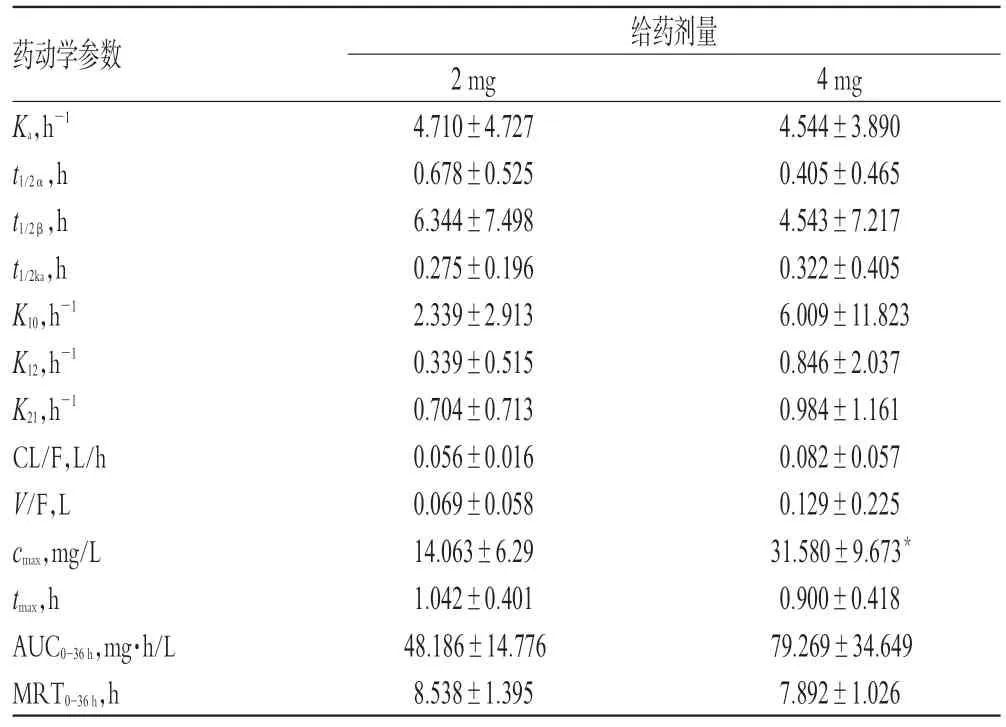
表2 盐酸苯环壬酯片在犬体内的药动学参数(,n=6)Tab 2 The pharmacokinetic parameters of PCH tablets in dogs(,n=6)
犬ig 盐酸苯环壬酯片剂2 mg 和4 mg 后,药动学参数tmax、t1/2α、t1/2β、MRT0-36h经t检验,差异无统计学意义(P>0.05),表明药物的吸收、分布、消除不受剂量影响;AUC0-36h、cmax经t检验,差异有统计学意义(P<0.05),并与服药剂量的倍增一致。此结果与人口服盐酸苯环壬酯片剂2 mg和4 mg的研究[7]相符。
3 讨论
3.1 流动相的选择
本实验中测定的盐酸苯环壬酯为外消旋体,因R-盐酸苯环壬酯、S-盐酸苯环壬酯在有机相比例较低的情况下易于色谱分离,因此采用较高的有机相比例。此时分析物和内标能达到色谱分离目的,但分析物峰形拖尾明显,保留时间较长(>5 min)。在水相中添加一定比例的甲酸,有利于正离子质子化,维持样品在流动相中的电离状态,此时分析物和内标的峰形得到改善,具有很好的对称性,且分析时间缩短至0.7 min。最终优化确定流动相为乙腈-0.01%甲酸水溶液(60∶40)。
3.2 内标的选择
本文建立的HPLC-MS/MS 法对于内标与盐酸苯环壬酯、与杂质的色谱分离要求更高。实验中曾筛选了硫酸阿托品、硝酸毛果芸香碱、盐酸戊乙奎醚等多个内标候选物[8-9],综合保留时间、杂质干扰因素,最终选择盐酸戊乙奎醚为内标。
3.3 方法的选择
在临床前研究盐酸苯环壬酯代谢时,曾采用过放射性同位素分析方法和放射受体分析方法,其给药剂量分别为1 mg/kg和0.5 mg/kg,检测灵敏度仅为5 ng/ml[10]。笔者建立了一种灵敏度高、选择性强的HPLC-MS/MS 法用于Beagle 犬血浆样品中盐酸苯环壬酯的定量分析,方法灵敏度达到了0.1 ng/ml,满足盐酸苯环壬酯在Beagle犬体内药动学研究的要求。
本方法采用盐酸戊乙奎醚为内标,较之同位素标记的内标物更容易获得也更价廉,具有可推广性;采用乙腈直接沉淀蛋白,简化了实验步骤,缩短了测定时间,有利于实现大批量样本的快速分析。笔者应用此方法进行了不同给药剂量的盐酸苯环壬酯片口服给药后Beagle犬体内药动学研究。在各分析批次样品中均匀随机放置高、中、低3 个浓度的质控样品,以此监控分析过程的有效性和准确性。结果显示,质控合格率为98%。
对于本研究结果中出现某些药动学参数s大于x的现象,考虑是由于试验样本量(n=6)少、实验对象存在个体差异造成的。在后期研究过程中,将通过增加样本量来避免此类问题的出现。
[1]刘传缋,恽馏红.中枢解胆碱能抗晕动病新药盐酸苯环壬酯[J].中国药理学与毒理学杂志,2005,19(4):311.
[2]孙建绪,林丐博,贾丽华,等.左旋盐酸苯环壬酯片的含量及溶出度测定方法[J].中国药物应用与监测,2008,5(5):10.
[3]王赟,王丽韫,郑建全,等.盐酸苯环壬酯及其衍生物抗胆碱作用比较研究[J].中国药科大学学报,2006,37(1):59.
[4]张芸,刘辉,樊光辉,等.HPLC法测定盐酸苯环壬酯渗透泵片的含量[J].中国药师,2013,16(11):1 621.
[5]李更.PCH 与PH 光学异构体的药效及药理学研究与pGEX-6p-2-Notch341-656及pGEX-6p-2-Notch3228-656载体的构建与表达及其单克隆抗体的制备[D].兰州:兰州大学,2007.
[6]张石革,孙定人.眩晕与抗眩晕药[J].中国药房,2005,16(5):400.
[7]袁淑兰,乔建忠,阮金秀,等.盐酸苯环壬酯人体药代动力学及生物利用度研究[J].中国临床药理学杂志,1995,11(2):98.
[8]郑露露,曾媛,刘辉,等.高效液相色谱法内标法测定盐酸苯环壬酯控释片的含量[J].中国药业,2014,23(23):47.
[9]于博,李敬来,王晓英,等.LC-MS/MS 法研究左旋去甲基苯环壬酯在比格犬体内的生物利用度[J].军事医学,2012,36(5):365.
[10]刘锋,胡绪英,李前远.人血中盐酸苯环壬酯的GC-MS/SIM定量测定[J].药学学报,1994,29(10):778.

