预防乙型肝炎病毒母婴传播:需要孕晚期抗病毒治疗吗?
林晓倩 周乙华 胡娅莉
(南京大学医学院附属鼓楼医院江苏省医学分子技术重点实验室,江苏南京 210008)
预防乙型肝炎病毒母婴传播:需要孕晚期抗病毒治疗吗?
林晓倩 周乙华 胡娅莉
(南京大学医学院附属鼓楼医院江苏省医学分子技术重点实验室,江苏南京 210008)

胡娅莉,博士,博士生导师,现任南京大学医学院附属鼓楼医院主任医师。中华医学会围产医学分会副主任委员,《中华围产医学杂志》、《中国产前诊断杂志(电子版)》副主编。曾在澳大利亚墨尔本皇家妇女医院,美国霍普金斯大学医学院表遗传研究室、西澳大利亚大学医学院附属KEMH学习。从事妇产科临床工作40余年,发表论文300余篇,其中SCI收录论文87篇。曾获部省级科技成果1、2、3等奖8项。
慢性乙型肝炎病毒(hepatitisBvirus,HBV)感染严重危害我国人民健康,目前我国普通人群乙型肝炎表面抗原(hepatitisBsurfaceantigen,HBsAg)阳性率仍高达7.18%[1],母婴传播是主要原因,预防HBV母婴传播是减少慢性感染的关键。经正规免疫预防,即新生儿在出生后12小时内,肌内注射1针乙肝免疫球蛋白(hepatitisBimmunoglobulin,HBIG),并在24小时内接种第1针乙型肝炎疫苗,1月龄和6月龄分别接种第2和第3针疫苗[2],总体保护率>95%,但仍存在婴幼儿感染[3-5],因此如何进一步减少HBV母婴传播是重要的研究课题。
母婴传播的主要危险因素是HBV载量,即HBVDNA水平,HBeAg阳性通常提示病毒复制活跃,病毒载量高,也是母婴传播的易感因素[3,5,6-10],故有学者推测对HBVDNA高水平孕妇在孕晚期抗病毒治疗可减少母婴传播。本文根据国内外在孕期进行抗HBV治疗预防母婴传播的研究结果,综述如下。
1 抗HBV药物
抗HBV药物有干扰素和核苷或核酸类似物,后者包括拉米夫定、阿德福韦、恩替卡韦、替比夫定和替诺福韦(表1)。
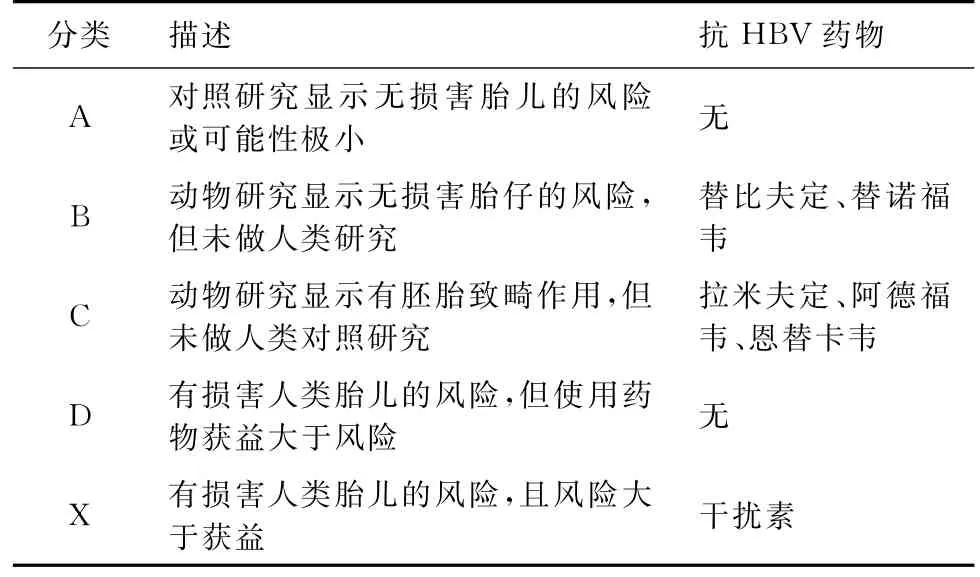
表1 抗HBV药物的妊娠安全性分类[8]
干扰素具有抑制细胞增殖的作用,阿德福韦和恩替卡韦可引起妊娠动物胚胎畸形或死胎,故孕妇禁用[8]。值得注意的是,虽然国内有报道孕期使用阿德福韦对胎儿无不良影响[11],但已有孕妇丈夫服用阿德福韦其胎儿发生多发畸形的病例报道[12],结合动物实验结果,孕妇应禁用阿德福韦和恩替卡韦这两种药物。
动物实验证明替比夫定和替诺福韦不影响胚胎生长发育,属于美国FDA妊娠用药安全性分类中的B类药[8]。拉米夫定无胚胎致畸作用,但有生殖毒性。动物实验表明,拉米夫定可经被动转运通过胎盘而增加兔的胚胎死亡率,属于C类药[13]。虽然动物实验表明这些药物不影响胚胎生长发育或无致畸作用,但因无法进行大规模孕妇人群的临床研究,其安全性有待在临床治疗中积累数据。既往孕期用药的经验表明,如果任何药物缺乏孕妇人群的应用结果,都不能得出安全的结论,例如,曾经被认为对孕妇和胎儿均安全的沙利度胺,大规模使用后导致了严重的不良后果;再如,近期美国FDA将妊娠期使用硫酸镁的安全等级从A类降到D类[14]。因此,孕期使用拉米夫定等抗病毒药物仍需充分权衡利弊。
2 孕期抗HBV治疗预防母婴传播的研究现状
HBV母婴传播的主要危险因素是HBV载量,即HBVDNA水平。抗病毒药物能抑制病毒复制,降低病毒载量,理论上可预防HBV母婴传播。相关研究较多,但其有效性及安全性有待深入的临床研究验证。
拉米夫定是首个用于抗HBV的核苷类似物,使用拉米夫定抗病毒预防母婴传播的报道较多,相关结果见表2。虽然多数研究提示孕晚期使用拉米夫定可减少母婴传播,但其中的一些研究[15-18],无论是治疗组还是对照组,纳入的病例数很少,甚至没有对照组,因此无法得出科学结论。另一些研究样本量虽然较大,但未行抗病毒治疗的对照组孕妇的婴幼儿感染率高达32.7%~39%[19,20],远高于高病毒载量或HBeAg阳性孕妇的婴幼儿正规免疫预防后的感染率(表3),与既往公认的预防效果明显不同,正是因为对照组的高母婴感染率,才反衬出治疗组的优越性。这一方面提示上述研究纳入的病例可能存在特殊性,抽样的代表性不够,或者对照组的婴幼儿可能未经正规预防,另一方面提示这些数据的严谨性有待提高。
同时,不同研究组报道的结果差异很大(表2)。既有报道孕妇使用拉米夫定治疗后,其婴幼儿均无慢性HBV感染[17,18,21-24],也有报道感染率仍高达12.5%~18%[16,19,20]。这些数据的不一致性,至少说明孕晚期使用拉米夫定抗病毒治疗预防HBV母婴传播的效果仍有待进一步验证。
替比夫定属于妊娠B类药(表1),临床研究显示,孕妇在孕中晚期开始使用该药,能减少HBV的母婴传播(表2)。其中,用替比夫定治疗257例、132例、50例和279例HBeAg阳性的感染孕妇,其婴儿6~12月龄左右随访,均无母婴传播发生[24-27],表明替比夫定可以有效预防母婴传播。
替诺福韦也属于妊娠B类药(表1),最近的临床研究提示,它能减少HBV母婴传播(表2)[23,28-30]。但这些研究纳入的病例都较少,有的甚至缺乏对照[28,30],无法得出科学结论。同时,研究报道的预防效果不一,有2项研究分别用替诺福韦治疗11例和21例孕妇,新生儿均未发生慢性感染[28,29],但另2项研究显示,治疗的44例和13例孕妇,各有1例发生母婴传播,感染率为分别为2%[23]和7.7%[30]。因此,替诺福韦在预防HBV母婴传播中的确切效果仍有待更多严格对照、多中心、大样本的研究。
孕期抗病毒治疗是否对母婴产生不良影响,始终是值得关注的问题。尽管有研究报道,抗HBV药物对母婴均无明显不良后果[19,25,27,28],但也有不少孕妇抗病毒治疗后胎儿或新生儿出现严重不良事件的报道[17,22,23,26,30,40-43]。
抗HBV药物对孕妇产生的副作用需引起关注。核苷或核酸类似物不能清除病毒,停药后病毒反跳,诱发肝功能损害[26,40,41],甚至发展为重型肝炎[41]。拉米夫定和替比夫定均可诱发病毒变异而产生耐药[17,22,42]。Ayres等[22]报道了21例孕妇平均用药53天后,4例(19%)产生病毒耐药变异株,1例(4.8%)检测出疫苗逃逸变异体。孕妇抗HBV治疗后易出现自然流产,92例拉米夫定治疗和89例替比夫定治疗的孕妇中各有11例(11.6%)[41]和6例(6.7%)[42]流产。其他罕见的严重不良反应包括肾功能不全、肌炎、横纹肌溶解、乳酸酸中毒等[43]。
多项研究发现,孕期抗病毒治疗后出现胎儿或新生儿不良事件增多,这值得高度重视。在73例拉米夫定治疗母亲的新生儿中,3例低出生体重,1例头皮血管瘤,1例脑瘫[41]。Greenup等[23]报道,43例接受拉米夫定治疗的孕妇分娩的新生儿中,1例低出生体重,1例多指畸形,1例单侧耳朵阙如,1例在3月龄时发生猝死。孕妇替比夫定治疗,其子女同样出现不良严重后果。53例接受替比夫定治疗的孕妇分娩的新生儿中,3例低出生体重,1例发生唇腭裂终止妊娠,1例单侧耳聋[42]。而本研究组对孕妇孕晚期用替比夫定治疗,随访的121例子女中,也发现1例耳廓阙如,1例行动发育迟缓,1例脑瘫,而151例对照组的子女,均无畸形发生(未发表资料)。孕期服用替诺福韦预防HBV母婴传播的报道虽然较少,但已有不良事件的报道。44例接受替诺福韦治疗的孕妇分娩的新生儿中,2例低出生体重,1例单侧耳聋[23]。另一组13例接受替诺福韦治疗的孕妇分娩的新生儿中,1例尿道下裂[30]。总体上,在不多的孕期治疗病例中,听力障碍、耳廓阙如、脑瘫等严重不良事件重复发生,高度提示与孕期抗HBV治疗可能存在一定关系,因此,抗HBV药物对胎儿及婴幼儿的影响仍有待进一步观察。

表2 孕妇抗HBV治疗后婴幼儿的感染率
3 孕晚期抗HBV治疗预防母婴传播,真的需要吗?
HBVDNA是确切反映病毒量高低的直接指标,HBV母婴传播多见于高病毒载量的孕妇,但易发生母婴传播的病毒载量阈值尚无定论。我国多数学者认为当孕妇血清HBVDNA>106拷贝/ml时易发生HBV母婴传播[3,9,10],国际上也有学者认为孕妇HBVDNA>2000IU/ml为母婴传播易感因素[44],但更多学者认为HBVDNA>108拷贝/ml,即2×107IU/ml,其子女才易发生慢性HBV感染[5-8]。这可能与不同研究对象有关,更重要的,可能与不同检测方法的灵敏度有关。
HBeAg与HBVDNA水平密切相关,也是母婴传播的易感因素,HBeAg阳性,病毒量高。国产试剂检测HBeAg结果稳定可靠,适合于各级医院。因此,将HBeAg阳性作为母婴传播的易感因素更适合我国国情。
研究显示,HBeAg阴性的HBV感染孕妇或育龄妇女,其HBVDNA的平均水平为2.7logIU/ml[4]或2.7log拷贝/ml[9],较HBeAg阳性感染者低1万~10万倍;其中HBV DNA>6 log IU/ml的比例仅0~1.9%[4,9],>8 log IU/ml的比例几乎为零[4,7,9],说明HBe Ag阴性的HBV感染母亲,其子女感染风险极小,这与实际研究结果相一致。大量临床观察显示,其感染率仅为0~1%(表3)。因此,对HBeAg阴性孕妇,其新生儿正规免疫预防后几乎不发生慢性HBV感染,无需抗病毒治疗预防母婴传播。
HBe Ag阳性的感染孕妇,其HBV DNA水平达7.4 log拷贝/ml[9]或8.1 log IU/ml[4],说明其体内病毒载量高,是母婴传播的易感因素。大量研究亦表明母婴传播基本发生在HBe Ag阳性孕妇中(表3),其婴幼儿感染率为10%左右,因此有必要进一步降低此类婴幼儿感染率。根据目前报道,孕晚期抗病毒治疗的确能减少甚至阻断HBV母婴传播[21,24-27],但如前所述,孕期抗病毒治疗后,孕妇以及胎儿和新生儿的严重不良事件似乎也增多[17,22,23,26,30,40-43]。因此,我们认为,对HBe Ag阳性孕妇是否抗HBV治疗,需要充分权衡利弊,目前尚不能对孕妇推荐以预防母婴传播为目的的孕期抗病毒治疗。
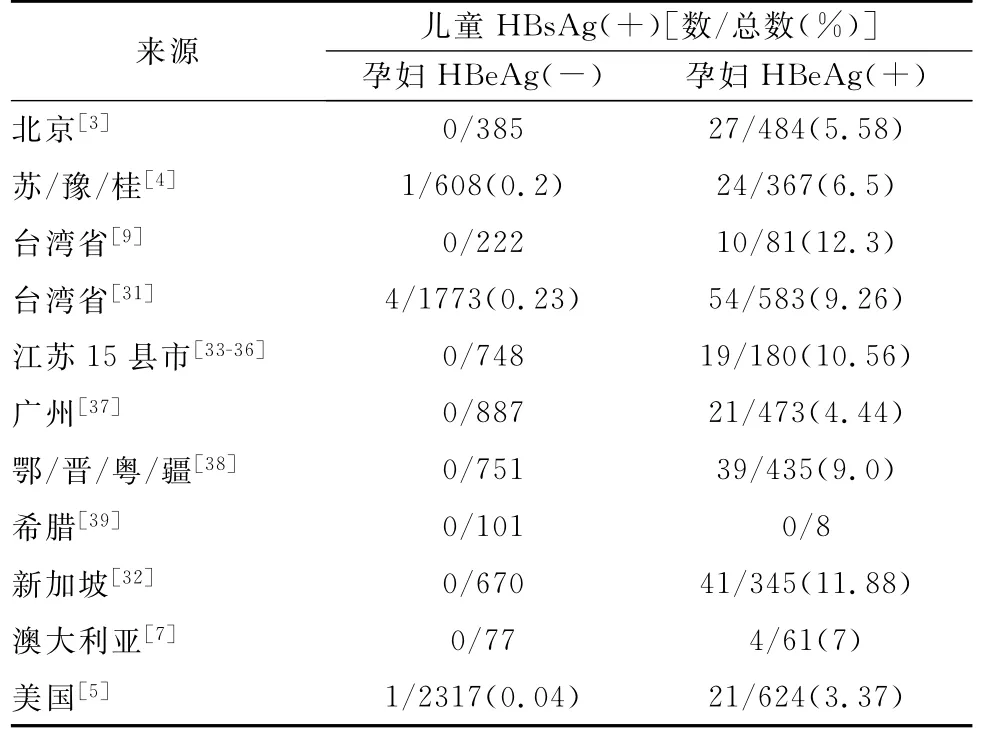
表3 HBV感染母亲的婴幼儿免疫预防后HBs Ag的阳性率
最新研究显示,HBe Ag阳性孕妇即使孕期不抗病毒治疗,其新生儿的感染率也可进一步降低。虽然既往报道HBeAg阳性孕妇的子女经过免疫预防后感染率为10%左右,但Kobo等[5]报道624例HBe Ag阳性母亲的子女,感染率仅3.37%。我国一项研究表明,352例HBe Ag阳性、HBV DNA平均水平为7.58 log拷贝/ml的孕妇,其新生儿感染率仅2.84%[24]。我们研究发现,77例HBe Ag阳性、HBV DNA平均水平为7.4 log IU/ml的孕妇,其新生儿出生后注射HBIG和第1针乙肝疫苗的中位数时间分别为0.5小时和0.3小时,并于1月龄和6月龄分别接种第2和第3针疫苗,12月龄时无一例慢性感染[26]。这些婴幼儿感染率下降的原因,主要与对新生儿更早采取正规的免疫预防有关。实际上,既往报道的免疫预防失败,多数与没有及时使用HBIG和(或)乙型肝炎疫苗有关[9,35]。因此,缩短新生儿出生后接受正规免疫预防的时间,能否进一步减少HBV母婴传播,值得严谨的多中心、大样本的研究。
4 总 结
对HBe Ag阴性或HBV DNA<106拷贝/ml的孕妇,其新生儿正规免疫预防后几乎无感染,因此无需抗病毒治疗预防母婴传播。对HBe Ag阳性或HBV DNA>106拷贝/ml者是否抗病毒治疗仍需进一步研究,理由如下:①正规免疫预防可有效保护高危新生儿,即使母亲不抗HBV治疗,子女保护率可达90%~95%;②出生后立即采取免疫预防,可进一步减少HBV母婴传播;③孕晚期抗病毒治疗后仍存在母婴传播;④抗HBV药物不能清除病毒,停药后病毒反跳,出现肝功能损害,甚至诱发重型肝炎;⑤拉米夫定和替比夫定均可诱发病毒变异,产生耐药;⑥抗HBV药物对胚胎和新生儿可能存在严重不良影响。因此,目前尚不能确定对HBeAg阳性或HBV DNA高载量孕妇孕晚期常规抗病毒治疗是否能有效降低母婴传播,这有待更多设计严谨、严格对照的大样本、多中心研究。通过缩短出生后到接种HBIG和乙肝疫苗的时间(出生后越快越好)以减少HBV母婴传播,值得进一步开展循证医学研究。
[1]Zhou YH,Wu C,Zhuang H.Vaccination against hepatitis B:the Chinese experience[J].Chin Med J(Engl),2009,122(1):98-102.
[2]中华医学会妇产科学分会产科学组.乙型肝炎病毒母婴传播预防临床指南(第1版)[J].中华妇产科杂志,2013,48(2):151-154.
[3]Zou H,Chen Y,Duan Z,et al.Virologic factors associated with failure to passive-active immunoprophylaxis in infants born to HBs Ag-positive mothers[J].J Viral Hepat,2012,19(2):e18-e25.
[4]Sun KX,Li J,Zhu FC,et al.A predictive value of quantitative HBs Ag for serum HBV DNA level among HBeAg-positive pregnant women[J].Vaccine,2012,30(36):5335-5340.
[5]Kubo A,Shlager L,Marks AR,et al.Prevention of vertical transmission of hepatitis B:an observational study[J].Ann Intern Med,2014,160(12):828-835.
[6]Ngui SL,Andrews NJ,Underhill GS,et al.Failed postnatal immunoprophylaxis for hepatitis B:characteristics of maternal hepatitis B virus as risk factors[J].Clin Infect Dis,1998,27(1):100-106.
[7]Wiseman E,Fraser MA,Holden S,et al.Perinatal transmission of hepatitis B virus:an Australian experience[J].Med J Aust,2009,190(9):489-492.
[8]Yogeswaran K,Fung SK.Chronic hepatitis B in pregnancy:unique challenges and opportunities[J].Korean J Hepatol,2011,17(1):1-8.
[9]Wen WH,Chang MH,Zhao LL,et al.Mother-to-infant transmission of hepatitis B virus infection:significance of maternal viral load and strategies for intervention[J].J Hepatol,2013,59(1):24-30.
[10]Zhang L,Gui X,Wang B,et al.A study of immunoprophylaxis failure and risk factors of hepatitis B virus mother-to-infant transmission[J].Eur J Pediatr,2014,173(9):1161-1168.
[11]赵克开,赵怡,苗千里.服用阿德福韦酯期间妊娠足月产婴儿的安全性分析[J].中华肝脏病杂志,2012,20(6):476-477.
[12]Gu Y,Ru T,Zhou YH,et al.Adefovir as a possible teratogen:Evidence from paternal exposure[J].Dig Liver Dis,2014,46(12):1134-1135.
[13]Giles M,Visvanathan K,Sasadeusz J.Antiviral therapy for hepatitis B infection during pregnancy and breastfeeding[J].Antiviral Therapy,2011,16(5):621-628.
[14]Food and Drug Administration.FDA Drug Safety Communication:FDA Recommends Against Prolonged Use of Magnesium Sulfate to Stop Pre-term Labor Due to Bone Changes in Exposed Babies[EB/OL].[2013-05-31].http://www.fda. gov/Drugs/DrugSafety/DrugSafetyPodcasts/ucm354762.htm
[15]van Nunen AB,de Man RA,Heijtink RA,et al.Lamivudine in the last 4 weeks of pregnancy to prevent perinatal transmission in highly viremic chronic hepatitis B patients[J].J Hepatol,2000,32(6):1040-1041.
[16]van Zonneveld M,van Nunen AB,Niesters HG,et al.Lamivudine treatment during pregnancy to prevent perinatal transmission of hepatitis B virus infection[J].J Viral Hepat,2003,10(4):294-297.
[17]Su GG,Pan KH,Zhao NF,et al.Efficacy and safety of lamivudine treatment for chronic hepatitis Bin pregnancy[J].World J Gastroenterol,2004,10(6):910-912.
[18]Köse S,Türken M,Devrim I,et al.Efficacy and safety of lamivudine treatment in late pregnancy with high HBV DNA:a perspective for mother and infants[J].J Infect Dev Ctries,2011,5(4):303-306.
[19]Li XM,Yang YB,Hou HY,et al.Interruption of HBV intrauterine transmission:a clinical study[J].World J Gastroenterol,2003,9(7):1501-1503.
[20]Xu WM,Cui YT,Wang L,et al.Lamivudine in late pregnancy to prevent perinatal transmission of hepatitis B virus infection:a multicentre,randomized,double-blind,placebocontrolled study[J].J Viral Hepat,2009,16(2):94-103.
[21]Yu M,Jiang Q,Ji Y,et al.The efficacy and safety of antiviral therapy with lamivudine to stop the vertical transmission of hepatitis B virus[J].Eur J Clin Microbiol Infect Dis,2012,31(9):2211-2218.
[22]Ayres A,Yuen L,Jackson KM,et al.Short duration of lamivudine for the prevention of hepatitis B virus transmission in pregnancy:lack of potency and selection of resistance mutations[J].J Viral Hepat,2014,21(11):809-817.
[23]Greenup AJ,Tan PK,Nguyen V,et al.Efficacy and safety of tenofovir disoproxil fumarate in pregnancy to prevent perinatal transmission of hepatitis B virus[J].J Hepatol,2014,61(3):502-507.
[24]Zhang H,Pan CQ,Pang Q,et al.Telbivudine or lamivudine use in late pregnancy safely reduces perinatal transmission of hepatitis B virus in real-life practice[J].Hepatology,2014,60(2):468-476.
[25]Han GR,Cao MK,Zhao W,et al.A prospective and openlabel study for the efficacy and safety of telbivudine in pregnancy for the prevention of perinatal transmission of hepatitis B virus infection[J].J Hepatol,2011,55(6):1215-1221.
[26]胡娅莉,温坚,徐飚,等.替比夫定阻断HBe Ag阳性孕妇预防HBV母婴传播的效果[C].第八次全国围产医学学术会议论文汇编,2013:321.
[27]Wu Q,Huang H,Sun X,et al.Telbivudine prevents vertical transmission of hepatitis B virus from women high viral loads:a prospective long-term study[J].Clin Gastroenterol Hepatol,2014,pii:S1542-3565(14)01356-1.
[28]Pan CQ,Mi LJ,Bunchorntavakul C,et al.Tenofovir disoproxil fumarate for prevention of vertical transmission of hepatitis B virus infection by highly viremic pregnant women:a case series[J].Dig Dis Sci,2012,57(9):2423-2429.
[29]Celen MK,Mert D,Ay M,et al.Efficacy and safety of tenofovir disoproxil fumarate in pregnancy for the prevention of vertical transmission of HBV infection[J].World JGastroenterol,2013,19(48):9377-9382.
[30]Tsai PJ,Chang A,Yamada S,et al.Use of tenofovir disoproxil fumarate in highly viremic,hepatitis B mono-infected pregnant women[J].Dig Dis Sci,2014,59(11):2797-2803.
[31]Chen HL,Lin LH,Hu FC,et al.Effects of maternal screening and universal immunization to prevent mother-toinfant transmission of HBV[J].Gastroenterology,2012,142(4):773-781.
[32]Oon CJ,Lim GK,Ye Z,et al.Molecular epidemiology of hepatitis B virus vaccine variants in Singapore[J].Vaccine,1995,13(8):699-702.
[33]王志群,张姝,刘启兰,等.常规应用免疫预防对阻断乙型肝炎病毒母婴感染效果的评价[J].中华围产医学杂志,2011,14(6):338-342.
[34]芮燕京,宋文英,陈洁,等.乙肝疫苗联合乙肝免疫球蛋白预防HBe Ag阴性的HBV感染母亲母婴传播的效果评估[J].实用妇产科杂志,2013,29(7):506-509.
[35]徐陈瑜,陈洁,温坚,等.乙型肝炎疫苗和乙肝免疫球蛋白阻断乙肝病毒母婴传播的效果[J].现代妇产科进展,2013,22(1):1-5.
[36]唐洁,许联红,陈洁,等.新生儿免疫预防乙型肝炎病毒母婴传播的效果及传播易患因素分析[J].中国妇幼保健,2014,21(29):3427-3430.
[37]Yin Y,Wu L,Zhang J,et al.Identification of risk factors associated with immunoprophylaxis failure to prevent the vertical transmission of hepatitis B virus[J].J Infect,2013,66(5):447-452.
[38]Zhang L,Gui X,Fan J,et al.Breast feeding and immunoprophylaxis efficacy of mother-to-child transmission of hepatitis B virus[J].J Matern Fetal Neonatal Med,2014,27(2):182-186.
[39]Papaevangelou V,Paraskevis D,Anastassiadou V,et al.HBV viremia in newborns of HBs Ag(+)predominantly Caucasian HBeAg(-)mothers[J].J Clin Virol,2011,50(3):249-252.
[40]Kim HY,Choi JY,Park CH,et al.Outcome after discontinuing antiviral agents during pregnancy in women infected with hepatitis B virus[J].J Clin Virol,2013,56(4):299-305.
[41]Yi W,Liu M,Cai HD.Safety of lamivudine treatment for chronic hepatitis B in early pregnancy[J].World J Gastroenterol,2012,18(45):6645-6650.
[42]Liu M,Cai H,Yi W.Safety of telbivudine treatment for chronic hepatitis B for the entire pregnancy[J].J Viral Hepat,2013,20(Suppl 1):65-70.
[43]Fontana RJ.Side effects of long-term oral antiviral therapy for hepatitis B[J].Hepatology,2009,49(Suppl 5):185-195.
[44]Pande C,Sarin SK,Patra S,et al.Prevalence,risk factors and virological profile of chronic hepatitis B virus infection in pregnant women in India[J].J Med Virol,2011,83(6):962-967.
R512.6+2
A
2014-11-30)
编辑:杨颖俊
10.13470/j.cnki.cjpd.2015.01.001
国家临床重点专科建设项目(2011271);江苏省科技发展计划项目(BL2012015);江苏省母胎医学重点学科建设项目(XK201102);南京市卫生人才工程项目(QRX11024)
*通讯作者:胡娅莉,E-mail:dtylhu@126.com
——以《推销员之死》对话选段为例
——论阿瑟•米勒的悲剧《推销员之死》

